Влияние вич инфекции на результаты двухэтапного эндопротезирования тазобедренного сустава при септическом коксите
Автор: Зубиков В.С., Перецманас Е.О., Герасимов И.А., Рукин Я.А.
Журнал: Кафедра травматологии и ортопедии @jkto
Рубрика: Оригинальное исследование
Статья в выпуске: 4 (62), 2025 года.
Бесплатный доступ
Введение. Двухэтапное эндопротезирование при деструктивной форме септического коксита (CK) с использованием цементных артикулирующих спейсеров с антибиотиками в настоящее время используется весьма ограниченным кругом авторов в отличие от похожей тактики, применяющейся при лечении перипротезной инфекции. Данные по эффективности метода на основе анализа значимого по объему клинического материала представлены лишь в единичных работах, и полностью отсутствуют данные о применении метода у больных с ВИЧ инфекцией. Цель исследования. Оценка эффективности метода двухэтапного эндопротезирования с использованием артикулирующих цементных спейсеров, насыщенных антибактериальными препаратами, при лечении деструктивных форм септического коксита, включая случаи с ВИЧ-инфекцией. Материал и методы. В исследование включено 50 пациентов с септическим кокситом, которым в 51 случае выполнялась санация тазобедренного сустава с использованием цементных артикулирующих спейсеров с антибиотиками. Больные были разделены на группы. В 1-ю группу вошли 40 пациентов (41 случай), не страдающих ВИЧ инфекцией, во 2-ю группу – 10 пациентов с ВИЧ инфекцией. В 1-й группе больных, интактных по ВИЧ инфекции, второй этап хирургического лечения выполнен в 37 (90,2 %) случаях, а во 2-й группе, с ВИЧ инфекцией – в 8 (80 %). Результаты. Положительным результатом проведенного хирургического лечения считали выполнение двух этапов хирургического лечения при отсутствии инфекции установленного эндопротеза, а также восстановление опороспособности конечности. Таким образом, в 1-й группе положительные результаты получены в 34 (82,9 %) из 41 случая. Во 2-й группе - только в 4-х (40 %) из 10 случаев. Функциональные результаты по системе HHS оценивали в отдельных группах только у пациентов, которым выполнены оба этапа хирургического лечения, включая случаи с тяжелыми инфекционными осложнениями, где эндопротез был удален. Оценка в баллах по системе ННS в первой группе больных (n = 37) дала существенное улучшение средних показателей: с 39,1±10,7 (до начала хирургического лечения) до 89,8±11,2 (после получения окончательного результата). Подобная оценка во 2-й группе у больных с ВИЧ инфекцией (n=8) дала следующие данные: 38,3±6,7 (до хирургического лечения) и 51±7,8 (после оценки окончательного результата). Заключение. Результаты исследования показали достаточную эффективность двухэтапного эндопротезирования тазобедренного сустава при деструктивной форме септического коксита у больных без ВИЧ инфекции. У ВИЧ инфицированных больных результаты были существенно хуже в связи с большим количеством инфекционных осложнений как на первом, так и на втором этапе хирургического лечения.
Септический коксит, двухэтапное эндопротезирование тазобедренного сустава, цементный артикулирующий спейсер с антибиотиками, ВИЧ инфекция
Короткий адрес: https://sciup.org/142246881
IDR: 142246881 | УДК: 617.3 | DOI: 10/17238/issn2226-2016.2025.4.102-111
Influence of hiv infection on the outcomes of two-stage hip arthroplasty in septic coxitis
Introduction: Two-stage total hip arthroplasty for destructive septic coxitis using cemented articulating spacers with antibiotics is currently used by a very limited number of authors, in contrast to a similar approach used to treat hip periprosthetic infection. Data on the effectiveness of this method, based on the analysis of significant clinical observations, are presented only in a few studies, and there are no data on its use in patients with HIV infection. Purpose of the study. Evaluation of the effectiveness of a two-stage hip arthroplasty using articulating cement spacers with antibiotics in the treatment of destructive forms of septic coxitis, including cases with HIV infection. Materials and Methods. The study included 50 patients with septic coxitis, 51 of whom underwent hip joint debridement using cemented articulating spacers with antibiotics. The patients were divided into groups. Group 1 included 40 patients (41 cases) who were HIV-negative, and Group 2 included 10 patients with HIV infection. In Group 1, the second stage of surgical treatment was performed in 37 (90.2%) patients, while in Group 2, the second stage of surgical treatment was performed in 8 (80%) patients. Results. A positive outcome of the surgical treatment was considered to be the completion of two stages of surgical treatment in the absence of infection of the hip endoprosthesis, as well as the restoration of the weight-bearing ability of the limb. Thus, in the Group 1, positive results were obtained in 34 (82.9%) of 41 cases. In the Group 2 - only in 4 (40%) of 10 cases. Functional results according to the HHS system were assessed only in patients who underwent both stages of surgical treatment, including cases with severe infectious complications, where the endoprosthesis was removed. The assessment in points according to the HHS system in the first group of patients (n = 37) gave a significant improvement in the average indicators: from 39.1 ± 10.7 (before surgical treatment) to 89.8 ± 11.2 (after obtaining the final result). A similar assessment in the 2nd group of patients with HIV infection (n=8) yielded the following data: 38.3±6.7 (before surgical treatment) and 51±7.8 (after assessing the final result). Conclusion. The study demonstrated the reasonable effectiveness of two-stage hip arthroplasty for destructive septic coxitis in patients without HIV infection. In HIV-infected patients, the results were significantly worse due to the higher incidence of infectious complications in both the first and second stages of surgery.
Текст научной статьи Влияние вич инфекции на результаты двухэтапного эндопротезирования тазобедренного сустава при септическом коксите
Септический коксит (СК) – достаточно редкое, но опасное заболевание, способное быстро разрушить тазобедренный сустав. Частота возникновения септического артрита тазобедренного и коленного суставов, по данным литературы, составляет от 2 до 10 случаев на 100 000 населения [1, 2]. Авторами подчеркивается, что в возникновении септического артрита важными факторами являются: сахарный диабет, состояния иммунодефицита, а также предшествующие внутрисуставные инъекции кортикостероидных препаратов [3]. Ключевым фактором в случаях СК являются сроки протекания инфекции (от ее возникновения до диагностики и начала активного лечения) При раннем выявлении инфекции сустава и выделении возбудителя может быть применена операция открытого или артроскопического дебридмента сустава на фоне этиотропной антибактериальной терапии [4]. Если уже выявляются деструктивные изменения суставного хряща и костной ткани, то требуется применение более радикальной хирургии. Однако, широко применяемая ранее резекционная артропластика по-Girdlestone, несмотря на успехи в лечении самой инфекции, давала неудовлетворительные ортопедические результаты из-за формирования укорочения конечности, нарушения подвижности сустава и ограниченной опоры на оперированную ногу [5]. При последующем эндопротезировании тазобедренного сустава после резекционной артропластики хорошее функциональное восстановление наблюдалось далеко не всегда [6]. Другими авторами у пациентов после резекционной артропластики отмечен весьма высокий уровень рецидивов инфекции – 31.6 % [7]. Для хирургического лечения деструктивной формы СК по аналогии с лечением перипротезной инфекции применяется двухэтапный метод эндопротезирования с использованием артикулирующих цементных спейсеров, насыщенных антибиотиками.
В последние годы накоплен определенный опыт по применению двухэтапного метода эндопротезирования при СК с использованием антибактериального артикулирующего спейсера из цемента с антибиотиками. Однако, приводимое авторами количество клинических наблюдений не так велико. Наибольшее количество наблюдений приведено в обзорах C. Xu и соавт. [8] и A.Russo и соавт. [9]. Рядом авторов приводится анализ от 20 до 28 наблюдений [10, 11, 12, 13, 14], другими – от 11 до 15 наблюдений [15, 16, 17, 18, 19, 20, 21], а некоторыми – всего от 5 до 9 случаев [22, 23, 24]. Эффективность применения данного метода остается недостаточно ясной, данные широко колеблются в зависимости от количества наблюдений.
В российской печати имеются лишь единичные работы, касающихся проблемы двухэтапного эндопротезирования тазобедренного сустава при СК [13, 20, 25].
В современной литературе имеются противоречивые данные влияния ВИЧ инфекции на результаты эндопротезирования суставов. По одним данным, наличие ВИЧ инфекции у пациента не является отягощающим обстоятельством при эндопротезировании суставов при условии постоянного применении высокоактивной антиретровирусной терапии [26, 27]. Другие авторы сообщают об ухудшении результатов эндопротезирования у ВИЧ инфицированных больных [28, 29]. В то же время, в доступной литературе мы не нашли данных как о фактах, так и о результатах эндопротезирования тазобедренного сустава у больных с СК и ВИЧ инфекцией, в частности, при применении двухэтапной методики.
Цель исследования
Оценить эффективность метода двухэтапного эндопротезирования с использованием артикулирующих цементных спейсеров, насыщенных антибактериальными препаратами, при лечении деструктивных форм септического коксита, включая случаи с ВИЧ-инфекцией.
Материал и методы
Проведено проспективное когортное моноцентровое исследование, в которое включено изучение результатов 51 случая хирургического лечения у 50 пациентов с деструктивной формой СК. У одного из пациентов имел место двусторонний процесс. Операции выполнены в период с 2012 по 2024 гг. Критериями включения являлись случаи активно протекающего СК неспецифической этиологии с наличием необратимой костно-хрящевой деструкции в суставе как при отсутствии, так и при наличии ВИЧ инфекции. Критериями исключения являлись случаи туберкулеза сустава.
Дизайн работы предусматривал осуществление эндопротезирования всем больным по двухэтапной методике с использованием на 1-м этапе артикулирующих спейсеров из цемента, насыщенного антибактериальными препаратами [31]. Предусматривалось получение данных о результатах лечения как по основной когорте пациентов, так и сравнительная оценка результатов в зависимости от ВИЧ-статуса пациента.
Все 50 пациентов подписали информированное согласие на участие и были включены в исследование, так как соответствовали критериям включения.
Анализ клинических данных
В общей когорте больных преобладали мужчины – 32 (64,0 %), пациентов женского пола было существенно меньше –18 (36,0 %).
Возраст больных на момент начала хирургического лечения составлял от 31 до 69 лет, в среднем –53,23 ± 11,97 лет.
Распределение пациентов по полу и возрасту представлено в таблице 1.
Таблица 1
Распределение пациентов общей когорты по возрасту и полу
|
Пол |
31–45 лет (группа молодых) |
46–59 лет (группа среднего возраста) |
60–69 лет (старшая возрастная группа) |
Итого: |
|
Мужской |
13 (26,0%) |
7 (14,0%) |
12 (24,0%) |
32 (64,0%) |
|
Женский |
5 (10,0%) |
4 (8,0%) |
9 (18,0%) |
18 (36,0%) |
|
Всего |
18 (36,0 %) |
11 (22,0%) |
21 (42,3%) |
50 (100%) |
Как видно из таблицы 1, случаи заболевания септическим кокситом не имели отчетливой связи с возрастом больных и встречались во всех возрастных группах в целом, несколько превалируя в старшей возрастной группе, как среди мужчин, так и женщин.
Для оценки результатов исследования все 50 пациентов с деструктивным септическим кокситом ретроспективно были разделены на две группы в зависимости от наличия или отсутствия ВИЧ инфекции:
Группа 1 – пациенты, не имеющая ВИЧ инфекции (40 пациентов);
Группа 2 – пациенты с ВИЧ инфекцией (10 пациентов).
При этом в первой группе нами пролечен пациент с двусторонним септическим кокситом, и количество наблюдений составило 41 (у 40 больных)
Всем пациентам с деструктивным септическим кокситом до назначения хирургического лечения осуществлялась инвазивная диагностика: трепанобиопсия головки бедренной кости с взятием биологического материала из зон костной деструкции (в одном или более локусов) с последующим микробиологическим, гистологическим и молекулярно-генетическим исследованием с использованием полимеразноцепной реакции (ПЦР). Последняя выполнялась с целью исключения туберкулеза сустава. Другой целью предоперационной диагностики была верификация возбудителя инфекции, что являлось непростой задачей, так как у целого ряда больных с септическим кокситом существовала история предшествующего лечения антибактериальными препаратами, в основном – антибиотиками широкого спектра действия. Поэтому верификация неспецифической инфекции была частично выполнена с помощью микробиологического исследования, частично – по анамнестическим данным или из представленной медицинской документации, а у части больных возбудитель инфекции выявить не удалось, хотя диагноз «септического коксита» сомнений не вызывал (таблица 2). В подавляющем большинстве случаев при септическом коксите мы наблюдали гематогенный путь инфицирования сустава и только в одном случае инфицирование возникло ятрогенным путем после хирургического вмешательства на суставе с оставлением в ране инородного тела. Характер выявленной инфекции и распределение по группам больных представлены в таблице 2. В отдельных случаях у больных при исследовании биологического материала получены ассоциации патогенных микроорганизмов. При возникновении осложнений разные патогены могли выявляться на разных этапах хирургического лечения.
Таблица 2
Характер бактериальной инфекции при септическом коксите в группе больных, интактных по ВИЧ инфекции и в группе ВИЧ инфицированных
|
Вид инфекции |
Группы больных |
||
|
Группа 1 интактные по ВИЧ |
Группа 2 ВИЧ инфицированные |
||
|
MSSA |
27 |
4 |
|
|
MRSA |
1 |
- |
|
|
Pseudomonas aerugenosa |
1 |
1 |
|
|
Klebsiella pneumonii |
1 |
- |
|
|
Enterococcus |
1 |
- |
|
|
Streptococcus |
1 |
- |
|
|
Acinetobacter baumanii |
- |
1 |
|
|
Mycobacterium chelonae |
1 |
- |
|
|
Proteus mirabilis |
1 |
- |
|
|
Полими-кробная инфекция: |
MRSA, Klebsiella pneumonii, Pseudomonas aerugenosa |
1 |
- |
|
Strept. Epidermidis, MSSA |
- |
1 |
|
|
Staph. Pettenkofen, Staph. Warner |
1 |
- |
|
|
Proteus mirabilis, E. coli, Pseudomonas aerugenosa |
1 |
- |
|
|
MSSA, Klebsiella pneumonii |
- |
1 |
|
|
Верифицировать не удалось |
5 (12,2%) |
1 (10%) |
|
|
ИТОГО: |
41 |
10 |
|
– MSSA – метициллин чувствительный золотистый стафилококк
– MRSA – метициллин резистентный золотистый стафилококк
Все пациенты с ВИЧ инфекцией (10 наблюдений) имели 4Б стадию заболевания. У этих больных оценивали как вирусную нагрузку, так и степень снижения иммунитета по уровню CD4 клеток в крови. У 4-х пациентов вирусная нагрузка в крови на время лечения септического коксита отсутствовала – (0), у остальных 6 пациентов она колебалась в значениях от 50 до 686 копий, в среднем – 167± 255 копий.
Уровень CD4 клеток в крови находился в диапазоне от 140 до 1072, в среднем – 447,7± 274,5.
Особенности хирургического лечения
В соответствии с принятым дизайном работы планировалось двухэтапное лечение. На первом этапе после санирующей резекции сустава устанавливали артикулирующий спейсер из цемента, насыщенного антибиотиками. На ранних этапах выполнения работы использовали премоделированный спейсер промышленного производства «Tecres», который изготовлен из цемента, официнально насыщенного гентамицином (рисунок 1г). Подобный спейсер установлен нами в 12 случаях (23,5%). Однако, ограниченность спектра антибактериального действия гентамицина, а также сложность адаптации стандартных размеров спейсера к индивидуальной анатомии нативного тазобедренного сустава при септическом коксите привели к необходимости выработки технологии индивидуального изготовления цементного артикулирующего спейсера из метилметакрилового цемента интраоперационно (рисунки 2б и 2в). Такие цементные спейсеры, изготовленные во время операции, использованы нами в 39 наблюдениях (76,5%). Индивидуальное изготовление спейсера на операции для случаев септического коксита осуществляли в два этапа, обычно используя две дозы цемента. Ножка такого спейсера с установленной внутри нее арматурой отливалась из цемента высокой вязкости в универсальной форме. Наш опыт показал, что для большинства случаев коксита (в отличие от случаев перипротезной инфекции) паз в канале бедренной кости для ножки спейсера может быть сформирован одним рашпилем выбранного (малого) размера, а для формирования ножки спейсера использована универсальная отливочная силиконовая форма. Головку спейсера отливали в серии полушаровидных силиконовых форм с разницей в диаметре в 2 мм (от 46 мм до 62 мм). Это давало возможность получить размер головки спейсера, соответствующий размеру удаленной головки бедра при ее относительной сохранности (или размеру полушаровидной фрезы, хорошо адаптирующейся в ацетабулярной ямке при ее обработке (рисунок 2б). Для улучшения качества элюирования цемента создана полезная модель цементного спейсера с двуслойной головкой, где антибактериальным препаратом насыщали только поверхностный слой цемента [32].
Как видно из таблицы 3, в большем количестве случаев [34] был использован цементный спейсер, сформированный хирургом в операционной.
Премоделированный спейсер «Tecres» из цемента с гентамицином применялся более ограниченно и, как указывалось, на ранних этапах работы, в основном в группе пациентов, интактных по ВИЧ инфекции. Более широкое применение спейсеров, изготовленных хирургом интраоперационно, было обусловлено их преимуществом, изложенным выше.
Следует отметить, что большее количество «самодельных» спейсеров в группе ВИЧ инфицированных больных давало возможность использования большего спектра антибиотиков в цементе и применения более анатомичных размеров.
Таблица 3
Характер установленного цементного спейсера в группе больных, интактных по ВИЧ инфекции и в группе ВИЧ инфицированных
|
Группы больных |
Характер установленного спейсера. (n -51) |
||
|
Премодели-рованный «Tecres» |
Сделанный в операционной с отливкой 2-х цементных модулей |
||
|
– с гомогенной головкой |
– с двуслойной головкой² |
||
|
Группа 1 |
11 |
28 |
2 |
|
Группа 2 |
1 |
6 |
3 |
|
Итого: |
12 |
34 |
5 |
|
Итого: |
12 |
39 |
|
Как видно из таблицы 3, премоделированные спейсеры промышленного производства с гентамицином использовались преимущественно с в группе пациентов без ВИЧ инфекции, что объясняется тем фактом, что набор клинического материала по ВИЧ инфекции начал осуществляться несколько позже, после того как были оценены негативные качества премоделированных спейсеров и возникла необходимость к отказу от их применения.
Таблица 4
Распределение пациентов общей когорты по возрасту и полу
|
Антибиотики |
Группы больных |
|
|
Группа 1 |
Группа 2 |
|
|
Гентамицин |
31 |
4 |
|
Ванкомицин |
2 |
1 |
|
Клиндамицин |
- |
1 |
|
Фторхинолоны |
2 |
1 |
|
Цефтриаксон |
- |
1 |
|
Амикацин |
2 |
- |
|
Линезолид |
4 |
1 |
|
Азитромицин |
- |
1 |
|
ИТОГО: |
41 |
10 |
В структуре применения антибактериальных препаратов для насыщения костного цемента в группе больных интактных по ВИЧ инфекции использование гентамицина почти в два раза превышало данные по группе с ВИЧ инфекцией, что, как уже упоминалось, связано с большим применением в группе 1 премоделированных спейсеров промышленного производства из цемента, насыщенного гентамицином.
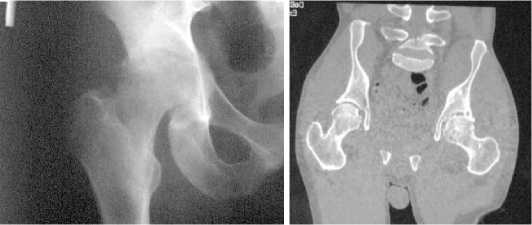
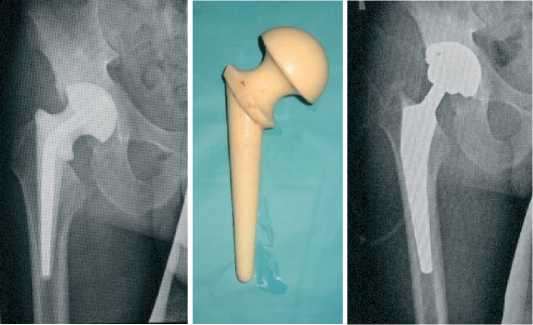
Приводим клинический пример случая двухэтапного хирургического лечения септического коксита с использованием премоделированного цементного спейсера (промышленного производства) из цемента, насыщенного гентамицином (рисунок 1).
б
а
в г д
Рисунок 1 . Случай двухэтапного эндопротезирования тазобедренного сустава у пациента 40 лет, с деструктивной формой правостороннего септического коксита с применением премоделированного цементного спейсера с генатмицином: а - рентгенограмма пораженного сустава; б – компьютерная томография сустава; в - рентгенограмма тазобедренного сустава после установки спейсера на первом этапе хирургического лечения; г -внешний вид премоделированного цементного спейсера тазобедренного сустава (после удаления); д - рентгенограмма тазобедренного сустава с установленным эндопротезом на втором этапе хирургического лечения
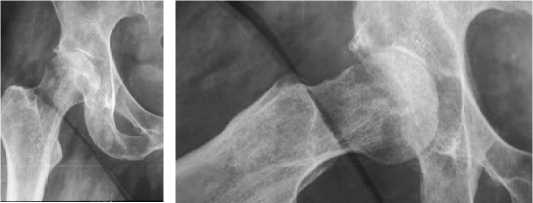
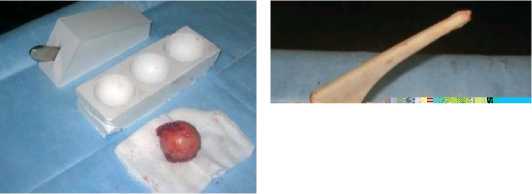
В качестве альтернативного варианта приводим пример случая двухэтапного эндопротезирования тазобедренного сустава при септическом стафилококковом коксите с использованием цементного спейсера, изготовленного интраоперационно с отливанием его компонентов в силиконовых формах.
а
б в
г д е
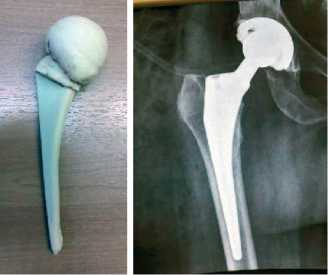
Рисунок 2 . Случай двухэтапного эндопротезирования тазобедренного сустава у больной М, 46 лет с деструктивной формой правостороннего септического коксита с использованием интраоперационно изготовленного спейсера: а – рентгенограммы больной перед операцией;
б - интраоперационное двухэтапное формирование анатомически адаптированного артикулирующего цементного спейсера в силиконовых формочках на 1-ом этапе хирургического лечения; в - рентгенограммы тазобедренного сустава с установленным спейсером; г - внешний вид удаленного цементного спейсера на 2-м этапе хирургического лечения; д - рентгенограммы тазобедренного сустава с установленным эндопротезом.
У 7 пациентов на фоне протекания септического коксита были отмечено формирование значительных анатомических изменений тазовой кости в области вертлужной впадины, в частности, – недостаточность верхнего края вертлужной впадины, что не позволяло устойчиво имплантировать головку цементного спейсера. В таких случаях на 1-м этапе хирургического лечения была осуществлена установка спейсера с созданием цементного надацетабулярного навеса по запантентованной методике (рисунок 3) [33].
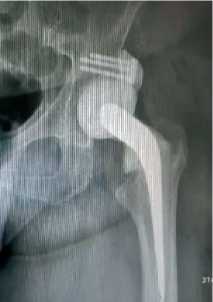
Рисунок 3 . Спейсер с армированным навесом у пациента с кокситом и дефектом тела подвздошной кости
Результаты
В подавляющем большинстве случаев 45 (88,2 %) у пациентов удалось выполнить оба этапа хирургического лечения и установить эндопротез. В двух случаях 2-й этап лечения с установкой эндопротеза не был выполнен в связи с неявкой пациентов на дальнейшее обследование. В 4-х наблюдениях как первичная установка спейсера, так и его замена не привели к купированию инфекции. Этим больным выполнена операция по-Girdlestone с удалением повторно установленного спейсера, и попытки дальнейшего хирургического лечения не предпринимались. В этих случаях был достигнут только санирующий эффект. Дальнейшая реабилитация осуществлялась с целью создания подвздошно-бедренного неоартроза и формирования частичной опороспособности нижней конечности при компенсации возникшего укорочения с помощью ортопедической обуви.
Сроки между этапами хирургического лечения оценивали отдельно в каждой из групп и только у 45 пациентов, которым были выполнены оба этапа хирургического лечения. Средние сроки между этапами хирургического лечения в группе 1 составили: 5,2±2,9 мес.; в группе 2 – 6,9±2,7 мес.
Полученные в ходе хирургического лечения осложнения имели место в обеих группах, что отражено в таблице 5.
Таблица 5
Осложнения при двухэтапом эндопротезировании при септическом коксите в группе больных, интактных по ВИЧ инфекции и в группе ВИЧ инфицированных
|
Характер осложнений на этапах хирургического лечения |
Группа 1 41 случай |
Группа 2 10 случаев |
|
Глубокая инфекция, в т.ч. при повторной установке, приведшая к полному удалению имплантата (1-й этап) |
2 |
2 |
|
Нестабильность головки установленного спейсера (1-й этап) |
5 |
- |
Окончание Таблицы 5
|
Характер осложнений на этапах хирургического лечения |
Группа 1 41 случай |
Группа 2 10 случаев |
|
Поломка металлической арматуры спейсера (1-й этап) |
2 |
- |
|
Глубокая инфекция после установки эндопротеза (2-й этап) |
2 |
5 |
|
Неявка больного для выполнения 2-го этапа хирургического лечения |
1 |
1 |
|
Всего (% к общему количеству): |
13 (31,7%) |
9 (90%) |
– двое пациентов (по одному в каждой группе) не явились для второго этапа лечения и были включены в статистику как «осложнения».
В 6 случаях у больных 1-й группы и в одном случае во 2-й группе на первом этапе хирургического лечения была выполнена дополнительная операция по замене или укреплению установленного цементного спейсера связи асептическим расшатыванием или вывихом головки. В двух случаях усталостного перелома металлической арматуры спейсера в сроки от 2 до 3 месяцев после установки последний был удален и установлен эндопротез.
Положительным результатом проведенного хирургического лечения считали выполнение двух этапов хирургического при соответствии двум основным критериям:
– отсутствие инфекции установленного эндопротеза (достижение санирующего эффекта);
– восстановление опороспособности оперированной конечности и функции ходьбы.
Таким образом, в группе 1-й группе у ВИЧ (-) больных, положительные результаты получены в 34 (82,9%) из 41 случая.
Во 2-й группе, у ВИЧ (+) пациентов – положительные результаты получены только в 4-х (40%) из 10 случаев.
Функциональные результаты по системе HHS подсчитывали в отдельных группах только у пациентов, которым выполнены оба этапа хирургического лечения и удалось установить эндопротез, включая случаи с инфекционными осложнениями, где эндопротез в итоге был удален.
Таким образом, функциональная оценка в баллах по системе ННS в первой группе больных (n = 37) дала существенное улучшение средних показателей: с 39,1±10,7 (до начала хирургического лечения) до 89,8±11,2 (после получения окончательного результата). Подобная оценка во 2-й группе у больных с ВИЧ инфекцией (n=8) дала следующие данные: 38,3±6,7 (до хирургического лечения) и 51±7,8 (после оценки окончательного результата). Как видно из полученных данных, в группе ВИЧ инфицированных пациентов показатели функционального восстановления были значительно ниже, чем в группе больных, интактных по ВИЧ, что явилось следствием относительно большего количества инфекционных осложнений, возникших у больных с ВИЧ инфекцией.
Отдаленные результаты в сроки от 1 года до 12 лет прослежены только у пациентов, имевших положительные результаты лечения: это – 34 случая в первой группе и 4 случая во второй группе. Средние сроки наблюдения больных в 1-й группе составили 7,5 ±3,2 года. Один из пациентов этой группы умер через 4 года после завершения лечения от причин, не связанных с основным заболеванием. В 2-х случаях пациенты 1-й группы были оперированы повторно в отдаленные сроки (8 и 9 лет) после установки эндопротеза в связи с развившейся асептической нестабильностью одного из компонентов. Им обоим успешно выполнена ревизионная операция, рецидива инфекции не выявлено.
Во 2-й группе отдаленные результаты прослежены у 4-х пациентов с установленным эндопротезом в сроки от 1 до 3-х лет, еще в одном наблюдении отмечен рецидив перипротезной инфекции через 6 месяцев после второго этапа ревизионного эндопротезирования.
Обсуждение
Следует отметить, что в литературе, преимущественно зарубежной, авторами достаточно четко разделяются такие патологические состояния как «перипротезная инфекция» и «септический артрит». Так в иностранной литературе укоренились устойчивые аббревиатуры для этих понятий «Prosthetic Joint Infection ( PJI) и «Septic Arthritis (SA) [30]. Нам не удалось найти ни одной публикации, в которых был бы представлен обобщенный анализ двух указанных видов патологии. А там, где «перипротезная инфекция» и «септический артрит» рассматриваются в одной статье, авторы представляют и анализируют их раздельно, что, с нашей точки зрения, дает весомые основания считать их различными нозологическими формами.
Анализ современной литературы, включая существующие обзоры [31], дополненные отечественными данными, позволил определить круг авторов, занимающихся проблемой двухэтапного эндопротезирования тазобедренного сустава при септическом коксите и географию этих исследований (Таблица 6).
Таблица 6
Авторские коллективы и география работ, посвященных двухэтапному эндопротезированию тазобедренного сустава при септическом коксите
|
Авторы |
Год |
Страна |
Количество наблюдений |
|
Chen C.E. и соавт. [10] |
2008 |
Китай |
28 |
|
Diwanji S.R. и соавт. [22] |
2008 |
Южная Корея |
9 |
|
Huang T.W. и соавт. [15] |
2009 |
Тайвань |
15 |
Окончание Таблицы 6
|
Авторы |
Год |
Страна |
Количе ство наблюдений |
|
Kelm J. и соавт. [23] |
2009 |
Германия |
8 |
|
Bauer T. и соавт. [16] |
2010 |
Франция |
13 |
|
Fleck E.E. и соавт. [17] |
2011 |
США |
14 |
|
Romanò C.L. и соавт. [11] |
2011 |
Италия |
20 |
|
Shen H. и соавт. [24] |
2013 |
Китай |
5 |
|
Anagnostakos K. и соавт. [12] |
2016 |
Германия |
23 |
|
Papanna M. C. и соавт. [18] |
2018 |
Великобритания |
11 |
|
Зубиков В.С. и соавт. [13] |
2019 |
Россия |
28 |
|
Li W. и соавт. [19] |
2019 |
Китай |
14 |
|
Xu C. и соавт. [8] |
2019 |
Китай |
55 |
|
Николаев Н.С. и соавт. [20] |
2020 |
Россия |
15 |
|
Kunze K.N. и соавт. [21] |
2020 |
США |
12 |
|
Russo A. и соавт. [14] |
2021 |
Италия |
25 |
|
Russo A. и соавт. [9] |
2024 |
Италия |
61 |
В отличие от собственных наблюдений анализ литературы показывает, что у ряда авторов значительную долю в причинах развития септического коксита составили предшествующие операции на тазобедренном суставе, такие как остеосинтез при переломах костей в области сустава [31], а у некоторых авторов это явилось основной причиной заболевания [8].
Что касается эффективности применения метода двухэтапного эндопротезирования, которые у авторов колеблется в пределах от 100 % до 85 %, то данный показатель зависит от количества и сроков клинических наблюдений. При малых количествах наблюдений и ограниченных сроках авторами приводятся лучшие результаты.
Наши данные двухэтапного эндопротезирования у больных с септическим кокситом при отсутствии ВИЧ инфекции близки к данным, представленным другими авторами. Однако, у больных с ВИЧ инфекцией процент положительных результатов значительно ниже. Полученные данные по ВИЧ инфекции мы не смогли сравнить с данными других авторов, так как. не нашли подобной информации в доступных источниках литературы.
Ограниченное количество наблюдений по двухэтапному эндопротезированию у больных с ВИЧ инфекцией не позволяют с доказательной достоверностью сравнить их результаты с результатами больных без ВИЧ инфекции. Однако, полученные нами предварительные данные могут свидетельствовать о возможности ухудшения результатов двухэтапного эндопротезирования при септическом коксите на фоне ВИЧ инфекции, чем при ее отсутствии. Это согласуется с данными некоторых авторов в отношении как первичного, так и ревизионного эндопротезирования тазобедренного сустава у ВИЧ инфицированных больных [28, 29].
Заключение
Результаты двухэтапного эндопротезирования тазобедренного сустава у больных с септическим кокситом подтверждают возможность получения положительных результатов у подавляющего большинства оперированных больных. Наличие у пациентов сопутствующей ВИЧ инфекции способно ухудшить результат лечения в связи с более частым возникновением инфекционных осложнений как на первом этапе хирургического лечения после установки артикулирующего цементного спейсера, так и на втором этапе после установки эндопротеза, что приводило к необходимости удаления установленного имплантата.


