Влияние вируса скручивания листьев винограда на эндогенную ан-тиоксидантную систему растений Vitis vinifera L., выращенных в полевых условиях
Автор: Султанова Н.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Фитопатология
Статья в выпуске: 1 т.61, 2026 года.
Бесплатный доступ
Вирусные инфекции оказывают выраженное негативное влияние на рост, развитие и продуктивность сельскохозяйственных культур, вызывая значительные потери урожая во всем мире. Одним из ключевых механизмов повреждающего действия вирусов служит индукция окислительного стресса, сопровождающегося избыточным накоплением активных форм кислорода (АФК) в растительных клетках. Для поддержания клеточного гомеостаза растения используют сложную антиоксидантную систему, включающую как ферментативные компоненты (каталаза, аскорбатпероксидаза и др.), так и неферментативные низкомолекулярные метаболиты — аскорбат, глутатион и токоферолы, формирующие взаимосвязанную аскорбат—глутатион—токофе-рольную систему защиты. Вирус скручивания листьев винограда GLRaV-3 относится к роду Ampelovirus (семейство Closteroviridae), это один из наиболее распространенных и экономически значимых патогенов виноградной лозы. Инфекция сопровождается характерными симптомами, включая покраснение или пожелтение листьев, их скручивание и снижение накопления сахара в ягодах, что в конечном итоге отражается на качестве и объеме урожая. В настоящей работе впервые установлено, что инфицирование вирусом GLRaV-3 приводит к скоординированной перестройке аскорбат—глутатион—токоферольной системы растений винограда, сопровождающейся достоверными изменениями содержания аскорбата, глутатиона и токоферолов и усилением активности ключевых антиоксидантных ферментов (каталазы и аскорбатпероксидазы). Показано, что повышение содержания компонентов триады аскорбат—глутатион—токоферол тесно коррелирует с интенсивностью вирусной нагрузки и степенью липидной пероксидации (содержание малонового диальдегида, МДА), что свидетельствует об их участии в регуляции клеточного редокс-гомеостаза при вирусном стрессе. Скоординированное функционирование этой триады сопровождается усилением антиоксидантной защиты и, по-видимому, может быть связано с метаболической перестройкой клеток, включая процессы, ассоциированные с биосинтезом вторичных метаболитов. Целью исследования было комплексное изучение антиоксидантного потенциала триады аскорбат—глутатион—токоферол для оценки ее роли в формировании устойчивости растений винограда к вирусу скручивания листьев серотипа 3 (GLRaV-3). В 2022-2023 годах были проведены обследования для выявления симптомов болезни скручивания листьев винограда (grapevine leafroll disease, GLD) в основных регионах Азербайджана (Шамахы, Исмаиллы и Сальян), где выращивается виноград. Образцы собирали с растений белого винограда сорта Баянширэ и красных сортов Мэдрэса и Кара Шаны. Контролем служили здоровые и полностью свободные от вирусов листья растений. Образцы были проанализированы на наличие вируса скручивания листьев винограда серотипа 3 (GLRaV-3) с использованием трех диагностических методов: быстрого одноэтапного иммунохроматографического анализа AgriStrip, иммуноферментного анализа DAS-ELISA (двойной сэндвич-метод) и метода обратной транскрипции с последующей полимеразной цепной реакцией (ОТ-ПЦР). Содержание токоферолов в образцах определяли спектрофотометрически с помощью реакции Эммери‑Энгеля, содержание восстановленного глутатиона — в реакции с 5,5´-дитиoбис-2-нитробензойной кислотой. Интенсивность процессов перекисного окисления липидов в растениях оценивали с пересчетом на содержание МДА в здоровых и инфицированных образцах листьев. Количество МДА определяли спектрофотометрическим методом, основанным на реакции с тиобарбитуровой кислотой. Также оценивали концентрацию аскорбиновой кислоты (АК). Активность фермента аскорбатпероксидазы АПО определяли посредством регистрации снижения оптической плотности за счет окисления аскорбиновой кислоты при l = 290 нм. Активность фермента каталазы (КАТ) определяли при l = 240 нм, измерения проводили на основе скорости разложения H2O2 за 1 мин. По результатам исследований вирусоподобные симптомы были выявлены на красных и белых сортах, а ОТ-ПЦР подтвердила наличие инфекции в 21 из 52 образцов (40,3 %). Наибольшая распространенность заболевания отмечена в регионе Сальян (32 %), меньшая — в Исмаиллы (28 %) и Шамахы (16 %), что свидетельствует о региональных особенностях циркуляции вируса. Биохимический анализ показал прямую зависимость между вирусной нагрузкой и выраженностью окислительного стресса у сорта Кара Шаны. Содержание МДА достоверно (p < 0,05) увеличивалось во всех инфицированных вариантах (6,5-7,9 мкмоль•г-1 сырой массы) по сравнению с контролем (2,27 мкмоль•г-1 сырой массы), что указывает на повреждение мембран. Одновременно наблюдалась активация антиоксидантной системы: активность аскорбатпероксидазы и каталазы возрастала соответственно в 1,5-2,2 и 1,6-2,0 раза (p < 0,05). Содержание восстановленного глутатиона увеличивалось в 1,6-2,4 раза, аскорбиновой кислоты и токоферолов — также возрастало, достигая максимальных значений при средней и высокой вирусной нагрузке.
Виноградная лоза, вирусы, метаболиты, антиоксидантные ферменты
Короткий адрес: https://sciup.org/142247339
IDR: 142247339 | УДК: 634.8:632.3:578 | DOI: 10.15389/agrobiology.2026.1.189rus
Influence of grapevine leafroll-associated virus 3 on the endogenous an-tioxidant system of field-grown Vitis vinifera L. plants
Viral infections exert a pronounced negative impact on the growth, development, and productivity of crops, causing significant yield losses worldwide. One of the key mechanisms underlying the damaging effects of viruses is the induction of oxidative stress, accompanied by excessive accumulation of reactive oxygen species (ROS) in plant cells. To maintain cellular homeostasis, plants utilize a complex antioxidant system that includes both enzymatic components (catalase, ascorbate peroxidase, etc.) and non-enzymatic low-molecular-weight metabolites ascorbate, glutathione, and tocopherols, forming an interconnected ascorbate—glutathione—tocopherol defense system. Grapevine leafroll-associated virus 3 (GLRaV-3) belongs to the genus Ampelovirus (family Closteroviridae) and is one of the most widespread and economically significant pathogens of grapevine. The infection is accompanied by characteristic symptoms, including reddening or yellowing of leaves, leaf rolling, and reduced sugar accumulation in berries, which ultimately affects both the quality and quantity of yield. In the present study, it was established for the first time that GLRaV-3 infection leads to a coordinated restructuring of the ascorbate—glutathione—tocopherol system in grapevine plants, accompanied by significant changes in the content of ascorbate, glutathione, and tocopherols, as well as enhanced activity of key antioxidant enzymes (catalase and ascorbate peroxidase). It was demonstrated that the increase in the components of the ascorbate—glutathione—tocopherol triad closely correlates with viral load intensity and the degree of lipid peroxidation (malondialdehyde, MDA content), indicating their involvement in the regulation of cellular redox homeostasis under viral stress. The coordinated functioning of this triad is accompanied by enhanced antioxidant protection and appears to be associated with metabolic reprogramming of cells, including processes related to secondary metabolite biosynthesis. The aim of the study was a comprehensive evaluation of the antioxidant potential of the ascorbate–glutathione–tocopherol triad to assess its role in the formation of grapevine resistance to GLRaV-3. During 2022-2023, surveys were conducted to identify symptoms of grapevine leafroll disease in the main grape-growing regions of Azerbaijan (Shamakhi, Ismayilli, and Salyan). Samples were collected from white grape cultivar Bayan Shire and red cultivars Madrasa and Kara Shany. Healthy, virus-free leaves served as controls. Samples were analyzed for the presence of GLRaV-3 using three diagnostic methods, the AgriStrip rapid immunochromatographic assay, double-antibody sandwich ELISA (DAS-ELISA), and reverse transcription followed by polymerase chain reaction (RT-PCR). Tocopherol content in the samples was determined spectrophotometrically based on the Emmerie-Engel reaction. Reduced glutathione content was measured using the reaction with 5,5′-dithiobis-2-nitrobenzoic acid at λ = 412 nm. The intensity of lipid peroxidation processes was assessed by calculating malondialdehyde (MDA) content in healthy and infected leaf samples. MDA content was determined spectrophotometrically using the thiobarbituric acid reaction. The concentration of ascorbic acid (AA) was also evaluated. Ascorbate peroxidase (APX) activity was determined by recording the decrease in optical density due to ascorbic acid oxidation at λ = 290 nm. Catalase (CAT) activity was determined at λ = 240 nm based on the rate of H₂O₂ decomposition over 1 minute. According to the results, virus-like symptoms were detected in both red and white cultivars, and RT-PCR confirmed infection in 21 out of 52 samples (40.3 %). The highest disease prevalence was observed in the Salyan region (32 %), followed by Ismayilli (28 %) and Shamakhi (16 %), indicating regional features of viral circulation. Biochemical analysis of the Kara Shany cultivar demonstrated a direct relationship between viral load and the severity of oxidative stress. MDA content increased significantly (p < 0.05) in all infected variants (6.5-7.9 µmolłg-1 fresh weight) compared to the control (2.27 µmolłg⁻1 fresh weight), indicating membrane damage. Simultaneously, activation of the antioxidant system was observed: ascorbate peroxidase and catalase activities increased 1.5-2.2 and 1.6-2.0 times, respectively (p < 0.05). Reduced glutathione content increased 1.6-2.4 times while ascorbic acid and tocopherol contents also increased, reaching maximum values under moderate and high viral load. The obtained data indicate that GLRaV-3 induces pronounced oxidative stress accompanied by activation of both enzymatic and non-enzymatic components of antioxidant defense. The increase in MDA levels alongside the enhanced antioxidant response suggests partial compensation of cellular damage and reflects specific features of the host–pathogen interaction.
Текст научной статьи Влияние вируса скручивания листьев винограда на эндогенную ан-тиоксидантную систему растений Vitis vinifera L., выращенных в полевых условиях
Растения, как и все живые организмы, сталкиваются с рядом биотических стрессов, вызываемых различными патогенами, такими как вирусы, грибы, бактерии, нематоды и насекомые (1). Вирусы, в частности, изменяют метаболические пути хозяина и приводят к значительному снижению урожайности и качества продукции. Тяжесть этих негативных последствий, однако, варьирует в зависимости от конкретного сочетания вирус-хозяин, вирулентности вируса, восприимчивости сорта и возраста растения на момент заражения. В настоящее время существует значительный объем информации о взаимодействии растений и вирусов, а также о влиянии вирусных инфекций на жизненный цикл однолетних растений. Многолетние растения, в отличие от однолетних, имеют большую продолжительность жизни, и вирусы сохраняются в них на протяжении всего существования. В результате динамика взаимодействий между хозяевами и вирусами у многолетних растений может быть сложной, на нее влияют различные факторы окружающей среды и сигналы развития в течение последующих сезонов, в отличие от относительно простых сценариев, наблюдаемых у однолетних растений (2).
Вирусные заболевания уже давно угрожают устойчивому получению продукции виноградной лозы. В частности, болезнь скручивания виноградной лозы (grapevine leafroll disease, GLD) вызывают экономически важные вирусы GLRaVs семейства Closteroviridae . Характерные симптомы поражения на листьях — обесцвечивание красного межжилкового пространства, скручивание, снижение выработки хлорофилла (3). GLRaV-3 ( Grapevine leafroll-associated virus 3 ) принадлежит к роду Ampelovirus и признан преобладающим возбудителем в группе GLRaV. Передача GLRaV-3 может происходить через мягкочешуйчатых насекомых (Homoptera: Coccidae ) или мучнистых червецов (Homoptera: Pseudococcidae ), а также через прививку (4).
Проявление симптомов GLD зависит от различных факторов, таких как сезон, сорт винограда и климатические условия в регионе выращивания. Кроме того, часть видов виноградной лозы могут вообще не проявлять симптомов, в том числе некоторые подвои и определенные белые сорта Vitis vinifera L.
Первые симптомы обычно возникают в начале-середине лета и сохраняются до поздней осени, постепенно усиливаясь с течением времени. Помимо визуальных проблем, GLD может серьезно влиять на урожайность и качество винограда, что подчеркивает необходимость комплексных стратегий управления виноградниками для смягчения экономических последствий (5).
Первичный вирусный стресс вызывает в растениях чрезмерное производство активных форм кислорода (АФК), таких как супероксид (O 2 - ), перекись водорода (H 2 O 2 ), гидроксильные радикалы COH) и синглетный кислород ( 1 O 2 ), после чего запускает сложные клеточные реакции, часто приводящие к нарушению нормальных клеточных функций, стимулируя 190
активацию защитных механизмов в ответ на эту инвазию в рамках своей защитной стратегии (6). Хрупкий баланс между АФК и клеточными антиоксидантами может быть нарушен во время вирусного стресса, что приводит к окислительному стрессу и потенциальному повреждению клеточных структур. Взаимодействие между вирусной инфекцией и передачей сигналов АФК представляет собой сложный и динамичный процесс, влияющий на способность хозяина вырабатывать эффективный противовирусный ответ при сохранении клеточной целостности (7, 8). Понимание этих взаимодействий имеет перспективы для разработки инновационных подходов к лечению заболеваний, которые нацелены на пути вирусного стресса и смягчают пагубные последствия окислительного стресса во время развития инфекций.
АФК обладают высокой реакционной способностью и токсичностью к белкам и углеводам клеточных компонентов, мембранным липидам и нуклеиновым кислотам, вызывая окислительный стресс. Растения развили сложную антиоксидантную систему для смягчения и устранения повреждений, вызванных АФК. Кроме того, вирусный стресс известен своей способностью изменять многочисленные биохимические и физиологические процессы, начиная от фотосинтеза и заканчивая синтезом белка и накоплением растворенных веществ. Чрезмерная продукция АФК вызывает окисление белков и перекисное окисление липидов при различных стрессовых факторах, включая биотический стресс (9, 10).
Ранее мы показали, что неблагоприятные последствия вирусного стресса приводят к значительному снижению содержания зеленых пигментов, таких как хлорофиллы (a, b и общий), постепенному уменьшению количества каротиноидов, а также снижению относительного содержания воды (RWC) и увеличению количества перекиси водорода во всех инфицированных листьях (11).
Существует много информации о влиянии вирусной инфекции на физиологические процессы растений, тем не менее, исследований об антиоксидантном потенциале триады аскорбат—глутатион—токоферол в повышении толерантности растений к вирусу в условиях вирусного стресса недостаточно. Аналогичные исследования проводятся во всем мире для изучения антиоксидантного потенциала триады аскорбат—глутатион—токоферол в повышении устойчивости растений преимущественно к грибным и бактериальным патогенам, а также к абиотическим стрессам (12, 13).
Триада аскорбат—глутатион—токоферол работает синергетически, обеспечивая комплексную защиту клеток от окислительного стресса: аскорбат регенерирует токоферол из его окисленной формы, глутатион восстанавливает окисленный аскорбат, а токоферол защищает липидные компоненты клеточных мембран (14-16). Комплексное применение этих антиоксидантов позволяет значительно повысить устойчивость виноградных растений к вирусным инфекциям, в том числе к GLRaV-3 — одному из самых распространенных вирусов, поражающих виноградники.
В настоящей работе впервые установлено, что инфекция, вызванная GLRaV-3, приводит к скоординированной перестройке аскорбат—глу-татион—токоферольной системы растений винограда, сопровождающейся достоверными изменениями содержания аскорбата, глутатиона и токоферолов и усилением активности ключевых антиоксидантных ферментов (каталазы и аскорбатпероксидазы). Показано, что повышение содержания компонентов триады аскорбат—глутатион—токоферол тесно коррелирует с интенсивностью вирусной нагрузки и степенью липидной пероксидации
(содержание МДА), что свидетельствует об их участии в регуляции клеточного редокс-гомеостаза при вирусном стрессе. Скоординированное функционирование этой триады сопровождается усилением антиоксидантной защиты и, по-видимому, может быть связано с метаболической перестройкой клеток, включая процессы, ассоциированные с биосинтезом вторичных метаболитов.
Целью исследования было комплексное изучение антиоксидантного потенциала триады аскорбат—глутатион—токоферол для оценки ее роли в формировании устойчивости растений винограда к вирусу скручивания листьев серотипа 3 (GLRaV-3).
Методика. В 2022-2023 годах были проведены обследования для выявления симптомов GLD в основных регионах Азербайджана (Шамахы, Исмаиллы и Сальян), где выращивается виноград. Образцы собирали с растений белого винограда сорта Баянширэ и красных сортов Мэдрэса и Кара Шаны. В процессе мониторинга методом визуальной диагностики было выявлено 52 растения с характерными симптомами поражения кло-стеровирусами. Собранные для исследования образцы листьев были транспортированы и хранились при температуре 4 ° C до дальнейшей обработки. Контролем служили здоровые и полностью свободные от вирусов листья растений.
Образцы были проанализированы на наличие вируса скручивания листьев винограда серотипа 3 (GLRaV-3) с использованием трех диагностических методов: быстрого одноэтапного иммунохроматографического анализа AgriStrip, иммуноферментного анализа DAS-ELISA (двойной сэндвич-метод) и метода обратной транскрипции с последующей полимеразной цепной реакцией (ОТ-ПЦР).
AgriStrip («Bioreba AG», Швейцария) — иммунохроматографическая тест-полоска, которая представляет собой узкую пленочную мембрану с несколькими функциональными зонами, обычно нанесенными на нитроцеллюлозную поверхность. При контакте образца с полоской раствор мигрировал по мембране за счет капиллярного эффекта, последовательно взаимодействуя с различными зонами реагентов: сначала с конъюгатной подушечкой, содержащей меченые антитела, а затем с мембраной, на которой иммобилизованы тестовая (захватная) и контрольная линии. При наличии в образце целевого антигена формировались иммунные комплексы, которые фиксировались на тестовой линии, создавая визуально различимую цветовую полосу, в то время как контрольная линия подтверждала корректность проведения теста. Окрашивание достигало высокой интенсивности в течение 10-20 мин, после чего результаты регистрировали.
Наличие GLRaV-3 в собранных образцах виноградной лозы также определяли методом DAS-ELIS в соответствии с опубликованной ранее методологией (18, 19) и рекомендациями, предоставленными производителем антисывороток («Bioreba AG», Швейцария). Ферментативная реакция, происходящая на планшете ИФА, сначала оценивалась по изменению цвета. Поглощение при X = 405 нм измеряли более двух раз с помощью считывателя ELISA, Stat Fax Microplate («Awareness Technology, Inc.», США).
Суммарную РНК очищали из 200 мг тканей листа с помощью реагента TRIzol™ («Invitrogen», США) и хранили при - 80 ° С. Количественную оценку выхода и качества общей РНК проводили с помощью спектрофотометра NanoDrop™ («Thermo Fisher Scientific», США) посредством измерения оптической плотности при длинах волн X = 260 нм (A 260 ) и X = 280 нм (A 280 ) и расчета соотношений A 260 /A 280 , а также A 260 /A 230 , что позво-192
лило оценить степень чистоты и отсутствие белковых и органических примесей в образцах перед проведением последующих молекулярных анализов.
Для анализа использовали вирус-специфические праймеры LR3 -9445c (5'-CTACTTCTTTTGCAATAGTT-3') и LR3 -8504v (5 '-ATGGCATTTGAA-CTGAAATT-3') для консервативной области генома GLRaV -3, как описа но ранее (19).
Размер ампликона составлял примерно 942 п.н. ОТ-ПЦР выполняли в два этапа. Для синтеза комплементарной цепи (кДНК) 2 мкл выделенной РНК подвергали обратной транскрипции в общем объеме 20 мкл с использованием 2 мкл буфера RT 10* (0,5 моль/л Tris -HCl, 0,7 моль /л KCl, 0,1 моль/л MgCl 2 , pH 8), 1 мкл DTT (100 мМ), 1 мкл dNTPs (10 мМ), 0,5 мкл ингибитора RNase (10 мМ), 2 мкл обратного праймера (100 пмоль/мкл) и 0,5 мкл M -M uLV обратной транскриптазы (200 Ед/мкл). Р еакцию проводили при 47 ° C в течение 1 ч. Для ПЦР использовали 5 мкл полученной кДНК. Реакционная смесь для ПЦР содержала в общем объеме 20 мкл: 20 нг кДНК, 10 мМ каждого dNTP («Solis BioDyne O U », Эстония), 1,6 мМ MgCl 2 , 1 Ед. Taq - ДНК - полимеразы («Solis BioDyne O U », Эстония), 0,5 мкл каждой пары праймеров (10 пмоль/мкл) и 1* буфер ПЦР.
Амплификацию выполняли на термоциклере SimpliAmp Thermal Cycler («Applied Biosystems», США). На первом этапе осуществляли предварительную денатурацию и комплементацию кДНК при 50 ° C в течение 30 мин, после чего следовала исходная денатурация при 95 ° C в течение 3 мин. Далее проводили 35 циклов амплификации, включавших денатурацию при 95 ° C в течение 30 с, отжиг праймеров при 55 ° C в течение 30 с и удлинение при 72 ° C в течение 45 с. В завершение выполняли заключительное удлинение при 72 ° C в течение 5 мин. Продукты амплификации ПЦР анализировали методом электрофореза в 1,5 % агарозном геле с использованием 1* TBE (Tris -Borate-EDTA буфер). Для визуализации ДНК гель окрашивали бромидом этидия (EtBr), после чего полосы амплифици-рованной ДНК детектировали с помощью системы UV -Gel Doc («Uvitec , Ltd.», Великобритания) — автоматизированного устройства для визуализации и документирования агарозных гелей. В качестве маркера молекулярной массы использовали Quick - Load® Purple 2 - Log DNA Ladder («New England Biolabs», Великобритания; Cat. № N0550S/N0550L), который обеспечивает диапазон фрагментов для ориентировочной оценки размеров ДНК - продуктов при электрофорезе.
Содержание токоферолов в образцах определяли спектрофотометрическим методом на основе реакции Эммери-Энгеля; метод широко используется для количественного анализа токоферолов. Принцип этой реакции основан на восстановлении ионов железа (Fe3+) токоферолами до ионов двухвалентного железа (Fe2+), которые в присутствии 2,2'-дипиридила образуют красный комплекс, поглощающий свет при 1 ® 520 нм. Поскольку в растительных экстрактах наряду с токоферолами присутствуют и каротиноиды, предварительно измеряли поглощение при 1 = 460 нм, что отражает вклад каротиноидов; после добавления хлорида железа и 2,2'-дипиридила второе измерение при 1 = 520 нм использовали для оценки общей концентрации токоферолов с учетом коррекции на каротиноиды. Перед этим токоферолы и каротиноиды экстрагировали из гомогенизированной растительной ткани с использованием ксилола или аналогичного органического растворителя, что позволяет отделить липофильные компоненты для последующего анализа. Концентрацию токоферолов в образце рассчитывали по калибровочному графику, построенному с использованием стан- дартного раствора токоферола, с учетом разницы оптической плотности (A520 - A460) пропорционально концентрации токоферолов в пробе.
Содержание восстановленного глутатиона (ГЛУ) в образцах определяли спектрофотометрически на основе реакции с 5,5'-дитиoбис-(2-нитробензойной кислотой) (ДБНК) при X = 412 нм, что соответствует максимальному поглощению продукта восстановления ДБНК 5-тио-2-нитробензойной кислоты (ТНБК), образующегося при взаимодействии тиольной группы ГЛУ с ДБНК по классическому методу Эллмана.
Для приготовления реакционной смеси использовали набор реагентов компании «Sigma - Aldrich» (США), включающий ДБНК и ферментативные компоненты, которые обеспечивают специфическую реакцию между ГЛУ и ДБНК.
Реакционная смесь состояла из 95 мМ калий-фосфатного буфера (pH 7,0), 0,95 мМ EDTA, 0,038 мг/мл НАДФ-Н (никотинамид- в -аденин динуклеотид фосфат восстановленный), 0,031 мг/мл ДБНК и 0,115 Ед/мл глутатионредуктазы, а также 0,24 % 5 - сульфосалициловой кислоты для депротеинизации. В качестве стандарта использовали растворы восстановленного глутатиона, приготовленные в градуировочной серии в 0,4 М Tris - HCl (pH 8,5) в диапазоне концентраций 0,5-20 мкг/мл. Поглощение реакционной смеси регистрировали на спектрофотометре при X = 412 нм, а концентрацию ГЛУ в пробе рассчитывали по калибровочной кривой стандартов.
Интенсивность процессов перекисного окисления липидов в растениях оценивали с пересчетом на содержание малонового диальдегида (МДА) в здоровых и инфицированных образцах листьев. Количество МДА определяли спектрофотометрическим методом с использованием Thermo Scientific™ Evolution™ 350 UV-Vis («Thermo Fisher Scientific», США), основанным на реакции с тиобарбитуровой кислотой (TBA). Оптическую плотность измеряли при X = 532 нм и X = 600 нм, что позволяет количественно оценить образование окрашенного комплекса МДА - TBA.
В кислой среде аскорбиновая кислота (АК) восстанавливает ионы железа(Ш) до железа(П), образуя комплекс гексацианоферрата железа, что позволяет количественно определять содержание АК в растительных экстрактах. Для этого 0,5 г свежих листьев измельчали в буферном растворе, содержащем 0,1 М цитрата натрия (pH 3,69), после чего полученный гомогенат переносили в пробирки. Экстракт центрифугировали при 12500 g в течение 5 мин и собирали надосадочную жидкость. К 500 мкл надосадочной жидкости добавляли по 25 мкл 1 % раствора калиевого гексацианоферрата K 3 [Fe(CN) 6 ] и 25 мкл 2 % раствора NaFe (предварительно приготовленного), перемешивали и выдерживали при комнатной температуре в течение 5 мин. Затем к смеси добавляли 1,9 мл дистиллированной воды и 50 мкл 2 % раствора хлорида железа (III) (FeCl s ). После инкубации при комнатной температуре в течение 5 мин оптическую плотность реакционной смеси измеряли при X = 680 нм на спектрофотометре Thermo Scientific™ Evolution™ 350 UV - Vis («Thermo Fisher Scientific», США), что обеспечивает точное определение поглощения образовавшегося комплекса.
Концентрацию аскорбиновой кислоты вычисляли по формуле:
C = (K х V х X)/(m х Am х L), где C — количество аскорбиновой кислоты в 1 г влажной биомассы, мкг, K — концентрация аскорбиновой кислоты, рассчитанная по калибровочной кривой, мкг/мл, V — общий объем реакционной смеси, мл, X — коэффициент разведения, L — оптическая плотность при X = 680 нм, m — влажная масса анализируемой биомассы, г, Am — коэффициент перехода от влажной массы к сухой массе.
Для определения активности ферментов листовой материал (0,5 г) подвергали быстрому замораживанию в жидком азоте и затем гомогенизировали в 100 мМ натрий-фосфатном буфере (pH 7,8), содержащем 1 мМ EDTA, 2 мМ FMSF, 1 % ПВП и 0,1 % Triton X - 100 при 4 ° C. Полученные гомогенаты центрифугировали (Eppendorf 5810 R, «Eppendorf», Германия) при 12000 g в течение 15 мин, после чего надосадочная жидкость использовалась для анализа активности фермента аскорбатпероксидазы (АПО).
Активность АПО определяли спектрофотометрическим методом, основанным на протоколе Y. Nakano и K. Asada (20) с модификациями, регистрируя снижение оптической плотности за счет окисления аскорбиновой кислоты ( X = 290 нм, спектрофотометр Thermo Scientific™ Evolution™ 350 UV - Vis, «Thermo Fisher Scientific», США). Активность фермента рассчитывали по изменению оптической плотности с использованием коэффициента экстинкции е = 2,8 мМ - 1 •см - 1 .
Активность фермента каталазы определяли спектрофотометрически (спектрофотометр Thermo Scientific™ Evolution™ 350 UV - Vis, «Thermo Fisher Scientific», США) при X = 240 нм по скорости разложения H 2 O 2 за 1 мин. Реакционная смесь состояла из 885 мкл 50 мМ натрий - фосфатного буфера (pH 7,8), 25 мкл ферментного экстракта и 90 мкл 3 % раствора H 2 O 2 . Активность каталазы выражали в мкмоль H 2 O 2 • мг белка - 1 • мин - 1, принимая коэффициент молярного поглощения е = 39,5 мМ - 1 •см - 1 .
Статистическую обработку экспериментальных данных выполняли с использованием программы IBM SPSS Statistics (Statistics 25.0, «IBM», США). С помощью SPSS рассчитывали показатели t -статистики, соответствующие p - значения и доверительные интервалы для сравниваемых показателей между здоровыми и инфицированными группами. Эксперименты проводились в трех биологических повторностях, а результаты считали достоверными при уровне значимости p < 0,05.
Результаты. В 2022-2023 годах на красных и белых сортах винограда были зарегистрированы симптомы, подобные наблюдаемым при вирусной инфекции, включая покраснение краев листьев и черешков, снижение вегетативной активности, скручивание и пожелтение листовой пластинки (рис. 1). Среди изученных сортов белого винограда Баянширэ проявлял минимальную выраженность симптомов и наименее заметное поражение листьев, тогда как у красных сортов Мэдрэса и Кара Шаны наблюдалась более высокая интенсивность проявления симптомов и выраженность поражений листовой ткани.

Рис. 1. Типичные симптомы проявления вируса GLRaV-3 на красном сорте винограда ( Vitis vinifera L.) Кара Шаны (слева) и белом сорте Баяншира (справа) . Фотографии сделаны автором в 2023 году в рамках проведения фитосанитарного мониторинга в регионе Шамахы.
Согласно результатам DAS-ELISA, в 21 из 52 образцов была выявлена инфекция GLRaV-3. Для валидации этих результатов провели анализ методом ОТ-ПЦР с использованием праймеров, предназначенных для амплификации фрагмента гена белка оболочки (СР). Показано, что 21 из 52 образцов дали положительный результат на наличие GLRaV-3 при использовании по крайней мере одного из праймеров, специфичных для областей гена CP. Средний уровень инфицирования GLRaV-3, определенный с помощью ОТ-ПЦР, составил 40,3 %. Примечательно, что ни у одного из растений без симптомов не было обнаружено признаков GLRaV-3 ни одним из методов. Образцы, идентифицированные с помощью DAS-ELISA как положительные по GLRaV-3, также дали положительные результаты в тестах с использованием ОТ-ПЦР.
Заболеваемость вирусом составила 32 % в Сальяне (южный регион), 28 % в Исмаиллы (северный регион) и 16 % в Шамахы (северо-восточный регион). При использовании экстрактов листьев здоровых виноградных лоз амплификацию не наблюдали.
Чтобы понять взаимодействие между растениями и патогенами, а также реакцию растений на вирусные инфекции, важно установить метаболические изменения, вызванные такими инфекциями. Для биохимического анализа был выбран сорт Кара Шаны, поскольку на нем наблюдали более высокое распространение заболевания и выраженность симптомов. Всего для анализа отобрали пять инфицированных вариантов на основе полуколичественной оценки вирусной нагрузки методом DAS - ELISA (E 405 ): образцы 1 и 2 — низкий уровень (E 405 ~ 0,4-0,5), образец 3 — средний (E 405 ~ 0,7), образцы 4 и 5 — высокий (E 405 ~ 0,9-1,1).
Взаимодействие между ферментативными и неферментативными антиоксидантами играет решающую роль в поддержании баланса окислительно-восстановительных процессов в растениях. В нашем исследовании мы сосредоточились на триаде аскорбат—глутатион—токоферол, которая активно участвует в клеточной защите от окислительного стресса. Аскорбат и глутатион действуют как восстановители, нейтрализуя активные формы кислорода, в то время как токоферол служит стабилизатором мембраны, предотвращая окисление (12, 13). Эти антиоксиданты не только функционируют по отдельности, но и взаимодействуют друг с другом, усиливая защитные механизмы. Примером такого взаимодействия может быть цикл восстановления окисленных форм глутатиона и аскорбата, что способствует поддержанию целостности клеточных структур и функциональности ферментов, участвующих в антиоксидантной защите (14). Включение всех этих компонентов антиоксидантной системы в наше исследование позволило более точно оценить ее эффективность и получить представление о механизмах, лежащих в основе клеточной защиты.
Хорошо известно, что передача сигналов через АФК играет решающую роль в устойчивости растения к патогенам (21-24). При заражении вирусами активность антиоксидантных ферментов блокирует поврежденные зоны в растениях, что приводит к повышению количества фенольных соединений. Следовательно, растения развили хорошо скоординированные системы антиоксидантной защиты для управления окислительным стрессом (25).
Токоферолы, благодаря своей антиоксидантной активности, играют решающую роль в обеспечении устойчивости к биотическим и абиотическим стрессам, таким как засоление, засуха, токсичность металлов, озон и ультрафиолетовое излучение (26). Токоферолы исполняют различные функции в росте растений и физиологических процессах, влияя на общую уро- жайность (27). Они принадлежат к отдельной группе мощных антиоксидантов и играют ключевую роль в передаче сигналов и экспрессии генов.
Мы выявили заметное увеличение содержания токоферола во всех инфицированных листьях виноградной лозы (рис. 2). Содержание токоферолов (витамина Е) в инфицированных листьях варьировало от 1,14 до 1,76 мг/г сырой массы.
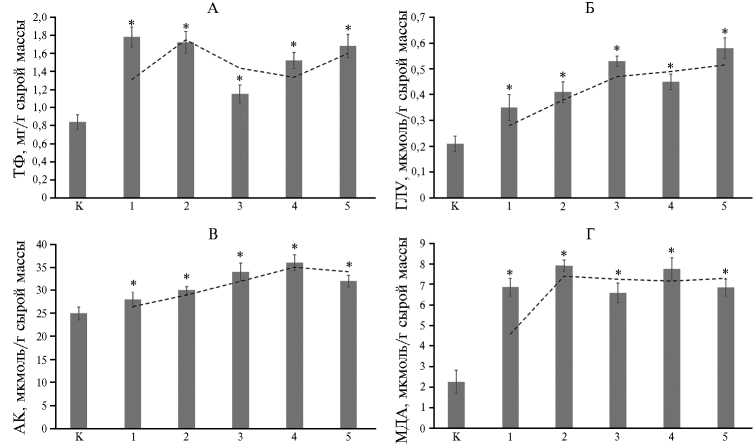
Рис. 2. Содержание токоферолов ( ТФ) (А) , восстановленного глутатиона (ГЛУ) (Б) , аскорбиновой кислоты (АК) (В) и малонового диальдегида (МДА) (Г) в здоровых (К) и инфицированных GLRaV-3 (1-5) листьях винограда ( Vitis vinifera L.) сорта Кара Шаны ( n = 3, M ±SD, Ша-махинский регион, период вегетации, 2023 год). Инфицированные варианты отобраны на основании полуквантитативной оценки вирусной нагрузки методом DAS-ELISA (E 405 ): 12 — низкий уровень, 3 — средний, 4-5 — высокий. Пунктирная линия иллюстрирует общую тенденцию изменения исследуемого параметра при возрастании степени инфекции.
* Различия с контролем статистически значимы при p < 0,001.
Аскорбиновая кислота (витамин С) играет ключевую роль в смягчении окислительного стресса, вызванного вирусными инфекциями, в первую очередь за счет нейтрализации свободных радикалов. Кроме того, АК служит как ферментным кофактором, так и регулятором сигналов в клетках, связывая синтез фитогормонов с действием различных сигнальных путей (28). Высказывается предположение, что более высокая концентрация АК у стрессоустойчивых генотипов свидетельствует о ее роли в регуляции роста, развития и адаптации растений к постоянно меняющимся факторам окружающей среды и внутренним стрессам (29-31). Аскорбиновая кислота содержится во всех компартментах клеток высших растений, однако наибольшие концентрации АК наблюдаются в хлоропластах и цитозоле клеток листьев, что отражает ее важную роль в детоксикации активных форм кислорода, продуцируемых при фотосинтезе и в других метаболических процессах.
Будучи ключевым метаболитом в растениях, АК взаимодействует с другими компонентами системы антиоксидантной защиты, такими как ас-корбат—глутатионовый цикл, чтобы защитить растения от окислительного повреждения, вызванного стрессом. В нашем эксперименте мы наблюдали увеличение количества аскорбиновой кислоты в каждом из образцов винограда, инфицированных GLRaV-3, по сравнению со здоровым листом (см. рис. 2). Установлено, что 4-й образец, характеризовавшийся высокой ви- русной нагрузкой по данным DAS-ELISA и наиболее интенсивными симптомами заболевания, содержал наибольшее количество аскорбиновой кислоты. Сравнение с другими образцами показало, что повышенное содержание АК коррелировало с интенсивностью проявления вирусного стресса, что подчеркивает ее ключевую роль в антиоксидантной защите растений и адаптивных реакциях на инфекцию GLRaV-3. Эти данные демонстрируют, что АК активно участвует в компенсации окислительного повреждения клеток при высокой степени вирусного поражения.
Глутатион (трипептидный тиол), присутствующий в различных клеточных компартментах, таких как цитозоль, эндоплазматический ретикулум, вакуоль, митохондрии, хлоропласты и пероксисомы, активно участвует в многочисленных физиологических процессах, включая гибель клеток, дифференцировку клеток, устойчивость к патогенам и ферментативную регуляцию (32-34). Эта молекула служит важнейшим антиоксидантом, играя ключевую роль в нейтрализации АФК, образующихся во время вирусной инвазии в растения. Учитывая, что восстановленный ГЛУ служит одним из наиболее важных метаболитов, противодействующих окислительному стрессу у растений, мы измерили его концентрацию в здоровых и инфицированных вирусом GLRaV-3 листьях винограда (см. рис. 2).
Мы обнаружили, что содержание ГЛУ под воздействием вируса увеличивалось примерно в 1,6 раза в образце 1, приблизительно в 2 раза в образцах 2 и 4, в 2,3 раза в образце 3 и в 2,4 раза в образце 5 (см. рис. 2). Наибольшая концентрация ГЛУ была зафиксирована в образцах 3 и 5, которые характеризовались средней и высокой вирусной нагрузкой, что соответствовало наиболее выраженным симптомам заболевания. Статистический анализ с использованием t -теста Стьюдента в программе SPSS, показал достоверное (р < 0,05) увеличение содержания ГЛУ во всех инфицированных образцах по сравнению с контролем; различия между образцами с низкой, средней и высокой вирусной нагрузкой также были статистически значимыми.
Примечательно, что как глутатион, так и аскорбиновая кислота продемонстрировали значительное увеличение количества у всех зараженных вирусом растений по сравнению со здоровыми (см. рис. 2). Это подчеркивает динамическое взаимодействие антиоксидантных молекул в ответ на вирусную инфекцию, при этом глутатион и аскорбиновая кислота играют ключевую роль в смягчении окислительного стресса у растений.
Содержание МДА используется для измерения перекисного окисления липидов в тканях растений. Этот показатель служит индикатором степени повреждения клеток, вызванного стрессом (35). В нашем исследовании содержание МДА значительно увеличивалось (примерно в 2,8-3,4 раза) в листьях виноградной лозы, инфицированных GLRaV-3, по сравнению с контрольными растениями.
Аналогичные результаты были получены на листьях, инокулированных вирусом желтой мозаики фасоли (27). Это исследование было направлено на оценку перекисного окисления липидов и общего содержания фенольных соединений в растениях бобов, пораженных вирусом желтой мозаики фасоли, а также на изучение эффективности биостимуляторов в борьбе с инфекцией. Показано, что зараженные вирусом растения испытывали повышенный стресс, о чем свидетельствовало повышение количества МДА, в то время как другие методы обработки приводили к снижению содержания МДА. Примечательно, что было обнаружено постепенное повышение накопления МДА с течением времени у инокулированных растений, причем в заметно большем количестве по сравнению с кон- трольной группой.
В ранее выполненных исследованиях изучался механизм, при котором свободные радикалы и H 2 O 2 получают электроны от молекул липидов внутри клеточной мембраны, что в конечном итоге приводит к перекисному окислению липидов (36). В сравнении с этими данными наше исследование (см. рис. 2) продемонстрировало значительное увеличение содержания МДА у всех зараженных вирусом растений, которое варьировало от 6,5 до 7,9 мкмоль т-1 сырой массы, по сравнению с контролем (2,27 мкмоль • г - 1 сырой массы).
Пероксиды, особенно перекись водорода (H 2 O 2 ), играют многогранную роль в растениях (37). Как и перекись водорода (H 2 O 2 ), полученная из субстратов, другие формы также могут оказывать вредное воздействие на растения. Каталаза (КАТ) играет решающую роль в смягчении токсического воздействия пероксидов за счет преобразования кислорода для защиты клетки (38). Аскорбатпероксидаза (АПО) также играет решающую роль у растений, особенно при вирусных инфекциях. Эти ферменты участвуют в детоксикации активных форм кислорода, таких как перекись водорода (H 2 O 2 ).
В наших опытах активность АПО увеличилась в 2,2 раза в образцах 4, примерно в 1,5 раза в образцах 1, 2 и 5 и в 1,7 раза в образцах 3 при вирусной инфекции (рис. 3). В листьях, инфицированных GLRaV-3, отмечалось значительное повышение активности антиоксидантных ферментов по сравнению с контрольными растениями.
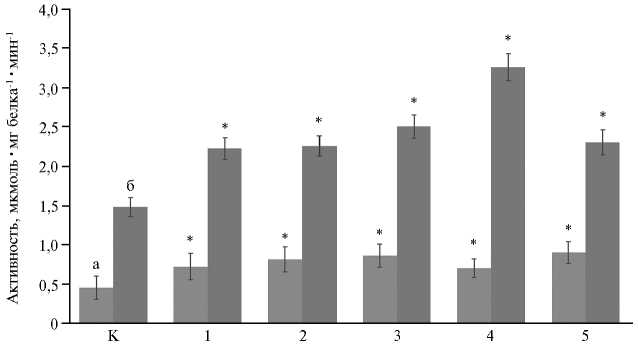
Рис. 3. Активность аскорбатпероксидазы (а) и каталазы (б) в здоровых (К) и инфицированных GLRaV-3 (1-5) листьях винограда ( Vitis vinifera L.) сорта Кара Шаны ( n = 3, M ±SD, Шама-хинский регион, период вегетации, 2023 год) . Инфицированные варианты отобраны на основании полуквантитативной оценки вирусной нагрузки методом DAS-ELISA (E 405 ): 1-2 — низкий уровень, 3 — средний, 4-5 — высокий.
* Различия с контролем статистически значимы при p < 0,001.
Вирусные инфекции часто вызывают окислительный стресс в растениях, что приводит к увеличению выработки АФК. АПО специфически обезвреживает H 2 O 2 , используя аскорбат в качестве восстановителя, с образованием воды и монодегидроаскорбата (39). Этот процесс детоксикации жизненно важен для предотвращения повреждения клеток, вызванного накоплением АФК. Повышение активности АПО при вирусных инфекциях служит адаптивной реакцией растения по поддержанию клеточного гомеостаза при окислительном стрессе.
Есть доказательства того, что при курчавости листьев хлопчатника вирусы оказывают значительное влияние на активность каталазы (КАТ).
Аналогичная тенденция наблюдалась и при инокуляции хлопка вирусом курчавости листьев хлопка (CLCuBuV) (24, 27). Кроме того, при заражении растений Passiflora edulis вирусом мозаики Telosma и растений Nicotiana benthamiana тобамовирусом мягкой крапчатости перца сообщалось об увеличении активности каталазы (6, 23). Сопоставимые результаты были получены при совместимых вирусных инфекциях GLRaV-3 (29). В наших исследованиях активность КАТ возросла в 1,6 раза в инфицированных вирусом образцах 1 и 4, в 1,8 раза — в образцах 2 и 3 и удвоилась в образце 5.
Показано, что при определенных взаимодействиях растений и вирусов активность фермента АПО усиливается, что указывает на его роль в защите растения против вирусных патогенов. Понимание этих процессов дает представление о молекулярных механизмах, лежащих в основе противовирусных реакций растений, что потенциально может привести к разработке стратегии повышения их устойчивости к вирусным заболеваниям. Избыточная продукция АПО может подавлять выработку пероксидазы, что приводит к накоплению большего количества активных форм кислорода (26). Высказывается предположение, что при совместимых отношениях хозяин—патоген активность АПО повышена в клетках как эпидермиса, так и мезофилла (15). Такая повышенная активность позволяет клетке сохранять жизнеспособность, несмотря на отсутствие механизма ограничения распространения патогена.
Синергетическое действие глутатиона и аскорбиновой кислоты представляет собой надежный защитный механизм от вредного воздействия окислительного стресса во время вирусных атак (40). Спровоцированные вирусами изменения окислительно-восстановительного статуса растительных клеток вызывают активацию ферментов, регулирующих метаболизм глутатиона и аскорбиновой кислоты, тем самым усиливая систему антиоксидантной защиты. Помимо нейтрализации АФК, глутатион и аскорбиновая кислота активно участвуют в регенерации других антиоксидантов, создавая каскадный эффект, который усиливает устойчивость растения к вирусным инфекциям. Поддержание баланса глутатиона и аскорбиновой кислоты имеет решающее значение для клеточного окислительно-восстановительного гомеостаза, который часто нарушается при окислительном стрессе, вызванном вирусом.
Таким образом, проведенное исследование позволило охарактеризовать физиолого-биохимический ответ растений винограда на инфекцию GLRaV-3. В 2022-2023 годах на территории Азербайджана вирусоподобные симптомы были выявлены на красных и белых сортах, а ОТ-ПЦР подтвердила наличие инфекции в 21 из 52 образцов (40,3 %). Наибольшая распространенность заболевания отмечена в регионе Сальян (32 %), меньшая — Исмаиллы (28 %) и Шамахы (16 %), что свидетельствует о региональных особенностях циркуляции вируса. У сорта Кара Шаны биохимический анализ показал прямую зависимость между вирусной нагрузкой и выраженностью окислительного стресса. Содержание малонового диальдегида (МДА) достоверно (р < 0,05) увеличивалось во всех инфицированных вариантах (6,5-7,9 мкмоль - г-1 сырой массы) по сравнению с контролем (2,27 мкмоль-г-1 сырой массы), что указывает на повреждение мембран. Одновременно наблюдалась активация антиоксидантной системы: активность аскорбатпероксидазы и каталазы возрастала соответственно в 1,5-2,2 и 1,6-2,0 раза (р < 0,05). Содержание восстановленного глутатиона увеличивалось в 1,6-2,4 раза, аскорбиновой кислоты и токоферолов — также возрастало, достигая максимальных значений при средней и высокой вирусной нагрузке. Полученные данные свидетельствуют о том, что инфи- цирование GLRaV-3 индуцирует выраженный окислительный стресс и сопровождается активацией ферментативных и неферментативных компонентов антиоксидантной защиты. Повышение количества МДА при усилении антиоксидантного ответа указывает на частичную компенсацию повреждений и отражает особенности взаимодействия хозяин-патоген. Взаимодействие между антиоксидантами отражает сложную природу реакции растения на вирусную инфекцию и подчеркивает важность глубокого понимания окислительно-восстановительных сигнальных путей. Изучение специфической роли глутатиона и аскорбиновой кислоты в инфицированных вирусом растениях улучшает наше понимание взаимодействия растений и вирусов, позволяя получить представление о потенциальных мишенях для разработки стратегий повышения устойчивости растений к вирусным патогенам.
Азербайджанский государственный университет нефти и промышленности,


