Влияние внутрисосудистого лазерного облучения крови на липидный метаболизм в ткани головного мозга при перитониальном эндотоксикозе
Автор: Спирина Мария Александровна, Бойнова Ирина Владиславовна, Зеленцов Павел Викторович
Журнал: Инженерные технологии и системы @vestnik-mrsu
Рубрика: Молодые ученые
Статья в выпуске: 1-2, 2014 года.
Бесплатный доступ
Эндогенная интоксикация является пусковым фактором в развитии полиорганной и полисистемной недостаточности. В ходе эксперимента исследовано антиоксидант-ное действие гелий-неонового лазерного облучения. Установлена способность вну-трисосудистого лазерного облучения крови нивелировать дисметаболические нарушения в тканевых структурах головного мозга. Зарегистрировано снижение концентрации токсических субстанций в церебральной ткани и мембраностабилизирующее действие лазеротерапии.
Эндогенная интоксикация, перитонит, перекисное окисление липи-дов, лазерное облучение крови, головной мозг
Короткий адрес: https://sciup.org/14720065
IDR: 14720065 | УДК: 612.014.469:001.895
Influence of intravascular laser irradiation of blood on lipid metabolism in brain tissue in peritoneal endotoxicosis
Endogenous intoxication is one of the major pathogenetic mechanisms in the development of multiple organ failure. The experiments on dogs were done. On the course of the study was investigated the antioxidant effect of helium-neon laser irradiation on the severity of peritoneal endotoxemia. The ability of intravascular laser irradiation of blood to reduce the level dysmetabolic violations in brain tissue was detected. Were registred the decline in the concentration of toxic substances in the cerebral tissue and the membrane-stabilizing effect of laser therapy.
Текст научной статьи Влияние внутрисосудистого лазерного облучения крови на липидный метаболизм в ткани головного мозга при перитониальном эндотоксикозе
Синдром эндогенной интоксикации (СЭИ) в силу широкой распространенности в клинической практике в настоящее время привлекает внимание специалистов различного профиля [1; 3]. Выраженность эндотоксемии влияет как на прогноз заболевания, так и на его исход [2].
Характерная при эндотоксемии гипоксия запускает ряд патологических модификаций на системном и регионарном уровнях. В результате формируется полиорганная и полисистемная недоста-
peritonitis, lipid peroxidation, laser irradiation of точность, существенно увеличивающая риск летального исхода.
Ткань головного мозга весьма уязвима к снижению оксигенации. Причиной тому являются особенности метаболизма органа: несовершенство собственных систем антиоксидантной защиты, специфическая структурная организация нейрональной ткани, значительная концентрация легко окисляемых липидов, высокая интенсивность метаболических реакций. Рациональным с целью эффективной церебропротекции пред
ВЕСТНИК Мордовского университета | 2014 | № 1-2
ставляется применение в комплексной терапии способов лечения, обладающих антиоксидантным действием [4; 5].
Экспериментальное исследование проводилось на взрослых беспородных собаках (n=46). Животным под тиопен-тал-натриевым наркозом моделировали острый каловый перитонит по способу А. П. Власова (1991). В контрольные сроки (на 1-е, 3-и, 5-е сутки после релапаротомии) фиксировались показатели, характеризующие липидный метаболизм в нейрональной ткани. После проведения санации брюшной полости применялась стандартная инфузионная и антибактериальная терапия (внутримышечные инъекции 2 раза в сутки раствора гентамицина из расчета 0,8 мг/кг массы тела; внутривенно 1 раз в сутки инфузии 5%-ного раствора глюкозы и 0,89%-ного раствора хлорида натрия из расчета 50 мл/кг массы тела животного).
Собаки были разделены на две равные группы методом случайной выборки. Изучались выраженность эндотоксикоза, показатели липопероксидации, липидный спектр в тканевых структурах головного мозга. В опытной группе наряду со стандартным комплексом лечения проводилось гелий-неоновое внутрисосудистое лазерное облучение крови с мощностью излучения на выходе световода 5 мВт и временем воздействия 15 мин (доза 0,1 Дж/см2).
В результате эксперимента у исследуемых животных было зафиксировано формирование СЭИ, что верифицировало адекватность модели острого перитонита. Существенно возрастала концентрация гидрофильных и гидрофобных токсинов в плазме крови. Так, титр молекул средней массы (λ = 254 нм и λ = 280 нм) достоверно увеличивался на 77,04–136,54 % и 54,66–137,05 % соответственно (р<0,05). Отмечено статистически значимое снижение общей и эффективной концентрации альбумина – на 18,96–30,73 % и 34,11–52,60 % (р<0,05) соответственно, а также резерва связывания альбумина на 21,21–50,00 % (р<0,05) относительно нормальных зна- чений исследуемых показателей. Повышение индекса токсичности плазмы крови составляло 158,18–336,36 % (р<0,05) по сравнению с исходными цифрами.
СЭИ приводил к значительной интенсификации процессов перекисного окисления липидов. Экспериментальный перитонит сопровождался статистически значимым ростом спонтанного (на 28,14–188,33 %) и индуцированного (на 21,35–72,99 %) малонового диальдегида (р<0,05). Фосфолиполитическая активность повысилась на 92,31–117,95% (р<0,05), параллельно зарегистрировано уменьшение энзимного потенциала су-пероксиддисмутазы на 31,90–59,05 % (р<0,05) относительно физиологических значений изучаемых показателей.
Формирование СЭИ приводило к метаболическим перестойкам и модификации фосфолипидного спектра мембран нервных клеток (рис. 1).
Анализ полученных данных показал изменение нормального соотношения фосфолипидных фракций в спектре – значительное повышение доли лизо-фосфолипидов и свободных жирных кислот. Вместе с тем процент легко-окисляемых суммарных фосфолипидов, холестерола и фосфатидилхолина снижался относительно нормы.
Высокое содержание свободных жирных кислот и лизофосфолипидов способствует дезорганизации и дестабилизации мембранных структур клеток. Таким образом, выявленные в ходе исследования дислипидные трансформации в церебральной ткани верифицируют значительную деструкцию биомембран нейроцитов при эндотоксикозе. Данные изменения являются одним из определяющих патогенетических механизмов при эндотоксическом повреждении головного мозга.
Включение низкоинтенсивного лазерного облучения в комплексное лечение приводило к снижению выраженности СЭИ, вызванного воспалением брюшины. В опытной группе зафиксировано уменьшение содержания гидрофильных и гидрофобных токсических субстанций в плазме крови животных на 14,54–31,49 % и 3,93-24,96 % (р<0,05) соответственно по сравнению с данными контроля. В группе, получавшей лазеротерапию, существенно снижался индекс токсичности плазмы крови – на 23,08–52,89 % (р<0,05) по сравнению с животными, проходившими стандартное лечение. Следует отметить, что на заключительном этапе эксперимента с применением гелий-неонового внутрисосудистого лазерного облучения крови индекс токсичности возвращался к начальному значению.
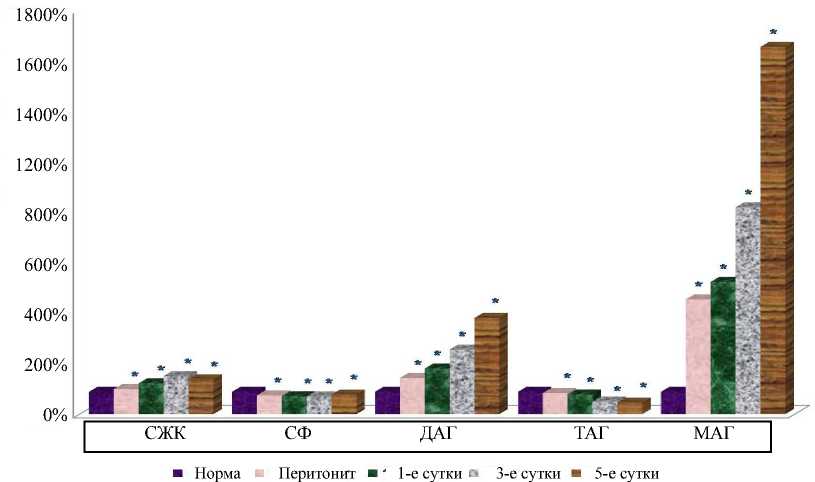
* – достоверность отличия по отношению к исходу при p<0,05; СЖК – свободные жирные кислоты; СФ – сфингомиелин; ДАГ – диацилглицеролы; ТАГ – триацилглицеролы; МАГ – моноацилглицеролы.
Серия «Естественные и технические науки»
Р и с . 1 . Модификация липидного спектра в ткани головного мозга при токсическом поражении органа
В опытной группе отмечалось уменьшение титра ТБК-активных продуктов в церебральной ткани. Титр спонтанного малонового диальдегида был на 43,96 % (р<0,05) ниже контрольных показателей в финале эксперимента. На 5-е сутки после санации брюшной полости содержание индуцированного малонового диальдегида также статистически значимо уменьшалось по сравнению с группой контроля на 9,48 % (р<0,05).
Внутрисосудистое лазерное облучение крови снижало интенсивность процессов липопероксидации при перитоните. На фоне комплексного лечения на 5-е сутки послеоперационного периода зарегистри- ровано снижение энзимного потенциала фосфолипазы А2 в тканевых структурах головного мозга на 21,05% (р<0,05) по сравнению с контрольными показателями. Также отмечалось увеличение ферментативной активности супероксиддисмута-зы на 3-и и 5-е сутки исследования – на 27,76 и 24,48% (р<0,05) соответственно. Приведенные данные демонстрируют увеличение собственного антиоксидантного потенциала нейрональной ткани в группе животных, получавших лазеротерапию.
Под воздействием лазеротерапии в ходе эксперимента отмечена тенденция к нормализации липидного спектра мембранных структур клеток головного мозга.
Применение гелий-неонового лазерного облучения крови снижало содержание свободных жирных кислот, моно- и диаци-лглицеролов в церебральной ткани относительно значений идентичных показателей в контрольной группе на 19,48, 22,18 и 42,21% (р<0,05) на 5-е сутки проводимого лечения. Отмечалось достоверное нарастание титра суммарных фосфолипидов в ткани головного мозга на 16,85% (р<0,05) вместе с уменьшением содержания фракций лизофосфолипидов и фосфатидилино-зита на 19,48 и 12,44 % (р<0,05) на заключительном этапе эксперимента (рис. 2).
300%
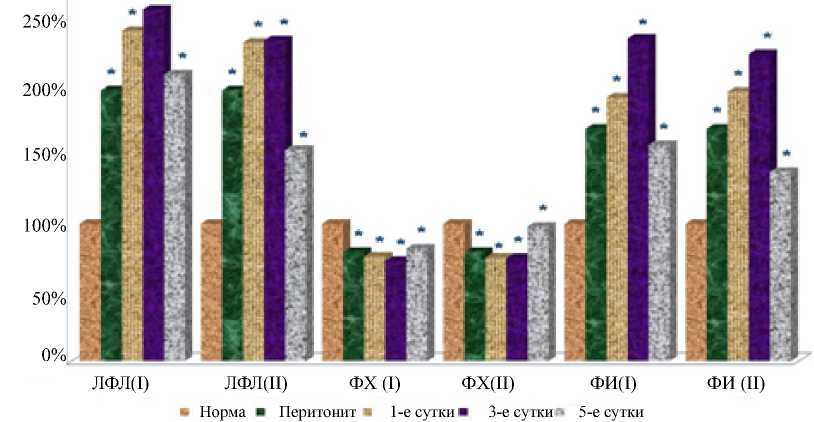
* – достоверность отличия по отношению к исходу при p<0,05; I – контрольная группа; II – опытная группа; ЛФЛ – лизофосфолипиды; ФХ – фосфатидилхолин; ФИ – фосфатидилинозит.
Рис. 2. Динамика соотношения фосфолипидных фракций на фоне применения лазеротерапии
ВЕСТНИК Мордовского университета | 2014 | № 1-2
На 5-е сутки послеоперационного периода доля фосфатидилхолина была выше контрольных значений на 19,69 % (р<0,05), достоверно не отличаясь от нормальных значений.
Таким образом, полученные в результате исследования данные показали, что низкоэнергетическое гелий-неоновое лазерное облучение крови при эндотоксикозе способствует снижению содержания токсичных продуктов перекисного окисления липидов в церебральной ткани за счет своего антиоксидантного действия.
Внедрение лазеротерапии в комплексное лечение на раннем послеоперационном периоде уменьшает интенсивность фосфолиполитических реакций в тканевых структурах изучаемого органа, корригируя возникающие при СЭИ дисметаболические нарушения.
Полученные в ходе эксперимента показатели верифицировали благоприятное действие внутрисосудистого лазерного облучения крови на липидный метаболизм нейрональных мембран, ингибируя также мембранодеструктивные процессы в клетках головного мозга.
Список литературы Влияние внутрисосудистого лазерного облучения крови на липидный метаболизм в ткани головного мозга при перитониальном эндотоксикозе
- Арбулиев, К. М. Местная сорбционная терапия и ее эффективность в коррекции эндогенной интоксикации у больных острым гнойным пиелонефритом паранефритом/К. М. Арбулиев [и др.]//Урология. -2013. -№ 2. -С. 28-34.
- Власов, А. П. Взаимосвязь функционально-метаболического статуса миокарда и печени при эндоксикозе/А. П. Власов [и др.]//Фундаментальные исследования. -2012. -№ 5. -Ч. 2. -С. 168.
- Матвеев, С. Б. Эндогенная интоксикация в раннем послеоперационном периоде у больных сочетанной травмой живота и массивной кровопотерей/С. Б. Матвеев [и др.]//Клиническая лабораторная диагностика. -2012. -№ 6. -С. 27-29.
- Gasparova, Z. Effect of antioxidants on functional recovery after in vitro-induced ischemia and longterm potentiation recorded in the pyramidal layer of the CA1 area of rat hippocampus/Z. Gasparova, V. Stara, S. Stolc//General Physiology and Biophysics. -2013. -August 12.
- Perrone, S. Oxidative stress and antioxidant strategies in newborns/S. Perrone [et al.]//Journal of Maternal-Fetal and Neonatal Medicine. -Oct. 2010. -Vol. 23. -№ S3. -P. 63-65.


