Внутрипортальный путь введения лекарственных растворов в коррекции нарушений гомеостаза при остром внепеченочном холестазе
Автор: Беляев А.Н., Тумайкин В.П., Беляев С.А., Мокшина Е.И., Рафик Х.А.
Журнал: Инженерные технологии и системы @vestnik-mrsu
Рубрика: Реаниматология и интенсивная терапия
Статья в выпуске: 2, 2006 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/14718714
IDR: 14718714
Текст статьи Внутрипортальный путь введения лекарственных растворов в коррекции нарушений гомеостаза при остром внепеченочном холестазе
-
А. Н. Беляев, доктор медицинских наук,
-
В. П- Тумайкин, кандидат медицинских наук,
-
С. А. Беляев, кандидат медицинских наук,
-
Е. И Мокшина,
-
X. А. Рафик
Лечение больных с механической желтухой является актуальной проблемой абдоминальной хирургии. При развитии обтурации желчных путей с последующим холангитом и печеночной недостаточностью оперативное лечение весьма рискованно и сопровождается высокой летальностью. Послеоперационная летальность, по данным литературы, при неопухолевой желтухе составляет 5,6 — 6,3 %, при опухолевой желтухе — 10,6 — 25,7 %.
Тяжесть развивающейся желтухи определяется степенью угнетения функционального состояния печени и прогрессирующей печеночной недостаточностью. Высокая летальность вследствие печеночной недостаточности после опвпзций пповедвнных на ^онв длительной желчной гипертензии, диктует необходимость выполнения декомпрессии желчных путей, направленную на восстановление функции печени и нормализации гомеостаза. Данный момент общепризнанно является первым этапом в лечении механической желтухи, однако его применение в качестве монотерапии не всегда позволяет достичь быстрого выздоровления больных.
Немаловажным этапом в лечении данной патологии является проведение в послеоперационном периоде медикаментозной коррекции функционального состояния печени. Среди лекарственных препаратов особое внимание привлекают средства, которые в силу своего многофакторного действия способны воздействовать на различные звенья патогенеза, проявляя тем самым свою высокую эффективность. Одним из таких препаратов является медицинский озон, обладающий бактерицидным, антигипоксантным, метаболическим, мемб-
Эффективным методом в лечении заболевания органов гепатопамкреатодуоденальной зоны является применение внутрипортальных инфузий лекарственных средств. Данный метод позволяет подводить лекарственные препараты непосредственно к очагу повреждения в более высокой концентрации и тем самым значительно повысить эффективность проводимого лечения [1; 4].
Целью исследования являлось изучение эффективности внутривенной и внутрипор-тальной озонотерапии при экспериментальном внепеченочном холестазе.
Нами были проведены эксперименты на 32 беспородных собаках обоего пола массой 10 — 34 кг под внутриплевральным тиопен-тал-натриевым (0,045 — 0,050 г/кг массы) наркозом. После ревизии подпеченочного пространства в толще печеночно-двенадцатиперстной связки находили общий желчный проток. Над протоком рассекали листок брюшины, и с помощью лигатурной иглы проводили под ним лигатуру. Концы лигатуры продевали через трубку диаметром 3 — 4 мм и затягивались на поперечно расположенной второй трубке.
На 3-и сутки эксперимента на высоте биохимических нарушений выполняли декомпрессию желчевыводящих путей посредством удаления лигатурной перетяжки. Инфузионную терапию проводили начиная с 3-х суток ежедневно 1 раз в сутки. В зависимости от соста- П. Тумайкин, С. А. Беляев. Е И Мокшина. X. А Рафик. 2006
ва инфузионных сред животные распределены на 4 серии. В контрольной серии (л = 8) лечение не проводилось. Во 2-й серии (п = 8) после выполнения декомпрессии желчевыводящих путей проводили внутривенное капельное (40 — 60 кап/мин) введение 0,9 % раствора натрия хлорида (физиологического раствора — ФР) в объеме 20 мл/кг.
В 3-й и 4-й сериях экспериментов проводили изучение влияния озонированного изотонического раствора натрия хлорида (озонированного физиологического раствора — ОФР). ОФР получали путем барботирования 0,9 % раствора NaCI озонокислородной смесью с помощью озонатора АОТ-01-Арз. Концентрация озона на выходе озонатора составляла 2 500 мкг/л, время барботирования — 10 мин. В 3-й серии (п = 8) проводили внутривенную инфузию ОФР со скоростью 40 — 60 кап/мин в объеме 10 мл/кг, после чего внутривенно вводился ФР (10 мл/кг). В 4-й серии (л = 8) после удаления лигатуры с холедоха осуществляли внутрипортальное введение ОФР (10 мл/кг) и внутривенное — ФР (10 мл/кг).
Оценка функционального состояния печени проводилась по показателям уровня общего билирубина, общего белка, малонового диальдегида (МДА), активности аланиновой (АлАТ) и аспарагиновой (АсАТ) трансаминаз, щелоч-нон фосфатазы и ката л азы j ли п иди о го сне кт-ра. Процессы свободнорадикального окисления изучали по показателям перекисного окисления липидов — 1ти и общей антиоксидантной активности — ^а1^ индуцированной биохемилюминисценции. Оценку нарушений гемостаза проводили по показателям коагулограммы и данным тромбоэластографии. Морфологическое строение печени оценивалось по данным световой микроскопии микропрепаратов, окрашенных гематоксилин-эозином. Эффективность лечения оценивали на 7-е сутки эксперимента.
Достоверность различий с вычислением критерия Фишера — Стьюдента определяли в каждой серии по отношению к исходному значению (р) и к значению на 3-и сутки эксперимента (р,).
Развитие механической желтухи в течение 1 — 4-х суток сопровождалось вначале резким, а затем медленно прогрессирующим повышением содержания маркеров холестаза и цитолиза гепатоцитов. На 7-е сутки эксперимента уровень общего билирубина относительно исходных значений возрос в 31,3 раза (р < 0,001, р, > 0,05), активность АлАТ и АсАТ — соответственно в 9,8 и 3,7 раза (р < 0,001, р, > 0,05), щелочной фосфатазы — в 5,4 раза (р < 0,001, р, > 0,05). Уровень общего белка венозной крови увеличивался в течение 1 — 3 суток, составляя на 3-и сутки 113,2 % относительно исхода (р < 0,001) с последующим недостоверным снижением на 4 — 7-е сутки (составляя на 7-е сутки 108,4 %; р < 0,01, р, > 0,05).
Исследование состояния про- и антиоксидантного статуса организма выявило резкое повышение уровня липоперолксидации с одновременным угнетением антиоксидантной системы. Показатель максимальной интенсивности индуцированной хемилюминисценции UmM> прогрессивно увеличивался, составляя на 7-е сутки 297,7 % (р < 0,001; р, > 0,05). Общая антиоксидантная активность U^/S) снижалась до 73,42 % (р < 0,01; р. < 0,001). Уровень МДА составлял 740 % (р < 0,001; р, < 0,001). Активность каталазы снижалась до 55,04 % (р < 0,01, р, > 0,05).
Показатель тромбоэластографии — /С, зависящий от концентрации образующегося тромбина, а также количества фибриногена, на 3-и сутки составил 130,54 % от исходного. Константа коагуляции R+K, выражающая об-
ГШХТТГЛ ТГ гтиг'га ТХТ-Т-ТГХ/'ТТ- rnanTLIDOUIin TZTinniJ ТГойГТУ. A-х*,j AX' #A^m , vrilll AX'4- • W A, A 1^1 МХЧт'А X V АЛ Af чилась на 12,02 %. Показатель t (время начала ретракции кровяного сгустка) возрос на 43,21 %, а константа синерезиса — на 41,20 %. В целом время свертывания крови увеличилось на 32,48 % по сравнению с исходом. Отмечено снижение эластичности и плотности кровяного сгустка, что сопровождалось снижением максимальной амплитуды на 8,46 %, а индекса эластичности сгустка Е — на 23,33 %. На 3-и сутки происходило увеличение времени фибринолиза до 825 с (168 %) при его исходном значении 490 с. Концентрация РФМК составляла в среднем 17,5 мг%, что более чем в 4 раза выше верхней границы нормы.
Уровень общих липидов плазмы крови значительно повышался, составляя 3-и сутки 199,1 % (р < 0,05) относительно исходного значения, а на 7-е сутки — 263,2 % (р < 0,01; Р] > 0,05). Одновременно с увеличением количества липидов плазмы крови, происходило значительное повышение концентрации обще-
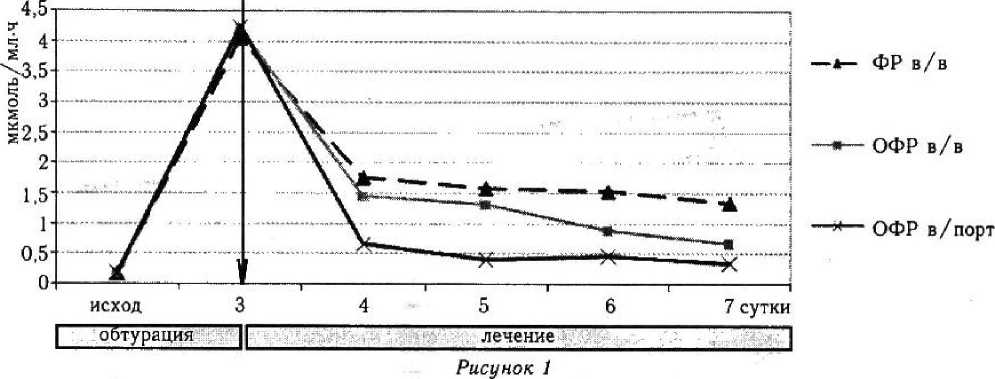
Сравнительная динамика активности АлАТ после декомпрессии холедоха на фоне внутривенной и внутриаортальной инфузии озонированного физиологического раствора
обтурация
■лечение
Рисунок 2
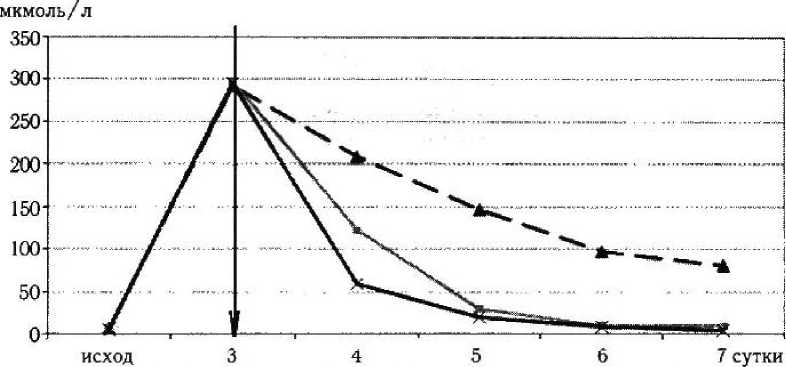
Сравнительная динамика содержания билирубина после декомпрессии холедоха на фоне внутривенной и внутриаортальной инфузии озонированного физиологического раствора
ОФР в/порт
го холестерина. На 3-и сутки его содержание увеличивалось до уровня 350,9 % (р < 0,001), на 7-е — до 436,0 % (р < 0,001; р, > 0,05).
При световой микроскопии на 7-е сутки внепеченочного холестаза наблюдался выраженный билирубиностаз в гепатоцитах, желчных канальцах и протоках. Гепатоциты были увеличены в объеме, со светлой пенистой цитоплазмой. Отдельные гепатоциты, имбибированные желчью, подвергались деструкции. В портальных трактах отмечался отек, лимфогистиоци-тарная инфильтрация. Центральные вены и синусоиды были расширены и полнокровны. Содержание жидкости в ткани печени, взятой с периферии, возрастало с 68,7 до 72,41 %, в области ворот — с 69,20 до 76,46 %.
Таким образом, развитие острого внепеченочного холестаза приводило к выраженным функциональным и морфологическим изменениям печени.
Во 2 серии экспериментов внутривенное введение ФР не приводило к полному восстановлению показателей функционального состояния печени. Содержание изучаемых маркеров холестаза и цитолиза снижалось, но оставалось достаточно высоким (рис. 1, 2). Уровень общего билирубина к 7-м суткам составлял 1 103,9 % относительно исходного значения (р < 0,05; р1 < 0,001). Активность АсАТ и АлАТ снижалась менее значительно, составляя на 7-е сутки 308,3 % (р < 0,01; р, < 0,001) и 710,5 % (р < 0,001; р, < 0,001) соответствен-
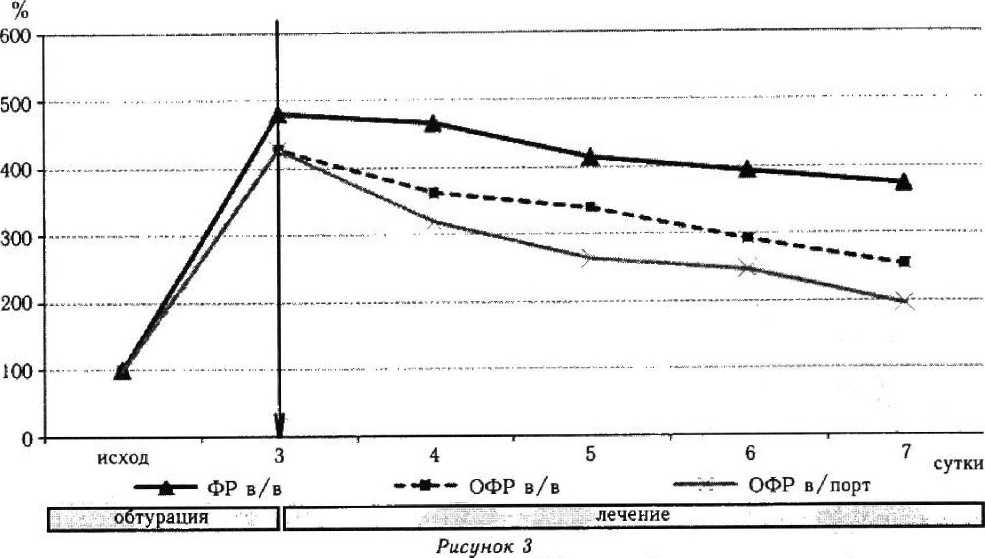
Сравнительная динамика концентрации МДА после декомпрессии холедоха на фоне внутривенной и внутриаортальной инфузии озонированного физиологического
раствора
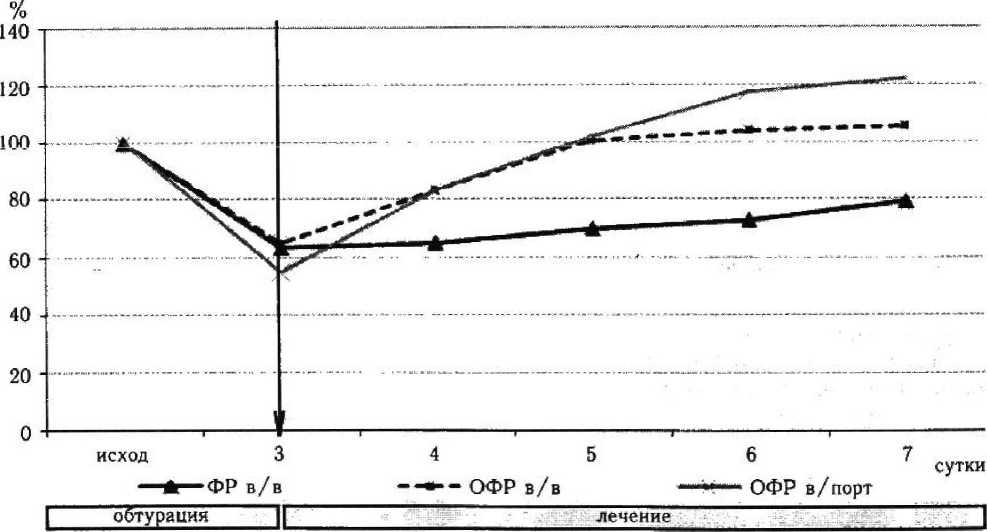
Рисунок 4
Сравнительная динамика активности каталазы после декомпрессии холедоха на фоне внутривенной и внутриаортальной инфузии озонированного физиологического раствора
но. Содержание щелочной фосфатазы соответствовало 245,9 % (р < 0,01; р, < 0,001). Концентрация общего белка снижалась до 89,0 % (р < 0,001; р, < 0,01).
Состояние про- и антиоксидантного статуса организма характеризовалось незначительными положительными изменениями (рис. 3, 4). Показатель 1^ снижался до 273,4 %
(р < 0,001; р( < 0,01), отношение lmM/S составляло 82,3 % (р < 0,01; р, < 0,05) “концентрация МДА — 375,2 % (р < 0,001; р, < 0,001), активность каталазы — 73,8 % (р < 0,01, р, > 0,05).
Проводимая инфузионная терапия не оказывала существенной положительной динамики на показатели жирового обмена и системы гемостаза.
При микроскопическом исследовании отмечались сохранение вакуольной и зернистой дистрофии гепатоцитов, отек портальных трактов, нарушение балочной ориентации гепатоцитов, наличие очагов некроза.
Проведение внутривенной озонотерапии характеризовалось значительным восстановлением показателей функционального состояния печени (рис. 1, 2). В 3-й серии экспериментов при внутривенном введении ОФР концентрация общего билирубина снижалась до уровня 143,7 % (р < 0,05, р, < 0,001). Активность АсАТ и АлАТ на 7-е сутки экслери- мента относительно исхода составляла 170,0 % (р > 0,05, р, < 0,001) и 372,2 % (р > 0,05, р, < 0,001) соответственно. Концентрация щелочной фосфатазы уменьша лась до уровня 167,9
(р < 0,05,
На фоне проводимой внутривенной озонотерапии содержание липидов в плазме уменьшалось в 1,3 раза — с 10,7 до 8,3 (р < 0,05; р, < 0,05), оставаясь, однако, на уровне, в 2 раза превышающем исходный. Концентрация холестерина снижалась более существенно, в 1,6 раза — с 11,45 до 7,2 ммоль/л (р > 0,05; р, < 0,05), что составляло 245,7 и 155,8 % относительно исхода (рис. 5).
Наблюдалось постепенное восстановление показателей гемостаза. Время фибринолиза, приближаясь к нормальным значениям, даже к 7-м суткам превосходило исходное. Концентрация РФМК к этому времени снижалась до верхней границы нормы. Показатель К приближался к исходным величинам на 6-е сутки и составил 103,25 % от исходного. Константа коагуляции R+K уменьшилась к 5-м суткам до исходных величин.
При внутривенном пути введения ОФР желчные тромбы в желчных канальцах не были обнаружены. Число дистрофических из- менений и некротизированных, пропитанных желчью гепатоцитов уменьшалось. В портальных трактах сохранялась лимфогистиоци-тарная инфильтрация. Синусоиды были расширены и содержали форменные элементы крови. Содержание жидкости на периферии печени составило 69,12 %, а в центре — 71,0 %.
р; < 0,001), содержание общего белка возрастало до 96,5 % (р > 0,05, р, < 0,05).
Уровень МДА уменьшился до 225,4 %, ак-
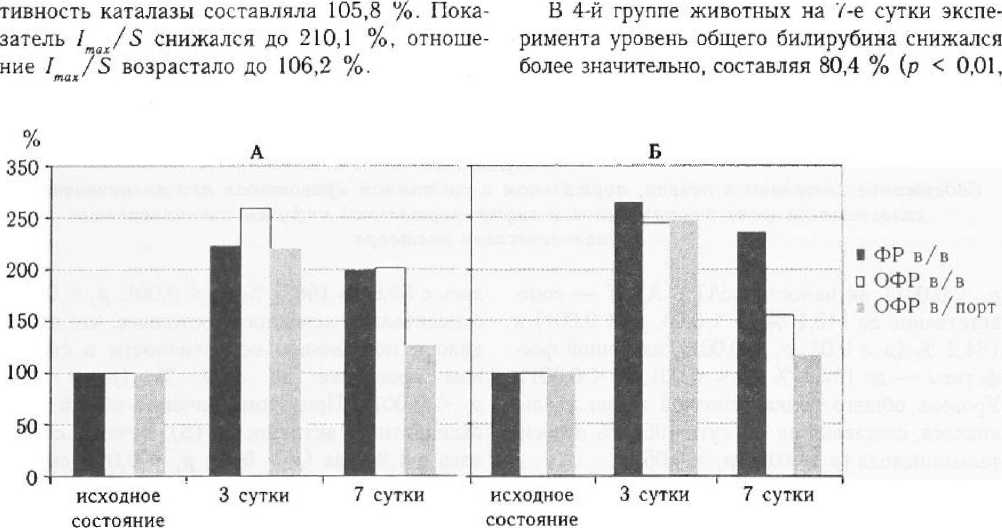
Рисунок 5
Динамика содержания общих липидов (А) и общего холестерина (Б) при внепеченочном холестазе на фоне внутривенной и внутриаортальной инфузии ОФР
состояние
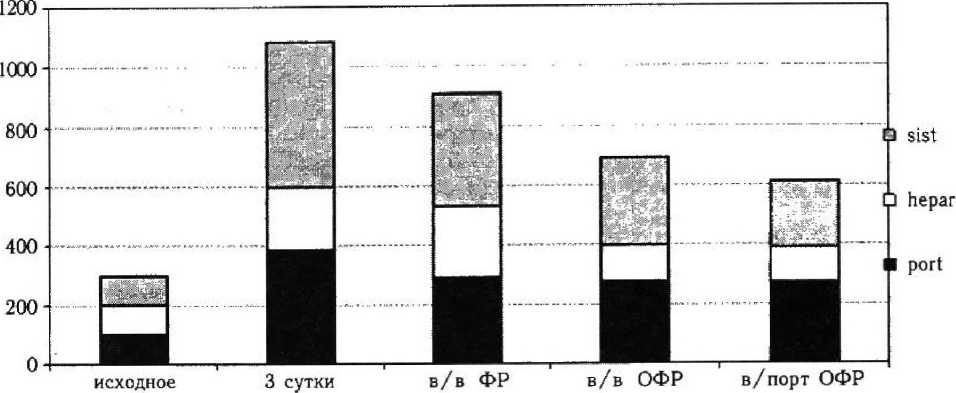
Рисунок 6
Содержание МДА в печени, портальном и системном кровотоках при внепеченочном холестазе на фоне внутривенной и внутриаортальной инфузии озонированного физиологического раствора
состояние
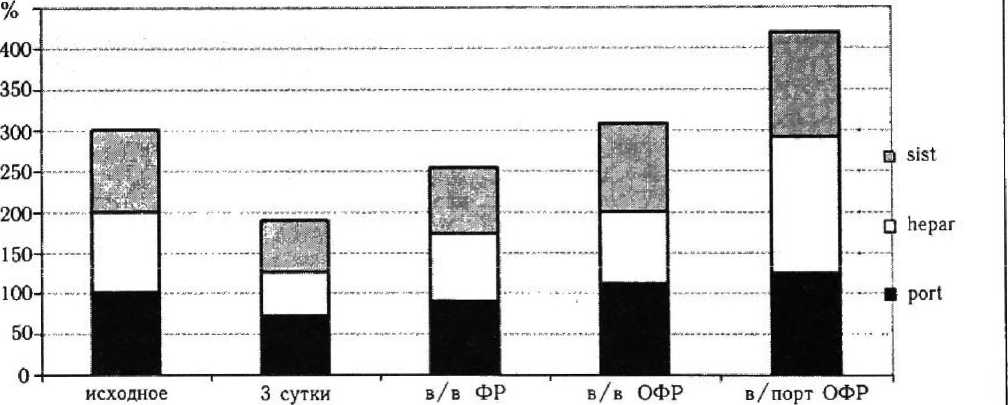
Рисунок 7
Содержание каталазы в печени, портальном и системном кровотоках при внепеченочном холестазе на фоне внутривенной и внутриаортальной инфузии озонированного физиологического раствора
р;< 0,001), активность АсАТ и АлАТ — соответственно до 142,1 % (р < 0,05, р, < 0,001) и 184,2 % (р > 0,05, р, < 0,001), щелочной фосфатазы — до 137,3 % (р < 0,001, р, < 0,001), Уровень общего белка венозной крови увеличивался, составляя на 7-е сутки 96,9 % относительно исхода (р > 0,05, р1 > 0,05).
Важнейшим моментом в лечении явилось восстановление баланса прооксидаитно-анти-оксидантного статуса организма (рис. 3, 4, 6, 7). В ответ на внутрипортальное введение ОФР содержание каталазы в печени увеличива лась с 52,6 до 166,5 % (р < 0,001; р, < 0,001) относительно исходного состояния, что приводило к повышению ее активности в системном кровотоке до 83,0 % (р > 0,05; р] < 0,001). При этом значение общей антиоксидантной активности (S) печени снижалась в 1,9 раза (р > 0,05; р( < 0,01), системного кровотока — в 2,2 раза (р > 0,05; Р, < 0,001).
Внутрипортальное введение ОФР сопровождалось снижением интенсивности свободнорадикальных реакций. При хемолюминес- центном анализе гомогената печени нами было выявлено снижение значения /^ в 3,5 раза (р > 0,05; р, < 0,05), в системном кровотоке — в 1,7 раза (р < 0,01; р, < 0,01). Концентрация МДА в ткани печени снижалась в 1,8 раза (р > 0,05; р, < 0,001), в оттекающей крови — в 2,1 раза (р < 0,01; р2 < 0,001).
Уровень общих липидов плазмы крови уменьшался на протяжении всего эксперимента в 1,7 раза, к 7-м суткам — до 5,8 (р > 0,05; р, < 0,05), оставаясь при этом на уровне 125,8 относительно исхода. Снижение содержания холестерина происходило пропорционально изменению уровня общих липидов (рис. 5). Время фибринолиза достигало нормальных величин к 5-м суткам, что свидетельствует о быстром восстановлении функциональной активности печени и исчезновении дефицита плазминогена. РФМК также быстро исчезали из кровотока, и уже к 4*м суткам их концентрация была в пределах нормы.
При внутрипортальном пути введения ОФР наблюдались гепатоциты, ориентированные в
Реаниматология и интенсивная гемотерапия соответствии с их балочной пространственной организацией, цитоплазма эозинофильная. В единичных гепатоцитах третьей зоны обнаруживалась зернистая дистрофия с умеренной нейтрофильно-клеточной инфильтрацией портальных трактов. Сохранялось полнокровие синусоидов. Содержание жидкости на периферии печени составило 69,12 %, в области ворот — 71,00 %.
Анализ изменений показателей функционального и морфологического состояния печени свидетельствует о благоприятном влиянии ОФР на печень при механической желтухе. Механизм лечебного воздействия связывается со способностью озона влиять на интенсивность липопероксидации и метаболический статус печеночной паренхимы, оказывая тем самым стабилизирующее влияние на мембраны гепатоцитов. Озон, обладая спазмолитическим эффектом, улучшает внут-риорганный кровоток в печени, предупреждает развитие необратимых некротических изменений в печени.
Список литературы Внутрипортальный путь введения лекарственных растворов в коррекции нарушений гомеостаза при остром внепеченочном холестазе
- Атясов Н. И. Вливания в венозное русло печени в лечебных и диагностических целях у тяжелообожженых/Н. И. Атясов, В. А. Лазарев, Е. Н. Матчин. Саранск: Изд-во Мордов. ун-та, 1993.
- с.
- Новые технологии внутрипортальных инфузий в хирургии и интенсивной терапии/А. Н. Беляев и др.//Общая реаниматология. 2006. Т. 2. № 4/1. С. 55 -57.
- Перетягин С. П. О многофакторном механизме лечебного действия озона/С. П. Перетяган//Нижегородский медицинский журнал. Приложение: Озонотерапия. 2003. С. 6 -7.
- Шкуратов А. Г. Современные принципы внутрипортального введения лекарственных растворов в хирургии диффузных и очаговых заболеваний печени: автореф. дис.. канд. мед. наук/А. Г. Шкуратов. Владивосток, 1997. 22 с.


