Внутривенное лазерное облучение крови в лечении цитомегаловирусной инфекции у женщин
Автор: Чернова Надежда Ивановна, Москвин Сергей Владимирович
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клиническая медицина
Статья в выпуске: 2 (10), 2013 года.
Бесплатный доступ
В статье представлен усовершенствованный метод терапии воспалительных заболеваний мочеполового тракта, сопровождающихся реактивацией цитомегаловируса с использованием низкоинтенсивного лазерного излучения.
Цитомегаловирусная инфекция, урогенитальный тракт, низкоинтенсивное лазерное излучение, противовирусная активность
Короткий адрес: https://sciup.org/14344041
IDR: 14344041 | УДК: 615.47:616-085
Intravenous laser blood irradiation as treatment of cytomegalovirus infection in women
The article represents a method of improving the treatment of inflammatory diseases of the urinary tract associated witha reactivation of cytomegalovirus using low intensity laser radiation.
Текст научной статьи Внутривенное лазерное облучение крови в лечении цитомегаловирусной инфекции у женщин
Актуальность. Цитомегаловирус (ЦМВ) относится к роду герпесвирусов, характерной особенностью которых является способность к пожизненной персистенции в организме человека и активации на фоне иммунодефицита [1, 2, 3, 4]. Цитомегаловирусная инфекция (ЦМВИ) представлена широким спектром клинико-патогенетических вариантов [3, 4]. Согласно Международной классификации болезней Х пересмотра (МКБ-10), выделяются следующие заболевания, связанные с ЦМВ: ЦМВ-болезнь, пневмонит, гепатит, панкреатит, ЦМВ-болезнь неспецифическая; мононуклеоз, врожденная ЦМВИ и другие болезни, вызванные ЦМВ. Однако в практической деятельности чаще используется классификация, предложенная Казанцевым А.П. и Поповой Н.И., в соответствии с которой выделяется врожденная ЦМВИ - в острой и хронической формах, и приобретенная ЦМВИ - в латентной, острой или генерализованной формах. В зависимости от тяжести заболевания, выделяют легкую, среднетяжелую и тяжелую формы, по длительности процесса - острую, затяжную и хроническую, непрерывно рецидивирующую формы.
Целью терапии ЦМВИ является устранение симптомов реактивации заболевания и удержание ЦМВ в неактивном состоянии. Если инфекция протекает бессимптомно, иммунитет у вирусоносителя нормальный, то в лечении нет необходимости [1, 2, 8, 9]. Специфические противовирусные препараты (ганцикловир, вальганцикловир, фоскарнет, цидофовир) имеют ряд серьезных побочных эффектов, таких как кардиотоксичность, гепатотоксичность, влияние на кроветворение. Противоцитомегаловирусные иммуноглобулины - высокую стоимость. В связи с этим проводится поиск новых средств и схем терапии, которые позволили бы избежать проявления побочных токсических эффектов при сохранении высокой противовирусной эффективности.
В данном аспекте определенный интерес представляет отечественный препарат панавир - высокомолекулярный полисахарид, относящийся к классу гексозных гликозидов. Очищен- ный экстракт побегов растения Solanum tuberosum, состоящий из глюкозы, рамнозы, арабинозы, маннозы, ксилозы, галактозы, уроновых кислот. Его уникальность состоит в сочетании прямого противовирусного и иммуномодулирующего действий, которые изучались в НИИ вирусологии им Д.И. Ивановского РАМН. В эксперименте противовирусные свойства препарата выявлены в отношении инфекций, вызываемых самыми разными вирусами, как ДНК, так и РНК-содержащими (ВПГ-1, ВПГ-2, ЦМВ, вирус гепатита С, гриппа А, В, аденовирусы), что свидетельствует о поливалентном характере противовирусной активности препарата. Характерными особенностями механизма противовирусной активности панавира являются его влияние на ингибирование синтеза вирусных белков и доказанное повышение жизнеспособности клеток в культуре, снижение титров вирусов в культуре клеток и во время экспериментов на животных, увеличение латентного периода развития экспериментальной инфекции in vitro и in vivo, митогенная активность в реакции бласттрансформации лимфоцитов, способность модулировать уровень лейкоцитарного интерферона (ИФ) у и а.
Препарат рекомендован к использованию в комплексной терапии герпесвирусных инфекций различной локализации, вторичных иммунодифицитных состояний на фоне инфекционных заболеваний, цитомегаловирусной инфекции у пациенток с привычным невынашиванием беременности, папилломавирусной инфекции, клещевом энцефалите [5, 8, 9] . В терапевтических дозах препарат нетоксичен (ЛД50 ~ 3000 терапевтических доз), хорошо переносится. Испытания показали отсутствие мутагенного, тератогенного, канцерогенного, аллер-гизирующего и эмбриотоксического действия.
Низкоинтенсивное лазерное излучение (НИЛИ) все шире применяется в самых различных областях медицины благодаря новым экспериментально-клиническим данным, свидетельствующим о высокой терапевтической эффективности, отсутствии осложнений и побочных эффектов [6]. Вторичные эффекты представляют собой комплекс адаптационных и компенсационных реакций, возникающих в результате реализации первичных эффектов в тканях, направленных на их восстановление: активизацию метаболизма клеток и повышение их функциональной активности, стимуляцию репаративных процессов, противовоспалительное и иммуностимулирующее действие, активизацию микроциркуляции крови [6].
Применение низкоинтенсивного лазерного воздействия на кровь больных устраняет необходимость использования многочисленных препаратов, что обусловлено универсальным механизмом иммуномодулирующего эффекта лазерного излучения, что приводит к стимуляции недостаточного иммунного ответа и супрессии гиперактивных процессов. При однократном воздействии на венозную кровь больных происходит облучение 25% крови, что достаточно для достижения модулирующего эффекта проводимой процедуры и приводит к длительному действию с нормализацией показателей иммунитета, устранению клинических симптомов острых и хронических инфекционных процессов [6].
Целью настоящего исследования являлось совершенствование терапии воспалительных заболеваний мочеполового тракта, сопровождающихся реактивацией ЦМВИ с использованием низкоинтенсивного лазерного излучения.
Материалы и методы. Под наблюдением находилось 25 женщин с реактивированным течением ЦМВИ на фоне ВЗОМТ, обусловленным условно-патогенной флорой в возрасте от 18 до 29 лет. Средний возраст пациенток составил 23, 25±4, 28 лет, то есть наиболее сексуально активный репродуктивный период. Для сравнения применялись результаты обследования 120 здоровых женщин соответствующего возраста.
Для детекции цитомегаловирусной инфекции использовали ИФА с выявлением в сыворотке крови специфических анти-CMV класса IgM (качественный анализ) и класса IgG (количественный анализ). Вирусологическое выявление ЦМВ проводили на культуре фиб- робластов лёгких эмбриона человека, в крови, слюне, моче, отделяемом цервикального канала и влагалища. ДНК ЦМВ в соскобах из урогенитального тракта (УГТ) определялась посредством полимеразной цепной реакции (ПЦР).
Условно-патогенных и патогенных возбудителей инфекционных заболеваний УГТ у женщин исследовали регламентируемыми методами: микроскопическим, бактериологическим и молекулярно генетическим.
Полученные результаты были обработаны статистическими методами вариационного и корреляционного анализа на ПК «IBM/PC Pentium 4» с использованием пакета прикладных программ для статистической обработки «Excel 7» и «Statistica 17.0» с использованием метода χ2 с поправкой Йетса на непрерывность для нахождения различий между качественными показателями, для вычисления которого прибегали к построению «сетки 2х2» и «3х2» и с использованием критерия Стюдента, для нахождения различий между количественными показателями. Различия считались достоверными при значениях p≤0,05 и/или p≤0,001.
Антимикробная терапия определялась чувствительностью к антибиотикам микрофлоры, возможностью создания в очаге инфекции концентрации препаратов, подавляющих жизнедеятельность микроорганизмов, отсутствием или маловыраженным побочным действием на организм больного. Учитывая этиологию, патогенез, клиническую симптоматику, всем пациентам проводилась терапия в соответствии с клиническими рекомендациями7: джозамицин по 500 мг 3 раза в сутки или доксициклина моногидрат по 100 мг в сутки. В зависимости от топического диагноза курс составлял 10-20 суток. Препараты применялись в комбинации с метронидазолом по 500 мг 2 раза в день 5-10 дней и панавиром в форме раствора для внутривенных инъекций по 0,004 мг - 3 инъекции через 48 часов в течение первой и 2 инъекции с интервалом 72 часа в течение второй недели. Одновременно назначалась комбинированная методика внутривенного лазерного облучения крови при помощи аппарата АЛТ «Матрикс-ВЛОК» с длиной волны 365 нм, 2 мВт (лазерное УФОК), 2 минуты + 530 нм, 2 мВт, 8 минут через день, всего 15 сеансов (8 сеансов лазерного УФОК и 7 сеансов ВЛОК зеленым спектром).
Результаты. При клиническом обследовании пациенток до лечения основные жалобы были представлены наличием повышенного количества выделений из влагалища, а также дизурическими расстройствами разной степени выраженности, неприятными ощущениями при половых контактах. Длительность перечисленных симптомов продолжалась в среднем от года до 2-х лет. Проведённое лечение способствовало выраженной регрессии клинических симптомов инфекционного поражения УГТ (табл. 1).
Таблица 1
Динамика жалоб
|
Жалобы |
Пациенты (n=25) абс/% |
Контр. группа (n=120) абс/% |
||
|
До лечения |
После лечения |
Через месяц после лечения |
||
|
Повышенное количество выделений |
21/84,00% |
0 |
0 |
32/26,67% |
|
Дизурия |
4/16,00% |
0 |
0 |
0 |
|
Зуд генитальной области |
1/4,00% |
0 |
1/4,00% |
14/11,67% |
|
Дискомфорт в генитальной области |
4/16,00% |
1/4,00% |
1/4,00% |
21/17,50% |
|
Тазовые боли |
0 |
0 |
0 |
0 |
|
Диспареуния |
5/20,00% |
0 |
0 |
0 |
|
Жалобы отсутствуют |
3/12,00% |
24/96,00% |
24/96,00% |
82/68,33% |
Примечание * различия достоверны по сравнению с показателями до лечения при p≤0,05
Осмотр женщин зеркалами соответствовал динамике симптомов поражения УГТ у женщин, вызванного сочетанной вирусо-бактериальной инфекцией.
Таблица 2
Динамика данных гинекологического обследования
|
Клинические симптомы |
Пациенты (n=25) абс/% |
Контр. группа (n=120) абс/% |
||
|
До лечения |
После лечения |
Через месяц после лечения |
||
|
Гиперемия и отечность слизистой :
|
0 1/4,00% 2/8,00% 0 |
0 0 0 0 |
0 0 0 0 |
0 0 0 0 |
|
Контактная кровоточивость шейки матки |
2/8,00% |
0 |
0 |
0 |
|
Количество выделений:
|
0 8/32,00% 17/68,00% |
0 2/8,00%* 23/92,00%* |
0 3/12,00%* 22/88,00%* |
18/15,00% 39/32,50% 63/52,5% |
|
Запах выделений: |
0 |
0 |
0 |
0 |
|
Цвет выделений :
|
18/72,00% 7/28,00% 0 0 |
22/88,00% 3/12,00% 0 0 |
24/96,00%* 0 1/4,00% 0 |
114/95,00% 0 6/5,00% 0 |
|
Гомогенность выделений :
|
25/100% 0 0 |
25/100% 0 0 |
25/100% 0 0 |
120/100% 0 0 |
|
Вязкость выделений :
|
16/64,00% 9/26,00% |
19/76,00% 6/24,00% |
11/44,00%* 14/56,00%* |
103/85,83% 17/14,17% |
|
Болезненность при пальпации |
3/12,00% |
0 |
0 |
0 |
|
Наличие спаечного процесса в м/тазу |
3/12,00% |
2/8,00% |
1/4,00% |
16/13,33% |
Примечание: * различия достоверны по сравнению с показателями до лечения при p≤0,05
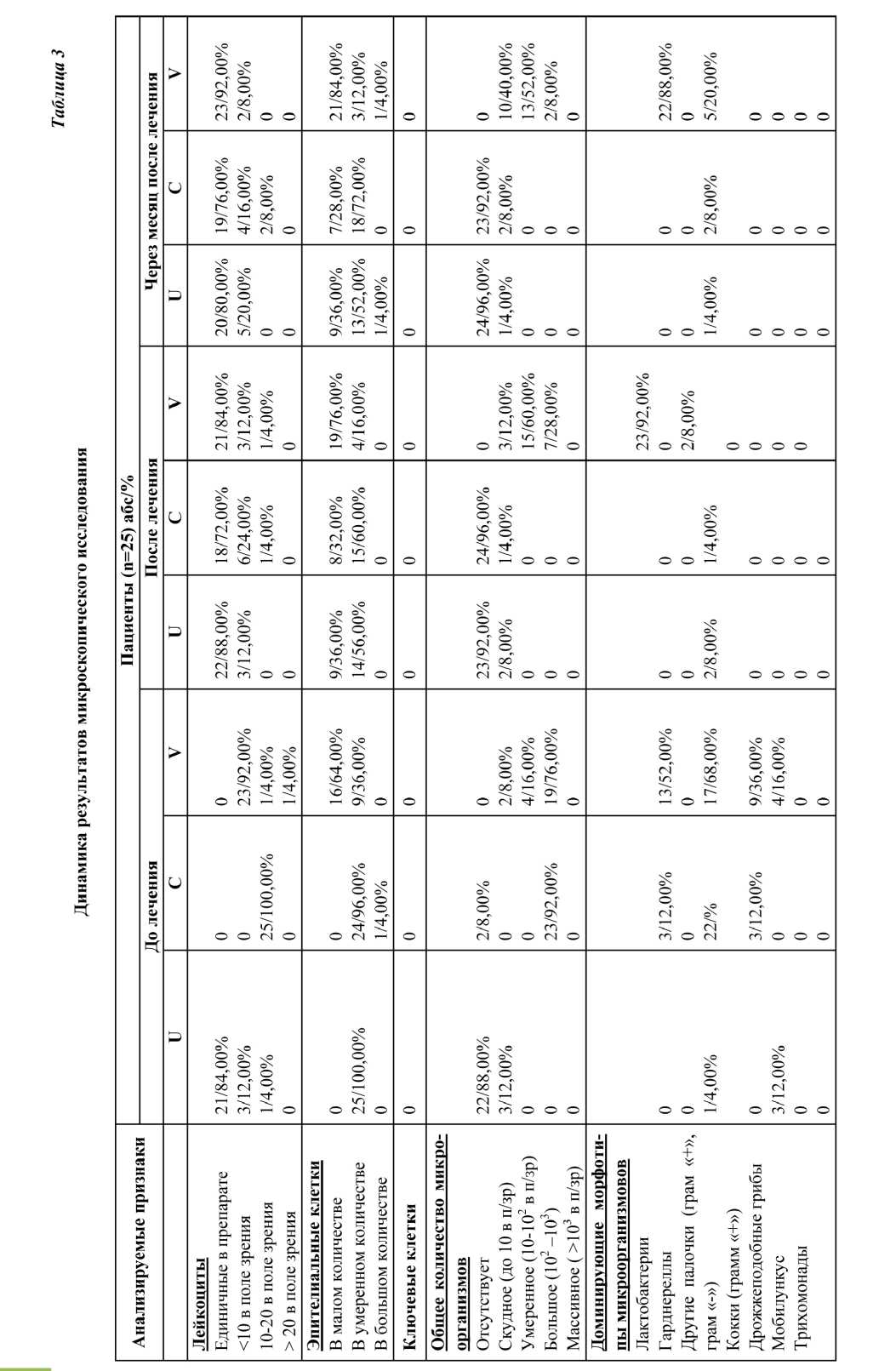
Из таблицы видно, что проведённое комплексное лечение способствовало устранению явлений гиперемии и отёчности слизистых оболочек половых органов у большинства больных. После лечения было констатировано преобладание пациенток со скудными выделениями преимущественно белого цвета и гомогенного характера. Важно подчеркнуть, что лечение способствовало достоверному уменьшению количества больных с болезненностью придатков при пальпации. Эффективность проводимого лечения оценивалась с использованием комплекса лабораторных тестов с целью всестороннего изучения реакции микроорганизмов и организма в целом на предложенный комплексный метод терапии. Показатели таблицы №3 свидетельствуют о выраженной эффективности проводимой комплексной терапии. Динамика результатов микроскопического исследования характеризовалась достоверным уменьшением количества пациенток с лейкоцитозом и с активным выделением микроорганизмов.
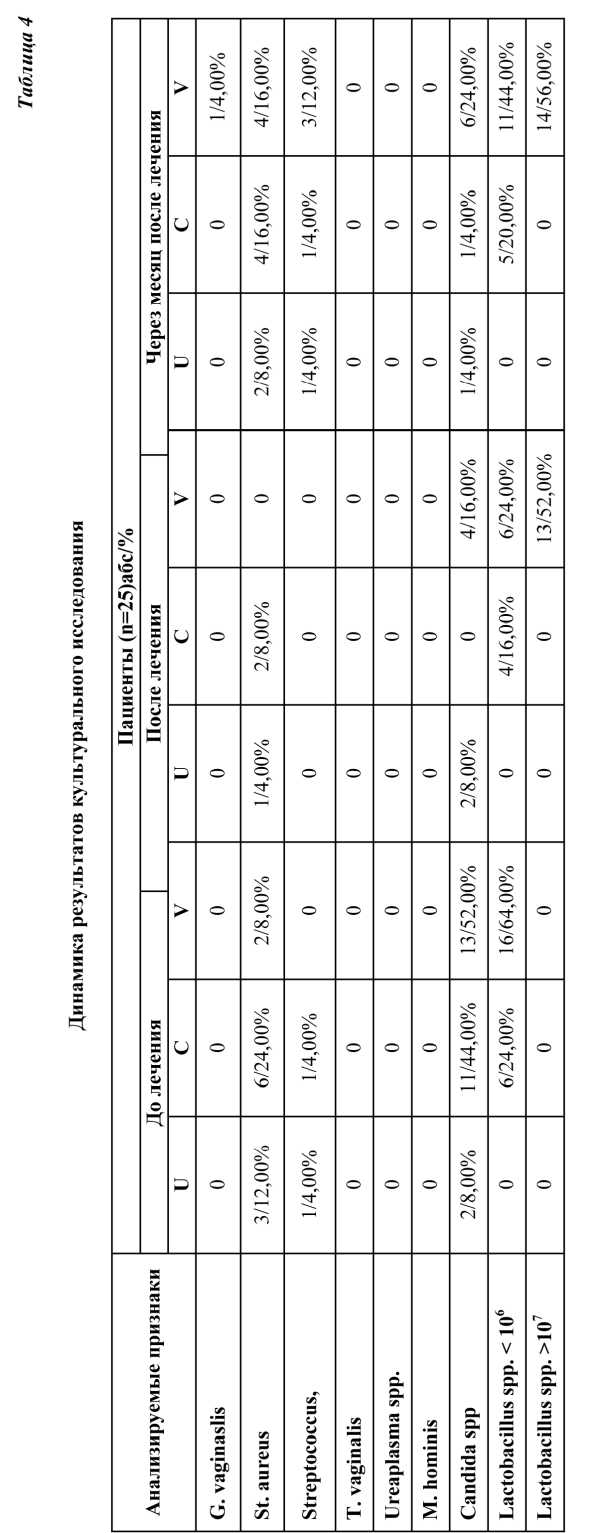
Результаты культурального исследования в динамике также иллюстрировали высокую эффективность проведенного лечения. Рост условно-патогенной флоры отмечался в единичных случаях после лечения, а облигатные патогены не выявлялись, тогда, как количество женщин с нормальными показателями роста лактобактерий увеличилось с 64% (p≤0,05) до 76% (p≤0,05) (табл. 4).
Для определения эффективности проводимой терапии была произведена оценка динамики маркёров цитомегаловирусной инфекции у обследованных женщин (табл. 5).
Таблица 5
Соотношение пациенток по выявлению маркёров CMV в результате лечения
|
Маркёры CMV |
Пациенты(n=25)абс/% |
||
|
До лечения |
После лечения |
Через месяц после лечения |
|
|
ДНК CMV из урогенитального тракта |
25/100,00% |
4/16,00% |
2/8,00% |
|
CMV в культуре фибробластов эмбрионов человека при исследовании крови |
0 |
0 |
0 |
|
CMV в культуре фибробластов эмбрионов человека при исследовании мочи |
14/56,00% |
0 |
0 |
|
CMV в культуре фибробластов эмбрионов человека при исследовании слюны |
0 |
0 |
0 |
|
CMV в культуре фибробластов эмбрионов человека при исследовании влагалищных выделений |
7/28,00% |
1/4,00% |
0 |
|
CMV в культуре фибробластов эмбрионов человека при исследовании отделяемого шейки матки |
25/100,00% |
3/12,00% |
2/8,00% |
|
Анти-CMV IgG в крови |
25/100,00% |
25/100,00% |
25/100,00% |
|
Анти-CMV IgM в крови |
0 |
0 |
0 |
Примечание * различия достоверны по сравнению с показателями до лечения при p≤0,05
Из таблицы видно, что поводом для постановки диагноза реактивации ЦМВИ служило обнаружение CMV в соскобах при исследовании с помощью ПЦР и на культуре фибробластов в моче, слюне, влагалищных выделениях и отделяемом шейки матки. В результате лечения при исследовании влагалищных выделений и отделяемого из шейки матки на культуре фибробластов эмбрионов человека, рост ЦМВ определялся в 1/4,00% и 3/12,00% (p≤0,05) случаях соответственно. Вирусологическое исследование слюны, мочи и крови показало отрицательный результат после лечения и через месяц наблюдения за больными.
Все пациентки переносили лечение хорошо, побочных эффектов или аллергических реакций отмечено не было.
Таким образом, результаты исследования демонстрируют высокую эффективность предложенного комплексного метода лечения с использованием противовирусных и антибактериальных препаратов в сочетании с низкоинтенсивным лазерным облучением крови. Необходимо отметить, что при наблюдении за пациентками в течение месяца показатели лабораторных исследований продолжали улучшаться, что объясняется пролонгированным воздействием лазерной терапии за счёт плеотропного эффекта на иммунный ответ и состояние микробиоценоза.
Список литературы Внутривенное лазерное облучение крови в лечении цитомегаловирусной инфекции у женщин
- Landini M.P., et al. Humoral Immune Response to Proteins of Human Cytomegalovirus Latency -Associated Transcripts.//Biol. of Blood and Marrow Transplantation, v.6: 100-108, 2000.
- Германенко, И.Г., Кудин А.П. Цитомегаловирусная инфекция: этиология, патогенез, клиника, диагностика, лечение. Пособие для врачей. -Минск: «Зималетто», 2009. -36 с.
- Ф.И.Ершов, Н.В.Касьянова, Цитомегаловирусная инфекция (современные данные об эпидемиологии, клинике, диагностике и терапии)/Сonsilium medicum. Том 04. N4. 2002, С.24.
- Козлова В.И., Пухнер А.Ф. Вирусные, хламидийные и микоплазменные заболевания гениталий. Санкт-Петербург, «Ольга», -2000. С. 36-40.
- Кархалис Л.Ю., Кучеров В.А., Стовбун С.В., Сафронов Д.Ю. «Оценка эффективности использования панавира в различных формах у пациенток репродуктивного возраста с цитомегаловирусной инфекцией»//Российский вестник акушера-гинеколога, 4, 2011, С. 90-93.
- Москвин С.В. Эффективность лазерной терапии. -М.:НПЛЦ «Техника», 2003. -256 с.
- Кубанова А.А. и соавторы, Ведение больных инфекциями, передаваемыми половым путем, и урогенитальными инфекциями, Клинические рекомендации, Москва, Деловой Экспресс, 2012, 112 с.
- Прилепская В.Н, Сергиенко В.И. Лечение цитомегаловирусной инфекции/Вопросы гинекологии, акушерства и перинатологии. Том 5. №3. 2006, С. 43-46.
- Гомберг М.А., Сергиенко В.И Новое в лечении вирусных инфекций, передающихся половым путем/Медицинская кафедра.


