Водный макрофит наяда мелкозубчатая в доочистке сточных вод
Автор: Быкова Галина Сергеевна, Шаталаев Иван Федорович, Воронин Александр Васильевич
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Промышленная экология
Статья в выпуске: 1-8 т.13, 2011 года.
Бесплатный доступ
В работе проведено исследование способности поглощения наядой мелкозубчатой (Najas microdon) металлов, фенольных соединений, а также ароматических аминов из образцов сточных вод. Показана возможность и целесообразность использования наяды мелкозубчатой для проведения доочистки сточных вод.
Загрязнение, сточные воды, металлы, фенолы, нафтолы, ароматические амины, наяда мелкозубчатая
Короткий адрес: https://sciup.org/148199964
IDR: 148199964 | УДК: 581.6:614.777:574.635
Aquatic macrophyte Najas microdon in sewage afterpurification
Research the ability of absorption by Najas microdon metals, phenolic compounds and also aromatic amines from samples of sewage is conducted in work. Possibility and expediency of using Najas microdon for carrying out the sewage afterpurification is shown.
Текст научной статьи Водный макрофит наяда мелкозубчатая в доочистке сточных вод
растительность способствует окислению органических веществ бактериями, одновременно используя полученные продукты распада для своей жизнедеятельности. Способность макрофитов к накоплению, утилизации, трансформации многих загрязняющих веществ позволяет использовать их для доочистки сточных вод от биогенных элементов, различных органических загрязнителей (в том числе и от нефтепродуктов), тяжелых и других металлов [3, 4].
Разные виды растений обладают неодинаковой степенью устойчивости к токсикантам. То, что способность поглощения зависит от различных факторов – вида растения (и даже подвида), его физиологических особенностей, возраста и стадии развития, от условий среды его обитания, отмечается разными авторами [5-7]. Выбор растения для доочистки воды диктуется также климатическими условиями. В умеренных широтах в зимний период использование большинства предлагаемых высших водных растений ограничено, поскольку при пониженных температурах их фотосинтезирующие части, находящиеся над водой, погибают. В связи с этим интерес представляют полностью погруженные в воду растения. К таковым относится наяда мелкозубчатая (Najas microdon).
Наяда мелкозубчатая – многолетнее растение из семейства наядовых (Najadaceae). Это вечнозеленое, многолетнее растение тропического происхождения с тонкими ломкими ветвистыми стеблями, с расположенными на них узколинейными листьями светло-зеленого цвета. Неприхотливое, легко размножается вегетативно – небольшие фрагменты побега быстро формируют новые растения. Питательные вещества наяда «всасывает» всей своей поверхностью.
Может существовать как в толще воды, так и в укорененном виде. Корневая система слабая, служит в основном для прикрепления растения. Оптимальный температурный режим жизнедеятельности наяды мелкозубчатой находится в интервале +12°С до +25°С.
Цель работы: исследование способности наяды мелкозубчатой поглощать из водных растворов некоторые металлы, а также органические вещества ряда ароматических аминов и ряда фенолов из образцов сточной воды.
Материалы и методы исследования. Объектом нашего исследования являлась фитомасса наяды мелкозубчатой (Najas microdon). Из числа наиболее распространенных фенольных компонентов сточных вод для эксперимента нами были выбраны фенол, о- крезол, м- аминофенол, тимол, пирокатехин, гидрохинон, резорцин, 1- и 2-нафтол. Из числа представителей ряда ароматических аминов были выбраны анилин, антраниловая кислота, о- толуидин, сульфаниловая кислота, сульфаниламид, бензидин, п- нитроанилин. Для исследования динамики поглощения органических соединений фитомассу наяды мелкозубчатой из расчета 5 г на 1 л раствора (сырой вес) помещали в водные растворы указанных веществ с концентрацией 50 мг/л (для бензидина, п- нитроанилина -10 мг/л). Отбор проб воды проводили с интервалом в 1 сутки в течение нескольких дней. Количественное определение ароматических аминов в водных растворах проводили с помощью фотометрического метода, основанного на образовании азокрасителя при взаимодействии диазотированного анализируемого первичного ароматического амина и тимола в щелочной среде [8]. Количественное определение содержания фенольных соединений в водных растворах проводили с помощью фотометрического метода, основанного на образовании окрашенных соединений фенола, его производных и гомологов с 4-аминоантипирином в присутствии калия гексацианоферрата (III) в щелочной среде [1]. Параллельно проводили анализ проб воды «контрольных» растворов органических веществ (без наяды мелкозубчатой) с такими же концентрациями. Интенсивность поглощения органического вещества рассчитывали как разницу между концентрациями вещества в «контрольном» и опытном растворах, отнесенную к 1 г фитомассы наяды мелкозубчатой. Таким образом, учитывали естественную убыль растворенного загрязнителя (аутоокисление).
Для выявления способности поглощения металлов в период с марта по сентябрь 2010 г. производился забор образцов сточных вод после первичного отстойника очистных сооружений МП «Самараводоканал». В исследуемых образцах сточных вод методом атомно-эмиссионной спектрометрии определяли содержание металлов – железа, цинка, меди, никеля, алюминия – в соответствии с нормативно-техническим документом [9]; прибор – эмиссионный спектрометр с индуктивно-связанной плазмой Optima 4000. Исследовали динамику поглощения фитомассой наяды мелкозубчатой вышеуказанных металлов из образцов сточных вод. Экспозиция фитомассы в образцах сточных вод составляла 12 часов; отбор проб воды производили с интервалом 3 часа; содержание фитомассы в сточной воде – 5 и 10 г/л.
Результаты и их обсуждение. Установлено, что присутствие наяды мелкозубчатой способствует снижению концентрации ароматических аминов и фенольных соединений в водных растворах. Интенсивность извлечения органического загрязнителя неодинакова и зависит от его природы. Исследования показали, что среди ароматических аминов наяда мелкозубчатая из водных растворов с концентрацией 50 мг/л наиболее эффективно поглощает анилин и антраниловую кислоту (рис. 1). Эффективность поглощения анилина наядой за 6 суток эксперимента составила 100%, тогда как концентрация его в контрольном растворе снизилась на 18,5%. Наличие в ароматическом кольце анилина в орто-положении карбоксильной группы приводит к небольшому снижению эффективности поглощения: антраниловая кислота за 10 суток эксперимента наядой поглощена на 98%, в контрольном растворе убыль составила 3%. При наличии в ароматическом кольце анилина других функциональных групп или углеводородных радикалов наблюдали значительное снижение эффективности поглощения (рис. 2). Убыль о- толуидина, сульфаниловой кислоты и ее амида в опытном растворе с наядой составила соответственно 32; 7 и 3%, в контрольном растворе – 24; 1,5 и 0%. Бензидин и п- нитроанилин из растворов с концентрацией 10 мг/л были поглощены наядой соответственно на 15 и 5%, в контрольном растворе их содержание осталось неизменным.
Исследования показали, что двухатомные фенолы (пирокатехин, гидрохинон, резорцин) поглощаются быстрее, чем монофенол. Интенсивность поглощения о- крезола ( о- метилфенола) сопоставима с таковой для фенола. Скорость поглощения м- аминофенола и тимола (2-изопропил-5-метилфенола) значительно меньше. Поглощение нафтолов наядой несколько менее эффективно, чем двухатомных фенолов, но тоже достаточно велико (рис. 3, 4).
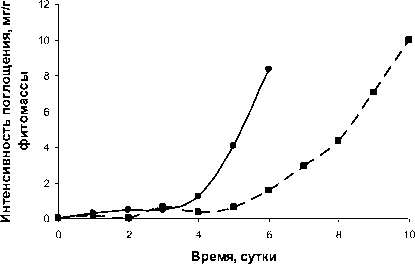
—•— Анилин
—■— Антраниловая кислота
Рис. 1. Интенсивность поглощения из водных растворов анилина, антраниловой кислоты наядой мелкозубчатой с плотностью фитомассы 5 г/л
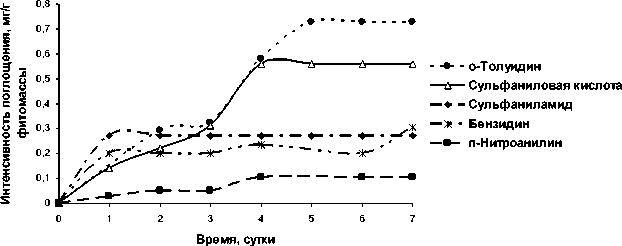
Рис. 2. Интенсивность поглощения из водных растворов о- толуидина, сульфаниловой кислоты, сульфаниламида, бензидина, п- нитроанилина наядой мелкозубчатой с плотностью фитомассы 5 г/л
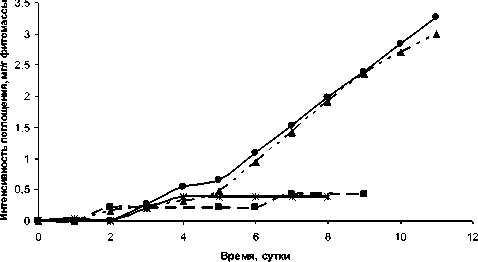
—•— Фенол
—* - о-Крезол
—■— м-Аминофенол
Тимол
Рис. 3. Интенсивность поглощения из водных растворов фенола, о- крезола, м- аминофенола, тимола наядой мелкозубчатой с плотностью фитомассы 5 г/л
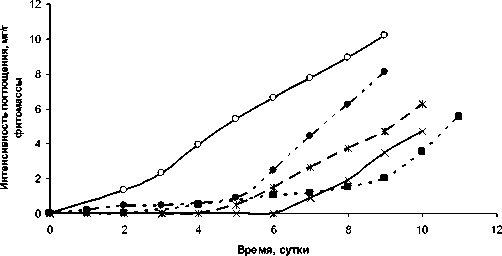
Пирокатехин
—е- - Гидрохинон 1-Нафтол 2-Нафтол
- -■- - Резорцин
Рис. 4. Интенсивность поглощения из водных растворов пирокатехина, гидрохинона, резорцина, 1- и 2-нафтолов наядой мелкозубчатой с плотностью фитомассы 5 г/л
Установлено также, что снижение концентраций фенольных соединений в растворах с наядой мелкозубчатой значительно выше, чем в контрольных растворах без растения. Так, в растворах с наядой содержание фенола снизилось на 34 %, о- крезола – на 41%. В контрольных растворах без растения наблюдали снижение концентрации фенола – 0%, о- крезола – 10%. Аутоокисление растворов двухатомных фенолов составило 10-15%. Концентрации же этих веществ в опытных растворах снизились на следующие величины: пирокатехин – 77%, гидрохинон – 49%, резорцин – 39%. Опытные растворы с наядой мелкозубчатой 1-нафтола и 2-нафтола показали снижение концентрации на 86 и 69% соответственно. В контрольных растворах в результате аутоокисления наблюдали убыль 1-нафтола на 39%, 2-нафтола – на 11%. Концентрация тимола снизилась на 23% при аутоокислении 19%, убыль содержания м- аминофенола составила 6% при аутоокислении 2%.
Наблюдения показали, что при окислении пирокатехина, 1-нафтола и 2-нафтола наядой мелкозубчатой образуются окрашенные вещества. Можно предположить, что образуется смесь различных продуктов конденсации фенолов и хинонов. Экспонирование наяды в растворах 1-нафтола и 2-нафтола на 10 сутки привело к появлению начальных признаков хлороза. После эксперимента растение не восстанавливалось и примерно на 14 сутки погибало. При экспонировании наяды в растворе пирокатехина на 9 сутки наблюдали изменение внешнего вида растения: появились признаки нежизнеспособности, ярко-зеленая окраска сменилась на бурую, растение выглядело как будто «обожженным». Примерно на 12 сутки растение погибало. В растворах других фенольных соединений, а также в растворах ароматических аминов изменений внешнего вида наяды мелкозубчатой не наблюдали. Тот факт, что пирокатехин, 1- и 2-нафтолы в концентрации 50 мг/л оказывают губительное действие на наяду мелкозубчатую, необходимо учитывать при залповых сбросах сточных вод, содержащих названные соединения.
Результаты измерения концентраций металлов (средние величины) в образцах сточных вод на различных этапах времени экспозиции в них фитомассы наяды мелкозубчатой представлены в таблицах 1 и 2. В отобранных образцах сточных вод диапазон исходных концентраций металлов был следующим: Fe (общее) – 0,257-0,672 мг/л; Zn – 0,0611-0,1010 мг/л; Cu – 0,0110-0,0520 мг/л; Ni – 0,00260,0042 мг/л; Al – 0,1680-0,4090 мг/л. Группа измерений при плотности фитомассы наяды мелкозубчатой 5 г/л составила 8 серий, при плотности 10 г/л – 5 серий.
Таблица 1. Динамика поглощения металлов из сточной воды наядой мелкозубчатой при плотности фитомассы 5 г/л
|
Металл |
Концентрация средняя, мг/л |
||||
|
исходная |
время экспозиции наяды мелкозубчатой |
||||
|
3 часа |
6 часов |
9 часов |
12 часов |
||
|
железо общее |
0,4991 |
0,3039 |
0,2619 |
0,3549 |
0,3547 |
|
цинк |
0,0785 |
0,0365 |
0,0349 |
0,0451 |
0,0471 |
|
медь |
0,0184 |
0,0180 |
0,0088 |
0,0110 |
0,0116 |
|
никель |
0,0036 |
0,0029 |
0,0029 |
0,0029 |
0,0032 |
|
алюминий |
0,3188 |
0,1212 |
0,1107 |
0,1598 |
0,1365 |
Таблица 2. Динамика поглощения металлов из сточной воды наядой мелкозубчатой при плотности фитомассы 10 г/л
|
Металл |
Концентрация средняя, мг/л |
||||
|
исходная |
время экспозиции наяды мелкозубчатой |
||||
|
3 часа |
6 часов |
9 часов |
12 часов |
||
|
железо общее |
0,3297 |
0,3150 |
0,1953 |
0,2243 |
0,1603 |
|
цинк |
0,0420 |
0,0420 |
0,0335 |
0,0400 |
0,0285 |
|
медь |
0,0234 |
0,0074 |
0,0065 |
0,0081 |
0,0060 |
|
никель |
0,0036 |
0,0032 |
0,0024 |
0,0027 |
0,0025 |
|
алюминий |
0,2423 |
0,1297 |
0,1037 |
0,1303 |
0,1037 |
Для всех рассмотренных случаев наблюдается положительная динамика поглощения металла фитомассой наяды мелкозубчатой.
Основное количество загрязнителя поглощается в первые 6 часов эксперимента. Максимальное поглощение в первые 3 часа характерно для Fe, Zn и Ni при плотности фитомассы 5 г/л; для Cu – при 10 г/л; для Al – при 5 и 10 г/л. Максимальное поглощение на момент 6 часов экспозиции характерно для Fe, Zn и Ni при плотности фитомассы 10 г/л; для Cu – при 5 г/л. Некоторое увеличение концентрации металлов в образцах сточных вод наблюдается после 9 часов экспозиции фитомассы наяды мелкозубчатой. Установлено, что в указанных концентрациях перечисленные металлы не оказывают заметного токсического действия на наяду мелкозубчатую.
В целом результаты проведенных опытов согласуются с предположением, что в присутствии наяды мелкозубчатой в воде ускоряется снижение концентрации загрязнителей.
Выводы: полученные данные указывают на перспективность использования макрофита наяды мелкозубчатой (Najas microdon) для целей фиторемедиации в условиях загрязнения воды ароматическими аминами, фенольными соединениями, металлами.
Список литературы Водный макрофит наяда мелкозубчатая в доочистке сточных вод
- Лурье, Ю.Ю. Аналитическая химия промышленный сточных вод. -М.: Химия, 1984. 448 с.
- Исидоров, В.А. Введение в химическую токсикологию. -СПб.: Химиздат, 1999. 144 с.
- Артамонов, В.И. Растения и чистота природной среды. -М.: Наука, 1986. 172 с.
- Диренко, А.А. Использование высших водных растений в практике доочистки сточных вод и поверхностного стока/А.А. Диренко, А.В. Кнуса, Е.М. Коцарь//Водоочистка. 2006. № 3. С. 70-73.
- Стом, Д.И. Значение окисления в детоксикации фенолов водными растениями//Самоочищение воды и миграция загрязнений по трофической цепи. -М.: Наука, 1984. С. 91-97.
- Дикиёва, Д. Химический состав макрофитов и факторы, определяющие концентрацию минеральных веществ в высших водных растениях/Д. Дикиёва, И.А. Петрова//Гидробиологические процессы в водоемах. -Л.: Наука, 1983. С. 107-213.
- Лукина, Л.Ф. Физиология высших водных растений/Л.Ф. Лукина, Н.Н. Смирнова. -К.: Наукова думка, 1988. 187 с.
- Полюдек-Фабини, Р. Органический анализ: Руководство по анализу органических соединений, в том числе и лекарственных веществ/Р. Полюдек-Фабини, Т. Бейрих. Пер. с нем. -Л.: Химия, 1981. 624 с.
- ПНДФ 14.1:2:4.135‑98 «Методика выполнения измерений массовых концентраций металлов методом атомно-эмиссионной спектрометрии с индуктивно-связанной плазмой в питьевой, природной и сточной водах и атмосферных осадках».


