Водородные и галогенные связи в трииодаминобензоатах азотистых оснований
Автор: Жеребцов Д.А., Шарутин В.В., Найферт С.А., Регель Р.Л., Раджакумар К., Адонин С.А., Полозов М.А., Спиридонова Д.В., Осипов А.А., Луценко А.И.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 1 т.16, 2024 года.
Бесплатный доступ
Описана кристаллическая структура трех органических солей трииодаминобензойной кислоты (1-3) и моногидрата трииодаминобензойной кислоты (4), особенности строения установлены методом РСА. Соединение 1: C20H19I6N3O6, М 1158,78; моноклинная сингония, пространственная группа - Сс; параметры ячейки: a = 32,0782(10), b = 9,5284(3), c = 9,3745(3) Å; a = 90, β = 90,0(1), g = 90 град; V = 2865,35(16) Å3, Z = 4, ρрасч. = 2,684 г/см3. Соединение 2: C16H15I6N3O4, М 1074,71; моноклинная сингония, пространственная группа - P21/c; параметры ячейки: a = 8,990(5), b = 28,541(11), c = 9,945(5) Å; a = g = 90, β = 91,23(2) град; V = 2551(2) Å3, Z = 4, ρрасч. = 2,798 г/см3. Соединение 3: C17H17I3N2O4, М 694,03; моноклинная сингония, пространственная группа - I2/a; параметры ячейки: a = 36,02(2), b = 7,254(5), c = 16,468(9) Å; a = g = 90, β = 105,29(2) град; V = 4150(4) Å3, Z = 8, ρрасч. = 2,222 г/см3. Соединение 4: C7H6I3NO3, М 532,83; ромбическая сингония, пространственная группа - Iba2; параметры ячейки: a = 30,2146(4), b = 13,9830(2), c = 5,80740(10) Å; a = β = g = 90 град; V = 2453,57(6) Å3, Z = 8, ρрасч. = 2,885 г/см3. Кристаллическая структура двух солей и моногидрата трииодаминобензойной кислоты отличается как доминированием водородных связей, так и наличием множества галогенных связей. Однако соль 7-метилхинолина лишена галогенных связей вследствие особенностей стопочной упаковки плоских молекул. Для двух соединений (3 и 4) определены особенности их термолиза методом синхронного термического анализа (атмосфера - аргон): на первом этапе (52 и 73 °С соответственно) происходит потеря кристаллизационной воды; при 700 °С в условиях термолиза обоих соединений продуктом разложения является стеклоуглерод.
Водородные связи, галогенные связи, трийодаминобензойная кислота, азотистые основания, термолиз
Короткий адрес: https://sciup.org/147243266
IDR: 147243266 | УДК: 548.3 | DOI: 10.14529/chem240111
Нydrogen and halogen bonds in triiodoaminobenzoates of amine bases
The crystalline structures of three organic salts of triiodoaminobenzoic acid (1-3) and triiodoaminobenzoic acid monohydrate (4) are described, the structural features are established by the X-ray diffraction method. Compound 1: C20H19I6N3O6, М 1158.78; monoclinic syngony, space group Сс; cell parameters: a = 32.0782(10), b = 9.5284(3), c = 9.3745(3) Å; a = 90, β = 90,0(1), g = 90 deg.; V = 2865.35(16) Å3, Z = 4, ρcalc. = 2.684 g/cm3. Compound 2: C16H15I6N3O4, М 1074.71; monoclinic syngony, space group P21/c; cell parameters: a = 8.990(5), b = 28.541(11), c = 9.945(5) Å; a = g = 90, β = 91.23(2) deg.; V = 2551(2) Å3, Z = 4, ρcalc. = 2.798 g/cm3. Compound 3: C17H17I3N2O4, М 694.03; monoclinic syngony, space group I2/a; cell parameters: a = 36.02(2), b = 7.254(5), c = 16.468(9) Å; a = g = 90, β = 105.29(2) deg.; V = 4150(4) Å3, Z = 8, ρcalc. = 2.222 g/cm3. Compound 4: C7H6I3NO3, М 532.83; rhombic syngony, space group Iba2; cell parameters: a = 30.2146(4), b = 13.9830(2), c = 5.80740(10) Å; a = β = g = 90 deg.; V = 2453.57(6) Å3, Z = 8, ρcalc. = 2,885 g/cm3. The crystalline structure of two salts and triiodoaminobenzoic acid monohydrate is distinguished both by domination of hydrogen bonds and multiple halogen bonds. However, the 7-methylquinoline salt is devoid of halogen bonds due to peculiarities of the stack packaging of flat molecules. For two compounds (3 and 4), the features of their thermolysis by thermal analysis (in argon atmosphere) are determined: at the first stage (52 and 73 °C, respectively), the loss of crystallization water occurs; at 700 ° C under the thermolysis conditions of both compounds the decomposition product is glass carbon.
Текст научной статьи Водородные и галогенные связи в трииодаминобензоатах азотистых оснований
Исследование галогенных связей – нековалентных взаимодействий с участием атомов галогена – составляет быстро развивающуюся отрасль структурной химии [1–7]. Наиболее сильные взаимодействия обычно наблюдаются для иодированных соединений из-за высокой поляризуемости атома иода [8, 9].
3-амино-2,4,6-трииодбензойная кислота – соединение, используемое исследователями во многих областях химии: данная кислота является стандартным соединением при анализе свободных ароматических аминов в рентгенодиагностических исследованиях [10]; N,N'-адипил бис (3-амино-2,4,6-трииодбензойная кислота) – вещество, которое начали использовать в медицине с 50-х годов ХХ века при рентгенологических исследованиях желчных путей и желчного пузыря в качестве рентгеноконтрастного вещества [11].
Соединения трииодаминобензойной кислоты (HTriIABA) с алифатическими и ароматическими азотистыми основаниями представляют интерес с точки зрения формирования в них галогенных связей. Ранее были исследованы особенности нековалентных взаимодействий 2,4,6-трииод-3-аминобензоатов никеля, которые описаны в статье [12]. В качестве оснований удобны- ми объектами являются γ-пиколин, диметиламин и 7-метилхинолин. В работе рассмотрены результаты исследования трех солей, структура которых до сих пор не была известна: γ-Pic(TriIABA)∙(HTriIABA)∙2H2O (1) H2NMe2(TriIABA)∙(HTriIABA) (2) и 7MQuin(TriIABA)∙2H2O (3), а также моногидрата трииодаминобензойной кислоты HTriIABA∙H2O (4).
Экспериментальная часть
Соединения 1 и 3 были приготовлены смешением горячих растворов трииодаминобензойной кислоты и соответствующего основания в соотношении 1 : 1 в растворе вода – ДМФА (70 : 30). Соединение 2 образовалось при длительной выдержке в горячем растворе HTriIABA-вода-ДМФА из-за гидролиза ДМФА с образованием диметиламина. Кристаллы 1 – 3 выращены при медленном охлаждении раствора от 100 °С. Кристаллы 4 выращены при медленном испарении водного раствора HTriIABA. Процессы термолиза 3 и 4 исследовали с помощью синхронного термического анализатора Netzsch STA 449 F1 Jupiter в атмосфере аргона.
Исследование четырех структур было проведено в двух лабораториях с использованием мо-нокристальных дифрактометров: для 1 и 4 – Rigaku XtaLab Synergy-S с детектором HyPix-6000HE, для 2 и 3 – BRUKER D8 Quest.
Первичная обработка экспериментальных данных 1 и 4 и поправка на поглощение выполнены в пакете программ CrysAlisPro (Agilent Technologies) [13]. Сбор, редактирование данных и уточнение параметров элементарной ячейки для 2 и 3 , а также учет поглощения проведены с применением SMART и SAINT-Plus [14]. Структуры соединений 1 – 4 решены с использованием программ Olex2 [15], SHELXS [16] и уточнены в анизотропном приближении для неводородных атомов с помощью программы SHELXL [17]. Положения атомов водорода уточняли с использованием модели «наездника».
Таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджский банк структурных данных (№ 2110029 для 1, № 2048320 для 2, № 2045165 для 3, № 2159588 для 4; ; . Кристаллографические параметры структур и данные дифракционного эксперимента приведены в табл. 1.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур 1‒4
|
Параметр |
1 |
2 |
3 |
4 |
|
Молекулярная формула |
C 7 H 4 I 3 NO 2 , C 7 H 3 I 3 NO 2 –, C 6 H 8 N+, 2(H 2 O) |
C 7 H 4 I 3 NO 2 , C 7 H 3 I 3 NO 2 –, C 2 H 8 N+ |
C 7 H 3 I 3 NO 2 –, C 10 H 10 N+, 2(H 2 O) |
C 7 H 4 I 3 NO 2 , H 2 O |
|
Брутто-формула |
C 20 H 19 I 6 N 3 O 6 |
C 16 H 15 I 6 N 3 O 4 |
C 17 H 17 I 3 N 2 O 4 |
C 7 H 6 I 3 NO 3 |
|
Молекулярная масса |
1158,78 |
1074,71 |
694,03 |
532,83 |
|
Температура, K |
100,0(1) |
293(2) |
293(2) |
99,9(5) |
|
Сингония |
моноклинная |
моноклинная |
моноклинная |
ромбическая |
|
Пр. гр. |
Cc |
P 2 1 / c |
I2/a |
Iba2 |
|
a , b , c , Å |
32,0782(10), 9,5284(3), 9,3745(3) |
8,990(5), 28,541(11), 9,945(5) |
36,02(2), 7,254(5), 16,468(9) |
30,2146(4), 13,9830(2), 5,80740(10) |
|
α, β, γ, град |
90, 90,0(1), 90 |
90, 91,23(2), 90 |
90, 105,29(2), 90 |
90, 90, 90 |
|
Объем ячейки V , Å3 |
2865,35(16) |
2551(2) |
4150(4) |
2453,57(6) |
|
Z |
4 |
4 |
8 |
8 |
|
ρ расч. , г/см3 |
2,684 |
2,798 |
2,222 |
2,885 |
|
Коэффициент поглощения μ, мм–1 |
6,544 |
7,333 |
4,543 |
59,935 |
|
F (000) |
2104,0 |
1928.0 |
2592,0 |
1904,0 |
|
Размер кристалла, мм |
0,16 × 0,12 × 0,05 |
0,45 × 0,2 × 0,15 |
0,48 × 0,14 × 0,04 |
0,16 × 0,05 × 0,04 |
|
Излучение |
Mo K α (λ = 0,71073) |
Mo K α (λ = 0,71073) |
MoK α ( λ = 0,71073) |
CuK α (λ = 1,54184) |
|
Диапазон углов 2θ, град |
6,228–59,428 |
5,7–57,52 |
5,74–58,5 |
5,85–139,728 |
Окончание табл. 1
|
Параметр |
1 |
2 |
3 |
4 |
|
Диапазоны индексов |
–41 ≤ h ≤ 41 –12 ≤ k ≤ 12, –11 ≤ l ≤ 12 |
–11 ≤ h ≤ 11, –38 ≤ k ≤ 38, –12 ≤ l ≤ 13 |
–48 ≤ h ≤ 49, –9 ≤ k ≤ 9, –22 ≤ l ≤ 21 |
–36 ≤ h ≤ 36, –16 ≤ k ≤ 17, –7 ≤ l ≤ 6 |
|
Измерено отражений |
15640 |
43818 |
44771 |
13276 |
|
Независимые рефлексы |
6065 [ R int = 0,0228, R sigma = 0,0263] |
5937 [ R int = 0,0570, R sigma = 0,0344] |
5593 [ R int = 0,1228, R sigma = 0,0687] |
2288 [ R int = 0,0699, R sigma = 0,0421] |
|
Данные / ограничения / параметры |
6065/2/326 |
5937/0/266 |
5593/0/244 |
2288/1/108 |
|
F 2 |
1,022 |
1,226 |
1,101 |
1,044 |
|
Фактор сходимости R [I> = 2σ (I)] |
R 1 = 0,0169, wR 2 = 0,0358 |
R 1 = 0,0614, wR 2 = 0,1634 |
R 1 = 0,0711, wR 2 = 0,1812 |
R 1 = 0,0488, wR 2 = 0,1235 |
|
Фактор сходимости R [все данные] |
R 1 = 0,0177, wR 2 = 0,0362 |
R 1 = 0,0719, wR 2 = 0,1683 |
R 1 = 0,1110, wR 2 = 0,2028 |
R 1 = 0,0491, wR 2 = 0,1240 |
|
Остаточная электронная плотность, э·Å–3 |
0,37/–0,78 |
1,21/–2,05 |
2,35/–1,77 |
2,13/–1,47 |
Для соединений 2 и 4 (табл. 2) была произведена оптимизация структуры кристалла с периодическими граничными условиями с помощью программного обеспечения CRYSTAL17 [18], применяя обменно-корреляционный функционал B3LYP. Был использован модифицированный базисный набор DZVP для атома иода и базисный набор TZVP для остальных атомов в молекуле. Локализация равновесной геометрии велась с сохранением параметров ячейки кристаллов. Квантово-топологический анализ электронной плотности [19] для оптимизированных структур кристаллов был произведён с помощью программы TOPOND [20].
Для характеристики галогенных связей в исследуемых структурах был применён электронный критерий [21]. Эффективный электронный критерий характеристики связи основан на анализе положения минимумов распределения электронной плотности и электростатического потенциала вдоль линии, соединяющей атомы.
Таблица 2
Результаты топологического анализа структур 2 и 4
|
Нековалентная связь |
Тип связи |
Длина связи, эксперимент, Å |
Длина связи, расчёт, Å |
ρ ( r bcp ), ат. ед. |
∇ 2 ρ ( r bcp ), ат. ед. |
g( r bcp ), ат. ед. |
v( r bcp ), ат. ед. |
|
2 |
|||||||
|
I2∙∙∙H1A |
(I∙∙∙H–N), внутримол. |
2 , 834 |
2 , 7826 |
0 , 0143 |
0 , 0503 |
0 , 0110 |
–0 , 0095 |
|
I2∙∙∙H15 |
(I∙∙∙H–C), межмол. |
3 , 426 |
3 , 2705 |
0 , 0060 |
0 , 0167 |
0 , 0034 |
–0 , 0026 |
|
I2∙∙∙H5 |
(I∙∙∙H–C), межмол. |
3 , 407 |
3 , 3959 |
0 , 0058 |
0 , 0181 |
0 , 0036 |
–0 , 0027 |
|
I1∙∙∙H1B |
(I∙∙∙H–N), внутримол. |
3 , 522 |
2 , 7132 |
0 , 0156 |
0 , 0498 |
0 , 0110 |
–0 , 0096 |
|
I1∙∙∙O3 |
(I∙∙∙O=), межмол. |
2 , 990 |
2 , 9618 |
0 , 0173 |
0 , 0568 |
0 , 0126 |
–0 , 0110 |
|
I1∙∙∙H9B |
(I∙∙∙H–CN), межмол. |
3 , 855 |
3 , 2282 |
0 , 0061 |
0 , 0154 |
0 , 0032 |
–0 , 0025 |
|
I3∙∙∙O4 |
(I∙∙∙O–H), межмол. |
3 , 064 |
3 , 0037 |
0 , 0169 |
0 , 0539 |
0 , 0122 |
–0 , 0109 |
|
I5∙∙∙H15 |
(I∙∙∙H–C), межмол. |
3 , 398 |
3 , 4194 |
0 , 0052 |
0 , 0160 |
0 , 0032 |
–0 , 0024 |
Окончание табл. 2
|
Нековалентная связь |
Тип связи |
Длина связи, эксперимент, Å |
Длина связи, расчёт, Å |
ρ ( r bcp), ат. ед. |
∇ 2 ρ ( r bcp ) , ат. ед. |
g( r bcp ), ат. ед. |
v( r bcp ), ат. ед. |
|
I6∙∙∙O2 |
(I∙∙∙O=), межмол. |
3 , 000 |
2 , 9305 |
0 , 0181 |
0 , 0608 |
0 , 0137 |
–0 , 0121 |
|
I4∙∙∙H8A |
(I∙∙∙H–CN), межмол. |
3 , 382 |
3 , 2737 |
0 , 0054 |
0 , 0141 |
0 , 0029 |
–0 , 0022 |
|
O2∙∙∙H9C |
(O∙∙∙H–CN), межмол. |
2 , 430 |
2 , 2725 |
0 , 0117 |
0 , 0476 |
0 , 0093 |
–0 , 0067 |
|
O2∙∙∙H9A |
(O∙∙∙H–CN), межмол. |
2 , 685 |
2 , 4547 |
0 , 0084 |
0 , 0316 |
0 , 0062 |
–0 , 0046 |
|
O3∙∙∙H1 |
(=O∙∙∙H–O), межмол. |
1 , 760 |
1 , 4838 |
0 , 0758 |
0 , 1491 |
0 , 0607 |
–0 , 0840 |
|
O4∙∙∙H3A |
(H–O∙∙∙H– CN), межмол. |
2 , 266 |
2 , 1074 |
0 , 0166 |
0 , 0694 |
0 , 0140 |
–0 , 0107 |
|
O4∙∙∙N3 |
(H–O∙∙∙N– (CH 3 ) 2 ), межмол. |
2 , 803 |
2 , 8046 |
0 , 0372 |
0 , 1238 |
0 , 0323 |
–0 , 0336 |
|
O1∙∙∙H8B |
(H–O∙∙∙H– CN), меж-мол. |
2 , 855 |
2 , 6095 |
0 , 0064 |
0 , 0229 |
0 , 0045 |
–0 , 0032 |
|
4 |
|||||||
|
I1∙∙∙O3 |
(I∙∙∙OH 2 ), межмол. |
3 , 075 |
3 , 0736 |
0 , 0143 |
0 , 0464 |
0 , 0101 |
–0 , 0086 |
|
I2∙∙∙H1A |
(I∙∙∙H–N), внутримол. |
2 , 992 |
2 , 7544 |
0 , 0144 |
0 , 0495 |
0 , 0108 |
–0 , 0092 |
|
I2∙∙∙H4 |
(I∙∙∙H–C), межмол. |
3 , 484 |
3 , 4795 |
0 , 0044 |
0 , 0135 |
0 , 0026 |
–0 , 0019 |
|
I3∙∙∙I3 |
(I∙∙∙I), межмол. |
3 , 973 |
3 , 9228 |
0 , 0086 |
0 , 0203 |
0 , 0044 |
–0 , 0037 |
|
O2∙∙∙H3A |
(=O∙∙∙H– OH), межмол. |
1 , 887 |
1 , 6656 |
0 , 0478 |
0 , 1434 |
0 , 0419 |
–0 , 0480 |
|
O2∙∙∙H3B |
(=O∙∙∙H– OH), межмол. |
1,926 |
1,7701 |
0 , 0332 |
0 , 1231 |
0 , 0302 |
–0 , 0297 |
|
N1∙∙∙H1A |
(N∙∙∙H–N), межмол. |
2,721 |
2,4866 |
0 , 0098 |
0 , 0324 |
0 , 0064 |
–0 , 0048 |
Обсуждение результатов
Во всех четырех структурах решающую роль играют ионные и водородные связи. В соединениях 1 – 3 происходит перенос протона от карбоксильной группы на неподеленную электронную пару азота органического основания с образованием ионной соли (рис. 1–3). Перенос протона происходит благодаря значительной разнице в константах диссоциации оснований и кислоты. рК а сопряженной кислоты для γ-пиколина и диметиламина равны соответственно 6,05 [22] и 10,64 [23]. Для 7-метилхинолина эта величина неизвестна, но может быть равна 5,0–6,0, поскольку для хинолина она равна 4,94 [24]. По собственным измерениям рКа трииодаминобензойной кислоты равна 3,3, что существенно отличается от бензойной и м-аминобензойной кислоты (4,21 и 4,74 соответственно) благодаря электроноакцепторным свойствам атомов галогена.
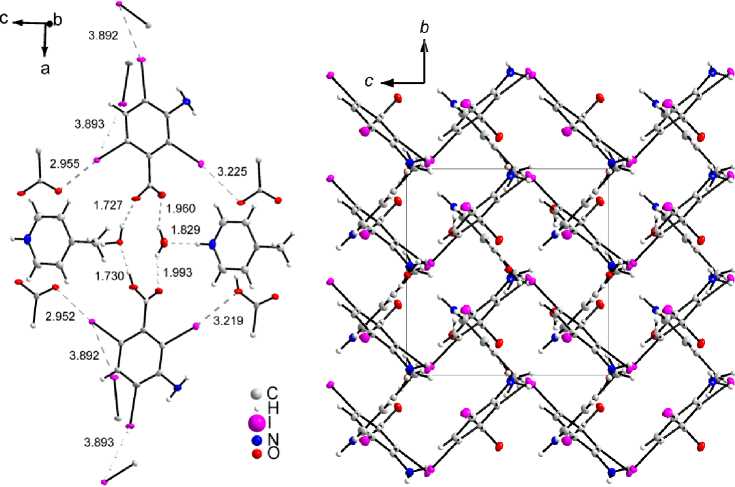
Строение солей 1–3 типично для ионных структур, в них отрицательно заряженные атомы кислорода карбоксильных групп анионов ориентированы в направлении атомов азота, несущих положительный заряд в органическом катионе. Соединения 1 и 2 относятся к кислым солям, в них содержатся два эквивалента кислоты на один эквивалент основания. Две молекулы кислоты в них связаны друг с другом с помощью водородных связей, образованных непосредственно между двумя карбоксильными группами в случае соединения 2 или опосредованно через две молекулы воды в случае 1 (рис. 1, 2). Один из протонов кислоты находится у неподеленной электронной пары атома азота γ-пиколина, второй сложно поддается локализации и находится, по-видимому, у неподеленных электронных пар молекул воды или у карбоксильной группы. Расстояния O···O между атомами, образующими в 1 водородную связь, составляют 2,58 и 2,79 Å. Следует отметить и водородную связь длиной 1,812 Å между протоном у пиколина и молекулой воды.
а) б)
Рис. 1. Структура соединения 1. Разорванные линии обозначают водородные связи и кратчайшие контакты I···I и I···O. На рисунках часть атомов соседних молекул опущена для ясности
а) б)
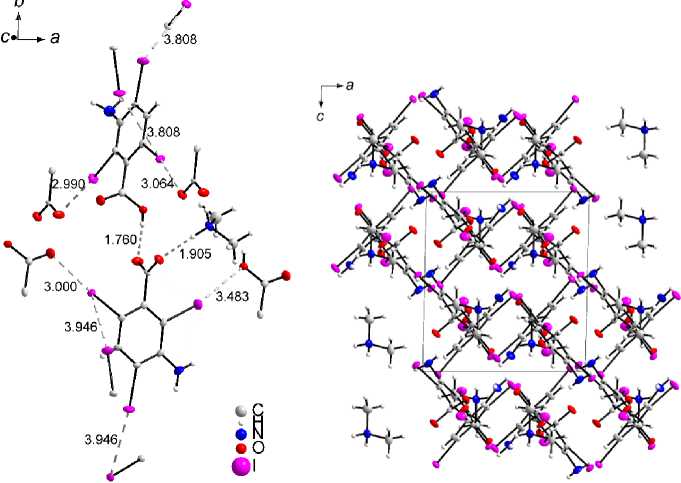
Рис. 2. Структура соединения 2. Разорванные линии обозначают водородные связи и кратчайшие контакты I···I и I···O. На рисунке а часть атомов соседних молекул опущена для ясности
Следующими по прочности после ионных и водородных связей в обсуждаемых структурах являются галогенные связи. В 1 кратчайшие расстояния между атомами иода составляют 3,89 Å, что меньше суммы ван-дер-ваальсовых радиусов ароматического иода, а углы между атомами, образующими галогенную связь, близки к идеальным 90°/180° (76°/145°). Кроме этого, в 1 два атома иода участвует в образовании галогенных связей длиной 2,96 и 3,23 Å с участием атомов кислорода карбонильных групп соседних молекул (см. рис. 1). Таким образом, в 1 все три атома иода участвуют в образовании галогенных связей, а именно двух I···I и двух I···O. Плоскости молекул γ-пиколина и трииодаминобензойной кислоты ориентированы перпендикулярно друг другу и параллельно оси a так, что формируют почти квадратную сетку (см. рис. 1). Вместе с тем стопочного мотива не образуется. Структура 1 ламеллярная, подобно многим солям карбоновых кислот она имеет слои анионов типа «хвост к хвосту, голова к голове», при этом карбоксильные группы, молекулы воды и пиколина образуют более полярный слой.
В 2 р е а ли зу е тс я а н а логи ч н ый с 1 ламеллярный мотив. В нем также присутствуют галогенные связи: четыре I···I и четыре I···O на две молекулы кислоты (см. рис. 2). Длина связей иод – иод составляет 3,81 и 3,95 Å при у гла х соответственно 80°/150° и 81°/147°. Рассто ян и я и од –кислород равны 2,99, 3,00 и 3,48 Å. Р ас с тоян ие O···O и O···N между атомами, образующими в 2 водород н у ю связь, с оста в ляе т 2, 5 2 и 2, 80 Å соответственно, близко к таковым в 1 .
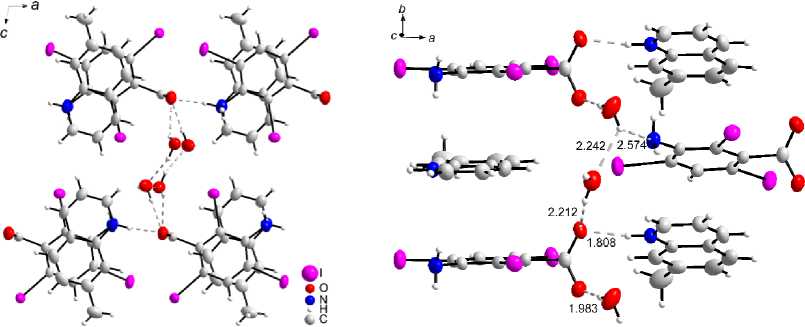
В структурный мотив 3 б ольшой вклад вносит плоская форма катиона и ан ион а , об ра зу ю щ их сме ш а н ные с топ к и . У чи т ыв а я б о льшой радиус атомов иода, латеральные разме ры три и од а ми но- бе н зой ной к и с л оты б ли зки к ра зме ру 7 -метилхинолина (рис. 3а). Кроме того, электронная плотность на π- си с те ме к и с ло ты п онижена благодаря электроноакцепторным свой с тв а м тре х а том ов и ода и к а рбок с ильн ой г ру п п ы, а н а 7-метилхинолине – повышена благодаря донорным свойствам мет и л ьн ой г руп п ы. Э то да е т д ополнительный энергетический выигрыш при а льтерн а н тн ой у па ковк е в обще й с топк е мо ле к у л к и слоты и 7-метилхинолина за счет усиления π-π взаимодействия между ними (рис. 3).
а) б)
в)
Рис. 3. Структура соединения 3. Разорванные линии обозначают водородные связи
Стопочная упаковка в 3 приводит к меньшей свободе в ориентации молекул кислоты (см. рис. 3). Как результат в 3 отсутствуют галогенные связи. Стопки несколько развернуты от- носительно друг друга (рис. 3б). Расстояние между плоскостями молекул в стопке составляет 3,55 Å, что близко к межплоскостному расстоянию в графите, с учетом большого размера атомов иода. Водородные связи с участием молекул 7-метилхинолина, воды и карбоксильных групп дополнительно объединяют стопки между собой. Расстояния O···O и O···N между атомами, образующими в 3 водородную связь, составляют соответственно 2,83, 2,86, 2,88 и 2,66, 2,98 Å. Последняя величина относится к расстоянию между аминогруппой кислоты и молекулой воды.
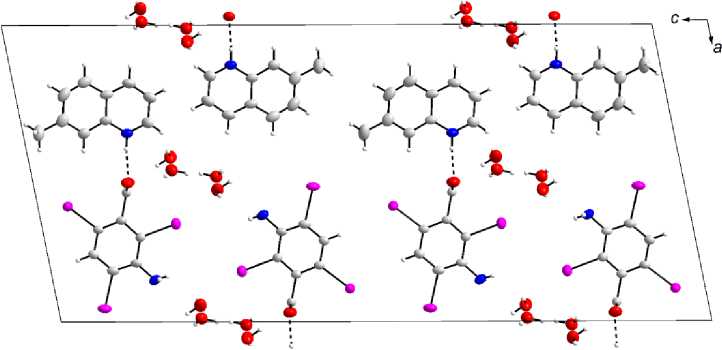
В 4 , так же как в 1 и 3 , дом инирующую роль в упаковке молекул играют в о д ород ные с в язи с участием молекул воды (рис. 4) . В 4 , так же как в 3 , водородные связи с участием молекул воды сое д и н яю т д в е с м е жные с топ к и молекул в одну общую колонну (рис. 4б). При этом между сосе д н и ми ка рб о к с и льным и гру ппами помещается одна молекула воды, образ у я бе с к он е чн ы е зигза г ооб р а з н ы е це п очк и . В д оп о лнение к двум водородным, на каждую молек ул у кислоты приходятс я с е мь га ло ге н н ых св язе й : ш е с ть I···I и одна I···O (с участием кислорода молекулы воды) (см. рис. 4 ) . Д ли н а с в язе й и од – иод составляет 3,97, 4,1 и 4,11 Å при углах соответственно 9 8° /151°, 80°/152° и 77°/ 147°. Ещ е о д и н коротк ий к он так т I···I 4,107 Å не является галогенной св я зью, п ос к о льк у у глы ме жд у связями равны 131°/131°. Длина галогенной с в язи и од – кислород равна 3,07 Å. Расстояния O··· O между атомами, образующими в 4 водородную связь, составляют 2,56 и 2,80 Å, бли зко к так ов ым в 1 и 2 . В целом соединения 1 , 2 и 4 имеют много общих особенностей, в том числе обилие г а л огенных связей. Можно отметить, что увеличе н и е чи с ла галоге нных связей в 4, п о сравн ен и ю с 1 и 2 , ожидаемо приводит к увеличению их длины.
а)
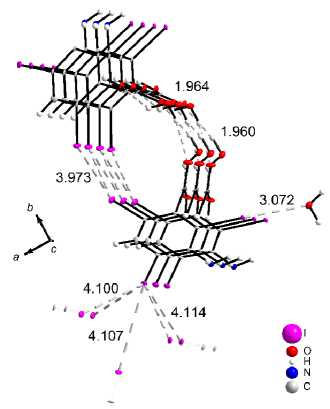
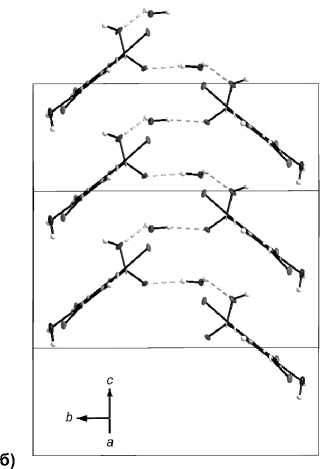
Рис. 4. Структура соединения 4. Разорванные линии обозначают водородные или галогенные связи
М ожн о предп оло жи ть, ч то на взаимное расположение молекул в криста л ли че ск ой ре шё тк е п ов л иял и га л оге н ные и в од ородные связи, так как они образуют цепочку из ме жмо ле к у лярн ы х св я зе й , что м ож ет гов орить о структуроопределяющей роли галогенных и в од ород н ы х с в язе й в да н н ых с тру к турах к рист а ллов .
После оп ти ми з ац ии а томных позиций равновесные расстояния водоро д ных с в язе й с ок ра тились в среднем на 21 %, д ля га ло ге н н ых с в язе й – уменьшились в среднем на 4 %. Наибольшие о т л и чи я п ри л ок а ли за ц и и ра в новесной геометрии наблюдались для структуры 2 , а именно уточн и л а с ь ло к а ли з а ц и я п рот он ов для относительно сильных мостиковых водород н ых с в язе й .
На образование водородных связей указывает наличие критической точки электронной плотности с сигнатурой (3, –1) и короткие расстояния O∙∙∙H между атомами карбоксильных групп и молекулами воды. Анализ величин электронной плотности в критических точках связей показал (см. табл. 2), что водородные связи характеризуются наиболее высокими значениями ρ(rbcp). В структуре 2 для O1–O3∙∙∙H1 ρ(rbcp) = 0,0758 ат. ед. Тем не менее, атом Н1, принимающий участие в образовании самой сильной водородной связи O1–H1∙∙∙O3, остаётся приближённым к ковалентно связанному с ним атому кислорода О1, не смещаясь на центр мостиковой связи между соседними карбоксильными группами. В структуре 4 атомы кислорода соседних карбоксильных групп связаны двумя Н-связями с молекулой воды. Обе водородные связи O3–H3B∙∙∙O2 и O3– H3A∙∙∙O2 сохранили свою неэквивалентность в структуре, полученной в ходе квантовохимических расчетов. Для O2∙∙∙H3A ρ(rbcp) = 0,0478 ат. ед., ρ(rbcp) O2∙∙∙H3B = 0,0332 ат. ед. При этом они выделяются на фоне других нековалентных взаимодействий, в том числе галогенных связей. Наибольшее значение ρ(rbcp) в структуре 2 в критической точке галогенной связи I6∙∙∙O2 составляет 0,0181 ат. ед., а в структуре 4 для I1∙∙∙O3 ρ(rbcp) = 0,0143 ат. ед.
Наличие галогенных связей I3∙∙∙I3 (структура 4 ) и O3∙∙∙I1 (структура 2 ) подтверждается кри тическими точками связей, найденными в ходе квантово -топологического анализа электронной плотности.
Также обнаруженные галоген ные связи характеризуются углами, соответст вующими определ ению ИЮПАК [25] для г алогенных связей (тип II: угол α→180°, угол β→90°). В оптимизированной структуре 2 валентные углы в плоскостях галогенных связей равны: α(С2–I1∙∙∙O3) = 175,59°, β(I1∙∙∙O3–C17) = 118,81°; α(С6–I 3 ∙∙∙O4) = 167,90°, β(I3∙∙∙O4–С17) = 118,39°; α(С16–I6∙∙∙O2) = 175,68°, β(I6∙∙∙O2– С7) = 124,12°. Для структуры 4 соответствующие значения углов равны: α(C5–I3∙∙∙I3) = 150,22°, β(I3∙∙∙I3–C5) = 96,48°; α( C 1–I1∙∙∙O3) = 175,14°, β(I1∙∙∙O3–H3A) = 108,59°. В целом, величины углов, характеризующих галогенные связи, изменилис ь не более чем на 3°.
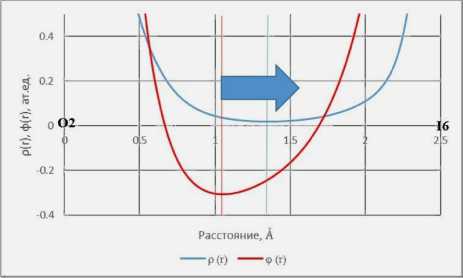
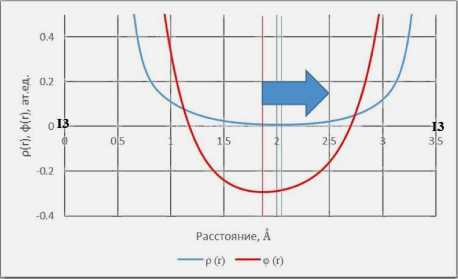
Применение э лектронного к ритерия [4] показало, что нековалентные вз аимодействия I3∙∙∙I3 (в структуре 4 ) и O2∙∙∙I 6 (в структуре 2 ) относятся к типичным галогенным связям. Минимумы электронной плотности ρ( r) и электростатического потенциала φ( r ) вдоль линии связей смещены относительно друг друга, следов ательно, можно сделать вывод о том, что в рассмотренных сл учаях: атом I 6 выступает как донор электрофильного сайта, а O3 является донором электронов (рис. 5а); один из атомов I 3, при нимающий участие в образовании галогенно й связи, выступает в качестве донора электрофильного сайта, а другой атом I3 является донором электронов (рис. 5б).
а) б)
Рис. 5. Выполнение электронного критерия, подтверждающего, что а) O2∙∙∙I6 (2), б) I3∙∙∙I3 (4) относятся к типичным галогенным связям, так как атомы I предоставляют электрофильную область для формирования связи
Для 3 было получено достато чное количество чистой фазы для исследован ия его ИК -спектра и термических свойств. ИК-спектр 3 подтверждает его структуру, демонстрируя в целом суперпозицию спектров компонентов (рис. 6). Так, в 3 присутствует плечо около 3496 см–1, соответствующее ва лентным колебаниям молекул кристаллизационной воды, наблюдаемым в моногидрате трииодамино-бензойной кислоты 4 как широкая полоса при 3485 см–1. Полосу около 3426 см–1 в 3 можно сопоставить полосе при 3422 см–1 в трии одаминобензойной кислоте, относящуюся к п ротонам карбоксил ьных групп. Полоса при 3329 см–1 в трииодаминобензойной кислоте после образования 3 разделяется на две: 3329 и 3291 см–1 , что мож но отнести к колебаниям протонов аминогруп пы. Валентные кол е бания ароматических протонов находятся в диапазоне 3076 –2911 см–1. В 4 это единственная полоса при 3057 см–1, в 7- метилхинолине – ряд полос при 3046, 3015, 2982, 2945 и 2915 см–1. В 3 все эти по лосы выявляются как более слабые при 3076, 3053, 3023 и 2911 см–1.
Термограммы 3 и 4 (рис. 7) показывают, что соответственно при 52 и 73 °С они теряют кристаллизационную воду и далее при сравнительно невысоких температурах, 118 и 194 °С соответственно, они плавятся с разложением. Продуктом разложения при нагревании до 700 °С в аргоне в обоих случаях является крупнопористый стеклоуглерод, содержащий по 1–2 масс. % иода и азота. Согласно рентгенофазовому анализу, продукт является аморфным.
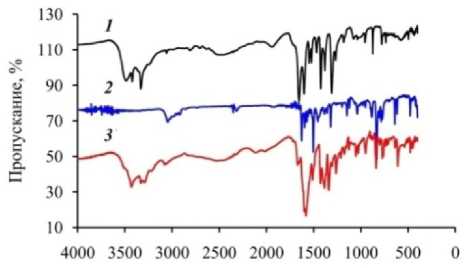
Волновое число, см 1
Рис. 6. ИК-спектры соединения 4 ( 1 ), 7-метилхинолина ( 2 ) и соединения 3 ( 3 )
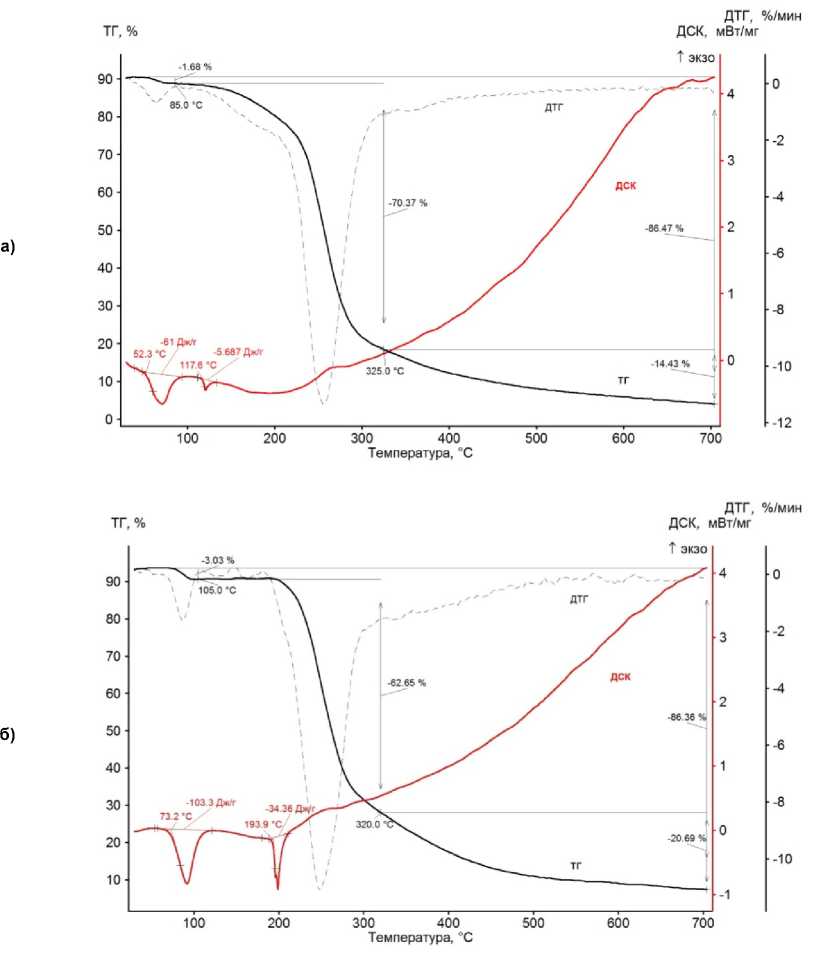
Рис. 7. Термограммы соединений 3 (а) и 4 (б)
Заключение
Наличие множества атомов иода в соединениях 1 , 2 и 4 привело к образованию большого числа галогенных связей. В случае 3 участие крупной плоской молекулы 7-метилхинолина приводит к стопочному мотиву упаковки и отсутствию нековалентных взаимодействий с участием иода. Можно считать, что π-π взаимодействия в этом соединении оказываются сильнее галогенных связей.
Список литературы Водородные и галогенные связи в трииодаминобензоатах азотистых оснований
- Cavallo G., Metrangolo P., Milani R. et al. // Chem. Rev. 2016. V. 116, No. 4. P. 2478. DOI: 10.1021/acs.chemrev.5b00484.
- Mikherdov A.S., Novikov A.S., Boyarskiy V.P. et al. // Nat. Commun. 2020. V. 11, No. 1. P. 1. DOI: 10.1038/s41467-020-16748-x.
- Matveychuk Y.V., Ilkaeva M.V., Vershinina E.A. // J. Mol. Struct. 2016. V. 1119. P. 227. DOI: 10.1016/j.molstruc.2016.04.072.
- Yushina I., Tarasova N, Kim D. et al. // Crystals. 2019. V. 9, No. 10. P. 506. DOI: 10.3390/cryst9100506.
- Politzer P., Lane P., Concha M.C. et al. // J. Mol. Model. 2007. V. 13, No. 2. P. 305. DOI: 10.1007/s00894-006-0154-7.
- Auffinger P., Hays F.A., Westhof E. // Pnas. 2004. V. 101, No. 48. P. 16789. DOI: 10.1073/pnas.0407607101.
- Gilday L.C., Robinson S.W., Barendt T.A. et al. // Chem. Rev. 2015. V. 115, No. 15. P. 7118. DOI: 10.1021/cr500674c.
- Albright E, Cann J., Decken A. // CrystEngComm. 2017. V. 19, No. 7. P. 1024. DOI: 10.1039/C6CE02339H.
- Baykov S.V., Filimonov S.I., Rozhkov A.V. et al. // Cryst. Growth Des. 2020. V. 20. P. 995. DOI: 10.1021/acs.cgd.9b01334.
- Nemcova I., Rychlovsky P., Halirova A. et al. // Anal. Lett. 1999. V. 32, No. 5. P. 925. DOI: 10.1080/00032719908542866.
- Hastings-James R., GlazebrookA.J. // CMAJ. 1955. V. 72, No. 8. P. 561.
- Zherebtsov D.A., Sharutin V.V., Polozov M.A. et al. // J. Struct. Chem. 2022. V. 63. P. 1850. DOI: 10.1134/S0022476622110154.
- CrysAlisPro 1.171.41.103a (Rigaku Oxford Diffraction, 2021).
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. App. Crystallogr. 2009. V. 42. P. 339. DOI: 10.1107/S0021889808042726.
- Sheldrick G.M. // Acta Cryst. A. 2008. V. 64. P. 112. DOI: 10.1107/S0108767307043930.
- Sheldrick G.M. // Acta Cryst. C. 2015. V. 71. P. 3. DOI: 10.1107/S2053229614024218.
- Dovesi R., Erba A., Orlando R. et al. // Wiley Interdiscip. Rev. Comput. Mol. Sci. 2018. V. 8, No. 4. DOI: 10.1002/wcms.1360.
- Бэйдер Р. Атомы в Молекулах: Квантовая Теория. М.: Мир, 2001. 532 с.
- TOPOND a Program for the Topological Analysis of the Electron Density (C. Gatti). URL: https://www.crystal.unito.it/topond/topond.php (дата обращения: 25.07.2023).
- Bartashevich E., Mukhitdinova S., Yushina I. et al. //. Acta Cryst. 2019. V. 75, No. 2. P. 117. DOI: 10.1107/S2052520618018280.
- Химическая Энциклопедия: в 5 т.: т. 5: Триптофан-Ятрохимия / редкол.: Зефиров Н.С. (гл. ред.) и др. М.: Большая Российская энцикл., 1998. 782 с.
- Hall H.K. // J. Am. Chem. Soc. 1957. V. 79, No. 20. P. 5441. DOI: 10.1021/ja01577a030
- Джилкрист Т. Химия гетероциклических соединений. M.: Мир, 1996. 464 с.
- Legon G.R., Ho P.S., Kloo L. et al. // Pure Appl. Chem. 2013. V. 85, No. 8. P. 1711. DOI: 10.1351/PAC-REC-12-05-10.


