Восстановление растений табака после обработки ионами меди
Автор: Тугбаева А.С., Ермошин А.А., Плотников Д.С., Киселева И.С.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Экология
Статья в выпуске: 4, 2020 года.
Бесплатный доступ
Последействие ионов меди (100 и 300 мкМ) на размеры органов, содержание маркеров стресса (перекись водорода, перекисное окисление липидов - ПОЛ) и компонентов антиоксидантного статуса (супероксиддисмутаза - СОД и гваяколовая пероксидаза - ГПО) были изучены в корнях, стебле и листьях Nicotiana tabacum L. Показано, что растения табака чувствительны к длительному воздействию 100 и 300 мкМ Cu2+. Обе концентрации ингибировали рост корней, тогда как длина, толщина побегов и площадь листьев уменьшались только в случае предварительной обработки 300 мкМ Cu2+; то есть рост надземных органов был подавлен значительно меньше, чем корней. Уровень ПОЛ и содержание перекиси водорода в корнях в этих условиях также были выше, что указывает на более сильную нагрузку на корни, чем на стебли и листья. Активность антиоксидантных ферментов СОД и ГПО в корнях и надземных органах специфически изменялась в зависимости от концентрации ионов меди и типа органа. В корнях наблюдалось снижение активности СОД и повышение активности ГПО при предварительной обработке 300 мкМ Cu2+ по сравнению с контролем и 100 мкМ Cu2+, тогда как в стебле и листьях активность ферментов снижалась. Полученные данные свидетельствуют о неполном восстановлении растений в условиях последействия ионов меди.
Ионы меди, пероксид водорода, перекисное окисление липидов, гваяколовая пероксидаза, супероксиддисмутаза, табак
Короткий адрес: https://sciup.org/147229670
IDR: 147229670 | УДК: 581.14, | DOI: 10.17072/1994-9952-2020-4-344-351
Recovery of tobacco plants after copper ions application
The aftereffects of copper ions (100 and 300 pM) on the organ size, the content of stress markers (hydrogen peroxide, lipid peroxidation - LPO) and components of the antioxidant status (superoxide dismutase -SOD and guaiacol peroxidase - GPO) were studied in the roots, stem, and leaves of Nicotiana tabacum L. It was shown that tobacco plants were sensitive to long-term exposure to 100 and 300 pM Cu2+. Both concentrations inhibited root growth, while shoot length and thickness, and leaf area decreased only in the case of pretreatment with 300 pM Cu2+. So, the growth of aboveground organs was suppressed significantly less than the root. The level of lipid peroxidation and the content of hydrogen peroxide in the roots under these conditions were also higher, which indicates a stronger stress, compared to stem and leaf. The activity of antioxidant enzymes SOD and GPO in roots and aboveground organs specifically changed depending on the concentration of copper ions and the type of organ. In the roots, there was a decrease in SOD activity and an increase in the activity of GPO under pretreatment with 300 pM Cu2+, compared to the control and 100 pM Cu2+, while in stem and leaves the activity of enzymes decreased. The data obtained indicate incomplete plant recovery under the aftereffect of copper ions.
Текст научной статьи Восстановление растений табака после обработки ионами меди
Загрязнение земель ионами тяжелых металлов (ТМ) представляет серьезную экологическую проблему для отраслей сельского хозяйства, приводя к потере урожаев и ухудшению качества продукции [Mohammed et al., 2011].
Некоторые из ТМ являются эссенциальными и в низких концентрациях необходимы для живых организмов. Так, ионы меди обеспечивают поддержание структуры белков, входят в состав каталитических центров ферментов, необходимы для работы электронтранспортных цепей митохондрий и хлоропластов, биосинтеза хлорофилла и т. д. [Yruela, 2005]. Диапазон толерантности живых организмов к ионам меди достаточно узок.
Ионы меди в клетках катализируют образование активных форм кислорода (АФК) в реакциях Фентона и Хабера – Вейса, что ведет к усилению окислительных процессов [Yruela, 2005; Abdelgawad et al., 2020]. У растений избыток Cu2+ в тканях листа вызывает хлорозы, негативно влияет на процессы фотосинтеза и фотодыхания, замедляет скорость роста и прирост биомассы [Yruela, 2005]. Однако после снятия стресса, вызванного действием ионов тяжелых металлов, растения способны восстанавливаться [Drost et al., 2007; Holubek et al., 2020]. Сведений об изменениях маркеров стресса в период последействия неблагоприятных факторов и восстановления роста не так много, в сравнении с данными о прямом действии стрессоров.
Типичным проявлением стресса является рост активных форм кислорода. Количество АФК регулируется ферментативными и неферментативными антиоксидантными системами. Показано, что активность антиоксидантных ферментов (каталазы, пероксидазы I и III класса, СОД) и накопление низкомолекулярных антиоксидантов зависят от силы и продолжительности действия стрессового фактора [Ku et al., 2012; Chen et al, 2015].
Несмотря на то, что эффекты ионов меди изучены на примере многих растений, далеко не все аспекты роста и физиологии растений после снятия действия стрессора охарактеризованы детально. Цель настоящей работы – изучение последействия разных концентраций ионов меди в среде на размеры органов и антиоксидантный статус растений N. tabacum в длительном модельном эксперименте.
Материал и методы исследования
В качестве объекта использовали растения табака ( Nicotiana tabacum L.), который является модельным и широко используется в лабораторных экспериментах. Растения табака сорта Petite Havana линии SR1 культивировали на предварительно проавтоклавированном субстрате – смесь перлит : вермикулит в соотношении 1 : 1 на среде Кноппа без добавления ионов меди (контроль) и при добавлении CuSO 4 в концентрации 100 (вариант 1) или 300 (вариант 2) мкМ/л в течение первых 20 дней после появления всходов. С 20 по 40 день растения выращивали на среде Кнопа без добавления ионов меди. Фотопериод составил 16/8 (день/ночь), температура 23°С. Все измерения проводили на 40-дневных растениях.
В предварительном опыте по оценке влияния ионов меди на всхожесть семян табака было выявлено, что добавление 100 мкМ Cu2+ стимулировало прорастание семян (28.6% от контроля), не влияло на длину корешка в 5-ти дневных проростках (4.8 мм против 5.0 мм в контроле); при 300 мкМ Cu2+ всхожесть семян не изменилась (-2.8% от всхоже- сти семян в контроле), но уменьшилась длина корешка (1.7 мм против 5.0 мм в контроле), следовательно, обработка этой концентрацией ионов меди ингибировала рост проростков табака. Это обусловило выбор концентраций CuSO4 в данной работе.
Для оценки последействия ионов меди на растения табака измеряли длину корня, стебля, длину и ширину третьего листа (без учета длины черешка). Выборка составила 30 растений для каждой группы. Толщину корня (зона проведения) и стебля (первое междоузлие выше семядолей) измеряли на поперечных срезах с использованием ПО SIMAGIS MesoPlant. Площадь листа рассчитывали как произведение длины на ширину, умноженное на коэффициент k =0.653 [Moustakas and Ntzanis, 1998].
Активность ферментов антиоксидантной защиты определяли в грубом экстракте тканей растений спектрофотометрически. Для получения грубого экстракта навески корней, стеблей и листьев (третий лист) гомогенизировали на холоде в 0.05 М Tris-HCl буфере (pH 7.0), центрифугировали при температуре 4°С.
Активность СОД оценивали по способности фермента ингибировать фотоокисление нитросине-го тетразолия и выражали в усл. ед. / мг бел-ка*мин [Beauchamp, Fridovich, 1971]. Активность ГПО измеряли по скорости окисления гваякола и выражали в мМ гваякола / мг белка*мин [Chance, Maehly, 1955]. Содержание белка в пробах определяли по Бредфорд [Bradford, 1976], используя в качестве стандарта бычий сывороточный альбумин [Zaia et al, 2005].
Грубый экстракт ферментов использовали также для определения содержания Н 2 О 2 с помощью метода, основанного на окислении пероксидом хелатов ксиленолового оранжевого с ионами железа (III) [Bellincampi et al., 2000] и выражали в мкМ пероксида / г сухой массы.
Интенсивность ПОЛ оценивали спектрофотометрически по количеству малонового диальдегида, взаимодействующего с тиобарбитуровой кислотой (ТБК), и выражали в мкМ ТБК-реагирующих продуктов (ТБК-РП) / г сухой массы [Uchiyama, Mihara, 1978].
Оптическую плотность растворов при определении активности СОД, ПОЛ, содержания белка и пероксида водорода измеряли в 96-луночном планшете на спектрофотометре Tecan Infinity M 200 Pro («Tecan», Austria), а при определении активности ГПО – на приборе Shimadzu UV-1800 («Shimadzu», Japan).
Измерения проводили в трех биологических и трех аналитических повторностях. Результаты представлены в виде значения среднего арифметического и ошибки. Статистическую обработку данных проводили в программе STATISTICA 10 для
Windows 10 с применением t -критерия Стьюдента, U -критерия Манна-Уитни, непараметрического коэффициента корреляции Спирмена при уровне значимости p < 0.05.
Результаты и их обсуждение
На этапе восстановления после снятия действия ионов меди наблюдали изменение размеров растений N. tabacum (рис. 1, табл. 1).
В варианте 1 (предобработка 100 мкМ Cu2+) длина главного корня была достоверно меньше относительно контроля, однако его толщина в зоне проведения увеличилась. Высота и толщина стебля, площадь листовой пластинки не изменились в этом случае, в сравнении с контролем, тогда как предобработка 300 мкМ Cu2+ привела к статистически значимому уменьшению длины и толщины корня на 14%, высоты и толщины стебля на 14% и 15%, площади листа 39% относительно контроля, соответственно.

Рис. 1 . Морфология растений N. tabacum в период восстановления после снятия действия Cu2+
Уменьшение длины главного корня, высоты растений и площади листа является неспецифической реакцией растений на действие тяжелых металлов. У проростков Trifolium repens L. в присутствии 200 мкМ Cu2+ показано 50%-ное уменьшение длины корня [Ермошин и др., 2013]; у Withania somnifera L. длина корня и высота побега также уменьшались [Khatun et al., 2008]. Утолще- ние корня при действии умеренных концентраций Cu2+ рассматривают как адаптивную реакцию, которая способствует увеличению внутренней поверхности корня, связыванию ионов меди в апо-пласте клеток ризодермы и коры [Bouazizi et al., 2010]. Уменьшение диаметра корня при действии высоких концентраций Cu2+ может быть причиной подавления роста клеток растяжением вследствие усиления их лигнификации и снижения эластичности клеточных стенок при связывании их с ионами тяжелых металлов, нарушения транспорта ауксинов и кислого роста, снижения активности экспан-синов [Hamim et al., 2018]. В исследованиях C.M. Cook и соавторов [1997] описано снижение площади листьев у Phaseolus vulgaris L. при действии 160 мкМ ионов меди. При изучении последействия ионов кадмия описано восстановление роста побега и первых листьев растений Glycine max L. У растений, предобработанных более высокими концентрациями Cd2+, отмечали сокращение длины корня как одного из признаков фитотоксичности этого металла [Holubek et al., 2020]. Уменьшение размеров органов растений при избытке ионов тяжелых металлов в среде связывают с накоплением АФК, усилением процессов ПОЛ [Khatun et al., 2008].
В период восстановления после действия ионов меди содержание пероксида водорода было выше в листьях во всех вариантах опыта по сравнению с тканями корня и стебля (табл. 2). В этих органах фотосинтез и дыхание являются источником Н 2 О 2. Несмотря на 20-дневный период восстановления содержание пероксида во всех органах было достоверно выше в сравнении с контрольным вариантом: в варианте 1 (100 мкМ Cu2+) в тканях корня выше в 2.1 раза, стебля и листа – в 1.4 раза по сравнению с контролем. В варианте 2 (300 мкМ Cu2+) эффекты были выражены сильнее: содержание Н 2 О 2 относительно контроля в корне было выше в 4.5 раза, в стебле – в 1.6 раза и в листе – в 2.3 раза, при уровне значимости различий p = 0.03.
Таблица 1
Влияние последействия ионов меди на размеры органов растений N. tabacum
|
Вариант (предобработка) |
Длина, см |
Диаметр, мкм |
Площадь листа, мм2 |
||
|
Корень |
Стебель |
Корень |
Стебель |
||
|
Контроль (H 2 O) |
3.79±0.02 |
4.93±0.02 |
739±16 |
1146 ± 58 |
443 ± 19 |
|
Вариант 1 (100 мкМ Cu2+) |
3.25±0.02* |
4.77±0.03 |
820±13* |
1100 ± 32 |
436 ± 19 |
|
Вариант 2 (300 мкМ Cu2+) |
3.24±0.01* |
4.23±0.03*a |
634 ± 25*a |
971 ± 48*a |
268 ± 13*a |
Примечание. * – Статистически значимое отличие относительно контроля (p < 0.05); a – статистически значимое отличие относительно условий 100 мкМ ионов меди (p < 0.05).
Наиболее высокий уровень ПОЛ показан в корнях во всех вариантах относительно стебля и листьев. В варианте 1 у предобработанных 100 мкМ Cu2+ растений количество ТБК-РП относительно контроля в тканях корня и стебля было больше в
1.4 и 1.6 раза соответственно, в тканях листа – в 1.1 раза. В варианте 2 этот эффект был выражен сильнее: в тканях корня интенсивность ПОЛ достоверно возросла относительно контроля в 2.1 раза (при p = 0.02). В стебле и листьях этот показа- тель превышал уровень в контроле в 3.7 и 2.9 раза, соответственно (отличие достоверно при p = 0.005).
Мы предполагаем, также как Printz et al, [2016], что в период восстановления растений по- сле действия стрессора, ионы Cu2+, непрочно адсорбированные в клеточных стенках, могли вымываться из них в апопласт и проникать в цитоплазму, вызывая образование АФК.
Таблица 2
Содержание пероксида водорода и ТБК-РП в органах N. tabacum , предобработанных разными концентрациями ионов меди (в расчете на г сухой массы)
|
Вариант (предобработка) |
Корень |
Стебель |
Лист |
|||
|
Н 2 О 2 , мкМ |
ТБК-РП, мкМ |
Н 2 О 2 , мкМ |
ТБК-РП, мкМ |
Н 2 О 2 , мкМ |
ТБК-РП, мкМ |
|
|
Контроль (H 2 O) |
0.71 ± 0.04 |
7.04 ± 0.25 |
3.50 ± 0.07 |
1.57 ± 0.04 |
8.43 ± 0.08 |
3.46 ±0.19 |
|
Вариант 1 (100 мкМ Cu2+) |
1.53 ± 0.13* |
9.85 ± 0.42* |
4.90 ± 0.19* |
2.46 ± 0.19* |
11.83 ± 0.36* |
3.91 ±0.10* |
|
Вариант 2 (300 мкМ Cu2+) |
3.22 ± 0.02*а |
15.02 ± 0.28a |
5.56 ± 0.17*а |
5.03 ± 0.09*a |
19.85 ±0.23*a |
9.97 ± 0.11*a |
Примечание. * – Статистически значимое отличие относительно контроля (p<0.05); a – статистически значимое отличие относительно условий 100 мкМ ионов меди (p<0.05).
Увеличение содержания пероксида водорода и интенсивности ПОЛ в органах табака и, как следствие, развитие стресса, вероятно, и привело к угнетению роста у предобработанных ионами меди растений в сравнении с контролем, что проявилось в уменьшении размеров осевых органов и площади листа. Полученные данные о накоплении АФК и продуктов ПОЛ в условиях последействия Cu2+ свидетельствуют о том, что полного восстановления физиологического состояния растений за 20 дней после действия стрессора не происходит.
Известно, что в поддержание окислительновосстановительного баланса в клетках вовлечены ферментные системы и низкомолекулярные антиоксиданты. Результаты наших исследований показали, что активность СОД статистически значимо снижалась в клетках корня и побега у предобрабо-танных ионами меди растений (рис. 2). Падение активности СОД в ответ на избыток Cu2+ в среде описано в растениях Zea mays L., Phyllostachys edulis J. Houz. и, возможно, является следствием инактивации работы фермента продуктом реакции – пероксидом водорода, или нарушения его конформации в результате окислительных процессов [Chen et al, 2015; Abdelgawad et al, 2020]. Возможно, и в условиях последействия ионов меди рост содержания пероксида водорода вызывал продукт-ное ингибирование СОД.
Другой фермент антиоксидантной защиты – ГПО ответственна за утилизацию перекисей. Этот фермент может освобождать клетки от Н2О2, образованного как ферментом СОД, так и другими ферментами, например, гликолатоксидазой. В стеблях и листьях N. tabacum во всех вариантах опыта активность ГПО была ниже, чем в корнях. Увеличение количества Н2О2 в корнях в условиях последействия 100 и 300 мкМ Cu2+ сопровождалось ростом активности ГПО на 90 и 106%, соответственно. При этом в стебле наблюдали снижение активности ГПО на 36% относительно кон- троля только в варианте 2, а в листьях – на 59 и 73%, соответственно, в 1-м и 2-м вариантах опыта (отличие статистически значимо, p = 0.03).
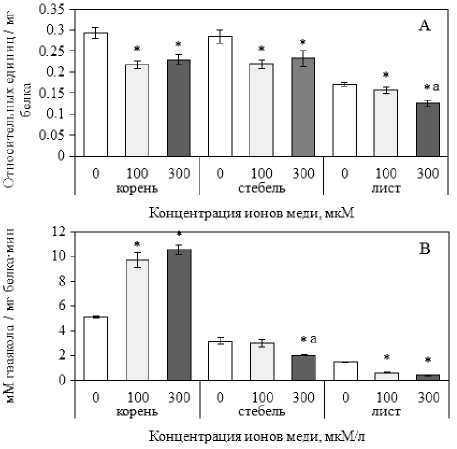
Рис. 2. Активность антиоксидантных ферментов в тканях растений N. tabacum , пред-обработанных разными концентрациями ионов меди:
А – супероксиддисмутаза; В – гваяколовая пероксидаза; * – статистически значимое отличие относительно контроля (p < 0.05); a – статистически значимое отличие относительно условий 100 мкМ ионов меди (p < 0.05)
Возможно, разница в трендах изменения активности ГПО в корнях и надземных органах связана с тем, что корень выполняет барьерную функцию и не позволяет ионам меди в больших количествах транспортироваться в стебель и листья [Cuypers et al., 2016; Abdelgawad et al., 2020]. Следовательно, в этих органах окислительный стресс не так сильно выражен, как в корнях, о чем свидетельствуют более низкие значения содержания ТБК-РП в них в сравнении с корнем. При этом важно отметить, что содержание пероксида водорода в стеблях и листьях больше, чем в корнях и в контроле, и в опытных вариантах. Вероятно, это связано со значительно более высокой активностью ГПО в корнях, быстро расщепляющей Н2О2, чем в стеблях и листьях. Кроме того, зеленые части растений, осуществляющие фотосинтез, имеют дополнительные источники пероксида водорода в фотосинтетической цепи переноса электронов [Abdelgawad et al., 2020] и в гликолатном пути фотосинтеза.
Кроме того, разные изоформы ГПО в корнях и побеге могут отличаться по чувствительности к АФК и продуктам ПОЛ [Maksimovic et al, 2008]. В клетках растений существуют также другие пероксидазы, избавляющие их от Н 2 О 2 .
Роль пероксидаз в реакциях на стресс, вызванный ионами меди, была отмечена у многих растений: Arabidopsis thaliana L. , Oryza sativa L. и др. [Mostofa and Fujita, 2013; Thounaojam et al., 2014].
Показано, что активность ГПО в тканях разных органов зависит от стадии жизненного цикла растений: на стадии вегетации максимальная активность в корнях и низкая в листьях, на стадии бутонизации она возрастает в листьях и снижается в корнях [Maksimovic et al, 2008].
Таким образом, у табака, предварительно обработанного ионами меди, в сравнении с контрольными растениями, в пост-стрессовый период наблюдали увеличение содержания пероксида водорода и ТБК-РП, являющихся маркерами стресса, что указывает на неполную реабилитацию растений. При этом рост надземных органов был подавлен значительно меньше, чем корня.
Заключение
Были определены реакции разных органов растений N. tabacum в период последействия 100 и 300 мкМ Cu2+. Установлено, что растения N. taba-cum чувствительны к этим концентрациям Cu2+, и в период после снятия действия стрессора растут хуже, чем растения, не подвергавшиеся стрессу. Уровень ПОЛ и содержание пероксида водорода были выше в предварительно стрессированных растениях. Одной из реакций растений на последействие избытка ионов меди в среде явилось увеличение активности ГПО в корне. Однако активность СОД во всех органах растения уменьшалась. При этом снижения количества стрессовых маркеров (пероксид водорода и ТБК-РП) не происходило. Органом, испытывающим наиболее сильное последействие Cu2+, являлся корень. Его вероятная барьерная роль ограничивала транспорт ионов меди в побег и обеспечивала менее существенное торможение роста этих органов. Таким образом, в 20-дневный период последействия ионов меди рас- тения табака восстанавливали рост, однако не достигали показателей контрольных растений.
Работа выполнена при поддержке Министерства науки и высшего образования Российской Федерации (соглашение № 02.A03.21.0006).
Список литературы Восстановление растений табака после обработки ионами меди
- Ермошин А.А., Цибизова М.Н., Киселёва И.С. Влияние ионов меди и алюминия на развитие проростков Trifolium repens L. // Вестник Томского государственного университета. Сер. Биология. 2013. Т. 3, № 23. С. 120-126.
- Abdelgawad H. et al. Maize roots and shoots show distinct profiles of oxidative stress and antioxidant defense under heavy metal toxicity // Environmental Pollution. 2020. Vol. 258. P. 113705.
- Beauchamp C., Fridovich L. Superoxide dismutase: Improved assays and an assay applicable to acrylamide gels // Analytical Biochemistry. 1971. Vol. 44, № 1. P. 276-287.
- Bellincampi D. et al. Extracellular H2O2 induced by oligogalacturonics is not involved in the inhibition of the auxin-regulated rolB gene expression in tobacco leaf explants // Plant Physiology. 2000. Vol. 122. P. 1379-1385.
- Bouazizi H. et al. Cell wall accumulation of Cu ions and modulation of lignifying enzymes in primary leaves of bean seedlings exposed to excess copper // Biological Trace Element Research. 2011. Vol. 139. P. 97-107.
- Bradford M.M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding // Analytical Biochemistry. 1976. Vol. 72. P. 248254.
- Chance B., Maehly A.C. Assay catalase and peroxi-dase // Methods in Enzymology. 1955. Vol. 2. P. 764-775.
- Chen J. et al. Copper induced oxidative stresses, anti-oxidant responses and phytoremediation potential of Moso bamboo (Phyllostachys pubescens) // Scientific Reports. 2015. Vol. 5, № 13554.
- Cook C.M. et al. Effects of copper on the growth, photosynthesis and nutrient concentration of Phaseolus plants // Photosynthetica. 1997. Vol. 34. P. 179-193.
- Cuypers A. et al. Hydrogen peroxide, signaling in disguise during metal phytotoxicity // Frontiers in Plant Science. 2016. Vol. 7. P. 470.
- Drost W. et al. Heavy metal toxicity to Lemna minor: studies on the time dependence of growth inhibition and the recovery after exposure // Chemo-sphere. 2007. Vol. 67, № 1. P. 36-43.
- Elleuch A. et al. Morphological and biochemical behavior of fenugreek (Trigonella foenum-graecum) under copper stress // Ecotoxicology and Environmental Safety. 2013. Vol. 98. P. 46-53.
- Hamim H., Miftahudin M., Setyaningsih L. Cellular and ultrastructure alteration of plant roots in response to metal stress. In Plant growth and regulation-alterations to sustain unfavorable conditions. London: IntechOpen, 2018. pp 21-41.
- Holubek R. et al. The recovery of soybean pants under short-term cadmium stress // Plants. 2020. Vol. 9. P. 782.
- Khatun S. et al. Copper toxicity in Withania somnifera: Growth and antioxidant enzymes responses of in vitro grown plants // Environmental and Experimental Botany. 2008. Vol. 64. P. 279-285.
- Ku H.-M. et al. The effect of water deficit and excess copper on proline metabolism in Nicotiana ben-thamiana // Biologia Plantarum. 2012. Vol. 56, № 2. P. 337-343.
- Maksimovic J.D. et al. Peroxidase activity and phenolic compounds content in maize root and leaf apoplast and their association with growth // Plant Science. 2008. Vol. 175, № 5. P. 656-662.
- Mohammed A.S., Kapri A., Goel R. Heavy metal pollution: source, impact, and remedies // Biomanagement of Metal-Contaminated Soils. 2011. P. 1-28.
- MostofaM.G., FujitaM. Salicylic acid alleviates copper toxicity in rice (Oryza sativa L.) seedlings by up-regulating antioxidative and glyoxalase systems // Ecotoxicology. 2013. Vol. 22. P. 959-973.
- Moustakas N.K., Ntzanis H. Estimating flue-cured tobacco leaf area from linear measurements, under mediterranean conditions // Agr. Med. 1998. Vol. 128. P. 226-231.
- Printz B. et al. Copper trafficking in plants and its implication in cell wall dynamics // Front. Plant Sci. 2016. Vol. 7. P. 601.
- Thounaojam T.C. et al. Zinc ameliorates copper-induced oxidative stress in developing rice (Oryza sativa L.) seedlings // Protoplasma. 2014. Vol. 251, № 1. P. 61-69.
- Uchiyama M., Mihara M. Determination of malo-naldehyde precursor in tissues by thiobarbituric acid test // Analytical Biochemistry. 1978. Vol. 86, № 1. P. 287-297
- Vijayarengan P., Jose M.D. Changes in growth, pigments and phytoremediating capability of four plant species under copper stress // Journal of Environmental Biology. 2014. Vol. 21, № 5. P. 119-126.
- Yruela I. Copper in plants // Brazilian Journal of Plant Physiology. 2005. Vol. 17. P. 145-156.
- Zaia D.M. et al. Spectrophotometric determination of total proteins in blood plasma: a comparative study among dye-binding methods // Brazilian archives of biology and technology. 2005. Vol. 48, № 3. P. 385-388.


