Возможно ли предсказать риск эмболии во время реваскуляризации головного мозга?
Автор: Виноградов Р.А., Косенков А.Н., Винокуров И.А., Здановская И.Н.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.12, 2017 года.
Бесплатный доступ
Основной причиной развития острого нарушения мозгового кровообращения после реваскуляризации экстракраниальных артерий головного мозга является эмболия. Поиск метода, способного предсказать риск развития эмболии - приоритетное направление данной проблемы. В исследование включено 200 больных, которым выполнили каротидную эндартерэктомию. Больные были разделены на 2 группы: с «немыми» ишемическими очагами и без них. Всем им было проведено стандартное обследование, а также тест на поток-зависимую вазодилатацию. У больных без эмболических осложнений после реваскуляризации головного мозга на плечевой артерии была меньше толщина комплекса интима-медиа, большая подвижность сосудистой стенки в покое и более выраженная вазодилатация при введении нитроглицерина. Выявлено, что метод исследования поток-зависимой вазодилатации позволяет оценить риски микроэмболии при выполнении реваскуляризации головного мозга с высоким уровнем чувствительности.
Реваскуляризация головного мозга, ультразвуковое исследование, поток-зависимая вазодилатация, эмболия, "немые" ишемические очаги
Короткий адрес: https://sciup.org/140188673
IDR: 140188673 | УДК: 616.831-005.7-089
Is it possible to predict the risk of embolism during the brain revascularization?
Embolism is the primary cause of stroke after cerebral revascularization. Priority of the problem is to search method that can predict the risk of embolism. We investigated 200 patients who underwent cerebral revascularization. The patients were divided into 2 groups: with a silent ischemic lesion (SIL) and without it. All of them were exposed to standard examination, and test for flow-dependent vasodilation. The thickness of the intima-media complex was less in patients without embolic complications after brain revascularization, and these patients had more expressed vasodilation after nitroglycerine test. Conclusions. The presented method for studying the flow-dependent vasodilatation evaluate microembolism risks of cerebral revascularization. The sensitivity of the method is 92.5%.
Текст научной статьи Возможно ли предсказать риск эмболии во время реваскуляризации головного мозга?
Основной причиной развития острого нарушения мозгового кровообращения (ОНМК) и транзиторных атак при наличии атеросклеротической бляшки во внутренней сонной артерии (ВСА) является ее деструкция и возможность «отрыва» части бляшки, вызывающие окклюзию дистальных отделов артерии. Бляшки подразделяются на эмболоопасные и «стабильные» [8]. До появления клинических симптомов точно определить тип бляшки не представляется возможным. По данным УЗ (ультразвуковое)-ангиосканирования можно оценить количество кальцинатов в структуре бляшки, наличие участков явной деструкции (изъязвлений), но нельзя с точностью предсказать риск эмболии до макроскопической визуализации атеромы [1].
Морфологически атерома может состоять из участков кальциноза, фиброза, липидной части, а также некроза и внутриатеросклеротического кровоизлияния. Последние два имеют явную корреляцию с рисками эмболии [11, 12, 14]. Для более точной дифференцировки структуры бляшки на дооперационном этапе было предложено использовать магнитно-резонансною томографию (МРТ). За счет высокой разрешающей способности метода появилась возможность оценивать структуру бляшки и ее состав на всей толщине [3, 13, 16]. Однако дороговизна метода ограничивает его применение в повседневной практике [2]. В целях достижения экономической эффективности этих операций необходимо разработать метод, позволяющий оценивать структуру бляшки и/или ее эмболоопасность без применения сложного и дорогостоящего оборудования.
В литературе нами обнаружен простой и доступный способ оценки функции эндотелия с помощью поток-за-висимой вазодилатации, определяемой на ультразвуке. Этот способ оказался эффективным в подтверждении микроэмболии при ОНМК и выявления «немых» ишемических очагов (НИО) у больных со стенозами ВСА без операции [9]. Мы предполагаем, что с помощью данного обследования возможно предсказать развитие эмболии во время операции.
Целью данного исследования является определение возможностей поток-зависимой вазодилатации в предсказании рисков эмболии во время реваскуляризации головного мозга.
Материалы и методы
В настоящее исследование было включено 200 больных, которым выполнили реваскуляризацию головного мозга (каротидная эндарктерэктомия). Всем им было проведено стандартное обследование, а также тест на поток-зависимую вазодилатацию (ПЗВД) [11]. Больных

разделили на 2 группы: с НИО и без них (табл. 1). Преимуществом метода поток-зависимой вазодилатации считаем его дешевизну и простоту применения.
Для проведения данного теста больного укладывают на кушетку, измеряют диаметр плечевой артерии в покое. Далее больному дают нитроглицерин. Мы использовали нитро-спрей 2 дозы под язык. Замеряют диаметр артерии. Оценивают дилатацию как разницу между результатом после нитроглицерина и исходным в процентах.
В нашем исследовании оценивалась только резистентность сосудистой стенки, так как плечевая артерия менее всего подвержена деструктивным изменениям у больного.
Для оценки достоверности различий количественного признака использовали критерий Стьюдента. При оценке качественного признака – критерий Кси-квадрат. Результаты считали достоверными при Р ≤ 0,05.
Расчеты проводили в программах Statistica 8.0 StatSoft, а также в программе Excel Microsoft Office 2007.
Результаты
При сравнительной характеристике двух групп было выявлено, что больные с НИО чаще страдали фибрилляцией предсердий (Р = 0,03) и у них чаще обнаруживались эмболоопасные бляшки (Р < 0,0001). Артериальное давление на момент исследования так же было выше в группе с НИО (Р < 0,0001).
Мы проводили исследование функции эндотелия на плечевой артерии в типичном месте. Кроме измерения диаметра артерии мы оценивали толщину комплекса интима-медиа, наличие стенозов в этой области, а также изменение диаметра артерии во время сердечного цикла. Для этого все исследования записывали на цифровой носитель в течение 30 секунд с последующими замерами при повторных просмотрах (табл. 2).
В нашем исследовании мы обнаружили, что у больных без эмболических осложнений после реваскуляризации головного мозга (ГМ) на плечевой артерии была меньше толщина комплекса интима-медиа (Р = 0,04), большая подвижность сосудистой стенки в покое (Р = 0,001) и более выраженная вазодилатация после введения нитроглицерина (Р < 0,0001). При компрессионной пробе уменьшение диаметра артерии было схоже для обеих групп.
Обсуждение
Основой для нашего исследования послужила теория о взаимосвязи ригидности сосудистой стенки, которая косвенно отражает глубину поражения организма атеросклеротическим процессом, и риском эмболии [5, 7, 10]. Другими авторами был проведен анализ взаимосвязи подвижности сосудистой стенки в покое и риска эмболии при стенозе ВСА [6]. Теоритически риск эмболии за счет деструкции атеросклеротического процесса носит системный характер, соответственно, риск разрыва капсулы атеромы следует оценивать на наименее измененных
Табл. 1. Сравнительная характеристика больных
|
Параметр |
С НИО, n = 89 |
Без НИО , n = 111 |
Р |
|
Возраст, лет |
62 ± 7 |
60 ± 9 |
0,58 |
|
Возраст старше 70 лет |
13 (14,6%) |
14 (12,6%) |
0,79 |
|
ИБС |
57 (64,0%) |
88 (79,3%) |
0,42 |
|
ХСН 3 ФК |
27 (30,3%) |
30 (27,0%) |
0,89 |
|
Фибрилляция предсердий |
14 (15,7%) |
5 (4,5%) |
0,03 |
|
Сахарный диабет 2 типа |
11 (12,4%) |
12 (10,8%) |
0,26 |
|
ХОБЛ |
5 (5,6%) |
7 (6,3%) |
0,82 |
|
ОНМК в анамнезе |
16 (17,9%) |
11 (9,9%) |
0,43 |
|
Эмболоопасная атеросклеротическая бляшка по данным УЗ-ангиосканирования |
35 (39,3%) |
13 (11,7%) |
<0,0001 |
|
Среднее систолическое АД на момент исследования, мм рт. ст. |
155,3 ± 27,1 |
121,9 ± 34,1 |
<0,0001 |
|
Среднее диастолическое АД на момент исследования, мм рт. ст. |
85,1 ± 12,2 |
74,5 ± 19,3 |
<0,0001 |
Примечание : процент указан от количества больных в группе.
Табл. 2. Ультразвуковые параметры стенки плечевой артерии
|
Параметр |
С НИО, n = 89 |
Без НИО, n = 111 |
Р |
|
Толщина интима-медиа |
1,1 ± 0,2 |
0,7 ± 0,3 |
0,04 |
|
Стенозы, % |
23 ± 9 |
12 ± 16 |
0,11 |
|
Изменение диаметра артерии в покое, % |
4,3 ± 2,8 |
7,2 ± 3,1 |
0,001 |
|
Увеличение максимального диаметра при введение нитроглицерина, % |
8,6 ± 4,7 |
17,2 ± 2,8 |
<0,0001 |
|
Уменьшение максимального диаметра после компрессионной пробы, % |
6,8 ± 3,1 |
7,4 ± 5,2 |
0,34 |
Примечание : процент указан от количества больных в группе.
артериях. Из всех легко доступных для исследования артерий редко поражается атеросклерозом плечевая артерия, поэтому мы выбрали ее для нашего исследования.
Наши результаты демонстрируют большую подвижность сосудистой стенки при отсутствии НИО после операции (7,2 ± 3,1% против 4,3 ± 2,8%), а также значительно лучшую реакцию вазодилатации на введение нитроглицерина (17,2 ± 2,8% против 8,6 ± 4,7%), что отражает функцию эндотелия.
Риск сосудистых осложнений тесно связан с функцией эндотелия и гладкомышечной мускулатуры сосудов. Когда эти функции работают удовлетворительно, происходит выраженная вазодилатация на введение эндогенного нитрата азота в сосудистой русло. При снижении функции эндотелия и/или нарушении сократительной способности гладкомышечных миоцитов эти изменения становятся менее значимыми. По данным нашего исследования при снижении степени вазодилатации возрастает риск развития НИО после операции. Таким образом, мы считаем, что после принятия решения о необходимости хирургического лечения больному следует выполнять тест на функцию эндотелия. Проанализировав полученные данные, мы пришли к выводу, что «безопасной» с точки

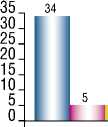
более 15%
■ ■ жировая
I I фиброзно-жировая кальцинированная
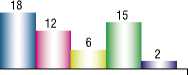
до 15%
I I некротическая
■ ■ кровоизлияние в бляшку
Рис. 1. Диаграмма частоты встречаемости различных типов атеросклеротических бляшек в сонных артериях в зависимости от показателя вазодилатации плечевой артерии после введения нитроглицерина зрения возможных рисков деструкции атеромы является порог вазодилатации в 15% после введения нитроглицерина. Мы проанализировали морфологию атеросклеротических бляшек, удаленных при КЭАЭ в зависимости от указанного порога вазодилатации (рис. 1).
При морфологическом исследовании мы обнаружили, что по данным УЗ-ангиосканирования невозможно оценить наличие кровоизлияния в бляшку и в 3-х случаях у больного с УЗ картиной гомогенной бляшки мы обнаружили некротизированную, распадающуюся атерому. Так же стоит отметить, что при более высокой степени вазодилатации мы чаще встречались с жировыми бляшками, которые имеют низкий риск эмболии, в тоже время фиброзная капсула у атеромы чаще обнаружилась в группе с низким показателем вазодилатации.
Полученные данные свидетельствуют о том, что при оценке рисков эмболии при реваскуляризации ГМ можно использовать предложенный тест. При анализе морфологии атеромы возможно полагаться на косвенные признаки. Преимущество этого метода заключается в его дешевизне. При выполнении МРТ диагностики морфологическая чувствительность метода составляет 85–95% [4, 15]. Учитывая высокую стоимость исследования, данный тест не может использоваться в повседневной практике хирурга. Для выполнения предложенного нами теста не требуется дорогостоящего дополнительного оборудования. Стандартный ультразвуковой аппарат и спрей с нитроглицерином позволяет определить риск эмболии и в зависимости от этого выбирать метод хирургической коррекции. Стоит отметить, что в группе с ПЗВД менее 15% НИО обнаружили у 49 больных, т.е. в 92,5% случаев.
Представленный метод исследования ПЗВД позволяет оценить риски микроэмболии при выполнении реваскуляризации ГМ. Хирургическая тактика у конкретного больного может подбираться с учетом данного параметра.
Список литературы Возможно ли предсказать риск эмболии во время реваскуляризации головного мозга?
- Кошурникова М.В., Балахонова Т.В., Карпов Ю.А. Возможности ультразвуковой трехмерной визуализации при изучении размеров и структуры атеросклеротической бляшки. Атеросклероз и дислипидемии//2013, -№ 4. -C. 31-38.
- Караськов А.М., Бахарев А.В., Чернявский А.М. и др. Диагностические характеристики ультразвукового сканирования, традиционной рентгеноконтрастной и многосрезовой спиральной компьютерно-томографической ангиографии в оценке стенозов внутренней сонной артерии по результатам каротидной эндартерэктомии//2008, -№ 4. -C. 54-60.
- Cappendijk V.C., Cleutjens K.B., Kessels A.G., et al. Assessment of human atherosclerotic carotid plaque components with multi-sequence MR imaging -initial experience//Radiology. -2005, -№ 234. -P. 487-92.
- Chu B., Kampschulte A., Ferguson M.S., et al. Hemorrhage in the ath-erosclerotic carotid plaque -high-resolution MRI study//Stroke. -2004, -№ 35 (1079) -84.
- Dijk J.M., Van Der Graaf Y., Grobbee D.E., et al. Increased arterial stiffness is independently related to cerebrovascular disease and aneurysms of the abdominal aorta -the second manifestations of arterial disease (SMART) study//Stroke -2004, № 35(7) -P. 1642-1646.
- Kanber B., Hartshorne T.C., Mark A. Horsfield et al. Wall motion in the stenotic carotid artery -association with greyscale plaque characteristics, the degree of stenosis and cerebrovascular symptoms//Cardiovascular Ultrasound. -2013, № 11 -37.
- Leone N., Ducimetière P., Gariépy J., et al. Distension of the carotid artery and risk of coronary events -the three-city study//Arterioscler Thromb Vasc Biol. 2008, № 28(7) -P. 1392-1397.
- North American Symptomatic Carotid Endarterectomy Trial Collaborators. Beneficial effect of carotid endarterectomy in symptomatic patients with high-grade carotid stenosis//N Engl J Med. 1991, -№ 53. -P. 325-445.
- Qing P., Yining H., Wei S. et al. Associations among cerebral microbleeds, cerebral large-artery diseases and endothelial function//Chin Med J. 2014, -№ 127 (18). -P. 3204-3208.
- Schmidt-trucksäss A., Grathwohl D., Schmid A., et al. Structural, functional, and hemodynamic changes of the common carotid artery with age in male subjects//Arterioscler Thromb Vasc Biol. -1999, № 19(4). -P. 1091-1097.
- Takaya N., Yuan C., Chu B., et al. Association between carotid plaque characteristics and subsequent ischemic cerebrovascular events -a prospective assessment with MRI-initial results//Stroke. -2006, -№ 37 (818) -23.
- Waki H., Masuyama T., Mori H., et al. Ultrasonic tissue characterization of the atherosclerotic carotid artery -histological correlates or carotid integrated backscatter//Circ J. -2003, -№ 67 (1013) -16.
- Watanabe Y., Nagayama M., Suga T., et al. Characterization of atherosclerotic plaque of carotid arteries with histopathological correlation -vascular wall MR imaging vs. color Doppler ultra-sonography (US).//J Magn Reson Imaging. -2008, -№ 28. -478-85.
- Yoshida K., Narumi O., Chin M., et al. Characterization of carotid atherosclerosis and detection of soft plaque with use of black-blood MR imaging. AJNR Am J Neuroradiol 2008, -№ 29. -P. 868-74.
- Yuan C., Mitsumori L.M., Ferguson M.S., et al. In vivo accuracy of multispectral magnetic resonance imaging for identifying lipid-rich necrotic cores and intraplaque hemorrhage in advanced human carotid plaques.//Circulation 2001, -№ 104. -P. 2051-56.
- Zhao X., Miller Z.E., Yuan C. Atherosclerotic plaque imaging by carotid MRI.//Curr Cardiol Rep. 2009, -№ 11. -P. 70-77.


