Возможность использования лабораторных предикторов в оценке развития асептической нестабильности при тотальном эндопротезировании тазобедренного сустава
Автор: Карякина Елена Викторовна, Персова Елена Александровна, Гладкова Екатерина Вячеславовна
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Клиническая лабораторная диагностика
Статья в выпуске: 2 т.7, 2011 года.
Бесплатный доступ
Представлены данные оценки возможностей прогнозирования результатов тотального эндопротезирования тазобедренного сустава (ТЭП ТБС) у больных коксартрозом по уровню биохимических маркеров резорбции и формирования кости, определяемых в сыворотке крови методом твердофазного иммунного анализа. На основании мониторинга клинико-лабораторных данных 50 больных и обследования 30 практически здоровых лиц определены биохимические предикторы асептической нестабильности эндопротеза при первичном бесцементном ТЭП ТБС
Биохимические маркеры резорбции и костеобразования, коксартроз
Короткий адрес: https://sciup.org/14917330
IDR: 14917330
Текст научной статьи Возможность использования лабораторных предикторов в оценке развития асептической нестабильности при тотальном эндопротезировании тазобедренного сустава
1Введение. Увеличение продолжительности жизни населения экономически развитых стран приводит к росту числа пациентов с заболеваниями ТБС и, соответственно, к росту числа лиц, нуждающихся в ТЭП ТБС [1–3]. Одним из часто встречающихся и грозных осложнений ТЭП ТБС является, как известно, асептическая нестабильность эндопротеза, уменьшение числа случаев которой можно отнести к одной из ведущих задач современной ортопедии [4]. В настоящее время не вызывает сомнения тот факт, что длительность нормального функционирования эндопротеза во многом определяется не только исходным состоянием костной ткани, непосредственно прилежащей к импланту, но и особенностями процессов стрессового ремоделирования кости в послеоперационном периоде [5,6].
Интенсификация метаболизма костной ткани, приводящая к повышению уровня биохимических маркеров её ремоделирования в биологических жидкостях организма после операции [7, 8], является одним из проявлений адаптационно-компенсаторной реакции. Требует уточнения количественная оценка степени интенсификации костного метаболизма, определяемого по уровню биохимических маркеров резорбции и костеобазования в сыворотке крови в раннем послеоперационном периоде. Кроме того, необходимо проведение анализа диагностической информативности данных биохимических тестов, их возможного использования с целью прогнозирования результатов ТЭП ТБС у больных коксартрозом.
Цель исследования: оценка возможностей прогнозирования результатов тотального эндопротезирования тазобедренного сустава (ТЭП ТБС) у больных коксартрозом по уровню биохимических маркеров резорбции и формирования кости, определяемых в сыворотке крови.
Методы . Для решения поставленной задачи в динамике обследовано 50 больных коксартрозом (II–III стадии), поступивших в СарНИИТО для оперативного лечения (максимальный срок наблюдения: 24 месяца после операции). У всех больных наблюдалось выраженное нарушение функции ТБС (ФНС II-ΙΙI). Среди обследованных было 20 мужчин и 30 женщин. Возраст мужчин: от 36 до 78 лет, все женщины старше 50 лет. Длительность заболевания — от 5 до 16 лет, длительность поражения тазобедренного суста-
Адрес: 410002, г. Саратов, ул. Чернышевского, 148.
Тел.: 232878.
ва: более пяти лет. Контрольную группу составили 30 практически здоровых лиц.
Все пациенты получали в прошлом различные нестероидные противовоспалительные препараты. Всем больным выполнено первичное бесцемент-ное ТЭП ТБС; послеоперационный период протекал гладко, ранние и поздние инфекционные осложнения, а также осложнения, связанные с техническими погрешностями во время оперативного вмешательства, отсутствовали.
Всем больным выполнялось тщательное клинико-рентгенологическое и лабораторное обследование, денситометрическое исследование (оценка минеральной плотности костной ткани (МПК) в поясничном отделе позвоночника L1-L4 в передне-задней проекции и проксимальных отделах обоих бедер — в шейке, большом вертеле и бедре в целом) с помощью костного денситометра Prodigy (№ DF+ 150451999 г.) фирмы GE LUNAR Corporation (США).
Выполняли стандартное клинико-лабораторное исследование крови и мочи и биохимическое исследование крови. В сыворотке крови методом твердофазного иммуноферментного анализа с помощью стандартных тест-систем на анализаторе с микропланшетным ридером Anthos-2020 определяли биохимические маркеры формирования (N-mid остеокальцин — ОК и костный изофермент щелочной фосфатазы — ЩФ) и резорбции (С-концевые тело-пептиды зрелого коллагена I типа — Serum CrossLaps) кости для оценки особенностей процессов ее ремоделирования.
Кровь для биохимических исследований получали при пункции локтевой вены утром натощак.
Лабораторное обследование больных выполнялось в следующие сроки: до операции, через 1,5; 3, 6, 12 (14) и 18–24 месяца после оперативного вмешательства.
Статистическая обработка проводилась с вычислением средней арифметической (М), средней ошибки средней арифметической (m), коэффициента достоверности (t). Полученные данные считались достоверными при показателе вероятности р<0,05.
Результаты. У всех больных имелся остеопенический синдром, проявлявшийся как локальным (пе-риартикулярным) остеопорозом или остеопенией, так и генерализованной остеопенией (снижение МПК в области L1-L4). До операции у 22 больных в области, прилежащей к ТБС, выявлено снижение МПК, характерное для остеопороза (Т-критерий –2,5 SD и ниже); у остальных больных — снижение МПК, характерное для остеопении (Т-критерий от –1,1 SD до –2,4 SD).
При динамическом изучении особенностей метаболизма костной ткани в процессе её адаптивной перестройки после ТЭП ТБС у 47 человек состояние эндопротеза в зависимости от клинико-рентгенологической картины оценивалось как стабильное в течение всего периода наблюдения. У этих больных статистически достоверное (р<0,05) повышение по сравнению с практически здоровыми лицами уровня Serum CrossLaps и костного изофермента ЩФ наблюдалось через 3 и 6 месяцев после операции. Через год эти показатели возвращались к дооперационным значениям, в то время как содержание остеокальцина оставалось несколько повышенным.
У трех пациентов диагностировано развитие ранней асептической нестабильности в течение 1,5–2 лет после операции на основании клинико-рентгенологических (жалобы, объем активных и пассивных движений в ТБС, миграция компонентов эндопротеза, перипротезный очаговый остеолиз, перипро-тезный остеопороз и потеря окружающей костной ткани) и денситометрических (снижение МПК вокруг компонентов эндопротеза в динамике) исследований, подтвержденной интраоперационно при реэндопротезировании. Диагностированная асептическая нестабильность сопровождалась значительной интенсификацией обмена костной ткани не только по сравнению с нормой, а также с показателями у больных при благоприятно протекающем стрессовом ремоделировании: повышение уровня маркеров резорбции в сыворотке крови (р<0,05), а также существенное (р<0,05), но менее выраженное повышение маркеров костеобразования.
В таблице представлены результаты исследования динамики биохимических маркеров при неблагоприятном протекании процессов стрессового ремоде- лирования (развитие асептической нестабильности в срок до двух лет после первичного ТЭП).
При анализе динамики уровня биохимических маркеров у каждого из трех больных было обращено внимание на характер изменения соотношения уровней Serum CrossLaps и ОК по сравнению с до-операционным уровнем. Так, у всех трех больных уровень Serum CrossLaps уже через 1,5 месяца после оперативного вмешательства возрос в 2 раза и более, а уровень ОК хотя и увеличился, но не более чем в 1,5 раза, т.е. уже через 1,5 месяца имела место выраженная интенсификация ремоделирования костной ткани с выраженным преобладанием процессов резорбции. Данные соотношения содержания Serum CrossLaps и ОК сохранялись относительно постоянными и через 3, и через 6 месяцев, приводя к еще более выраженному преобладанию процессов резорбции, которое не компенсировалось соответствующим усилением процессов костеобразования в сроки 12–24 месяцев после операции. Очевидно, грубые нарушения процессов стрессового ремоделирования костной ткани, сопровождающиеся выраженным отрицательным костным балансом, обнаруженным при анализе индивидуальных особенностей метаболизма костной ткани, развившимся в ранние сроки и длящимся более шести месяцев после операции, приводили у этих больных к развитию асептической нестабильности эндопротеза в ближайшие 1,5–2 года после ТЭП.
Для иллюстрации приводим клинический пример. Больная Ц., 1947 г.р. наблюдается в СарНИИТО в течение двух лет. Больной себя считает с 2000 г., когда стала беспокоить боль в области правого тазобедренного сустава, возникающая при ходьбе, ограничение движений в правом тазобедренном суставе.
Маркеры резорбции и костеобразования у больных остеоартрозом после ТЭП ТБС с ранней асептической нестабильностью (n=3)
|
Сроки исследования |
Тесты |
||
|
Serum CrossLaps (нг/мл) |
остеокальцин (нг/мл) |
костный изофермент ЩФ (ед/л) |
|
|
1–0,65 |
1–12,48 |
1–31,31 |
|
|
До операции |
2–0,41 |
2–14,20 |
2–30,03 |
|
3–0,53 |
3–13,90 |
3–32,04 |
|
|
1–1,30 |
1–18,7 |
1–32,52 |
|
|
1,5 месяца после операции |
2–0,95 |
2–19,4 |
2–31,03 |
|
3–1,10 |
3–20,0 |
3–32,00 |
|
|
1–1,70 |
1–19,9 |
1–32,50 |
|
|
3 месяца после операции |
2–1,14 |
2–20,1 |
2–31,00 |
|
3–1,73 |
3–21,7 |
3–32,06 |
|
|
1–1,61 |
1–20,8 |
1–32,50 |
|
|
6 месяцев после операции |
2–1,17 |
2 — нет |
2–31,07 |
|
3–2,01 |
3–21,0 |
3–32,04 |
|
|
1–1,83 |
1–21,2 |
1–32,6 |
|
|
12–14 месяцев после операции |
2–1,42 |
2–23,0 |
2–31,0 |
|
3 — нет |
3–21,9 |
3–32,05 |
|
|
1–1,78 |
1–20,3 |
1–32,57 |
|
|
18–24 месяца после операции |
2 — нет |
2–23,4 |
2–31,02 |
|
3–1,95 |
3 — нет |
3–32,03 |
|
В поликлинике по месту жительства поставлен диагноз: «Деформирующий остеоартроз тазобедренных суставов справа II ст., слева — I ст.» Проводилось неоднократное консервативное лечение без эффекта. В 2006 г. боль усилилась, объем движений в правом тазобедренном суставе значительно уменьшился, появилось укорочение правой ноги, было рекомендовано выполнить тотальное эндопротезирование правого тазобедренного сустава, для которого больная поступила в СарНИИТО.
Данные денситометрии : AP Spine=–3,0 SD; Left Femur=–2,5 SD; Right Femur=–3,7 SD. Заключение: МПК при обследовании поясничного отдела позвоночника (Т-критерий=–3,0 SD) и проксимальных отделов бедер (слева Т-критерий=–2,5 SD; справа Т-критерий=–3,7 SD) соответствует системному остеопорозу.
Биохимические маркеры костной ткани:
-
1. Serum CrossLaps 0,65 нг/мл.
-
2. Остеокальцин 12,48 нг/мл.
-
3. Костный изофермент щелочной фосфатазы 27,1 ед/л.
Диагноз: «Двусторонний деформирующий остеоартроз тазобедренных суставов справа — III ст., слева — I ст. Укорочение правой ноги на 2 см».
Выполнено бесцементное тотальное эндопротезирование правого тазобедренного сустава. Послеоперационный период протекал без осложнений.
В течение первого года после операции больная регулярно являлась в СарНИИТО для динамического клинико-лабораторного контроля. Жалоб не предъявляла. При проведении инструментальных методов обследования (рентгенография, денситометрия) видимых изменений не выявлено.
Уровень биохимических маркеров костной ткани через 1,5 месяца после операции:
-
1. Serum CrossLaps 1,3 нг/мл.
-
2. Остеокальцин 18,7 нг/мл.
-
3. Костный изофермент щелочной фосфатазы 32,52 ед/л.
Уровень биохимических маркеров костной ткани через 3 месяца после операции:
-
1. Serum CrossLaps 1,7 нг/мл.
-
2. Остеокальцин 19,9 нг/мл.
-
3. Костный изофермент щелочной фосфатазы 32,5 ед/л.
Уровень биохимических маркеров костной ткани через 6 месяцев после операции:
-
1. Serum CrossLaps 1,61 нг/мл.
-
2. Остеокальцин 20,8 нг/мл.
-
3. Костный изофермент щелочной фосфатазы 32,50 ед/л.
Через 1,5 года после операции больная обратилась с жалобами на боль в области правого тазобедренного сустава, правого бедра, усиливающуюся при движении. Ходит с опорой на костыли. Длина ног равная. Движения в правом тазобедренном суставе ограничены из-за боли. Осевая нагрузка резко болезненная.
Рентгенограмма тазобедренных суставов. Справа — состояние после тотального эндопротезирования тазобедренного сустава, имеется зона резорбции вокруг бедренного компонента эндопротеза; слева — сужение суставной щели (рисунок).
Данные денситометрии: AP Spine=–2,9 SD; Left Femur=–2,6 SD.
Заключение: МПК при обследовании поясничного отдела позвоночника (Т-критерий=–2,9 SD) и проксимального отдела левого бедра (слева Т-критерий=–2,6 SD) соответствует системному осте- опорозу. МПК вокруг эндопротеза справа имеет тенденцию к снижению.
Биохимические маркеры костной ткани:
-
1. Serum CrossLaps 1,78 нг/мл.
-
2. Остеокальцин 20,3 нг/мл.
-
3. Костный изофермент щелочной фосфатазы 32,57 ед/л.
Больной выполнено реэндопротезирование, нестабильность импланта подтверждена интраоперационно.
В данном примере уже через 1,5 месяца после операции уровень Serum CrossLaps увеличился почти в 2 раза, а уровень ОК в 1,5 раза по сравнению с дооперационным уровнем. Данные соотношения содержания Serum CrossLaps и ОК сохранялись в течение всего времени наблюдения. Через 1,5 года после операции диагностирована асептическая нестабильность эндопротеза, подтвержденная интраоперационно при реэндопротезировании.
Полученные нами данные позволили предложить способ прогнозирования результатов эндопротезирования тазобедренного сустава в ранние послеоперационные сроки путем исследования крови пациента в динамике до и через 1,5 месяца после операции. В указанные сроки определяют биохимические маркеры резорбции и формирования кости и, если в послеоперационном периоде по сравнению с дооперационным уровень С-концевых телопептидов зрелого коллагена I типа (Serum CrossLaps) возрастает не менее чем в два раза, а уровень ОК возрастает не более чем в полтора раза, диагностируют выраженное преобладание процессов резорбции, не компенсируемое усилением костеобразования, и прогнозируют высокий риск развития асептической нестабильности эндопротеза (патент РФ № 2373539, опубл. 20.11.09).
Обсуждение. До настоящего времени не только прогнозирование возникновения, но и своевременная диагностика асептической нестабильности является сложной проблемой [9]. Попытки прогнозирования результатов ТЭП ТБС у больных коксартрозом с помощью лабораторных тестов, в том числе возникновения асептической нестабильности в ранние сроки после операции, приводятся в целом ряде исследований, причем в некоторых используются и биохимические способы оценки особенностей ремоделирования кости [7, 8, 10]. Однако, как свидетельствуют литературные источники, описываемые способы отличаются сложностью, длительностью, трудоемкостью и не всегда позволяют оценить про-
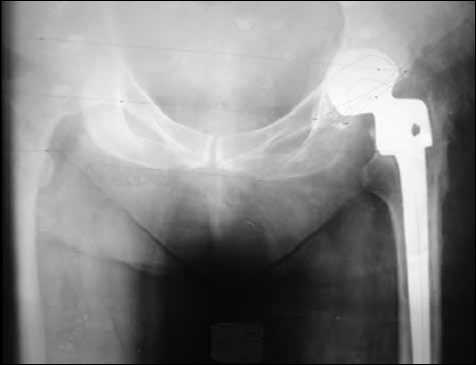
Рентгенограмма тазобедренных суставов больной Ц. через 1,5 года после оперативного вмешательства цессы ремоделирования костной ткани. Были попытки прогнозирования течения костеобразования на дооперационном этапе с помощью исследования биохимических параметров в биологических жидкостях больного (кровь, моча). В сыворотке крови определяли общую активность щелочной фосфатазы и ее костной фракции, а в суточной моче — содержание Са, общего гидроксипролина и креатинина и рассчитывали соотношения указанных величин, при изменении этих расчетных показателей прогнозировали замедленное течение костеобразования. В данном способе необходимо исследовать два биологических субстрата — кровь и мочу, причем приходится собирать суточную мочу, что создает определенные неудобства для амбулаторного больного; определяют 5 параметров и дополнительно проводят расчет еще трех показателей. Кроме того, существенным недостатком способа является его недостаточная точность, что связано с использованием определения общего гидроксипролина мочи, не отражающего обмен коллагена I типа, специфичного именно для костной ткани, а отражающего результирующую метаболических процессов всех соединительно-ткан-ных образований организма, содержащих коллаген не только I, но и других типов (II тип, характерный для хряща и стекловидного тела; III тип, характерный для кровеносных сосудов и т.д.).
Предлагалось проводить прогнозирование результатов эндопротезирования тазобедренного сустава путем динамического обследования пациента до операции и через 1 и 3 месяца после нее и в сыворотке крови определять содержание иммуноглобулинов А и Е, уровня эозинофилов, наличия антител к солям металлов или полимеров эндопротеза. При отличии показателей от дооперационного уровня прогнозировали неблагоприятный результат эндопротезирования [10]. Способ также достаточно сложен (три раза проводят исследование широкого спектра иммунных тестов, в том числе с применением методов, обычно не используемых в широкой практике клинико-диагностических лабораторий (определение антител к составляющим эндопротеза), длителен (требует для своего осуществления не менее трех месяцев) и трудоемок (определяют целый ряд лабораторных параметров — иммуноглобулины А, Е, антитела к солям металлов или полимеров, входящим в состав эндопротеза, эозинофилы). Способ позволяет оценить не особенности стрессового ремоделирования костной ткани, а особенности реагирования иммунной системы организма на составляющие эндопротеза, что в определенной мере связано именно с особенностями металлоконструкции, а в определенной мере с особенностями реакции на нее иммунной системы, и не отражает метаболизм костной ткани.
Нами предложен оригинальный способ прогнозирования результатов ТЭП ТБС в ранние сроки после оперативного вмешательства с помощью динамического исследования маркеров резорбции и
Список литературы Возможность использования лабораторных предикторов в оценке развития асептической нестабильности при тотальном эндопротезировании тазобедренного сустава
- 1.3агородний Н.В., Дирин В. А., Магомедов Х.М. Эндо-протезирование тазобедренного сустава эндопротезами нового поколения//Актуальные вопросы практической медицины: сб. тр. М., 2000. С. 377-387.
- Корнилов Н. В. Состояние эндопротезирования тазобедренного сустава в Российской Федерации//Эндопротезиро-вание крупных суставов: тез. докл. симп. с междунар. участ М.,2000. С. 49-52.
- Абельцев В. П. Десятилетний опыт эндопротезирования тазобедренного сустава при диспластическом коксартро-зе//Вестник травматологии и ортопедии им. Н.Н. Приорова. 2002. №1. С. 54-56.
- Ахтямов И.Ф. К вопросу о преемственности в хирургическом лечении диспластического коксартроза//Вестник травматологии и ортопедии им. Н.Н. Приорова. 2005. № 2. С. 70-75.
- Родионова С.С, Нуждин В. И., Морозов А. К. Остеопо-роз как фактор риска асептической нестабильности при эндо-протезировании тазобедренного сустава//Вестник травматологии и ортопедии им. Н. Н. Приорова. 2007. № 2. С. 35-40.
- Клюшниченко И. В. Независимые от импланта факторы риска развития асептической нестабильности эндопроте-за тазобедренного сустава: автореф. дис.... канд. мед. наук. М.,2008. 15 с.
- Effects upon Metabolism Following Total Hip and Total Knee Arthroplasty/U. Schneider [et al.]//Pathobiol. 2002/2003. Vol. 70. P. 26-33.
- Der Einsatz neuer biochemischer Markerin der Diagnostik aseptischer Huftendoprothesenlockerungen/U. Schneider [et al.]//Zeitschr. Orthop. Grenzgebiete. 1997. Bd. 135. S. 297-300.
- Истомин СЮ. Прогнозирование и диагностика нестабильности после тотального эндопротезирования при деформирующем остеоартрозе тазобедренного сустава: автореф. дис.... канд. мед. наук. М., 2009. 23 с.
- Способ прогнозирования результатов эндопротезирования тазобедренного сустава: пат. 2128341 РФ. № 97113823/14; заявл. 11.08.97. опубл. 27.03.99. Бюл. №9.


