Возможность повышения надежности кишечного шва во время операций на толстой кишке
Автор: Горский В.А., Агапов М.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Экспериментальные и лабораторные исследования
Статья в выпуске: 2 (36), 2014 года.
Бесплатный доступ
В эксперименте на 54 беспородных собаках были исследованы механическая прочность, микробная проницаемость и особенности заживления анастомозов при наложении пластин фибринколлагеновой субстанции (ФКС). В клинике ФКС был использован у 56 больных. И в эксперименте, и в клинике было показано, что использование дополнительного укрепления шва клеевой субстанцией ФКС в условиях тяжелой внутрибрюшной инфекции либо скомпроментированной кишечной стенки является патогенетически оправданным, т.к. помимо придания дополнительной механической прочности, включается эффект стимуляции репаративных процессов.
Кишечный шов, несостоятельность шва, перитонит, клеевая субстанция
Короткий адрес: https://sciup.org/142211154
IDR: 142211154 | УДК: 616-089;
Текст научной статьи Возможность повышения надежности кишечного шва во время операций на толстой кишке
Развитие несостоятельности швов при операциях на толстой кишке возможно в 5–30% случаев [1–6]. При этом последняя цифра обозначает количество больных, у которых данное осложнение возникает в случае неотложных операций. Вероятность несостоятельности повышается при ушивании дефектов или формировании анастомозов в условиях «компроментированной» кишечной стенки. А это характерно для распространенного перитонита и запущенной кишечной непроходимости [7–10]. Высок также риск возникновения осложнений при вмешательствах на правой половине ободочной и терминальном отделе тонкой кишки (например, правосторонняя гемиколэктомия) [2]. Высокий процент несостоятельности швов после вмешательств на толстой кишке связывают с анатомо-физиологическими особенностями строения, характером и вирулентностью населяющей ее микрофлоры [1]. Поэтому следует стремиться создать оптимальные условия для заживления швов и анастомозов при операциях на толстой кишке.
А.А. Запорожец и соавт. [11] обосновал понятие биологической негерметичности швов. Было показано, что в первые три дня после операции на кишечнике брюшная полость инфицируется миллионами кишечных микробов. Микроорганизмы проникают из просвета органов через
«физически» герметичный шов. Временная биологическая проницаемость соустий может привести к образованию порочного круга. Проницаемость хирургического шва для микрофлоры приводит к инфицированию брюшной полости и развитию перитонита. В свою очередь, парез кишечника, который сопровождает перитонит, способствует развитию несостоятельности швов.
Подобная ситуация заставила хирургов разрабатывать различные методы укрепления кишечного шва. С этой целью использовали большой сальник, лоскут париетальной брюшины, твердую мозговую оболочку, аутодермальный имплантат и прочие биологические ткани. При этом установлено, что большой сальник не может полностью обеспечить физическую и биологическую герметичность. Кроме того, в отдаленные сроки он подвергается рубцеванию, что может привести к деформации и стенозу органа [12–15]. Такие виды пластического закрытия анастомоза, как дему-козированный лоскут большой кривизны желудка на сосудистой ножке, стенка толстой и тонкой кишки, не всегда могут быть использованы в ургентной хирургии из-за высокой сложности и опасности [9, 16].
Противоречивы данные применения различных полимерных материалов и биологических клеевых субстанций. Не нашли широкого практического отклика цианокрилат- ные и фибриновые клеи, наносимые поверх кишечного шва [17–23]. Вызывая значительное воспаление тканей, они приводят к возникновению рубцовой деформации и формированию выраженного спаечного процесса [24].
Таким образом, актуален дальнейший поиск средств и методов повышения надежности кишечного шва [25, 26– 29]. С 1997 года мы применяем комбинированную фибринколлагеновую субстанцию (ФКС) «Тахокомб», которая состоит из коллагена, фибриногена, тромбина. В клинике ФКС используют для гемостаза на паренхиматозных органах. Однако ФКС обладает прекрасной адгезией, что делает ее перспективной для укрепления кишечного шва.
Материалы и методы
Нами впервые было проведено экспериментальное исследование по укреплению кишечных швов препаратом ФКС, результаты которого внедрены в клиническую практику.
В эксперименте на 54 беспородных собаках были исследованы механическая прочность, микробная проницаемость и особенности заживления анастомозов при наложении пластин ФКС.
Сравнительную механическую прочность анастомозов исследовали в остром и хроническом эксперименте методом определения давления разрыва анастомоза (ДРА). В опытной группе линию кишечных швов циркулярно закрывали пластиной ФКС. В остром эксперименте ДРА изучали через 5, 10, 30 и 60 минут после аппликации ФКС, сравнивая показания с контрольными соустьями. В хроническом эксперименте механическую прочность анастомоза исследовали на 1, 3, 7 и 14 сутки после операции.
Микробную обсемененность укрепленных ФКС и контрольных анастомозов исследовали в 1 и 3 сутки послеоперационного периода.
Исследование посевов с линии шва, зон наложения ФКС на укрепленном анастомозе, а также из просвета кишки производили методом отпечатков на 3%-ный кровяной агар методом секторных высевов. Для этого готовили специальные пластиковые транспортные кюветы с помещенной в них твердой питательной средой. Кюветы имели герметически закрывающуюся крышку и прозрачное дно, разделенное на 4 равных сектора для визуальной ориентации. Сектора нумеровались от 1 до 4 по часовой стрелке с наружной части дна. Перед исследованием крышка кюветы открывалась. Исследуемая поверхность отпечатывалась на среде в проекции каждого сектора от первого до четвертого в строгой последовательности. Кювета вновь герметизировалась и доставлялась в лабораторию. Кюветы инкубировались при 37 о С 18–24 часа, после чего подсчитывалось число колоний, выросших в разных секторах. Величины выражали в стандартных общепринятых колониеобразующих единицах на грамм исследуемого материала (КОЕ/г).
Особенности заживления укрепленных тонкокишечных соустий изучали в хроническом эксперименте. Визуальный контроль и взятие материала для морфологического исследования осуществляли на 1, 3, 7, 14, 30 сутки после наложения анастомозов.
В клинике ФКС был использован у 56 больных.
Результаты и обсуждение
В остром эксперименте недостоверное различие в показателях механической прочности укрепленного ФКС анастомоза с контрольным соустьем наблюдали только на 5 минуте, при этом в основной группе ДРА составило 135,0±8,7 мм рт. ст., и в контрольной – 131,7±7,3 мм рт. ст. На 10, 30 и 60 минутах после аппликации пластины ФКС разница в прочностных характеристик укрепленных анастомозов была достоверно выше. На 10 минуте ДРА в основной группе в среднем составило 178,3±10,1 мм рт. ст., а в контрольной группе – 128,3±9,3 мм рт. ст. На 30 минуте ДРА опытных соустий составила 185,0±8,7, контрольных – 128,3±8,8 мм рт. ст. Еще более значительным различие отмечены на 60 минуте после апликиции ФКС (табл. 1).
В хроническом эксперименте ДРА через 1 сутки после оперативного вмешательства была невысока, хотя и была выше в основной группе 290,0±18,3 мм водн. ст., чем с контрольной 130,6±10,2 мм водн. ст. На 3 сутки после операции ДРА опытных анастомозов повышалось почти в 3 раза и составило в среднем 940,0±22,2 мм вод. ст., а контрольных – 280,3±7,6 мм водн. ст. (Р<0,01), рис. 1.
На 7 сутки и 14 сутки избыточное давление жидкости приводило к разрыву стенки кишки, а не анастомоза при давлении 2300–2600 мм водн. ст. Достоверных различий между сегментами кишки с опытными и контрольными анастомозами выявлено не было.
Микробная обсемененность опытного анастомоза через 1 сутки после операции составила 45,0±12,7 КОЕ/г ткани и была почти в 3 раза ниже контрольного (130,0±13,4 КОЕ/г). На 3 сутки обсемененность укрепленного анастомоза была в 16 раз ниже контрольного (5,0±3,8 и 80,0±7,1 КОЕ/г соответственно, Р<0,001) (рис. 2).
Таблица 1
Сравнительные результаты исследования механической прочности анастомозов укрепленных ФКС в остром эксперименте на собаках, N = 18
|
Сроки исследования |
Давление разрыва анастомоза (ДРА) в мм. рт. ст. |
Критерий достоверности |
|
|
Основная группа N = 9 |
Контрольная группа N = 9 |
||
|
5 минут |
135,0±8,7 |
131,7±7,3 |
Р±0,01 |
|
10 минут |
178,3±10,1 |
128,3±9,3 |
Р±0,01 |
|
30 минут |
185,0±8,7 |
128,3±8,8 |
Р±0,01 |
|
60 минут |
195,0±2,9 |
128,3±8,8 |
Р±0,01 |
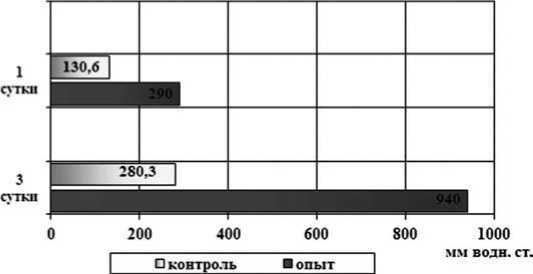
Рис. 1. Сравнительные результаты механической прочности опытного и контрольного анастомозов на 1 и 3 сутки у экспериментальных животных
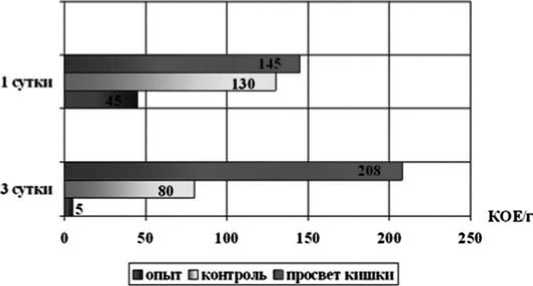
Рис. 2. Сравнительные результаты исследования микробной обсемененности анастомозов и просвета толстой кишки на 1 и 3 сутки (в КОЕ/г)
Изучение особенностей заживления тонкокишечных анастомозов в хроническом опыте позволило выявить эффект стимуляции биополимером репаративных процессов в стенке кишки. ФКС способствовал более быстрой регенерации кишечной стенки по сравнению с контрольными анастомозами. При этом эпителизация дефекта слизистой оболочки опытных анастомозов начиналась уже к 3 суткам, а регенерация железистого аппарата в слизистой оболочке наблюдалась к 14 суткам. У контрольных животных неполное заживление шва со стороны слизистой оболочки в виде однослойной эпителиальной выстилки наблюдали лишь к 14 суткам после операции. В случаях укрепления анастомоза ФКС воспалительная реакция вокруг шовного материала в ранние сроки была выражена меньше, чем у контрольных животных, что проявлялось слабой лейкоцитарной инфильтрацией на 3–7 сутки эксперимента. Реакция на шовный материал в укрепленном кишечном шве чаще имела характер асептического воспаления и не приводила к абсцедированию вокруг лигатур.
Морфологическое исследование позволили в некоторой степени объяснить процесс адгезии биополимера к тканям. Первоначальная адгезия коллагеновой основы ФКС проис- ходит за счет сил сцепления фибрина. В дальнейшем, начиная с 3 суток после аппликации, прочность сцепления биополимера с серозной оболочкой возрастает за счет миграции фибробластов в ячеистую структуру композиции и прорастания ее соединительной тканью. Этот механизм замедляется, если протектором между субстанцией и тканью служит сгусток крови.
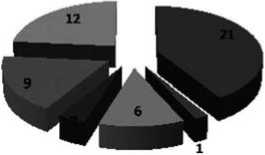
В клинике при операциях на толстой кишке ФКС применили у 56 больных. При этом пластические свойства использовали у 51 больного (рис. 3), гемостатические – у 5 пациентов.
Правостороннюю гемиколэктомию (20 больных) с наложением илеотрансверзоанастомоза и укреплением его биополимером ФКС выполняли по поводу опухолей правой половины ободочной кишки, осложненных перфорацией с распространенным перитонитом либо кишечной непроходимостью. В 1 случае поводом для проведения подобной операции послужило острое нарушение мезентериального кровообращения с развитием некроза участка тонкой и правой половины ободочной кишки.
Ушивание дефектов толстой кишки произвели у 6 больных. У 1 пациента выполнена резекция купола слепой кишки по поводу перфорации в зоне основания червеобразного отростка и выраженного тифлита. У 2 больных – субтотальная колонэктомия при обтурирующих опухолях сигмовидной кишки с кишечной непроходимостью.
В 9 случаях укрепление колоректальных анастомозов производили после ликвидации колостом в плановом порядке. При операциях на толстой кишке все укрепленные швы и анастомозы оказались состоятельны.
Пластические свойства клеевой субстанции были использованы нами у 12 больных в совершенно новом качестве – для профилактики перфорации стенки кишки в случаях возникновения десерозированной поверхности. Ушивание обширных десерозированных участков, особенно при измененной кишечной стенке, может привести к деформации просвета
-
• Правосторонняя гем и колэктомия
-
■ Резекция купола слепой кишки
-
■ Ушивание дефекта кишки
-
■ Субтотальмал колокэктомия
-
■ Ликвидация колостом
-
■ Закрытие десе роз н рован мыт учасіков
Рис. 3. Количество больных, которым использовали пластические свойства ФКС при операциях на толстой кишке
= Тахокомб®
Эластичный гемостатический пластырь
Оригинальная КЛЕЕВАЯ композиция фибриногена, тромбина и коллагена для БЫСТРОЙ обработки ;
тканей операционной раны
-
• Быстрый и надёжный окончательный гемостаз за 3-5 минут'
-
• Обеспечивает герметизацию, непроницаемую для жидкости и воздуха'
-
• Подвергается естественной биодеградации за 3-6 недель'
-
• Готов к применению, не требует подготовки

1. Frilling A, Stavrou G, Mischinger HJ, de Hemptinne B, Rokkjaer M, Klempnauer J et al. Effectiveness of a new carrierbound fibrin sealant versus argon beamer as hemostatic agent during liver resection: a randomized prospective trial. Langenbeck's Arch Surg 2005; 390 (2): 114-120.
Takada
Сокращённая информация по медицинскому применению: Торговое название препарата: Тахокомб®. Активные компоненты: фибриноген 5,5 мг, тромбин 2 ME. Показания к применению: показан для вспомогательного применения у взрослых при хирургических вмешательствах с целью улучшения гемостаза, обеспечения соединения тканей, а также для укрепления швов в сосудистой хирургии, когда результаты стандартных методов недостаточны, Противопоказания: повышенная чувствительность к компонентам губки Тахокомб®, возраст до 18 лет, беременность, период лактации. Способ применения и дозы: Тахокомб® следует наносить на хирургические раневые поверхности в стерильных условиях. Перед наложением губки раневая поверхность должна быть очищена от крови, дезинфицирующих и других жидкостей. Побочные реакции: также как и любой белковый продукт, губка Тахокомб® может вызывать у пациентов реакции гиперчувствительности аллергического типа, обструкцию дыхательных путей, гипотензию и анафилактический шок, Особые указания: внутрисосудистое применение препарата недопустимо. Используйте только ненарушенную упаковку. Повторная стерилизация невозможна. Полная информация по препарату в инструкции по применению.
ООО «Такеда Фармасьютикалс»: ул. Усачёва, 2, стр. 1, 119048, Москва, т.: (495) 933 5511, 502 1626, ф.: (495) 502 1625. Информация для специалистов здравоохранения. Per. уд. М3 РФ: П № 012888/01 от 19.12.2007. Перед применением ознакомьтесь с инструкцией. Имеются противопоказания, www.tachocomb.ru, www.takeda.com.ru . Дата выхода рекламы: декабрь 2013 г.
либо к прорезыванию швов и возникновению перфорации. Избежать этого весьма легко, укрыв поврежденный участок клеевой субстанцией ФКС. Осложнений при подобных манипуляциях на ободочной кишке не наблюдали.
Биополимер ФКС при операциях на толстой кишке использовали и в качестве гемостатика. У 3 больных возникли ятрогенные повреждения селезенки при манипуляциях в левом поддиафрагмальном пространстве (у 1 – при санации брюшной полости, у 2 – при мобилизации селезеночного угла ободочной кишки). В 2 случаях пришлось останавливать обильные капиллярные кровотечения из брыжейки поперечно-ободочной и сигмовидной кишок в условиях распространенного перитонита на этапе мобилизации. Гемостаз другими средствами был не эффективен или опасен повреждением крупных сосудов.
Технические особенности аппликации ФКС
Препарат наносится в один слой. Конфигурация пластины должна моделировать линию шва с захождением краев ФКС на серозный покров не менее чем на 2 см. Перед аппликацией препарат необходимо смочить, кратковременно (1–2 сек.) поместив в раствор антибиотика широкого спектра действия, который предполагается использовать в послеоперационном периоде парентерально. Фиксация осуществляется смоченным в том же растворе марлевым тампоном в течение 5 минут. Удалять тампон необходимо с осторожностью, обязательно от края к центру, придерживая соответствующий край инструментом.
При аппликации препарата ФКС на анастомозы следует соблюдать следующие условия: анастомозы, наложенные «конец в конец» или «конец в бок» укрываются полностью с захватом части брыжейки кишки на 2 см; при наложении боковых соустий укрепляется не только передняя и задняя губа анастомоза, но в обязательном порядке – ушитая культя приводящей петли, т.к. она, как правило, является слабым местом анастомоза; культю отводящей петли можно не укреплять; аппликацию препарата необходимо проводить в последнюю очередь перед зашиванием раны передней брюшной стенки. В противном случае во время проведения санации брюшной полости пластина препарата может быть случайно сдвинута или оторвана при манипуляциях.
Заключение
В результате эксперимента выяснили, что ФКС на 3 сутки послеоперационного периода увеличивает механическую прочность швов в 3 раза, снижая микробную обсеменен-ность зоны дополнительно закрытого анастомоза в 16 раз. При этом был установлен выраженный эффект стимуляции репаративных процессов – нанесение ФКС способствовало более быстрой регенерации кишечной стенки. Эпителиза-ция зоны опытных анастомозов начиналась уже к 3 суткам, а появление железистого аппарата в слизистой оболочке на- блюдалось к 7 суткам. У контрольных животных эти процессы происходили значительно позднее.
Считаем, что использование метода дополнительного укрепления шва клеевой субстанцией ФКС в условиях тяжелой внутрибрюшной инфекции либо скомпроментированной кишечной стенки является патогенетически оправданным, т.к. помимо придания дополнительной механической прочности, включается эффект стимуляции репаративных процессов.
Список литературы Возможность повышения надежности кишечного шва во время операций на толстой кишке
- Карякин А.М. Клинико-экспериментальные данные к выбору анастомоза при правосторонней гемиколэктомии//Вестник хирургии. 1990. № 5. С. 154-157.
- Наумов, Н. В. Решение проблемы несостоятельности толстокишечных анастомозов при ручном шве. Актуальные вопросы колопроктологии: тез. докл. V Всерос. конф. с междунар. участием. Ростов н/Д, 2001. С. 48-49.
- Biondo S., Pares D., Creisltr E. et al. Anastomotic dehiscence after resection and primary anastomosis in left-sided colonic emergenies//Dis. Colon Rectum. 2005. Vol. 48. P. 2272-2280.
- Branagan G., Finnis D. Prognosis after anastomotic leak in colorectal surgery//Dis. Colon Rectum. 2005. Vol. 48. P. 1021-1076.
- Gurjar S.V., Forshaw M.J., Ahktar N., Stewart M., Parker M.C. Indwelling trans-anastomotic rectal tubes in colorectal surgery: a survey of usage in UK and Ireland//Colorectal Dis. 2007. Vol. 9. P. 47-51. .
- Воробей А. В. Принципы обследования больных с энтеро-и колостомами//Проблемы колопроктологии. 2000. Вып. 17. С. 55-58.
- Воробьев Г. И. Хирургия толстой кишки. 50 лекций по хирургии. М.: Мedia Medica, 2003. С. 183.
- Горский В.А., Шуркалин Б.К., Леоненко И.В. Применение Тахокомба в абдоминальной хирургии. М.: «Атмосфера», 2003. 168 с.
- Жебровский В.В. Осложнения в хирургии живота. М.: МИА, 2006. 445 с.
- Запорожец А.А. Роль биологической негерметичности кишечного шва в развитии послеоперационного перитонита.//Тезисы докладов объединенного пленума научных обществ хирургов и травматологов-ортопедов Белоруссии. Минск. 1976. С. 41-42.
- Jones S.A., Steman R.A. Management of chronic infected perforation by the serosal patch technic//Am. J. Surg. 1969. №5. P. 731-734.
- Kimura H. et al. Strangulation ileus resulting from encasement of a loop of the small intestine by the great omentum caused by abnormal adhesion//J. of Gastroenterology. 1996. Vol. 31, №5. P. 711-716.
- Matthiessen P. Risk factors for anastomotic leakage after anterior resection of the rectum//Colorectal Dis. 2006. Vol. 8. P. 366.
- Bruce J., Krukowski Z.H., Al-Khairy G., Russell E.M., Park K.G. Systematic review of the definition and measurement of anastomotic leak after gastrointestinal surgery//Br. J. Surg. 2001. Vol. 88. P. 1157-1168.
- Мохов Е.М., Бредихин Е.И. Укрепление тонко-толстокишечных анастомозов демукозированым трансплантатом толстой кишки//Вестник хирургии. 1990. №6. С. 115-117.
- Загретдинов А.Ш., Нартайлаков М.А., Сакаев Р.Ш. Клеевая герметизация кишечных швов при перитоните у больных различных возрастных групп.//Тезисы докл. 53-й научной конференции молодых ученых БГМИ. Уфа, 1988. С. 52.
- Истомин Н.П., Ратов В.Г. Шовно-клеевое цианокрилатное соединение (критический опыт).//Сборник научн. работ: «Проблемы неотложной хирургии». М., 1998. С. 33.
- Нартайлаков М.А. Клинико-экспериментальное обоснование целесообразности применения шовно-клеевого способа в хирургии кишечника: Дис..канд. мед. наук. Казань, 1989. 95 с.
- Bulow S., Bulut О., Christensen I.J., Harling H. Transanal stent in anterior resection does not prevent anastomotic leakage//Colorectal Dis. 2006. Vol. 8. P. 494-496.
- Tsereteli Z., Sporn E., Geiger T.M., Cleveland D., Frazier S., Rawlings A., Bachman S.L., Miedema B.W., Thaler K. Placement of a covered polyester stent prevents complications from a colorectal anastomotic leak and supports healing: randomized controlled trial in a large animal model//Surgery. 2008. Vol.144. P. 786-792.
- Scileppi T., Li J.J., Iswara K., Tenner S. The use of a Polyflex coated esophageal stent to assist in the closure of a colonic anastomotic leak//Gastrointest. Endosc. 2005. Vol. 62. P. 643-645.
- Ye F., Wang D., Xu X., Liu F., Lin J. Use of intracolonic bypass secured by a biodegradable anastomotic ring to protect the low rectal anastomosis//Dis. Colon Rectum. 2008. Vol. 51. P. 109-115.
- Василевич А.П., Шотт А.В., Запорожец А.А. Использование биологических клеевых композиций при наложении кишечного шва//Здравоохранение Белоруссии. 1989. № 5. С. 14-18.
- Винник Ю. С., Маркелова Н. М., Кузнецов М. Н., Соляников А. С. К вопросу о применении биополимеров для профилактики несостоятельности кишечных анастомозов//Хирургическая практика.-2013. -№ 1.-С. 30-35.
- Kolkert J.L., Havenga K., ten Cate Hoedemaker H.o., Zuidema J., Ploeg R.J. Protection of stapled colorectal anastomoses with a biodegradable device: the C-Seal feasibility study//Am. J. Surg. 2011. Vol. 201. P. 754-758.
- Matthiessen P., Strand I., Jansson K., Tornquist C., Andersson M., Rutegard J., Norgren L. Is early detection of anastomotic leakage possible by intraperitoneal microdialysis and intraperitoneal cytokines after anterior resection of the rectum for cancer?//Dis. Colon Rectum. 2007. Vol. 50. P. 1918-1927.
- Komen N., de Bruin R.W., Kleinrensink G.J., Jeekel J., Lange J.F. Anastomotic leakage, the search for a reliable biomarker. A review of the literature//Colorectal Dis. 2008. Vol. 10. P. 109-115; discussion 115-117.
- Den Dulk M., Noter S.L., Hendriks E.R., Brouwers M.A.,Frilling A, Stavrou G, Mischinger HJ, de Hemptirme B, Rokkjaer M, Klempnauer J et at Effectiveness of a new camerijound fibrin sealant versus argon beamer as hemostatic agent during liver resection: a randomized prospective trial Langenbeck'sArch Surg 2005; 390 (2): 114-120.


