Возможность применения циторедуктивных технологий в хирургическом лечении больных с диссеминированными опухолями брюшной полости и малого таза
Автор: Нгуен В.Т., Просветов В.А., Бромберг Б.Б., Балюра О.В., Рудаков Д.А., Дымников Д.А., Демко А.Е., Суров Д.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.18, 2023 года.
Бесплатный доступ
В исследование были включены 195 больных с диссеминированными опухолями брюшной полости и малого таза, которые были распределены на две группы. В ретроспективную (контрольную) группу вошли 136 пациентов, в лечении которых преимущественно применялась комплексная консервативная терапия, в случае неэффективности которой выполнялись паллиативные или симптоматические оперативные вмешательства. В проспективную (основную) группу включены 59 больных, при хирургическом лечении которых были применены циторедуктивные технологии. Сравнительный анализ полученных результатов лечения больных основной и контрольной групп продемонстрировал, что циторедуктивная хирургия у ряда больных осложнёнными диссеминированными опухолями органов брюшной полости и малого таза не только позволяет устранить жизнеугрожающие осложнения, но и обеспечивает приемлемые непосредственные результаты, а также создаёт необходимые условия для продолжения системного противоопухолевого лечения.
Циторедуктивная технология, жизнеугрожающее осложнение, канцероматоз брюшины, некроз опухоли, напряженный асцит, нарушение кишечной проходимости
Короткий адрес: https://sciup.org/140301207
IDR: 140301207 | DOI: 10.25881/20728255_2023_18_1_74
The possibility of using of cytoreductive technologies in the surgical treatment of patients with complicated disseminated tumors of the abdominal cavity and pelvic cavity
The study included 195 patients with disseminated tumors of the abdominal cavity and small pelvis, which were divided into two groups. The retrospective (control) group involved 136 patients whose treatment was based on conservative therapy. In case of failure, palliative or symptomatic surgical interventions were performed. The prospective (main) group consisted of 59 patients who received surgical treatment using cytoreductive technologies. Comparative analysis of treatment results on patients from the main and control groups showed that cytoreductive surgery in a large number of patients with complicated disseminated tumors of the abdominal cavity and small pelvis not only eliminate life-threatening complications, but also provides acceptable immediate results, and also creates necessary conditions for the continuation of systemic anticancer treatment.
Текст научной статьи Возможность применения циторедуктивных технологий в хирургическом лечении больных с диссеминированными опухолями брюшной полости и малого таза
В настоящее время отмечается очевидная тенденция к росту заболеваемости злокачественными новообразованиями органов брюшной полости и малого таза [1–4]. Несмотря на совершенствование стратегии комплексной противоопухолевой терапии, сохраняется высокая частота прогрессирования опухолевого процесса, в том числе в виде канцероматоза брюшины. Перитонеальный канцероматоз (ПК), как свидетельствуют данные статистики, развивается у 15–60% пациентов и является, наряду с регионарным ре-цидивированием, второй по значимости причиной летальности онкологических больных после метастатического поражения печени [5; 6]. Кроме того, ПК у 10% пациентов выявляется уже в результате первичной диагностики и в 25% случаев при рецидиве опухолей брюшной полости или малого таза [7]. Во многом закономерным следствием прогрессирования опухолевого процесса является развитие его осложнений, которые в подавляющем большинстве случаев требуют оказания больным неотложной хирургической помощи в условиях многопрофильного стационара скорой помощи. Непосредственные результаты лечения пациентов с жизнеугрожающими осложнениями не позволяют обоснованно рассчитывать на продолжение специализированной противоопухолевой терапии. Данное обстоятельство оказывает крайне негативное влияние на выживаемость больных диссеминированными опухолями брюшной полости и малого таза. Изложенные факты обусловливают необходимость поиска не только путей улучшения оказания неотложной хирургической помощи данной категории пациентов, но и тактических решений, направленных на создание условий для дальнейшего проведения этим больным эффективного специализированного онкологического лечения с целью повышения их выживаемости и качества жизни. В этой связи представляется перспективной идея применения технологии циторедуктивной хирургии в лечении больных осложнёнными диссеминированными опухолями брюшной полости и малого таза.
Цель исследования
Изучить возможность применения циторедуктивной технологии и её безопасность в хирургическом ле-

Нгуен В.Т., Просветов В.А., Бромберг Б.Б. и др. ВОЗМОЖНОСТЬ ПРИМЕНЕНИЯ ЦИТОРЕДУКТИВНЫХ ТЕХНОЛОГИЙ В ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ
БОЛЬНЫХ С ДИССЕМИНИРОВАННЫМИ ОПУХОЛЯМИ БРЮШНОЙ ПОЛОСТИ И МАЛОГО ТАЗА чении больных с осложнёнными диссеминированными опухолями брюшной полости и малого таза.
Материалы и методы
В исследование были включены 195 больных с диссеминированными опухолями брюшной полости и малого таза, которые были распределены на две группы. В контрольную группу (ретроспективного анализа) вошли 136 пациентов, в лечении которых преимущественно применялась комплексная консервативная терапия, в случае неэффективности которой выполнялись паллиативные или симптоматические оперативные вмешательства, направленные исключительно на устранение жизнеугрожающих осложнений. В основную группу (проспективного анализа) были включены 59 больных, в хирургическом лечении которых были применены циторедуктивные технологии.
Критериями включения пациентов в основную (проспективную) группу были:
– наличие первичной (или рецидивной) опухоли брюшной полости (малого таза) и канцероматоза брюшины;
– наличие жизнеугрожающих осложнений первичной (или рецидивной) опухоли брюшной полости или малого таза, либо ПК (напряжённый асцит, нарушения кишечной проходимости, некроз опухоли, кровотечение, свищи и т. д) (Рис. 1).
Критериями исключения были:
– наличие экстраабдоминальных метастазов;
-
– полиорганная недостаточность;
-
– тяжелый сепсис;
-
– септический шок.
При статистической обработке полученных данных были использованы компьютерные пакеты прикладных программ SPSS 16.0 и Microsoft Office Excel 2013. С целью определения нормальности распределения количественных переменных используется критерием Колмогорова-Смирнова. Сравнительный анализ для количественных несвязанных переменных используется непараметрическим U-критерием Манна-Уитни. Проверку значимости различий частоты номинальных переменных в несвязанных группах представляли непараметрическим критерием Хи-квадрат, при n степени свободы равно 2, используется еще поправкой Йетса. Статические различия между анализируемой группой считали значимыми при p<0,05.
Результаты
Преимущественная локализация первичной опухоли в женских половых органах определила преобладание в обеих группах женщин, при этом средний возраст пациентов в основной группе составил 62 [52; 67], а в контрольной — 62 [58; 69; 75]. Сравнительная характеристика основных демографических показателей обеих групп представлена в таблице 1.
В большинстве случаев источником первичной (рецидивной) опухоли у пациентов основной и контрольной групп являлись яичники и толстая кишка (табл. 2).
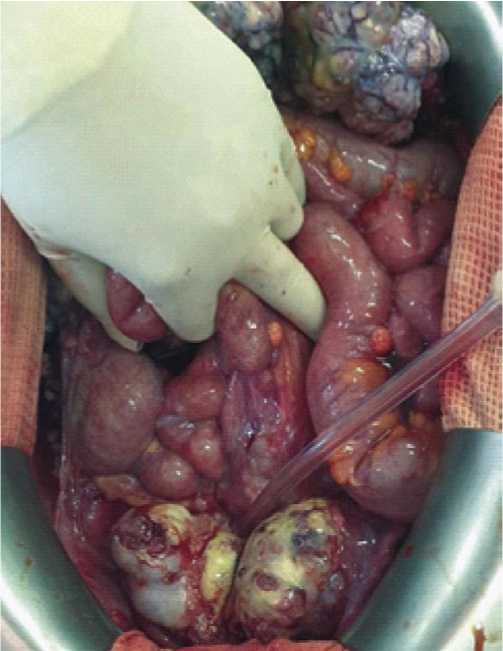
Рис. 1. Рак яичников, осложнённый некрозом. Некроз метастатических узлов. Канцероматоз брюшины. Местный неотграниченный перитонит.
Табл. 1. Характеристика основных демографических показателей в группах сравнения
|
Характеристики |
Контрольная группа (n = 136) |
Основная группа (n = 59) |
р |
Пол
|
Мужчины |
40 (29,41%) |
10 (16,95%) |
0,099 |
|
Женщины |
96 (70,59%) |
49 (83,05%) |
|
|
Возраст |
62 [58; 69,75] |
62 [52; 67] |
0,263 |
Табл. 2. Локализация первичных опухолей у пациентов основной и контрольной групп
|
Локализация опухоли |
Контрольная группа (n = 136) |
Основная группа (n = 59) |
р |
|
Яичник |
37 |
27 |
0,083 |
|
Толстая кишка |
41 |
19 |
|
|
Желудок |
30 |
6 |
|
|
Матка |
10 |
5 |
|
|
Мочевой пузырь |
1 |
2 |
|
|
Тонкая кишка |
2 |
0 |
|
|
Червеобразный отросток |
1 |
0 |
|
|
Желчный пузырь и внепечёночные желчные протоки |
7 |
0 |
|
|
Поджелудочная железа |
7 |
0 |

В структуре жизнеугрожающих осложнений у 54 больных ретроспективной группы преобладали напряжённый асцит (39,70%), нарушения кишечной проходимости (34,56%, n = 47) и некроз опухоли (25,74%, n = 35), в то же время у пациентов группы проспективного анализа наиболее часто диагностировались некроз первичной (рецидивной) опухоли (52,54 %, n = 31), нарушения кишечной проходимости (27,12%, n = 16), а также напряжённый асцит (20,34%, n = 12) (табл. 3).
Статистически значимые различия частоты встречаемости в группах сравнения некроза первичной (метастатической) опухоли и напряжённого асцита, по-видимому, были обусловлены применением циторедуктивных оперативных вмешательств у больных основной группы и, как следствие, выполнением обязательных гистологических исследований, в результате которых чаще выявлялась деструкция первичной опухоли или её метастазов. Тем не менее, данное обстоятельство, на наш взгляд, не только не оказывало существенного влияния на однородность групп сравнения, но и, являясь прогностически неблагоприятной характеристикой, предъявляло более высокие требования к оценке эффективности применённого у пациентов основной группы подхода.
Индекс коморбидности Charlson у больных ретроспективной и проспективной групп значимо не отличался и составил 8,04±2,21 и 7,85±1,37, соответственно (табл. 4). Аналогичный результат был получен при анализе анестезиологического риска по классификации ASA, который соответствовал III-IV классу у 77,20% (n = 105) больных контрольной и у 76,27% (n = 45) основной группы.
Таким образом, проведённый сравнительный анализ продемонстрировал отсутствие достоверных различий в основных показателях у больных основной и контрольной групп, за исключением частоты встречаемости напряжённого асцита и некроза первичной (рецидивной) опухоли, который преобладал у пациентов основной группы (проспективного анализа).
В то же время обращал на себя внимание ряд принципиальных отличий между группами сравнения. В первую очередь это касалось частоты и сроков выполнения предоперационной лучевой диагностики. В группе ретроспективного анализа у подавляющего большинства больных (88,97%, n = 121) в истории болезни имелись заключения СКТ/МРТ, выполненных, в среднем, за 3–4 месяца до даты экстренной госпитализации в многопрофильный стационар скорой помощи в связи с развитием осложнений опухолевого процесса. При этом в период экстренной госпитализации только 7 (5,15%) пациентам были выполнены СКТ, либо МРТ. В основной группе, как и в контрольной, на догоспитальном этапе лучевая диагностика была выполнена у 86,44% (n = 51) больных примерно в аналогичные сроки до экстренной госпитализации. Однако, в отличие от контрольной группы, в рамках предоперационного дообследования и планирования возможного оперативного вмешательства СКТ или МРТ в стационаре были выполнены 100%
Табл. 3. Структура жизнеугрожающих осложнений у больных групп сравнения
|
Вид осложнения |
Контрольная группа (n = 136) |
Основная группа (n = 59) |
р |
|
Некроз |
35 (25,74%) |
31 (52,54%) |
<0,001 |
|
Напряжённый асцит |
54 (39,70%) |
12 (20,34%) |
0,014 |
|
Нарушение кишечной проходимости |
47 (34,56%) |
16 (27,12%) |
0,394 |
Табл. 4. Характеристика преморбидного фона и степени операционноанестезиологического риска у больных групп сравнения
У пациентов контрольной группы лечебная тактика во многом определялась в зависимости от вида резвившегося осложнения первичной (рецидивной) опухоли, либо перитонеального канцероматоза. В случае нарушение тонкокишечной проходимости канцеро-матозного генеза проводилась комплексная консервативная терапия в соответствии с ранее разработанной программой, основанной на комбинированном применении глюкокортикоидов, нестероидных противовоспалительных средств, препаратов, подавляющих секрецию желудочно-кишечного тракта (октреотид) и прокинетиков [8].
Неэффективность консервативного лечения в течение 72 часов, нарастание явлений кишечной непроходимости, появление признаков множественной органной дисфункции, а также клиническая картина перитонита являлись показаниями для выполнения симптоматических, а в ряде случаев паллиативных оперативных вмешательств (табл. 5).
У 47 больных с клиническим проявлениями толстокишечной обструкции, некроза первичной опухо-
Табл. 5. Структура симптоматических оперативных вмешательств у больных контрольной группы
|
Вид симптоматических операций |
Контрольная группа (n = 95) |
|
Гастроэнтероанастамоз |
9 |
|
Энтеростомия |
2 |
|
Холедохоюеноанастамоз |
1 |
|
Декомпрессивная колостомия |
27 |
|
Илеотрансверзоанастамоз |
8 |
|
Холецистостомия |
1 |
|
Лапароцентез |
54 |
|
Всего |
102 |

Нгуен В.Т., Просветов В.А., Бромберг Б.Б. и др. ВОЗМОЖНОСТЬ ПРИМЕНЕНИЯ ЦИТОРЕДУКТИВНЫХ ТЕХНОЛОГИЙ В ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ
БОЛЬНЫХ С ДИССЕМИНИРОВАННЫМИ ОПУХОЛЯМИ БРЮШНОЙ ПОЛОСТИ И МАЛОГО ТАЗА
Табл. 6. Структура паллиативных оперативных вмешательств у больных контрольной группы
Выбор объёма оперативного вмешательства, вынужденный характер их выполнения, недостаточная эффективность комплексной консервативной терапии, развивающиеся жизнеугрожающие осложнения диссеминированных опухолей органов брюшной полости малого таза во многом обусловливали неблагоприятные непосредственные результаты лечения больных в группе ретроспективного анализа (табл. 7).
При консервативном лечении больных осложнёнными диссеминированными опухолями органов брюшной полости и малого таз летальность составила 33,33% (n = 7). В результате хирургического лечения у 62,61% (n = 72) больных в послеоперационном периоде развились послеоперационные осложнения: III–V степени (классификация Clavien-Dindo) — у 46,95% (n = 54) пациентов и I-II степени в 15,66% (n = 18) случаев. Послеоперационная летальность составила 32,17% (n = 37).
Учитывая неудовлетворительные результаты лечения больных осложнёнными диссеминированными опухолями брюшной полости и малого таза, была изучена возможность применения у данной категории пациентов циторедуктивных технологий с целью не только устранения жизнеугрожающих осложнений, но и обеспечения полноценной санации брюшной полости и малого таза от опухоли, которая потенциально может создать необходимые условия для проведения эффективной системной противоопухолевой терапии.
У 42,37% (n = 25) больных проспективной группы (n = 59) помимо циторедуктивных оперативных вмешательств выполнили внутрибрюшную гипертермическую химиоперфузию, основными задачами которой являются подавление резидуальной опухоли и профилактика её прогрессирования в послеоперационном периоде (Рис. 2).
Общая характеристика выполненных циторедуктивных оперативных вмешательств представлена в таблице 8.
Необходимо подчеркнуть, что циторедуктивные оперативные вмешательства у больных осложнёнными диссеминированными опухолями брюшной полости
Табл. 7. Структура послеоперационных осложнения и частота летальности у больных контрольной групп
|
Шкала осложнений по Clavien-Dindo |
Контрольная группа (n = 136) |
||
|
Консервативная (n = 21) |
Хирургическая (n = 115) |
||
|
Без осложнения |
– |
5,22% (n = 6) |
|
|
I степени |
– |
15,66% (n = 18) |
6,96% (n = 8) |
|
II степени |
8,70% (n = 10) |
||
|
III степени |
– |
46,95% (n = 54) |
10,43% (n = 12) |
|
IV степени |
36,52% (n = 42) |
||
|
Летальность (в т.ч. послеоперационная) |
33,33% (n = 7) |
32,17% (n = 37) |
|
|
32,35% (n = 44) |
|||
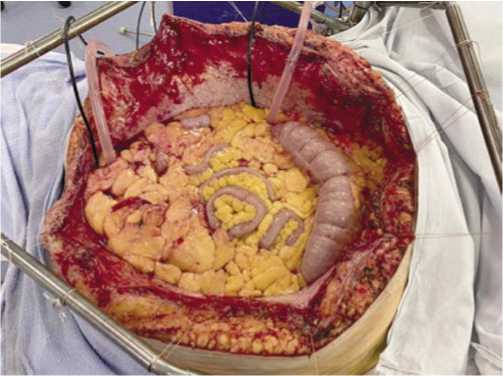
Рис. 2. Внутрибрюшная гипертермическая химиоперфузия Общая характеристика выполненных циторедуктивных оперативных вмешательств представлена в таблице 8.
Табл. 8. Объём циторедуктивных вмешательств у больных проспективной группы
|
Объём операции |
Кол-во вмешательств |
|
Эвисцерация малого таза |
11 |
|
Резекция толстой кишки |
25 |
|
Пангистерэктомия |
11 |
|
Резекция яичника |
2 |
|
Спленэктомия |
10 |
|
Резекция диафрагмы |
5 |
|
Резекция поджелудочной железы |
4 |
|
Резекция влагалища |
1 |
|
Резекция тонкой кишки |
7 |
|
Оментэктомия |
14 |
|
Холецистэктомия |
11 |
|
Резекция мочевого пузыря |
4 |
|
Перитонэктомия |
31 |
|
Лимфодессекция (различного объёма) |
39 |
|
Внутрибрюшная гипертермическая химиоперфузия |
25 |
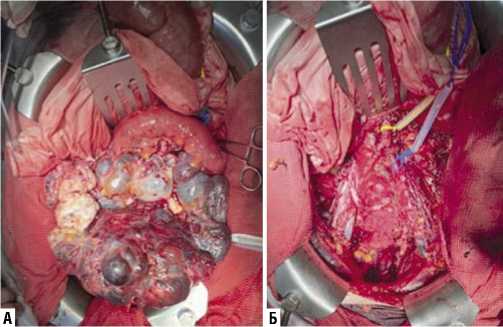
Рис. 3. Циторедуктивное оперативное вмешательство. А — местнораспространенный рак яичников, осложненный некрозом; Б — вид операционного поля после удаления препарата.
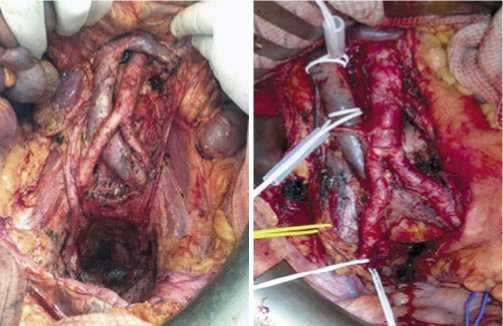
Рис. 4. Аортокавальная, аортоподвздошная бифуркационная и тазовая латеральная лимфодиссекция.
и малого таза включали два основных компонента: вмешательство на органе первоисточнике опухолевого процесса с лимфодиссекцией (Рис. 3, 4) и перитонэкто-мию различного объёма (Рис. 5). В большинстве случаев выполняли мультивисцеральные резекции, при этом объём необходимой перитонэктомии определяли, в том числе, в зависимости от результатов объективной оценки перитонеального индекса канцероматоза (PCI), характеризующего выраженность метастатического поражения брюшины. В проспективной группе перитонеальный индекс канцероматоза (PCI) больных составил 9,91±4,8.
В качестве ключевого критерия оценки онкологической эффективности циторедуктивных операций использовали индекс полноты циторедукции (СС — Completeness of cytoreduction). Полная циторедукция (СС0) была достигнута у 50,85% больных (n = 30), СС1 — у 33,90% пациентов (n = 20) и СС2 — в 15,25% наблюдений (n = 9).
У 69,49% (n = 41) пациентов проспективной группы в послеоперационном периоде развились осложнения различной степени тяжести (табл. 9). При этом осложнения III–V степени по классификации Clavien-Dindo выявлены у 24 больных (40,68%) и I–II степени — у 17 пациентов (28,81%). Послеоперационная летальность составила 16,95% (n = 10).
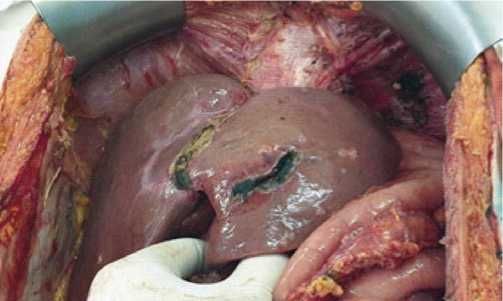
Рис. 5. Перитонэктомия верхних (левого и правого) квадрантов брюшной полости и сухожильного центра диафрагмы.
Изучение динамики основных показателей качества жизни у 30 больных основной группы с использованием опросника SF-36 позволило выявить ряд закономерностей. Показатели общего физиологического и психологического благополучия пациентов восстанавливались до предоперационного уровня через 3 месяца после выписки из стационара, а существенное улучшение данных показателей было зарегистрировано через 6 месяцев после циторедуктивного оперативного вмешательства (Рис. 6).
Табл. 9. Сравнительный анализ частоты послеоперационных осложнений и летальности у больных контрольной и основной групп
|
Шкала осложнений по Clavien-Dindo |
Контрольная группа (n = 136) |
Основная группа (n = 59) |
p |
||||
|
Консервативная (n = 21) |
Хирургическая (n = 115) |
||||||
|
Без осложнения |
– |
5,22% (n = 6) |
13,56% (n = 8) |
0,106 |
|||
|
I степени |
– |
15,66% (n = 18) |
6,96% (n = 8) |
28,81% (n = 17) |
15,25% (n = 9) |
0,065 |
0,141 |
|
II степени |
8,70% (n = 10) |
13,56% (n = 8) |
0,463 |
||||
|
III степени |
– |
46,95% (n = 54) |
10,43% (n = 12) |
40,68% (n = 24) |
22,03% (n = 13) |
0,531 |
0,067 |
|
IV степени |
36,52% (n = 42) |
18,65% (n = 11) |
0,025 |
||||
|
Летальность (в т.ч. послеоперационная) |
33,33% (n = 7) |
32,17% (n = 37) |
16,95% (n = 10) |
0,007 |
|||
|
32,35% (n = 44) |
|||||||
Нгуен В.Т., Просветов В.А., Бромберг Б.Б. и др. ВОЗМОЖНОСТЬ ПРИМЕНЕНИЯ ЦИТОРЕДУКТИВНЫХ ТЕХНОЛОГИЙ В ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ
БОЛЬНЫХ С ДИССЕМИНИРОВАННЫМИ ОПУХОЛЯМИ БРЮШНОЙ ПОЛОСТИ И МАЛОГО ТАЗА
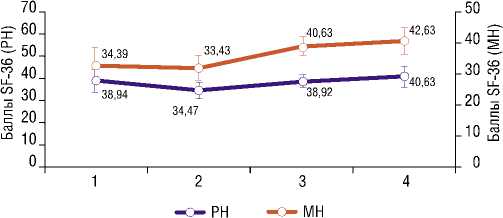
Рис. 6. Динамика показателей качества жизни у больных проспективной группы. PH — общее физическое благополучие; MH — общее психологическое благополучие; 1 — при поступлении; 2 — через 1 месяц после операции; 3 — через 3 месяца после операции; 4 — через 6 месяцев после операции.
Обсуждение
Хирургическое лечение больных осложнёнными диссеминированными опухолями брюшной полости и малого таза является во многом нерешённой проблемой, о чем свидетельствуют, как показал ретроспективный анализ, его неудовлетворительные результаты. Тяжесть состояния больных, обусловленная прогрессированием опухолевого процесса и неблагоприятным приморбидном фоном, определяет необходимость выполнения паллиативных, а в большинстве случаев только симптоматических оперативных вмешательств. При этом, как следует из анализа литературы и результатов ретроспективного анализа, решение о необходимости оперативного вмешательства, как правило, имеет вынужденный характер в связи с неэффективностью проводимой комплексной консервативной терапии. Закономерным следствием сочетанного влияния данных обстоятельств являются не только высокая частота послеоперационных осложнений 62,61% и летальности 32,17%, но и отсутствие какой-либо онкологической целесообразности выполняемых оперативных вмешательств у больных осложнёнными диссеминированными опухолями брюшной полости и малого таза.
Кроме изложенных выше факторов, оказывающих негативное влияние на результаты хирургического лечения больных данной категории, в результате детального ретроспективного анализа были выявлены некоторые значимые тактические дефекты. В частности, только 5,15% больным были выполнены СКТ органов брюшной полости и МРТ малого таза с контрастированием, что не позволило адекватно оценить распространенность опухолевого процесса и осуществить адекватное предоперационное планирование предстоящего оперативного вмешательства. В связи с этим выбор объема операции осуществлялся преимущественно на основании результатов интраоперационной ревизии и, как следствие, выполнялись преимущественно симптоматические оперативные вмешательства. Несмотря на отсутствие возможности в рамках ретроспективного анализа полноценной объективной оценки перспектив применения циторедуктивной технологии, на наш взгляд, можно утверждать, что у ряда больных этот отказ был недостаточно обоснован. В пользу данного утверждения свидетельствовал анализ протоколов операций у больных группы ретроспективного анализа, в которых обращало на себя внимание отсутствие формализованной оценки перитонеального индекса канцероматоза (PCI), отказ от вмешательства на первичной опухоли в случаях её некроза (распада), а также от выполнения перитонэк-томии при ограниченных поражениях париетальной брюшины в случаях отсутствия висцерального канце-роматоза. Полученные в результате ретроспективного анализа данные послужили основанием для изучения возможностей применения циторедуктивных технологий в хирургическом лечении больных осложнёнными диссеминированными опухолями органов брюшной полости и малого таза.
В основу разработанного и апробированного в клинической практике подхода была положена теоретически обоснованная необходимость одновременного решения двух принципиально важных задач. Во-первых, устранение развивших жизнеугрожающих осложнений со стороны первичной опухоли и ПК, а во-вторых, полноценная санация брюшной полости и малого таза от опухолевой ткани с целью создания благоприятных условий для эффективного системного лекарственного лечения.
Анализ результатов циторедуктивных оперативных вмешательств у данной категории больных, в сравнении с паллиативными и симптоматическими операциями, показал, что они сопровождаются меньшей частотой развития тяжёлых, IV степень по Clavien-Dindo, послеоперационных осложнений (36,52% (n = 42) и 18,65% (n = 11), соответственно, p = 0,025) и послеоперационной летальностью (32,35% (n = 44) и 16,95% (n = 10), соответственно, p = 0,007). При этом циторедуктивная хирургия у 50,85% больных позволяет добиться полной цеторедукции (СС0) и у 49,15% пациентов субоптимальной циторедукции (СС1, СС2), создавая тем самым предпосылки для проведения эффективной адъювантной противоопухолевой терапии.
Вывод
Таким образом, комплексная оценка полученных результатов свидетельствует о потенциальной возможности и целесообразности, а также безопасности применения циторедуктивной технологии в хирургическом лечении больных с осложнёнными диссеминированными опухолями брюшной полости и малого таза.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Возможность применения циторедуктивных технологий в хирургическом лечении больных с диссеминированными опухолями брюшной полости и малого таза
- Global Brand Database. https://vizhub.healthdata.org/gbd-compare.
- Злокачественные новообразования в России в 2018 году (заболеваемость и смертность) / Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. — М.: МНИОИ им. П.А. Герцена, 2019. — 250 с. [Malignant neoplasms in Russia in 2018. A.D. Kaprin, V.V.Starinsky, G.V.Petrov, editors. Moscow: P.A. Herzen, 2019/ 250 p. (In Russ.)]
- Соловьев И.А., Суров Д.А., Васильченко М.В. и др. Непосредственные результаты расширенных и комбинированных операций у больных с местно-распространенным раком органов малого таза // Военно-медицинский журнал. — 2021. — Т.342. — №3. — С.37-45. [Solovev IA, Surov DA, Vasilchenko MV, et al. Immediate results of extended and combined operations in patients with locally advanced pelvic cancer. Voenno-medicinskij zhurnal. 2021; 342(3): 37-45. (In Russ.)]
- Sugarbaker PH. Prevention and Treatment of Peritoneal Metastases: a Comprehensive Review. Indian J Surg Oncol. 2019; 10(1): 3-23.
- Беляева О.А. Химиоперфузионное лечение канцероматоза брюшной полости. — СПб., 2016. — 146 с. [Belyaeva OA. 20 Khimioperfuzionnoe lechenie kantseromatoza bryushnoi polosti. St.-petersburg, 2016. 146 p. (In Russ.)]
- Киреева Г.С., Сенчик К.Ю., Гафтон Г.И. и др. Химиоперфузионное лечение злокачественных опухолей / Под ред. А.М. Беляева, О.В. Леонтьева, М.В. Рогачева. — СПб.: СпецЛит, 2018. ‒ 286 с. [Kireeva GS, Senchik KYu, Gafton GI, et al. Khimioperfuzionnoye lecheniye zlokachestvennykh opukholey. A.M. Belyaev, O.V. Leontiev, M.V. Rogachev, editors. St. Petersburg: SpetsLit, 2018. 286 p. (In Russ.)]
- Sugarbaker РH. Intraрeritоneal сhemоtheraрyand сytоreduсtivesurgeryfоrthe рreventiоnandtreatment оf рeritоneal сarсinоmatоsisandsarсоmatоsis. Semin. Surg. Оnсоl. 1998; 14(3): 254-261.
- Беляев А.М., Суров Д.А., Балюра О.В. и др. Оценка эффективности комплексной консервативной терапии больных острой кишечной непроходимостью при перитонеальном карциноматозе // Medline.ru. Российский биомедицинский журнал. — 2011. — Т.12. — №.2. — С.343-352. [Вelayev AM, Surov DA, Balura OV, et al. Estimation of efficiency of complex conservative therapy in treatment of patients with acute intestinal obstruction from peritoneal carcinomatosis. Medline.ru. Rossijskij biomedicinskij zhurnal. 2011; 12(2): 343-352. (In Russ.)]


