Возможности коррекции синдрома эндогенной интоксикации при интраоперационном облучении больных раком желудка
Автор: Афанасьев С.Т., Авдеев С.В., Ли А.А., Рудык Ю.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 1 (21), 2007 года.
Бесплатный доступ
Проведено изучение эффективности методики корригирующей медикаментозной терапии, включающей мексидол, токоферол ацетат и гордокс, которая дополнительно назначалась на периоперационном этапе комбинированного лечения рака желудка, по сравнению со стандартным ведениемпослеоперационного периода. В исследование включено 56 больных с местнораспространен-ной опухолью, которым была выполнена радикальная операция в сочетании с интраоперационным облучением на зоны лимфогенного метастазирования в дозе 10 Гр. По результатам проведенного исследования установлено, что применение корригирующей медикаментозной терапии в раннем послеоперационном периоде достоверно снижает уровень основных маркеров эндогенной интоксикации и улучшает непосредственные результаты операции. В основной группе нехирургические осложнения наблюдались в 9,1 %, послеоперационная летальность равнялась 3,0 %; в контрольной группе - 34,8 % и 8,7 % соответственно.
Рак желудка, интраоперационная лучевая терапия, синдром эндогенной интоксикации
Короткий адрес: https://sciup.org/14054540
IDR: 14054540
Correction of endogenous intoxication syndrome after intraoperative radiation therapy for stomach cancer patients
The study of the efficacy of corrective drug therapy including mexidol, tocopherol acetate and gordox administered in early postoperative period to stomach cancer patients was carried out. The study included 56 patients with locally advanced stomach cancer who underwent radical surgery in combination with 10 Gy intraoperative radiation therapy delivered to the areas of potential metastatic spread. Corrective drug therapy administered in early postoperative period was found to result in the decrease in the level of the main markers of endogenous intoxication and improvement of short-term treatment results. Non-surgical complications were observed in 9,1 % of the study group patients. Postoperative lethality rate was 3,0 %. The corresponding values forthe control group were 34,8 % and 8,7 %, respectively.
Текст научной статьи Возможности коррекции синдрома эндогенной интоксикации при интраоперационном облучении больных раком желудка
Общий уровень интоксикации онкологического больного в раннем послеоперационном периоде при комбинированном лечении в сочетании с интраоперационной лучевой терапией (ИОЛТ) складывается из интоксикации, связанной с опухолевым процессом, последствий хирургического вмешательства, действия электронного облучения на фоне повреждающего воздействия операционной травмы и препаратов наркоза. Развитие злокачественных новообразований приводит к стресс-индуцированным реакциям, нарушению всех видов обмена, активации протеолиза, дисбалансу в системе перекисного окисления, энергодефициту. На этом фоне хирургическое воздействие на опухолевые и окружающие здоровые ткани влечёт за собой также повреждение клеток, что ведёт к образованию и выбросу в кровь продуктов их жизнедеятельности, а также биологически активных веществ [6, 9, 11].
I группа (основная) – 33 больных, которым была выполнена радикальная операция в сочетании с ИОЛТ в однократной дозе 10 Гр на фоне специальной корригирующей медикаментозной терапии (КМТ), направленной на предупреждение периоперационных осложнений.
II группа (контрольная) – 23 больных, получивших хирургическое лечение в сочетании с интраоперационным облучением в дозе 10 Гр.
Формирование исследуемых групп осуществлялось после комплексного обследования, включавшего клинико-лабораторные, рентгенологические, ультразвуковые, эндоскопические и морфологические исследования методом «случай-контроль». В сравниваемых группах распределение по полу и возрасту было одинаковым: мужчин – 33 (58,9 %), женщин – 23 (41,1 %), в возрасте от 39 до 71 года, средний возраст – 56,7 ± 4,9 года. Состав групп больных по распространенности и гистологическому типу опухолевого процесса также был практически однороден. Объем радикальных операций, выполненных в сравниваемых группах (табл. 1), одинаков (p>0,05), что позволило провести адекватный сравнительный анализ результатов исследования.
Таблица 1
Распределение больных в сравниваемых группах по объему оперативного вмешательства, абс.ч.,%
Источником энергии при выполнении ИОЛТ служил малогабаритный бетатрон, генерирующий пучок быстрых электронов с энергией 6 МэВ, аппарат размещен непосредственно в операционной, на специальной потолочной подвеске. Во время операции, после органоуносящего этапа вмешательства, проводилось облучение ложа удаленной опухоли и зон регионарного метастазирования в разовой дозе 10 Гр.
В качестве метода общей анестезии взята за основу комбинированная эндотрахеальная анестезия с ингаляцией закиси азота и галогеносодержащих анестетиков (галотана, севофлюрана), внутривенным введением фентанила. Для проведения анестезиологического пособия использовался наркозный аппарат Dreger «Fabius». В основной группе в схему наркоза добавлена корригирующая медикаментозная терапия (КМТ), которая может рассматриваться как специальный компонент общей анестезии и послеоперационной интенсивной терапии. Целью последней являлись предупреждение и коррекция избыточной активности систем перекисного окисления ли- пидов и связанных с ними нарушений регуляции агрегатного состояния крови и детоксикации в предоперационном, операционном и послеоперационном периодах. Методика КМТ включала комплекс антиоксидантной терапии, применение мексидола, токоферола ацетата в сочетании с антиферментными препаратами, ее начинали за 1 ч до операции путем внутримышечного введения токоферола ацетата в дозе 300 мг и мексидола внутривенно в дозе 200 мг. На этапе удаления опухоли и выполнения лимфодис-секции, за 45–50 мин до проведения ИОЛТ, внутривенно вводили мексидол в дозе 400 мг и гордокс в дозе 100 000 ЕД. После завершения операции продолжалось внутримышечное введение токоферола ацетата в дозе 300 мг через каждые 8 ч и мексидола в дозе 200 мг внутривенно через каждые 6 ч в течение 3–5 сут раннего послеоперационного периода.
Оценку эффективности методики корригирующей медикаментозной терапии проводили по динамике лабораторных методов, отражающих уровень эндогенной интоксикации, для этого производилось определение общей (ОКА) и эффективной концентрации альбумина (ЭКА), резерва связывающей способности альбумина (РСА), лейкоцитарного индекса интоксикации (ЛИИ) по Я.Я. Кальф-Калиф, ядерного индекса интоксикации (ЯИИ) по Г.А. Даштаянц, индекса токсичности (ИТ), уровня молекул средней массы (МСМ) по Н.И. Габриэлян [7]. Забор крови для исследования осуществляли в установленные сроки: перед операцией; во время операции, после завершения сеанса ИОЛТ; в 1, 3, 5-е сут раннего послеоперационного периода.
Полученные данные подвергались статистической обработке при помощи программы STATISTICA 6.0. Достоверность различий оценивали с помощью непараметрических критериев U-критерия Манна-Уитни, W-критерия Уилкоксона и точного теста Фишера для качественных признаков. Различия считали достоверными при p<0,05. Для определения существования корреляций между параметрами вычисляли коэффициент корреляции Спирмана (R), который считали достоверным при p<0,05 [10].
Результаты и обсуждение
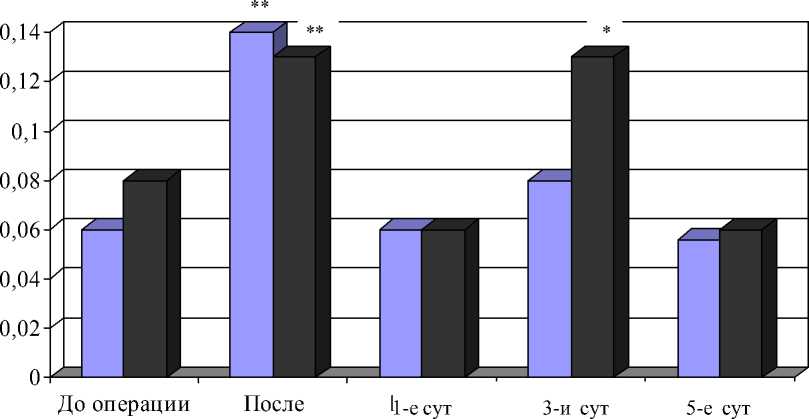
Для оценки степени токсического воздействия нами проанализирована динамика показателей, харак- теризующих степень интоксикации организма. По полученным данным об изменении индекса «ядер-ного сдвига» можно заключить, что обе группы пациентов показали адекватную реакцию на операционный стресс, которая выразилась в увеличении значения ЯИИ. Непосредственно по окончании оперативного вмешательства его величина у пациентов контрольной группы, возросла в 1,6 раза, а в основной группе – в 2,3 раза. На 3-и сут после операции у больных контрольной группы значение ядерного индекса интоксикации превышало аналогичный показатель у пациентов основой группы в 1,6 раза (рис. 1).
В литературе имеются данные о том, что ИОЛТ может рассматриваться в качестве дополнительного повреждающего фактора [2, 3]. Наблюдаемое различие в показателях ядерного индекса интоксикации можно объяснить проводимой медикаментозной коррекцией эндогенной интоксикации в основной группе больных. Таким образом, у этих пациентов наблюдалась менее выраженная реакция нейтрофильного ростка кроветворения на одинаковый раздражитель.
По данным проведенного анализа непосредственно после операции уровень МСМ в обеих сравниваемых группах недостоверно повысился. При этом в контрольной группе в несколько большей степени, чем в основной (табл. 2). При этом в обеих группах снизились общая и эффективная концентрации альбумина, возрос показатель РСА. Непосредственно после операции индекс токсичности у больных контрольной группы остался без изменений, а у пациентов основной группы он оказался снижен относительно исходных значений в 1,5 раза (р<0,05).
Интегральный показатель эндогенной интоксикации – индекс токсичности возрастал в послеопераци-
операции
□ I группа (основная) □ II группа (контроль)
Рис. 1. Значение ядерного индекса интоксикации у пациентов сравниваемых групп. Примечание: * – различия статистически значимы между сравниваемыми группами (p<0,05); ** – различия статистически значимы по сравнению с исходным уровнем (р<0,05)
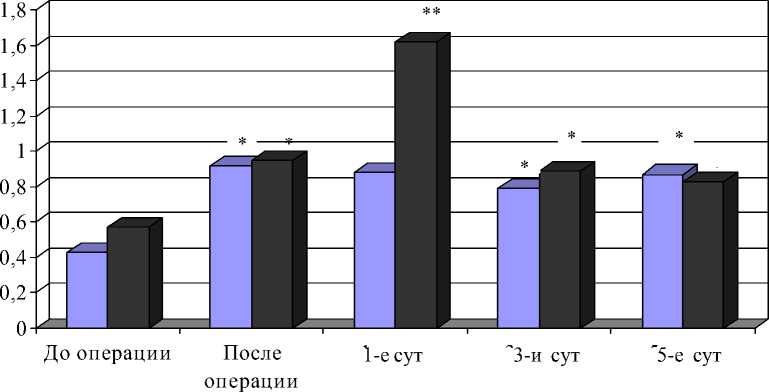
□ I группа (КМТ) □ II группа (контроль)
Таблица 2
Динамика показателей эндотоксикоза в сравниваемых группах
|
Маркеры интоксикации |
До операции |
После операции |
||
|
КМТ |
Контроль |
КМТ |
Контроль |
|
|
МСМ, ед. опт. плот. |
0,46 ± 0,089 |
0,46 ± 0,050 |
0,46 ± 0,069 |
0,47 ±0,052 |
|
ОКА, г/л |
52 ± 3 |
51 ±2 |
42 ± 1** |
43 ±2* |
|
ЭКА, г/л |
40 ±3 |
40±2 |
35 ± 2** |
34±1* |
|
РСА, % |
76,9 ± 4,6 |
78,4 ± 5,2 |
79,5 ± 3,9 |
84,6 ± 3,1 |
|
ИТ, усл.ед. |
0,30 ± 0,05 |
0,28 ± 0,06 |
0,20 ± 0,03* |
0,26 ± 0,02 |
Примечание: * – р<0,05; ** – р<0,01, различия статистически значимы по сравнению с исходными показателями.
Таблица 3
Динамика показателей эндогенной интоксикации в раннем послеоперационном периоде
|
Маркеры интоксикации |
1-е сут после операции |
3-и сут после операции |
5-е сут после операции |
|||
|
КМТ |
Контроль |
КМТ |
Контроль |
КМТ |
Контроль |
|
|
МСМ, ед. опт. плот. |
0,43 ± 0,49 |
0,50 ± 0,30 |
0,43 ± 0,40 |
0,51 ± 0,49 |
0,41 ± 0,48 |
0,49 ± 0,59 |
|
ОКА, г/л |
43 ± 1* |
39 ± 1 |
42 ± 1 |
38 ± 1 |
42 ± 1 |
40 ± 2 |
|
ЭКА, г/л |
35 ± 1 |
33 ± 2 |
33 ± 1* |
29 ± 2 |
33 ± 1 |
30 ± 1 |
|
РСА, % |
81,4 ± 5,4 |
82,5 ± 6,2 |
78,6 ± 1,4 |
76,3 ± 2,9 |
78,6 ± 4,1 |
75,0 ± 3,8 |
|
ИТ, усл.ед. |
0,23 ± 0,09 |
0,22 ± 0,08 |
0,27 ± 0,09 |
0,31 ± 0,05 |
0,27 ± 0,08* |
0,33 ± 0,03 |
Примечание: * – различия статистически значимы по сравнению с исходными показателями (р<0,05).
онном периоде в обеих группах обследованных пациентов. Однако если в контрольной группе пациентов нарастание показателя носило непрерывный характер, то проведение КМТ в основной группе больных позволило сдержать рост ИТ и стабилизировать его на 3-и сутки после операции. Таким образом, к 5-м суткам ИТ в контрольной группе пациентов превышал аналогичный показатель у больных основной группы в 1,2 раза (р<0,05) (табл. 3).
Изучение маркеров эндотоксикоза позволяет сделать заключение о том, что оперативное вмешательство в сочетании с интраоперационным облучением является мощным повреждающим фактором и может привести к ухудшению «лабораторного» состояния больного, что является платформой для последующего развития общесоматических послеоперационных осложнений. Однако проведение профилактических мероприятий, направленных на предупреждение эндогенной интоксикации и уменьшение выраженности последствий хирургической и лучевой агрессии – применение методики КМТ, – способствует более эффективному репаративному процессу в послеоперационном периоде.


