Возможности новой методики эндоскопической визуализации у пациентов с рубцовым стенозом гортани и трахеи
Автор: Овчинников А.Ю., Горбан Д.Г., Коржева И.Ю.
Журнал: Московский хирургический журнал @mossj
Статья в выпуске: 4 (50), 2016 года.
Бесплатный доступ
В статье представлены результаты применения эндоскопической эхографии в диагностике и лечении 49 пациентов с рубцовым стенозом гортани и трахеи. Описана методика выполнения эндоскопической эхографии, сформулированы показания и противопоказания к ее выполнению у пациентов с рубцовым стенозом гортани и трахеи. Сделаны выводы о диагностической ценности этого метода исследования.
Рубцовый стеноз гортани и трахеи, эндоскопическая эхография
Короткий адрес: https://sciup.org/142211270
IDR: 142211270
Текст научной статьи Возможности новой методики эндоскопической визуализации у пациентов с рубцовым стенозом гортани и трахеи
Проблема диагностики и хирургического восстановления просвета дыхательных путей при рубцовом стенозе гортани и трахеи привлекает к себе внимание отоларингологов, торакальных хирургов, эндоскопистов и врачей других специальностей сложностью, целым кругом не решенных вопросов и имеет не только медицинское, но и большое социальное значение [3, 6, 8]. Число пациентов со стенозами и дефектами гортани и трахеи не имеет устойчивой тенденции к снижению и остается достаточно высоким. Это объясняется не снижающимся уровнем травматизации органов шеи, развитием реанимации, увеличением числа интубационных повреждений гортани и трахеи, увеличением хирургической активности по поводу опухолей органов шеи [1, 3, 7, 12].
Сроки медицинской реабилитации данной категории пациентов продолжительны, а успех лечения и уменьшение его длительности во многом зависят от своевременности и полноты обследования пациента, применения современного оборудования, современных методик, как во время обследования, так и при хирургическом лечении [8, 9].
В настоящее время фиброларинготрахеоскопия, является одним из основных методов обследования пациентов со стенозом гортани и/или трахеи [3, 5, 10, 11]. Эндоскопическая картина состояния дыхательных путей, в совокупности с клиническими данными и данными рентгенологического исследования, является основой диагностики патологического процесса, критерием, позволяющим, определив ха- рактер, распространенность, выраженность патологического процесса в гортани и трахеи, верифицировать диагноз, достоверно оценить эффективность проводимого лечения.
В тоже время, достижения медицинской науки последних лет, позволяют заключить, что возможности эндоскопических методов диагностики и лечения различной патологии гортани и трахеи, на наш взгляд не реализованы в полной мере и перечень показаний для их реализации будет расширяться по мере развития эндоскопической техники.
Цель исследования: оценка диагностической ценности эндоскопической эхографии (ЭЭ) при рубцовом стенозе гортани и трахеи.
Материалы и методы
Обследовано 49 пациентов с хроническим рубцовым стенозом гортани и трахеи, поступивших на лечение в ГКБ им. С.П. Боткина г. Москвы. Возраст пациентов варьировал в пределах от 16 до 68 лет, мужчин - 29 (59,2%), женщин – 20 (40,8%). Анализ причин, приведших к стенозу гортани и трахеи выявил, что развитие стеноза было обусловлено продленной ИВЛ и трахеостомией, травмами органов шеи. По поводу устранения рубцового стеноза гортани и трахеи выполнено 49 операций: в плановом порядке – 21 (42,8%), экстренно – 28 (57,2%). У 13(46%) пациентов с декомпенсацией дыхания операции по восстановлению дыхания (тра-хеостомия/ретрахеостомия) сочетались с одномоментно выполняемой ларинготрахеопластикой. Методы обследования пациентов со стенозом гортани и трахеи примененные переоперационно представлены в таблице 1.
Таблица 1
Методы диагностики, примененные у пациентов со стенозом гортани и трахеи
|
Методы диагностики |
Пациенты, госпитализированные планово |
Пациенты, госпитализированные экстренно |
|
|
Стандартный оториноларингологический осмотр |
21 (100%) |
28 (100%) |
|
|
Рентгенография шеи в прямой и боковой проекции |
21 (100%) |
15 (53,6%) |
|
|
КТ-шеи (МСКТ) |
21 (100%) |
3 (10,7%) |
|
|
Ультразвуковое исследование мягких тканей шеи. |
21 (100%) |
0% |
|
|
Фиброларинготрахеоскопия |
Предоперационно |
21 (100%) |
10 (35,7%) |
|
Интраоперационно |
0% |
28 (100%) |
|
|
Послеоперационно |
21 (100%) |
28 (100%) |
|
|
Эндоскопическая конвексная эхография |
Предоперационно |
21 (100%) |
0% |
|
Интраоперационно |
14 (66,7%) |
28 (100%) |
|
|
Послеоперационно |
21 (100%) |
28 (100%) |
|
Всем пациентам выполняли эндоскопическое исследование (ЭИ) в соответствии с алгоритмом обследования и лечения пациентов со стенозом гортани и трахеи:
-
• при поступлении (дооперационно);
-
• интраоперационно;
-
• по окончании операции;
-
• в динамике лечения (на 5-6, 10 сутки после операции).
ЭИ предполагало выполнение традиционной фиброла-ринготрахеобронхоскопии, а также ультразвукового кон-вексного сканирования гортани и трахеи.
Для сравнительной оценки диагностической информативности ЭЭ гортани и трахеи всем пациентам выполнено традиционное ультразвуковое сканирование шеи линейным датчиком. Ультразвуковое исследование шеи выполняли на аппарате Toshiba Aplio MX датчиком PLT – 1204BT с частотой 12 Mhz.
В доступной литературе описание методики ультразвукового исследования гортани и трахеи при ЭИ нами не обнаружено, поэтому в ходе проводимого исследования была разработана методика ЭЭ гортани и трахеи.
Методика исследования. Ультразвуковое сканирование проводили при помощи специального видеобронхоскопа (BF-UC160F-OL8 фирмы “OLYMPUS”), оснащенного кон-вексным датчиком с частотой сканирования 7,5 Mhz (рис. 1). Поверх датчика одевается латексный баллон, который наполняется дистиллированной водой для лучшего контакта со слизистой оболочкой. Датчик расположен дистальнее оптики, это позволяет визуализировать область сканирования. Сканирование линейное, направлено параллельно оси органа. Ширина датчика 6,9 мм, диаметр вводимой трубки 6,2 мм. Видеобронхоскоп оснащен боковой оптикой 30º, поэтому имеются особенности его проведения. Датчик располагается таким образом, чтобы его сканирующая по-
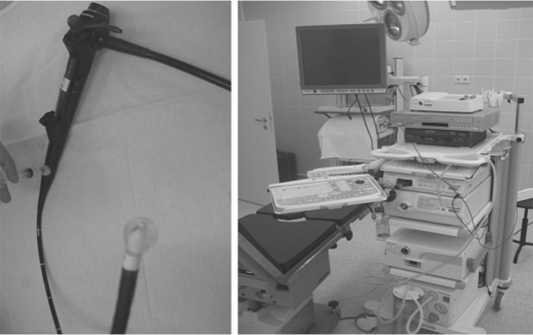
Рис. 1. Видеобронхоскоп BF-UC160F-OL8 фирмы OLYMPUS для ультразвукового конвексного сканирования и система для эндоскопических исследований (фото – Горбан Д.Г.)
верхность была ориентирована кпереди. Через голосовую щель его следует проводить, визуализируя внутреннюю поверхность надгортанника, затем переднюю комиссуру и далее переднюю стенку подскладкового отдела гортани. При входе в трахею также визуализируется ее передняя стенка. Исследование выполняется под местной анестезией в положении больного лежа на спине. Эндоскоп подводится к исследуемой области под контролем зрения, затем баллончик ультразвукового датчика наполняют водой объемом 0,5 мл и, вплотную прижимая к слизистой оболочке, начинают сканирование. Перемещать ультразвуковой датчик следует медленными плавными движениями. При ультразвуковой визуализации исследуемой области возможно «замораживание» изображения и измерение интересующих структур. Также имеется функция пошагового просмотра ультразвукового изображения для поиска наилучшего ракурса. Имеющийся режим допплерографии используется с целью
лучшей визуализации сосудов, а также оценки степени кровоснабжения тканей. Аспирационный канал позволяет эвакуировать содержимое гортанно-глотки, гортани и трахеи при наличии повышенной саливации или секреции. ЭИ выполняли под местной анестезией (10% раствор лидокаина апликационно), после предшествовавшей примедикации (за 30 минут до исследования вводилось 2,0 мл раствора реланиума в/м, 1 мл 0,1% раствора атропина п/к). Первым этапом проводилась рутинная ларинготрахеоскопия обычным видеобронхоскопом с анестезией голосовых складок и слизистой трахеи. Ультразвуковой бронхоскоп вводили через полость рта, у части больных через трахеостомическое отверстие. Доступ через трахеостомическое отверстие возможен у пациентов с Т-образными трахеостомическими трубками и ларинготрахеостомами, т.к. диаметр дефекта передней стенки трахеи в таких случаях значительно больше, чем стандартная трахеостома. Через стандартную трахеостому размером до 1,5 см в диаметре, провести ультразвуковой видеобронхоскоп не представляется возможным из-за значительной длинны его несгибаемой дистальной части (место соединения датчика с основной трубкой). Вторым препятствием осмотра конвексным датчиком через «небольшую» трахеостому является отсутствие возможности его ротации при наличии изгиба.
Результаты и их обсуждение
Существующие сообщения о применении ЭЭ касаются, прежде всего, их возможностей в эндоскопической диагностике предопухолевых и опухолевых заболеваний нижних дыхательных путей, позволяющих определять архитектонику слизистой оболочки, прогнозировать ее гистологическую структуру, выполнять прицельную биопсию патологических участков [14, 20, 21]. В частности, высоко оценивается эффективность эндобронхиального ультразвукового исследования в диагностике опухолей средосте- ния, внебронхиально локализованных опухолей легкого, саркоидозе легких [17-19]. Сообщений о применении ЭЭ оториноларингологии практически нет. Как нет и сообщений о сравнительной оценке эффективности этой методики с другими видами эндоскопии (обычная эндоскопия, увеличительная эндоскопия, хромоэндоскопия) или другими методами объективной визуализации при стенозе гортани и трахеи.
Сравнительная характеристика преимуществ и недостатков эндоскопической конвексной эхографии и ультразвукового сканирования шеи у пациентов со стенозом гортани и трахеи представлена в таблице 2.
ЭЭ, выгодно отличаясь от рентгенологических методов визуализации отсутствием лучевой нагрузки, обладает высокой разрешающей способностью и информативностью, позволяет четко визуализировать хрящи гортани и трахеи, оценить их размер, однородность, протяженность, взаимное расположение, а также состояние параларингеальных, паратрахеальных тканей (рис. 2, 3).
При наличии изменений хрящевого каркаса гортани и трахеи, возможно качественное определение их характера в зависимости от этиологии повреждения: воспалительной, травматической или опухолевой. В частности, у 2 пациентов выявлена различная степень изменений хрящевых имплантатов (без видимых внешних проявлений), частичный лизис хряща с одной стороны при имплантации хрящей паратра-хеально с двух сторон, неоднородность структуры хрящевого имплантата боковой стенки трахеи с фокусами резорбции (по плотности ткани), что заставило нас воздержаться на данном этапе от планируемой деканюляции пациентов, продлить наблюдение и лечение (рис 3); у 4 пациентов, по динамике диаметра стенки гортани и трахеи оценивали течение воспаления – хондроперихондрита гортани и трахеи, эффективность проводимого лечения (рис. 4).
Таблица 2
Сравнительная характеристика эндоскопической конвексной эхографии и ультразвукового сканирования у пациентов со стенозом гортани и трахеи
|
Методы диагностики |
Преимущества |
Недостатки |
|
Ультразвуковое исследование линейным датчиком |
широкая зона обзора; неинвазивность (безвредность); не требует специальной подготовки пациента |
трудность (невозможность) получения данных при исследовании через костную, хрящевую ткани, газосодержащие структуры; относительная удаленность датчика от структур, подлежащих исследованию. |
|
Эндоскопическая ультразвуковое исследование конвексным датчиком |
достаточная зона обзора; близость к датчику структур, подлежащих исследованию; высокая разрешающая способность; высокая информативность исследования за-грудинно расположенных структур. |
требуется подготовка пациента; «инвазия без повреждения»; относительная длительность исследования. |
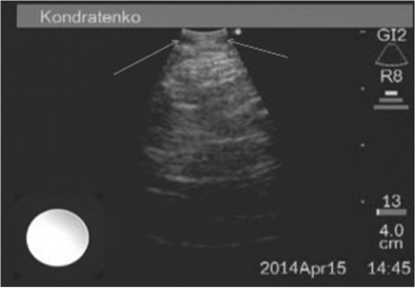
Рис. 2. УЗ-изображение не измененных хрящевых полуколец трахеи при ультразвуковом конвексном сканировании трахеи (фото - Горбан Д.Г.)
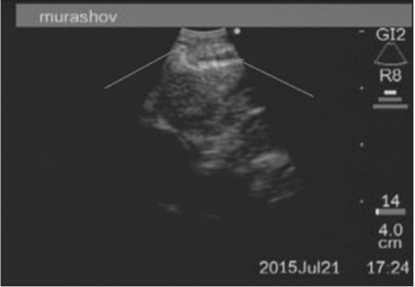
Рис. 3. УЗ-изображение трахеальной стенки при конвексном сканировании трахеи. Слева не измененное хрящевое полукольцо трахеальной стенки, справа состоятельный ранее имплантированный аллохрящ. Четко видно их взаимное расположение, структура и размер (фото - Горбан Д.Г.)
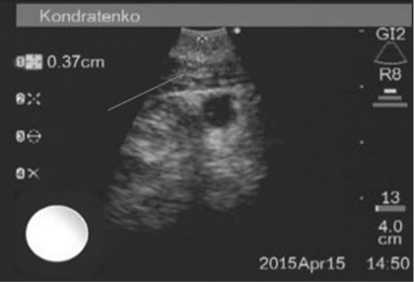
Рис. 4. УЗ-изображение трахеи. Лизис хрящей трахеальной стенки с замещением рубцовой тканью после перенесенного хондроперихондрита (фото - Горбан Д.Г.)
У 16 пациентов по диаметру хряща трахеальной стенки на протяжении оценивалась протяженность хондромаля-ции, что в сочетании с данными КТ трахеи на доопераци-онном этапе, позволило более точно оценить область, подлежащую протезированию, оптимально рассчитать размер имплантата (рис 7).
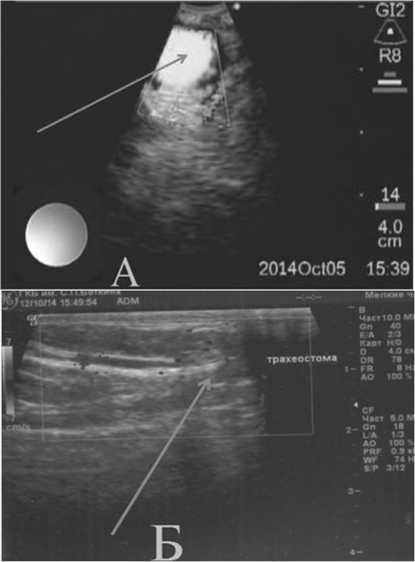
Рис. 5. УЗ-изображения области нижнего края трахеостомы-яремной вырезки грудины у одного и того же пациента: а - сосуд, прилежащий к передней стенке трахеи в верхнегрудном отделе, выявленный при эндоскопической эхографии; б – отсутствие данных о наличии сосуда при традиционном ультразвуковом исследовании мягких тканей области трахеостомы (фото - Горбан Д.Г.)
Расположение и взаимоотношение магистральных сосудов: плечеголовного ствола, безымянной артерии, левой общей сонной артерии, дуги аорты с трахеей, очень вариабельно (рис. 6) [4]. Кровотечение может возникнуть при любой хирургической манипуляции на трахее: трахеостомии, резекции трахеи, этапных хирургических вмешательствах. Источник кровотечения, чаще всего, плечеголовной ствол, интимно прилежащий к трахее [12]. Впервые на это осложнение указал Korte в 1897 г. (приведено по Maddaus M. и Pearson F.G. [15]). B. Nelems (1987) на основании анализа данных литературы указывает на 175 сообщений о кровотечении в трахею из плечеголовного ствола. Частота этого осложнения составила от 0,5-4,5%, выжило 24 пациента (13,7%) [16]. T. Grundmann с соавт. (1999) приводит случай смертельного кровотечения из безымянной артерии у пациента после трахеостомии [13]. В.Д. Паршин (2007) указывает на 3 случая смертельного кровотечения из плечеголовного ствола при циркулярной резекции трахеи [3]. О расположении магистрального сосуда в непосредственной близости от трахеи при выполнении трахеостомии/ретрахеостомии с трахеопластикой, оториноларинголог может судить, только по так называемой передаточной пульсации от сосуда к окружающим тканям, при ее выраженности. В ургентных
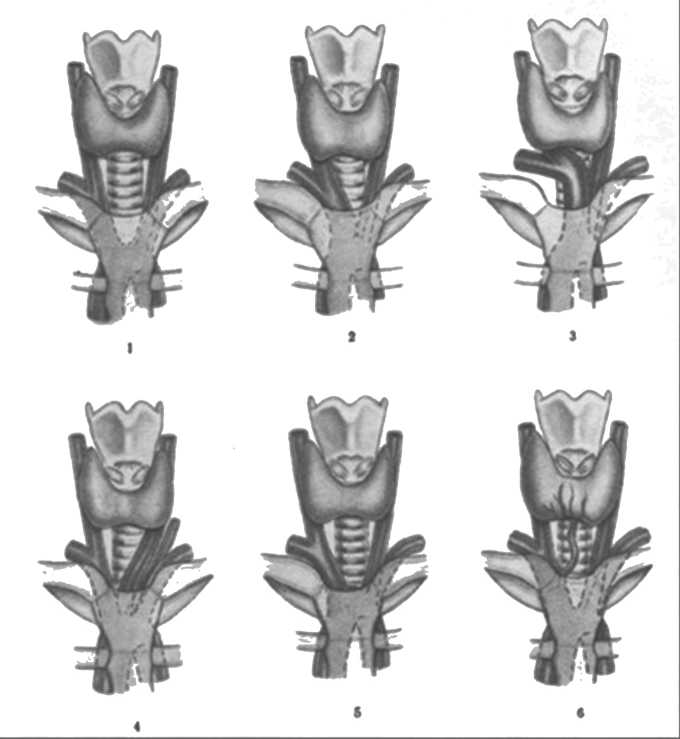
Рис. 6. Взаимоотношения между трахеей и крупными артериями по Ю.Л. Золотко [4]: 1 - крупные артерии располагаются по бокам трахеи; 2 - плечеголовной ствол закрывает частично шейную и полностью грудную части трахеи; 3 - плечеголовной ствол расположен впереди трахеи; 4 – левая общая сонная артерия частично закрывает шейную и грудную части трахеи; 5 - над яремной вырезкой грудины выступает дуга аорты;
6 - спереди трахеи проходит нижняя щитовидная артерия
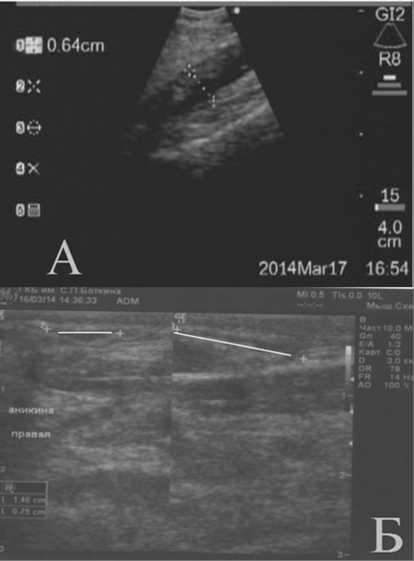
Рис. 7. УЗ-изображения паратрахеально расположенных имплантатов при: а - эндоскопической конвекс-ной эхографии; б - при сканировании мягких тканей шеи линейным датчиком. В обоих случаях исследования информативны для оценки состояния имплантационного материала. (фото - Горбан Д.Г.)
ситуациях, при стенозах гортани или трахеи с декомпенсированным дыханием, как правило, нет возможности выполнить диагностические мероприятия по обнаружению и идентификации сосуда, а при загрудинно расположенном сосуде и необходимости выполнения трахеопластики верхнегрудного отдела трахеи (мобилизации трахеи, рассечении ее передней стенки, трахеопексии), доступное ультразвуковое исследование шеи неинформативно (рис. 5б). В этой связи риск возникновения смертельного кровотечения при повреждении магистрального сосуда значительно возрастает.
В связи с этим, очень интересной и важной в практическом отношении, является установленная возможность ЭЭ обнаружения и характеристики (диаметр, синтопия) крупных сосудов, прилежащих к передней или боковым стенкам трахеи в шейном и грудном отделах (рис. 5а). У 3 пациентов с хроническим рубцовым стенозом шейного и начального грудного отделов трахеи, было выявлено прилежание круп- ных сосудов к передней стенке начального грудного отдела трахеи (плечеголовного ствола - в 2 случаях, безымянной артерии – в 1), что позволило избежать ранения этих сосудов в ходе дальнейшего хирургического лечения. Таким образом, обладая высокой диагностической информативностью, возможностью одномоментно осуществлять санационные мероприятия, ЭЭ, может эффективно применяться интрооперационно минимизирует риски и осложнения при выполнении операций на трахее.
В целом дополнительная информация о состоянии гортани и трахеи, повлиявшая на лечебно-диагностическую тактику ведения пациента, была получена при ЭЭ у 36% пациентов, оперированных экстренно и у 24% пациентов, госпитализированных в плановом порядке.
На основании полученных результатов сформулированы показания и противопоказания к проведению эндоскопической эхографии.
Показания:
-
1. оценка состояния хрящевого каркаса трахеи;
-
2. оценка состояния имплантированного паратрахеаль-но ауто и/или алло материала в различные сроки после операций;
-
3. выявления крупных прилежащих к стенке трахеи образований шеи (сосудов, лимфатических узлов, ткани щитовидной железы) перед реконструктивными операциями.
Предполагаем, что данная методика будет высокоэффективной в диагностике опухолевых поражений гортани и трахеи, для оценки степени инвазии опухоли в стенку органа, хотя специальных исследований этого вопроса нами не проводилось.
Противопоказания общие с традиционной методикой фиброларинготрахеобронхоскопии.
Выводы
Эндоскопическое исследование с ультразвуковым сканированием гортани и трахеи позволяет:
а - определить наличие, размер, структуру, расположение и взаимоотношение анатомических образований со стенкой гортани и трахеи, например, прилежание магистральных сосудов, что важно при выборе метода хирургического лечения;
б - определить толщину (диаметр) хрящевой стенки гортани и трахеи, оценить протяженность хондромаляции, подтвердить наличие явлений хондроперихондрита, оценить динамику изменений в хрящевой ткани на фоне лечения;
в - оценить состояние (размер, однородность, очаги резорбции), расположение имплантатов, установленных па-раларингеально, паратрахеально и в целом сделать вывод об их состоятельности.
Заключение
Применение эндоскопии с ультразвуковым сканированием гортани и трахеи значительно расширяет диагностические возможности у пациентов с рубцовым стенозом гортани и трахеи. Дополнительная информация, получаемая в ходе исследования в совокупности с клиническими данными и данными рентгенологического исследования, позволяют определить оптимальную тактику лечения пациентов, объективно оценивать эффективность проводимого лечения.
Список литературы Возможности новой методики эндоскопической визуализации у пациентов с рубцовым стенозом гортани и трахеи
- Абакумов М.М. Множественные и сочетанные ранения шеи, груди, живота. -М.: «Бином-Пресс», 2013. -688с.
- Зенгер В.Г., Наседкин А.Н. Современные технологии в лечении заболеваний уха, горла и носа. -М.: «Медкнига», 2008. -355с.
- Зенгер В.Г., Наседкин А.Н., Паршин В.Д. Хирургия повреждений гортани и трахеи. -М.: «Медкнига», 2007. -364с.
- Золотко Ю.Л. Атлас по топографической анатомии. -М.: «Медицина», 1967. -Т1. -186с.
- Кирасирова Е.А., Горбан Д.Г., Мальцева И.М., и др. Роль и место эндоскопии в диагностике, лечении и профилактике постинтубационных повреждений гортани и трахеи. Матер. 1 Российского Конгресса по неотложной эндоскопии. Москва, 6-7 декабря 2012г.
- Оториноларингология: национальное руководство/под. Ред. В.Т. Пальчуна. -М.: ГЭОТАР-Медиа, 2008. -960с.
- Паршин В.Д. Трахеостомия. Показания, техника, осложнения и их лечение. -М.: ГЭОТАР-Медиа,2008. -176с.
- Паршин В.Д., Порханов В.А. Хирургия трахеи с атласом оперативной хирургии. -М.: Альди-Принт», 2010. -480с.
- Перельман М.И., Бирюков Ю.В., Королева Н.С. и др. Протезирование трахеи//Хирургия. -1987. -№9. -С.43-48.
- Чернеховская Н.Е., Андреев В.Г, Поваляев А.В. Лечебная бронхоскопия в комплексной терапии заболеваний органов дыхания: Учебн. пособие. -М.: МЕДпресс-информ, 2008. -128с.
- Чернеховская Н.Е., Коржева И.Ю., Мальцева И.М., Волова А.В. Возможности современной бронхоскопии. Пульмонология, 2010. -N 2. -С.120-124.
- Grillo H.C. Surgical treatment of postintubation tracheal injures//J.thorac.cardiovasc.Surg.-1979.-Vol.78, №6.-P.860-875.
- Grundman T., Brachtel E., Kehrl W. Fistula between the trachea and innominate artery a reare complication following tracheostenosis treatment with silastic tubes. Tracheo-arterielle Anonymafistel//Laryngorhinootolog. -1999. -Vol. 78, №2. -P.91-96.
- Herth F.J.F., Morgan R. K., Eberhardt R., and Ernst A. Endobronchial Ultrasound-Guided Miniforceps Biopsy in the Biopsy of Subcarinal Masses in Patients with Low Likelihood of Non-Small Cell Lung Cancer. Ann. Thorac. Surg., June 1, 2008; 85(6): 1874 -1878.
- Maddaus M., Pearson F.G. Postintubation injury. In: «Thoracic Surgery». Ed. Pearson F. Griffith. -N.Y. -1995. -P. 251-265.
- Nelems B. Tracheoarterial fistula. -In: International trends in general thoracic surgery/Ed.H.C. Grilo. -Philadelphia. 1987. -P.69-73.
- Trisolini R., Tinelli C., Cancellieri A., Paioli D., Alifano M., Boaron M., and M. Patelli. Transbronchial needle aspiration in sarcoidosis: Yield and predictors of a positive aspirate. J. Thorac. Cardiovasc. Surg., April 1, 2008; 135(4): 837 -842.
- Wong M. et al. Endobronchial ultrasound: new insight for the diagnosis of sarcoidosis. Eur Respir J 2007; 29:1182-1186
- Yasufuku K, Chiyo M, Koh E, et al. Endobronchial ultrasound guided transbronchial needle aspiration for staging of Lung Cancer. Lung Cancer 2005; 50:347-354.
- Yasufuku K, Chhajed PN, Sekine Y, et al. Endobronchial ultrasound using a new convex probe: a preliminary study on surgically resected specimens. Oncol Rep 2004; 11:293-296.
- Yasufuku K, Chiyo M, Sekine Y, et al. Real-time endobronchial ultrasound-guided transbronchial needle aspiration of mediastinal and hilar lymph nodes. Chest 2004; 126:122-128.


