Возможности реваскуляризации свободным мышечным лоскутом у пациентов с критической ишемией нижних конечностей при различной этиологии поражения дистального русла
Автор: Калитко И.И., Файбушевич А.Г., Калитко И.М., Черняев М.В.
Журнал: Московский хирургический журнал @mossj
Рубрика: Сердечно-сосудистая хирургия
Статья в выпуске: 1 (95), 2026 года.
Бесплатный доступ
Введение. У части пациентов с критической ишемией нижних конечностей невозможно выполнить прямую реваскуляризацию из-за отсутствия приемлемого дистального артериального русла (no-option). Цель исследования. Оценить эффективность реваскуляризации пересадкой свободного мышечного лоскута у пациентов с критической ишемией нижних конечностей разной этиологии поражения. Материалы и методы исследования. Проведен анализ историй 37 пациентов (10 с облитерирующим тромбангиитом (болезнью Бюргера), 15 с сахарным диабетом, 12 с атеросклерозом артерий нижних конечностей), оперированных с 2016 по 2025 гг. которым была выполнена реваскуляризация нижних конечностей с использованием свободного мышечного лоскута (gracilis, latissimus dorsi). Результаты лечения. Общий показатель технического успеха операции составил 62 % – у 23 из 37 пациентов, для группы болезни Бюргера – 90 %, для группы атеросклероза – 75 %, для группы сахарного диабета – 33,3 %. Показатель одногодичного спасения конечности составил 88,9 %, 77,8 % и 80 % соответственно, с общим показателем спасения конечности в 82,6 %. Средний период наблюдения за пациентами составил 29,7 месяцев (M ± SD: 29,7 ± 24,9 месяцев, n=19), самое долгое наблюдение составило более 9 лет. Наличие неоваскулогенеза в окружающих пересаженный лоскут тканях подтверждено гистологически. Заключение. Непрямая или комбинированная реваскуляризация с использованием свободного мышечного лоскута является хорошей альтернативой большой ампутации у пациентов с критической ишемией no-option. Необходимо дальнейшее исследование метода, в особенности у пациентов с сахарным диабетом.
Реваскуляризация, спасение конечности, свободный мышечный лоскут, свободный лоскут, критическая ишемия нижних конечностей
Короткий адрес: https://sciup.org/142247243
IDR: 142247243 | УДК: 616.13-005.4-089 | DOI: 10.17238/2072-3180-2026-1-77-84
Possibilities of revascularization using a free muscle flap in patients with critical lower limb ischemia of different distal arterial lesions etiologies
Introduction. In some patients with critical limb ischemia, direct revascularization is not feasible due to the absence of an adequate distal arterial bed (no-option). The purpose of the study. To evaluate the effectiveness of revascularization using free muscle flap transfer in patients with critical lower limb ischemia of various etiologies. Materials and methods of research. A retrospective analysis was conducted on 37 patients (10 with throm boangiitis obliterans [Buerger’s disease], 15 with diabetes mellitus, and 12 with atherosclerosis of the lower limb arteries) operated on between 2016 and 2025, who underwent lower limb revascularization using free muscle flaps (gracilis, latissimus dorsi). Treatment results. The overall technical success rate was 62 % (23 of 37 patients): 90 % in the Buerger’s disease group, 75 % in the atherosclerosis group, and 33,3 % in the diabetes group. The one-year limb salvage rate was 88,9 %, 77,8 %, and 80 %, respectively, with an overall limb salvage rate of 82.6 %. The mean follow-up period was 29,7 months (M ± SD: 29,7 ± 24,9 months, n = 19), with the longest follow-up exceeding 9 years. The presence of neovascularization in tissues surrounding the transferred flap was confirmed histologically. Conclusion. Indirect or combined revascularization using a free muscle flap is a valuable alternative to major amputation in no-option critical limb ischemia patients. Further research is warranted, particularly in diabetic patients.
Текст научной статьи Возможности реваскуляризации свободным мышечным лоскутом у пациентов с критической ишемией нижних конечностей при различной этиологии поражения дистального русла
В международных клинических рекомендациях сказано, что основным методом лечения пациентов с критической ишемией нижних конечностей является прямая реваскуляризация, но в ряде случаев, ввиду отсутствия дистального артериального русла, у некоторых пациентов её выполнение невозможно [1]. У таких больных методы непрямой реваскуляризации в ряде случаев помогают избежать большой ампутации конечности, приводящей к инвалидизации и высокой периоперационной летальности [2–4]. Реваскуляризация путем пересадки свободного лоскута, применяющаяся как изолированно, так и в комбинации с предшествующей реконструкцией более проксимального сегмента артериального русла является одним из таких методов [5, 6]. Несмотря на то, что пересадка лоскута при травматических повреждениях хорошо изучена, имеется относительно небольшое число исследований, посвященных методу реваскуляризации пересадкой свободного лоскута у пациентов с критической ишемией нижних конечностей [7]. Из-за технической сложности метода и относительной редкости пациентов с полной компрометацией дистального русла он применяется лишь отдельными командами специалистов. Мало данных о непосредственных и отдаленных результатах оперативного вмешательства у пациентов с различной этиологией поражения дистального артериального русла.
Цели исследования:
-
1) Провести оценку непосредственных и отдаленных результатов и определить вероятность сохранения конечности при реваскуляризации нижней конечности свободным мышечным лоскутом у пациентов с различной этиологией поражения дистального артериального русла.
-
2) Подтвердить неоангиогенез в окружающих тканях из тканей лоскута гистологически.
-
3) Сравнить используемый метод с отсутствием хирургического лечения при дистальной форме артериального поражения по данным научной литературы.
Материалы и методы
Проанализированы истории 37 пациентов с критической ишемией нижних конечностей III–IV стадии по Фонтейну-Покровскому (10 с болезнью Бюргера, 15 с сахарным диабетом, 12 с атеросклерозом), оперированных с 2016 по 2025 гг. на базе отделения сосудистой хирургии ООО “Клиника инновационной хирургии”, которым была выполнена реваскуляризация нижних конечностей с использованием свободного мышечного лоскута (musculus gracilis, musculus latissimus dorsi). Пациентам с отсутствием дистального артериального русла голени и стопы выполнялась пересадка лоскута как единственный метод лечения. У больных с комбинацией проксимального поражения и отсутствием или полной компрометацией дистального артериального русла была выполнена комбинированная реваскуляризация с аутовенозным шунтированием и/или эндоваскулярной коррекцией притока и разгрузкой в лоскут. При наличии некрозов или гангрены стопы перед пересадкой лоскута выполнялась некрэктомия. Предоперационная подготовка ран проводилась по схеме – санация растворами перекиси водорода 3 %, 0,05 % хлоргексидина биглюконата, марлевые повязки с раствором повидон-йода (1–10 % в зависимости от реакции возбудителя на перевязки). Для подтверждения процессов неоваскулогенеза в окружающих лоскут тканях у некоторых пациентов после приживления лоскута с их согласия выполнялось гистологическое исследование лоскута и окружающих тканей. Степень компенсации кровотока в дистальных отделах конечности оценивалась объективно с помощью ультразвукового исследования, термографии и, при необходимости, ангиографии (рис. 1).
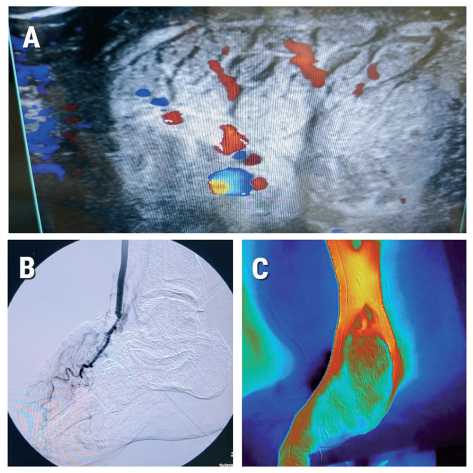
Рис. 1. Инструментальные методы исследования: А – УЗИ сосудов лоскута; B – ангиография сосудов лоскута, C – термография лоскута в периоперационном периоде
Fig. 1. Instrumental diagnostic methods: A – ultrasound of the flap vessels; B – angiography of the flap vessels; C – thermography of the flap in the perioperative period
После оперативного лечения большая часть пациентов приходила на контрольные осмотры, выполнялось фотографирование ран, отдельные пациенты опрашивались по телефону. Всего была выполнена пересадка 11 свободных лоскутов m. gracilis, 24 лоскутов m. latissimus dorsi.
Результаты
Общий показатель технического успеха (жизнеспособность лоскута в течение 1 месяца) составил 62 % – 23 из 37 пациентов.
Самый высокий уровень приживления свободных лоскутов наблюдался у группы болезни Бюргера 90 % – 9 из 10 пациентов, у группы атеросклероза артерий нижних конечностей он составил 75 % – 9 из 12 пациентов. Самый низкий процент наблюдался у группы сахарного диабета – 33,3 % – 5 из 15 пациентов, но больные последней группы в среднем были более возрастными, с более тяжелой сопутствующей патологией и недостаточной компенсацией сахарного диабета. Несмотря на такие удручающие результаты оперативного вмешательства у больных с сахарным диабетом, у тех из них, у кого лоскут выживал в течение 2–3 месяцев, в дальнейшем конечность была спасена.
Показатели спасения конечности после успешного приживления лоскута в течение 1 года составили: для группы болезни Бюргера 88,9 % – 8 из 9 пациентов, для группы атеросклероза 77,8 % – 7 из 9 пациентов и для группы диабета 80 % – 4 из 5 пациентов, с общим показателем спасения конечности в течение года в 82,6 % (19 из 23). В целом, у 51,4 % (19 из 37) больных после пересадки лоскута конечность была спасена (рис. 2, табл. 1).
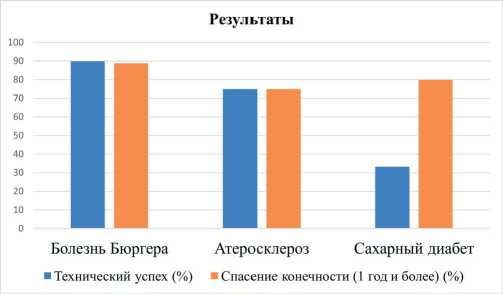
Рис. 2. Диаграмма. Результаты реваскуляризации свободным мышечным лоскутом
Fig. 2. Chart. Results of free muscle flap revascularization
Таблица 1
Результаты реваскуляризации свободным мышечным лоскутом
Table 1
Results of free muscle flap revascularization
|
Группа Пациентов, Patient group |
Возраст (лет) / Age (years) |
Технический успех (%) / Technical success (%) |
Спасение конечности (более 1 года в %) / Limb salvage (>1 year, %) |
|
Болезнь Бюргера, Buerger’s disease (n=10) |
44,2±10,2 |
90 |
88,9 |
|
Атеросклероз, Atherosclerosis (n=12) |
62,9 ± 11,3 |
75 |
77,8 |
|
Сахарный диабет II типа, Type II diabetes (n=15) |
66,0 ± 9,2 |
33,3 |
80 |
Средний период наблюдения за пациентами составил 29,7 месяцев (M ± SD*: 29,7 ± 24,9 месяцев, n=19), самое долгое наблюдение составило более 9 лет (рис. 3–6).
Период наблюдения за пациентами после успешной пересадки лоскута
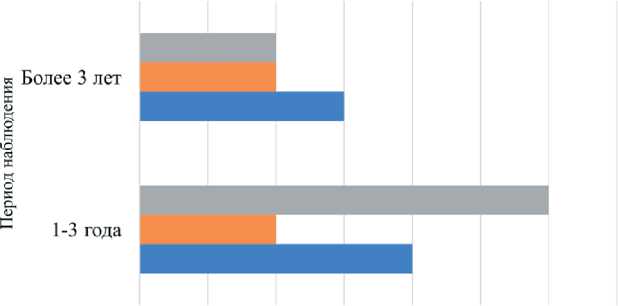
Количество пациентов
Болезнь Бюргера Сахарный диабет ■Атеросклероз
Рис. 3. Диаграмма. Период наблюдения за пациентами после успешной пересадки лоскута
Fig. 3 . Chart. Follow-up period of patients after successful flap transplantation
На рисунке видно, что у всех пациентов в ходе операции после острого растяжения поперечной мышцы живота происходило уменьшение диастаза задних листков футляров прямых мышц живота.
Пример результата острого растяжения показан на следующем рисунке (рис. 4).
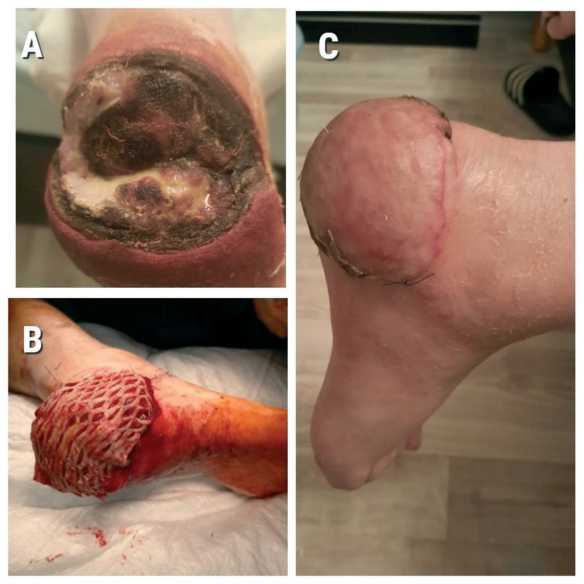
Рис. 4. Пациент с атеросклерозом артерий н/к, остеомиелитом пяточной кости – период наблюдения более 9 лет: А – рана пяточной области, B – пересаженный лоскут, С – через несколько лет после вмешательства
Fig. 4 . Patient with atherosclerosis of the lower limb arteries and calcaneal osteomyelitis, follow-up period over 9 years: A – heel wound, B – transplanted flap, C – several years after the procedure
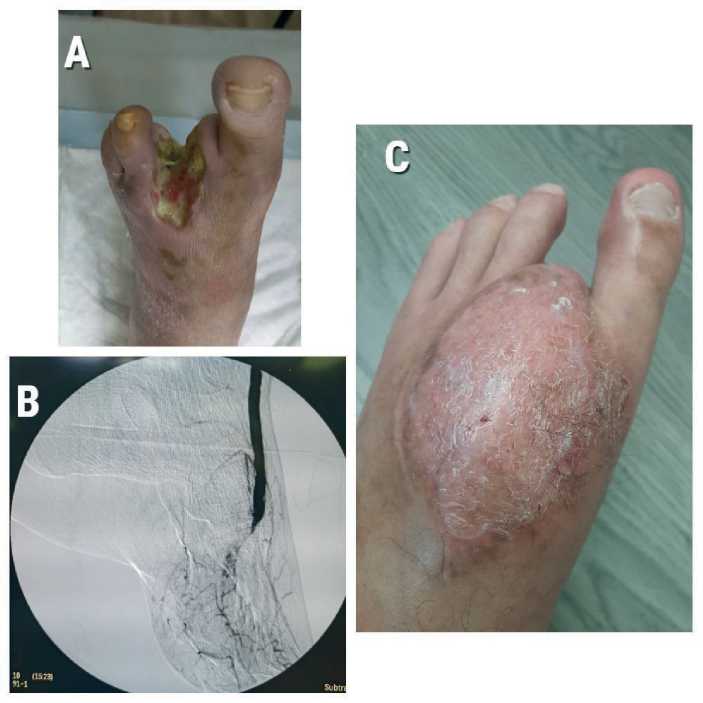
Рис. 5. Пациент с болезнью Бюргера, период наблюдения более 4 лет: A – раневой дефект левой стопы, B – ангиография сосудов лоскута, С – вид стопы через 3 года
Fig. 5. Patient with Buerger’s disease, follow-up period over 4 years:
A – wound defect of the left foot, B – angiography of the flap vessels, C – appearance of the foot 3 years after surgery
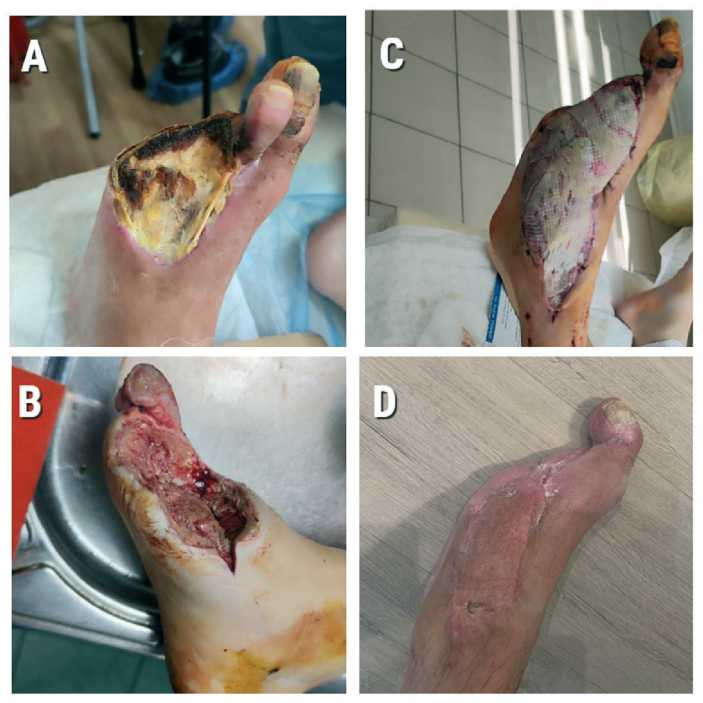
Рис. 6. Пациент с сахарным диабетом, наблюдение более 1,5 лет: A – рана до обработки, B – после некрэктомии, С – после пересадки лоскута, D – через год
Fig. 6 . Patient with diabetes mellitus, follow-up period over 1.5 years: A – wound before debridement, B – after necrectomy, C – after m. gracilis flap transplantation, D – one year later
Пациенты с облитерирующим тромбангиитом и атеросклерозом отмечали постепенное исчезновение болей в течение полутора месяца после успешной пересадки лоскута; болевой синдром у пациентов с сахарным диабетом, зачастую изначально не был выражен из-за периферической нейропатии.
Клинический случай
Непрямая реваскуляризация у пациента с болезнью Бюргера при помощи пересадки лоскута m. latissimus dorsi.
Пациент, мужчина 59 лет, поступил с жалобами на боли покоя в левой стопе и незаживающую рану.
При дообследовании выявлена окклюзия всех артерий левой голени и стопы с типичными штопорообразными коллатералями, некротическая рана переднего отдела левой стопы после предшествующей хирургической обработки по месту жительства (рис. 9–7).
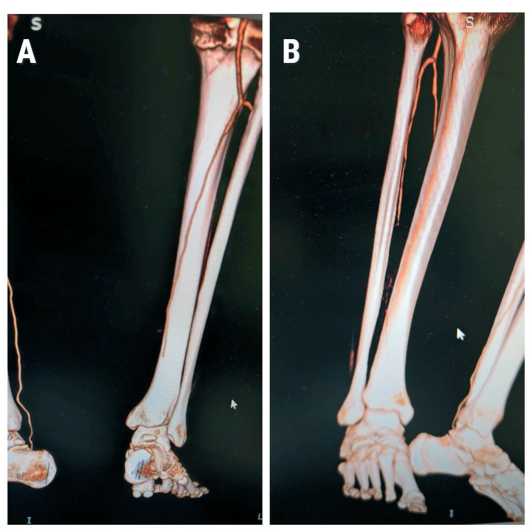
Рис. 7A, B . Предоперационная КТ-ангиография (вид на артерии правой голени и стопы сзади и спереди): видна окклюзия артерий в н/3 голени и стопы
Fig. 7A, B. Preoperative CT angiography (posterior and anterior views of the arteries of the right lower leg and foot): showing occlusion of the arteries in the distal third of the lower leg and foot
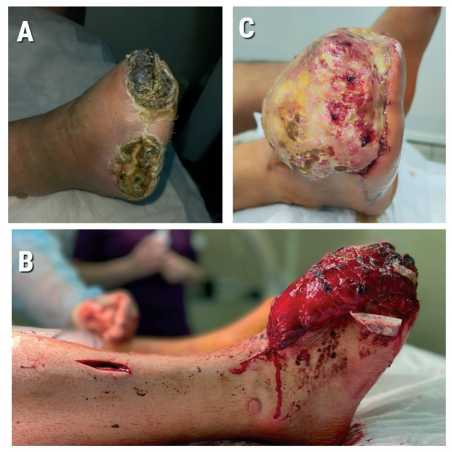
Рис. 8. Пациент с болезнью Бюргера: A – вид стопы после некрэктомии, незаживающие раны, B – пересаженный лоскут m. latissimus dorsi интраоперационно, С – отёк лоскута через 3 месяца
Fig. 8. Patient with Buerger’s disease:
A – appearance of the foot after necrectomy with non-healing wounds, B – intraoperative view of the transplanted latissimus dorsi flap, C – flap edema 3 months later
Был пересажен лоскут m. latissimus dorsi на правую стопу с удлинением артерии лоскута в подколенную артерию при помощи аутовенозного кондуита, анастомозом вены лоскута и передней большеберцовой вены конец в конец.
Fig. 9 Flap at 7 months (showing resolution of edema):
A, B – flap before skin grafting; the area of the flap tissue and surrounding skin near the forceps was biopsied, C – skin grafting of the flap
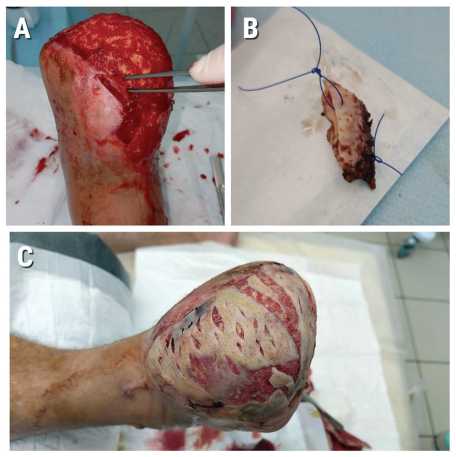
Рис. 9. Лоскут через 7 месяцев (видно исчезновение отека): А, B – лоскут перед аутодермопластикой, участок ткани лоскута и окружающей кожи около пинцета взят на биопсию, С – аутодермопластика лоскута
Пациент отметил постепенное исчезновение болей в стопе в течение 1,5 месяцев, около 3 месяцев лоскут был отёчным, после чего атрофировался и принял форму раны. Спустя 7 месяцев пациент был вновь госпитализирован для выполнения аутодермопластики лоскута, во время операции с согласия пациента была взят участок лоскута и окружающих тканей стопы для гистологического исследования, которое подтвердило неоангиогенез из тканей лоскута в окружающую дерму (рис. 9–11).
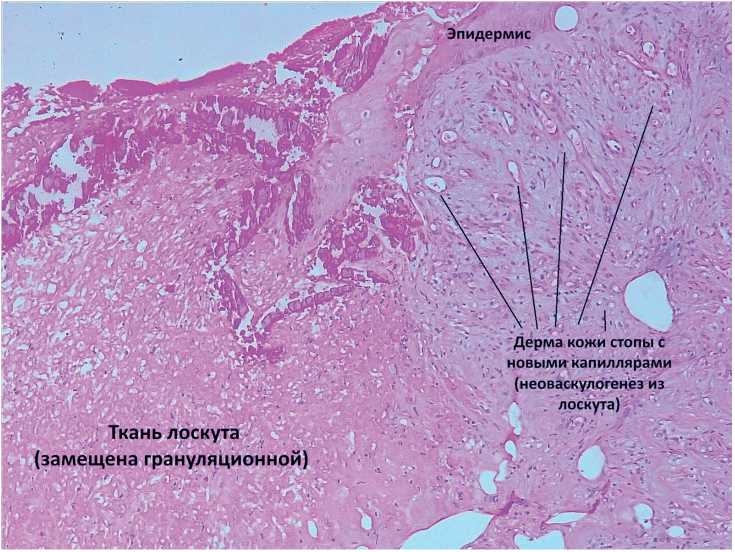
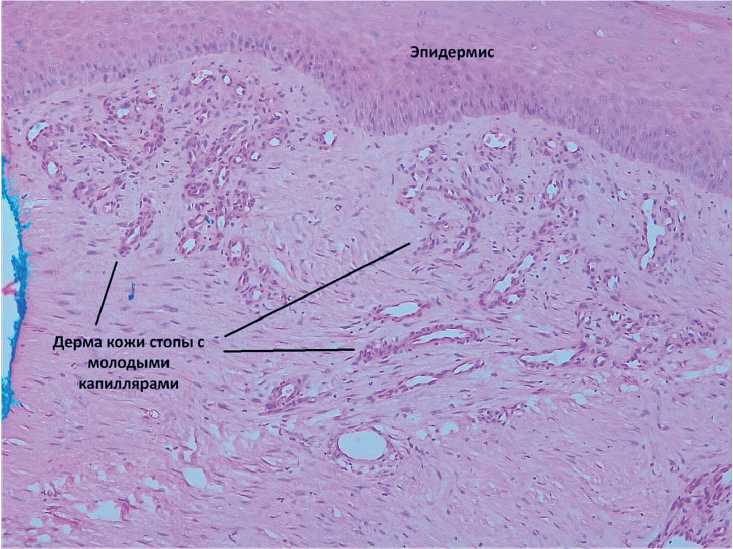
Рис. 10, 11. Гистологическое исследование лоскута и окружающей ткани: Образование новых капилляров из стромы лоскута в дерме окружающей ткани (окраска гематоксилин-эозин, увеличение в 100 раз)
Fig. 10, 11. Histological examination of the flap and surrounding tissue:
Formation of new capillaries extending from the flap stroma into the dermis of the surrounding tissue (hematoxylin and eosin staining, magnification × 100x)
Обсуждение
По данным литературы при выполнении открытой или эндоваскулярной реваскуляризации при пригодном дистальном артериальном русле показатель одногодичного спасения конечности составляет около 80–90 % в зависимости от этиологии поражения и падает с течением времени [8, 9]. Однако некоторым пациентам с критической ишемией невозможно выполнить прямую реваскуляризацию, а исключительно консервативные мероприятия, по мнению академика А.В. Покровского, эффективны у больных с критической ишемией лишь в 15–20 % случаев [10]. Одногодичная выживаемость конечности у пациентов с КИНК при консервативном подходе составляет около 57,4 %, также он связан со значительно более высокими шансами большой ампутации или смерти в стационаре по сравнению с пациентами, перенесшими малую ампутацию (в 1,59 раза), эндоваскулярное (в 2,08 раза) или открытое вмешательство (в 2,12 раза) [11]. По нашим данным, у тех пациентов, кому удавалось успешно пересадить лоскут, сохранить конечность в долгосрочной перспективе удавалось у примерно 80 % больных, что является отличным результатом, по сравнению с консервативным методом лечения. Метод довольно сложен, но при должных микрохирургических навыках и правильном отборе пациентов и лоскутов дает хорошие результаты, одновременно восстанавливая кровообращение в конечности и закрывая большие раневые дефекты.
Заключение
Непрямая реваскуляризация при помощи пересадки лоскута пациентам с критической ишемией нижних конечностей в основном является операцией “последнего шанса”, используемой при полном отсутствии или компрометации дистального артериального русла, для разгрузки зоны реконструкции при плохом оттоке, а также сопутствующей пластики раневых дефектов после некрэктомии. Несмотря на техническую сложность, при грамотном применении метод способен спасти конечность и улучшить качество жизни большинству пациентов с критической ишемией нижних конечностей и нереконструктабельным артериальным руслом, которым в противном случае грозила бы большая ампутация.


