Возможности видеоэндохирургической техники при экстирпации и пластике пищевода
Автор: Перескоков С.В., Буриков М.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.4, 2009 года.
Бесплатный доступ
Представлены результаты хирургического лечения 83 больных с рубцовыми стриктурами и раком пищевода разработанными способами с использованием видеоэндохирургической техники, основанными на топографо-анатомических исследованиях и медико-математическом моделировании оптимального эндохирургического доступа к органам заднего средостения. Показаны положительные клинические эффекты видеоэндохирургических доступов в зависимости от уровня поражения пищевода и типа телосложения пациента, видеоэндохирургической внутрипросветной методики наложения соустья между пищеводом и трансплантатом на шее, как при выполнении второго этапа пластики пищевода, так и при эндоскопической реконструкции анастомоза между пищеводом и трансплантатом на шее в связи с рубцовым сужением анастомоза.
Пищевод, эзофагопластика, внутрипросветный анастомоз, видеоэндохирургия
Короткий адрес: https://sciup.org/140188716
IDR: 140188716 | УДК: 616-089.87-072.1
Текст научной статьи Возможности видеоэндохирургической техники при экстирпации и пластике пищевода
Проблема хирургического лечения заболеваний пищевода по праву считается одной из самых сложных в области реконструктивно-пластической хирургии [1, 2, 4]. Видеоэндохирургические операции получили широкое распространение и прочно внедрились в хирургическую практику при лечении нервно-мышечных и доброкачественных заболеваний пищевода (лапаро-или торакоскопическая эзофагокардиомиотомия с фундопликацией по Дору; лапаро- или торакоскопическая энуклеация лейомиомы), грыжах пищеводного отверстия диафрагмы (задняя круроррафия с фундопликацией по Ниссену) [3]. Наряду с этим, поиск новых методов и технологий, позволяющих снизить травматизм сложных оперативных вмешательств при рубцовых стриктурах (РСП) и раке пищевода (РП), представляется по-прежнему актуальным.
Цель исследования – улучшение результатов хирургического лечения больных с РСП и РП путем разработки и внедрения малотравматичных оперативных вмешательств с использованием видеоэндохирургической техники.
В работе представлены результаты хирургического лечения 83 больных с РСП и РП разработанными способами с использованием видеоэндохирургической техники.
Проведены топографо-анатомические исследования и медико-математическое моделирование оптимального эндохирургического доступа к органам заднего средостения. Установлено, что на критерии выполнения эндоторакальных манипуляций на пищеводе оказывает существенное влияние как тип телосложения пациента, так и угол наклона (пронации) его грудной клетки к плоскости операционного стола (патент РФ №2269941). Разработаны и внедрены в клиническую практику видеоэндохирургические доступы в зависимости от уровня поражения пищевода и типа телосложения пациента (патент РФ № 2312620). При тотальной позадигрудин-ной эзофагопластике формирование ретростернального тоннеля выполнялось с использованием видеоэндохирургической техники (патент РФ № 2285463). При наличии показаний к двухэтапному формированию соустья на шее для внутрипросветного наложения анастомоза также применялась видеоэндохирургическая техника и оригинальное устройство (патент РФ №54304).
Спектр оперативных вмешательств у больных с РСП и РП, выполняемых с помощью разработанных способов с использованием видеоэндохирургической техники, представлен в табл. 1.
Результаты
В соответствии с типом телосложения больного определяется оптимальный угол наклона грудной клетки пациента к плоскости операционного стола (при долихоморфном типе телосложения – на левом боку с пронацией под углом 70°, под углом 60° при мезоморфном типе телосложения и под углом 50° при брахиморфном типе). Устанавливаются места введения троакаров в соответствии с локализацией патологического процесса в пищеводе и типом телосложения больного (рис. 1). После отведения правого легкого рассекается медиастинальная плевра над пищеводом (рис. 2) и производится его мобилизация на всем протяжении грудного отдела (рис. 3). После выделения и пересечения пищевода на шее из отдельного доступа, лапаротомным доступом мобилизованный пищевод удаляется, формируется трансплантат из желудка или ободочной кишки, который проводится в заднем средостении на шею, где накладывается соустье.
Сравнительные результаты видеоторакоскопической и трансхиатальной (наименее травматичной из открытых операций) экстирпации пищевода с одномоментной эзофагопластикой у больных с РСП и РП представлены в табл. 2.
При невозможности выполнения эндохирургической операции в связи: с распространённостью патологического процесса или сложностями анатомических взаимоотношений органов; осложнениями, возникшими во время эндоторакальной операции, которые невозможно устранить с помощью видеоэндохирургической техники; безуспешностью развития операции в течение 30–40 минут; техническими неполадками аппаратуры, возникшими во время операции, – показана конверсия (переход к открытой операции). В нашем исследовании конверсия осуществлена у одного больного (4,2%) в связи с распространенностью опухолевого процесса.
Отличительными особенностями выполняемой нами тотальной шунтирующей позадигрудинной эзофагопла-стики являлось создание тоннеля в ретростернальном клетчаточном пространстве в условиях дозированного введения в него газа видеоэндохирургическими инструментами под контролем видеокамеры. При этом нами установлено, что количество вводимого газа определяется типом телосложения пациента. Так, у больных долихоморфного типа телосложения его объем составляет от 500 до 700 мл, от 800 мл до 1000 мл – у пациентов мезоморфного типа и от 1100 до 1300 мл – брахиморфного типа телосложения.
В случаях тотальной шунтирующей пластики пищевода толстой кишкой операция выполнялась в один или два этапа. Первый этап: формирование и проведение трансплантата из ободочной кишки по загрудинному тоннелю, созданному по оригинальной методике (рис. 4, 5), выведение орального конца трансплантата на шею. Осмотр его сосудистой ножки в загрудинном клетчаточ-ном пространстве (рис. 6).
При выполнении операции в один этап накладывался анастомоз между трансплантатом и шейным отделом пищевода. Завершение операции осуществлялось по общепринятой методике. Брюшная полость и шейная рана дренировались.
Вскрытие правой плевральной полости отмечено у 1 пациента (4,5%). Кровотечений в процессе форми-
Табл. 1. Оперативные вмешательства у больных с РСП и РП, выполненные с использованием видеоэндохирургической техники
|
Заболевания пищевода |
Виды оперативных вмешательств Количество больных |
|
Рубцовые стриктуры пищевода |
Шунтирующая тотальная эзофагопластика с видеоэндохирургическим 22 формированием позадигрудинного тоннеля Внутрипросветное наложение или реконструкция анастомоза 37 между пищеводом и трансплантатом на шее Видеоассистированная торакоскопическая экстирпация пищевода с эзофагопластикой 7 |
|
Рак пищевода |
Видеоассистированная торакоскопическая экстирпация пищевода 17 с лимфодиссекцией и эзофагопластикой |
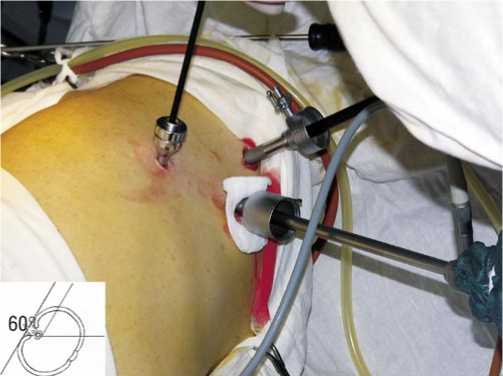
Рис. 1. Больной мезоморфного типа телосложения. Расположение на операционном столе
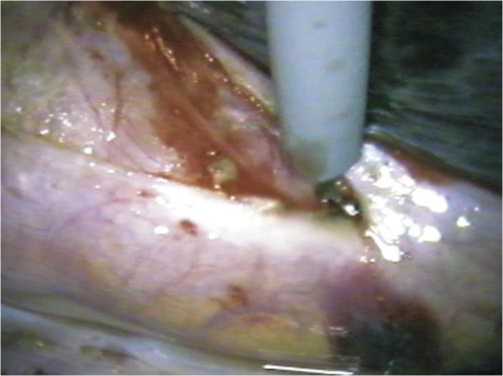
Рис. 2. Рассечение медиастинальной плевры вдоль пищевода
рования загрудинного тоннеля не было. Из гнойных осложнений отмечалась несостоятельность анастомоза и частичное нагноение швов послеоперационной раны на шее у 2 больных (9,0%). Длительность послеопера-
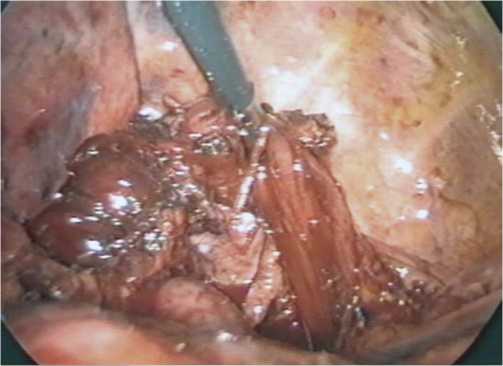
Рис. 3. Мобилизованный грудной отдел пищевода ционного пребывания в стационаре составила 21,3±2,9 суток. Сравнительные результаты шунтирующей поза-дигрудинной эзофагопластики открытым способом и с использованием видеоэндохирургической техники у больных РСП представлены в табл. 3.
При сомнительной «жизнеспособности» трансплантата, тяжелом соматическом состоянии пациента наложение анастомоза на шее выполнялось вторым этапом через 1–1,5 месяца. Через гастростомическое отверстие и желудочно-толстокишечный анастомоз эндоскоп проводился в просвет трансплантата до места наложения анастомоза в зоне ранее подшитого к пищеводу десерозированного орального конца трансплантата.
Через ротовую полость в глотку вводили оригинальное устройство (рис. 7). В условиях трансиллюминации (рис. 8) визуализировался светящийся конец эндоскопа, в направлении которого электрохирургическим крючком формировали отверстие между просветом пищевода и трансплантатом. Затем стенку пищевода и трансплантата рассекали на протяжении 3–4 см эндоскопической насадкой аппарата Liga Sure, формировали анастомоз
Табл. 2. Результаты трансхиатальной и видеоторакоскопической экстирпации пищевода с одномоментной эзофагопластикой у больных с РСП и РП
|
Трансхиатальная экстирпация пищевода с одномоментной эзофагопластикой, n=14 |
Видеоторакоскопическая экстирпация пищевода с одномоментной заднемедиастинальной эзофагопластикой, n=24 |
|
|
Длительность эзофагэктомии + эзофагопластики, (мин.) |
337,8±45,9 |
379,3±41,9 (p<0,05) |
|
Кровотечение, потребовавшее торакотомии |
2 (14,3%) |
1 (4,2%) |
|
Вскрытие обеих плевральных полостей |
3 (21,4%) |
1 (4,2%) (p<0,01) |
|
Отделяемое по дренажам в первые 3 суток, (мл) |
1197,5±532,2 |
683,2±189,1(p<0,01) |
|
Длительность назначения наркотических аналгетиков, (сут.) |
3,8±1,0 |
2,9±1,1(p<0,05) |
|
Послеоперационная пневмония |
5 (35,7%) |
5 (20,8%) |
|
Несостоятельность анастомоза |
3 (21,4%) |
4 (16,7%) |
|
Летальность |
1 (7,1%) |
1 (4,2%) |
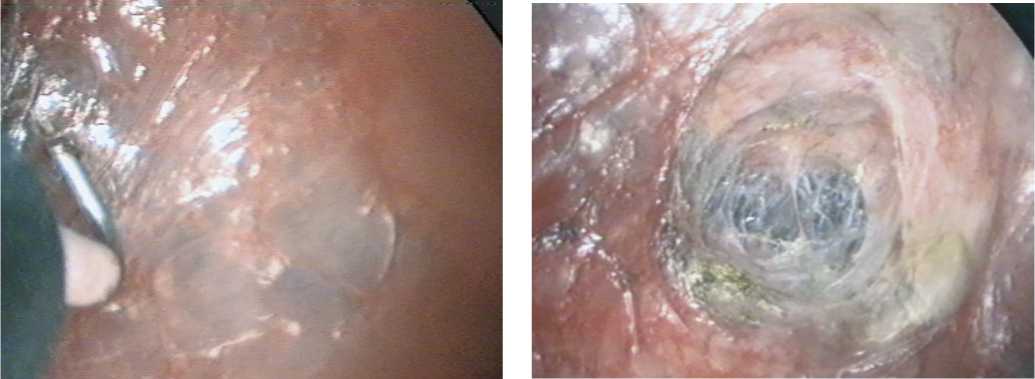
Рис. 5. Сформированный загрудинный тоннель
Рис. 4. Формирование загрудинного тоннеля
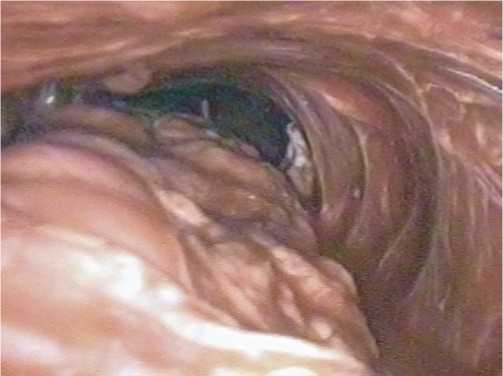
Рис. 6. Проведение трансплантата по сформированному загрудинному тоннелю. Осмотр трансплантата и его сосудистой ножки
«бок в бок» (рис. 9). Аналогичным способом при стенозах ранее наложенных анастомозов производилась их реконструкция.
Клинические результаты формирования и реконструкции анастомоза на шее у больных с РСП представлены в табл. 4.
Выводы
Определение оптимального угла наклона грудной клетки пациента к плоскости операционного стола, достижение максимально эффективных критериев оперативного доступа к пищеводу, сокращение количества необходимых портов, снижение частоты интра- и послеоперационных осложнений основано на топографоанатомическом исследовании и медико-математическом моделировании.
Сравнительный анализ результатов экстирпации и пластики пищевода с использованием абдомино-церви-
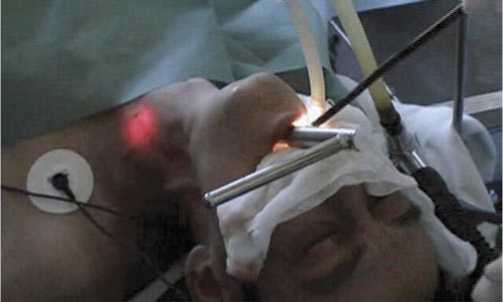
Рис. 7. Использование оригинального устройства для наложения пищеводного анастомоза
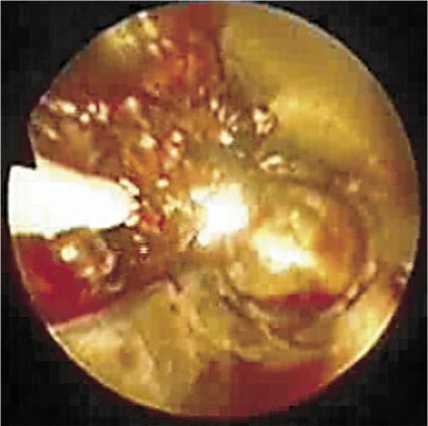
Рис. 8. Наложение пищеводно-толстокишечного анастомоза. Использование аппарата Liga Sure
Табл. 3. Результаты шунтирующей позадигрудинной эзофагопластики открытым способом и с использованием видеоэндохирургической техники у больных рубцовыми стриктурами пищевода
|
Шунтирующая позадигрудинная эзофагопластика открытым способом n=23 |
Шунтирующая позадигрудинная эзофагопластика с использованием видеоэндохирургической техники, n=22 |
|
|
Длительность этапа формирования загрудинного тоннеля и проведения трансплантата (мин.) |
39,5±8,7 |
47,5±11,3 |
|
Длительность операции, (мин.) |
347±49,1 |
327±31,7 |
|
Вскрытие одной плевральной полости |
5 (21,7%) |
1 (4,5%) |
|
Вскрытие обеих плевральных полостей |
3 (13,0%) |
– |
|
Кровотечение |
2 (8,7%) |
– |
|
Отделяемое по дренажам в первые 3 суток, (мл) |
174,5±42,2 |
108,7±29,3 |
|
Несостоятельность анастомоза |
3 (13,0%) |
2 (9,0%) |
|
Летальность |
2 (8,7%) |
1 (4,5%) |
Табл. 4. Результаты формирования и реконструкции анастомоза на шее у больных с РСП
Преимущества видеоэндоскопического формирования позадигрудинного тоннеля заключаются в адекватной визуализации всех этапов отделения внутригрудной фасции от грудины, существенно более низкой частоте интра- и послеоперационных осложнений, снижения общей травматичности операции.
Дифференцированное количество вводимого газа в загрудинную клетчатку, зависящее от типа телосложения пациента, не вызывает напряженной эмфиземы и экстраперикардиальной тампонады сердца, позволяет создавать тоннель оптимальных размеров для свободного проведения трансплантата и сохранения его жизнеспособности.
Видеоэндохирургический способ формирования тоннеля и проведения трансплантата обеспечивает контроль положения сосудистой ножки трансплантата, снижает риск интраоперационных осложнений (повреждение париетальной плевры и неконтролируемого кровотечения в ретростернальном клетчаточном пространстве), и в целом повышает качество хирургической техники при лечении больных с протяженными РСП.
Получены положительные клинические эффекты разработанной видеоэндоскопической внутрипросветной методики наложения анастомоза между пищеводом и трансплантатом на шее как при выполнении второго этапа пластики пищевода, так и при эндоскопической реконструкции анастомоза между пищеводом и трансплантатом на шее в связи с рубцовым сужением анастомоза.
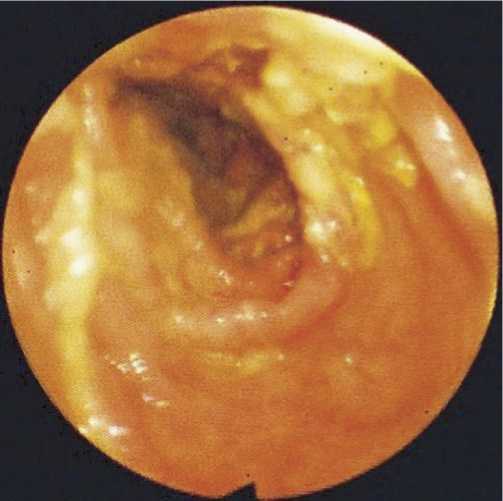
Рис. 9. Зона вмешательства после наложения соустья
Список литературы Возможности видеоэндохирургической техники при экстирпации и пластике пищевода
- Бакиров А.А. Восстановительные операции при сочетанных ожоговых стриктурах пищевода и желудка/А.А. Бакиров//Хирургия. Журнал им. Н.И. Пирогова. -2001. -№5. -С. 19-23.
- Марийко В.А. Эзофагэктомия у больных с ожоговыми стриктурами пищевода/В.А.Марийко, В.С.Нечай, В.Н.Титов и др.//Анналы хирургии. -2005. -№ 4. -С. 22-26.
- Черкасов М.Ф. Видеоэндохирургическое лечение доброкачественных заболеваний пищевода (клинико-анатом. и эксперим. исследования): Автореф. дис... докт. мед. наук/М.Ф. Черкасов. -Ростов-на-Дону, 1999. -45 с.
- Черноусов А.Ф. Хирургия пищевода: Руководство для врачей/А.Ф. Черноусов, П.М. Богопольский, Ф.С. Курбанов. -М.: Медицина, 2000. -352 с.


