Возникновение "передува" на жидкостекольных смесях при отверждении углекислым газом
Автор: Фирстов Александр Петрович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Литейное производство
Статья в выпуске: 3 т.22, 2022 года.
Бесплатный доступ
К одним из первых упоминаний о применении жидкого стекла в литейном производстве относятся работы А.И. Жилина, И.Н. Завьялова середины 30-х гг. XX в. В это время отверждение жидкого стекла осуществлялось сушкой, с целью ускорения процесса затвердевания. Внедрение жидкого стекла, отверждаемого химическим путем, в литейном производстве для приготовления форм и стержней в СССР было начато в 1948-1949 гг., что позволило сократить технологический процесс, повысить производительность производства, снизить трудоемкость и значительно уменьшить брак отливок. Но с перечисленными выше положительными чертами при продувке формы углекислым газом литейщики столкнулись с трудностями при применении СО2-процесса. Такими трудностями оказались наличие пригара и затруднительная выбивка стержней, что препятствует активному внедрению процесса химического твердения. Основной причиной недостатков при химическом отверждении оказался передув химического реагента, то есть углекислого газа. Оптимальным и научно доказанным временем отверждения жидкого стекла является стехиометрическое отношение коэффициентов в определенном уравнении реакции. Чрезмерное время продувки жидкостекольных смесей при отверждении углекислым газом приводит к понижению прочности фасонного изделия. Этот недостаток во многом зависит от значительного накопления в формовочной смеси легкоплавкого гидрокарбоната натрия, приводящего к возникновению термического пригара. Одной из причин возникновению термического пригара является появление гидрокарбоната натрия, имеющего низкую температуру плавления, приводящую к легкоплавким включениям, которые и приводят к появлению пригара. Убрать легкоплавкий гидрокарбонат возможно при добавлении в разделительное покрытие растворимых в воде солей меди.
Жидкостекольная смесь, прочность, время продувки, гидрокарбонат натрия, сульфат меди, разделительное покрытие, со2-процесс
Короткий адрес: https://sciup.org/147238584
IDR: 147238584 | УДК: 675.92.027 | DOI: 10.14529/met220301
The occurrence of “blowing” on liquid-glass mixtures during curing with carbon dioxide
One of the first mentions of the use of liquid glass in foundry production are the works of A.I. Zhilin, I.N. Zavyalov in the mid-30s of the XX century. At this time, the curing of liquid glass was carried out by drying, in order to accelerate the solidification process. The introduction of chemically cured liquid glass in the foundry for the preparation of molds and rods in the USSR was started in 1948-1949, which made it possible to shorten the technological process, increase production productivity, reduce labor intensity and significantly reduce the marriage of castings. But with the positive features listed above, when blowing the mold with carbon dioxide, foundry workers faced difficulties when using the CO2-process. Such difficulties were the presence of a prig and difficult knocking out of the rods, which prevents the active introduction of the chemical hardening process. The main reason for the shortcomings in chemical curing was the overdrive of a chemical reagent, that is, carbon dioxide. The optimal and scientifically proven curing time of liquid glass is the stoichiometric ratio of the coefficients in a certain reaction equation. Excessive purging time of liquid glass mixtures during curing with carbon dioxide leads to a decrease in the strength of the shaped product. This disadvantage largely depends on the significant accumulation of low-melting sodium bicarbonate in the molding mixture, which leads to the appearance of thermal burn. One of the reasons for the occurrence of thermal burn is the appearance of sodium bicarbonate, which has a low melting point, leading to low-melting inclusions, which lead to the appearance of burn. It is possible to remove fusible bicarbonate by adding water-soluble copper salts to the separation coating.
Текст научной статьи Возникновение "передува" на жидкостекольных смесях при отверждении углекислым газом
Применение жидкого стекла в литейном производстве решило определенные задачи [1–3], особенно при получении массивных отливок, а опробование и внедрение химического отверждения жидкостекольной формы завоевало определенную нишу для получения качественных литейных отливок. Это касается повышенной точности, снижения припусков на механическую обработку, снижения расхода свежего песка, и самое главное – отпадает необходимость сушки стержней и форм, что приводит к снижению времени технологического процесса [4, 5].
При внедрении СО 2 -процесса на производстве обнаружились определенные проблемы по качеству литейной отливки [6–8]. Основной проблемой оказался термический пригар, особенно на термических узлах отливки.
Авторы считают, что возможность снизить или убрать основной недостаток жидкостекольной смеси, как пригар и снижение прочности в интервале температур 400–600 °С, при СО 2 -процессе, без введения улучшающих смесь добавок, сводится к уменьшению подачи в жидкостекольную смесь углекислого газа. Но снижение подачи газового реагента скажется на пониженной прочности смеси. Повышенная подача углекислого газа приведет к пересыщению образовавшегося карбоната натрия в формовочной смеси с дальнейшим его распадом на гидрокарбоната натрия, который будет накапливаться в приграничных и глубинных слоях формовочной смеси, а дальнейшее тепловое воздействие приведет к образованию углекислого газа и паров воды [9, 10].
Таким образом, при стехиометрических отношениях исходных веществ реакция идет по уравнению (1) с образованием карбоната натрия (Na 2 CO 3 ) средней соли с температурой плавления, равной 852 °С, а избыток СО 2 приводит к образованию гидрокарбоната натрия (NaHCO3), и реакция идет по уравнению (2) с образованием кислой соли с температурой плавления, равной 270 °С [11]. В водных растворах при повышенных температурах гидрокарбонат натрия начинает разлагаться в интервале температур 60–200 °С с образованием водяного пара и углекислого газа (3) [12], что приведет к возникновению внутренних напряжений и трещин в отвердевшей жидкостекольной смеси с резким снижением прочности [13, 14].
Na 2 H 2 SiO 4 + CO 2 + H 2 O =
= H4SiO4↓ + Na2CO3;(1)
Na 2 H 2 SiO 4 + 2CO 2 + 2H 2 O =
= H4SiO4↓ + 2NaHCO3;(2)
2NaHCO 3 (р.) =
= Na2CO3(р.) + CO2(г.) + H2O(пар).(3)
Получившиеся продукты реакции по своим свойствам различны по температуре плавления, и данная разница в температурных параметрах приводит к возникновению «плавней», имеющих повышенную адгезию к песку, и, как следствие, возникновению термического пригара, который, в свою очередь, ухудшит поверхностные слои будущего фасонного изделия с пониженными прочностными характеристиками.
Выявление причин появления пониженной прочности сравнивали с накоплением продуктов реакции в жидкостекольной смеси при различном времени продувки формовочной смеси. Состав жидкостекольной смеси был следующим:
– песок кварцевый Басьяновского месторождения марок 5К 3 О 4 016 – 100 %;
– натриевое жидкое стекло М = 2,56, ρ = 1200 кг/м3 – 5 %.
Жидкостекольная смесь имела газопроницаемость 80 м4/Н∙с, прочность на разрыв в сухом состоянии 1,75 МПа, продуваемая углекислым газом при давлении 0,15 МПа. Предел прочности на разрыв в сухом состоянии для жидкостекольной смеси вели по ГОСТ 23409.7–78.
Опытные испытания проводили с той же жидкостекольной смесью, но на её поверхность наносили разделительное покрытие, имеющее в своем составе соль, катионом которой является металл с положительным электродным потенциалом, а анионом являлся кислотный остаток, больший по силе, чем угольная кислота [15]. Примером данной соли являлся сульфат меди. Молекулярное соотношение жидкого стекла и соли было в соотношении 2 : 1.
Результаты испытаний по продувке жидкостекольной смеси углекислым газом с изменением прочности на разрыв в сухом состоянии представлены на рис. 1.
Определение карбоната натрия и гидрокарбоната натрия определяли методом потенциометрического титрования по ГОСТ 26424–85 с фиксацией точек: для карбоната натрия – до рН = 8,3, а гидрокарбоната натрия – до рН = 4,4 [16].
Результаты испытаний по продувке жидкостекольной смеси углекислым газом с процентным содержанием карбоната натрия и гидрокарбоната натрия представлены на рис. 2.
В зависимости от продолжительности продувания углекислым газом прочность жидкостекольной смеси изменяется. В начальный момент продувки происходит быстрое возрастание прочности (см. рис. 1). Затем достигается некоторый максимум, а в дальнейшем происходит постепенное снижение прочности (явление «передува»). Снижение прочности в сухом состоянии наступает при продолжительности продувки выше двух минут.
Максимальное значение прочности жидкостекольной смеси соответствует моменту максимального содержания карбоната натрия (Na 2 CО 3 ). Поэтому увеличение длительности продувки свыше оптимального времени понижает прочностные свойства смеси. При фронтальной подаче реагента различные слои
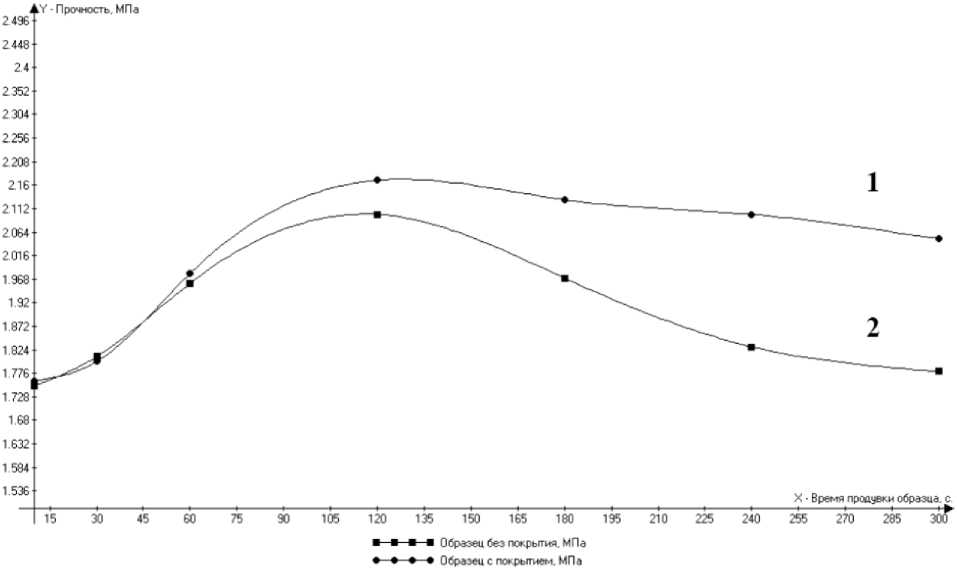
Рис. 1. Зависимость прочности в сухом состоянии от времени продувки углекислым газом: 1 – жидкостекольная смесь с покрытием; 2 – жидкостекольная смесь без покрытия
Fig. 1. Dependence of strength in a dry state on the time of purge with carbon dioxide:
1 – liquid glass mixture with a coating; 2 – uncoated liquid glass mixture
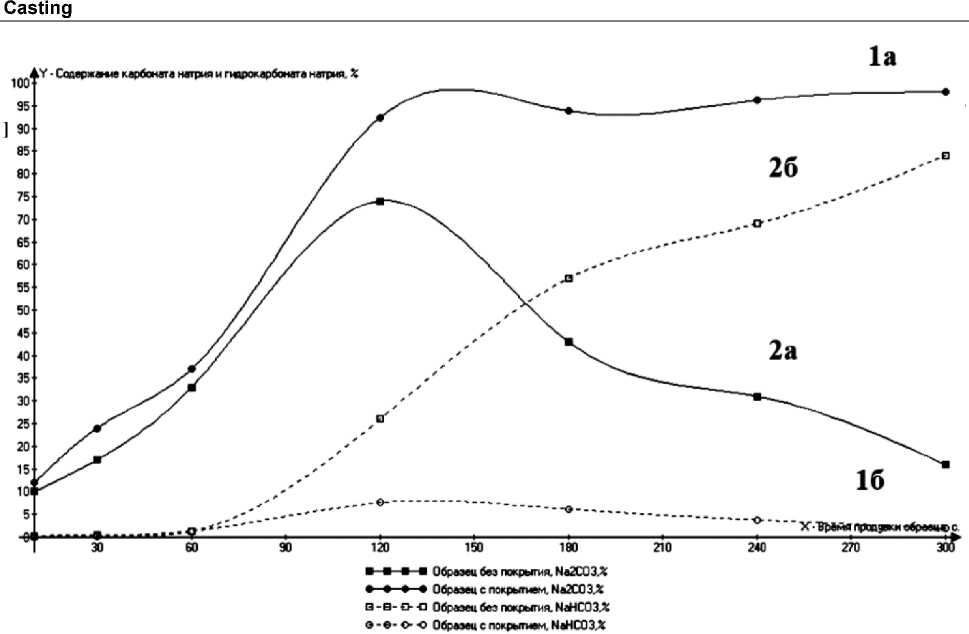
Рис. 2. Зависимость процентного содержания карбоната натрия и гидрокарбоната натрия от времени продувки углекислым газом: 1 – жидкостекольная смесь с покрытием; 2 – жидкостекольная смесь без покрытия Fig. 2. Dependence of the percentage of sodium carbonate and sodium bicarbonate on the time of purge with carbon dioxide: 1 – liquid glass mixture with a coating; 2 – uncoated liquid glass mixture
смеси в форме достигают наибольшей прочности в разное время. Первыми максимальную прочность приобретают слои, находящиеся близко к месту подвода углекислоты, т. е. поверхностные. По мере насыщения слоев углекислым газом максимум прочности смеси начинает перемещаться в глубь формы, в то время как в первых слоях развивается процесс пересыщения СО 2 с образованием гидрокарбоната натрия (NaHCО 3 ), приводящего к разупрочнению формы.
Незначительное снижение идет на жидкостекольной смеси с покрытием, в состав которого входит сульфат меди.
Объяснение можно увидеть на рис. 2, где видно, что наибольшее накопление карбоната натрия происходит при достижении двух минут (см. рис. 2, линии 1а и 2а) и при дальнейшей подаче углекислого газа идет его резкое снижение за счет образования гидрокарбоната натрия (см. рис. 2, линия 2б).
Устранение «передува» будет происходить за счет реакции (4), приводящей практически к полной ликвидации гидрокарбоната натрия (см. рис. 2, линия 1б):
CuSO 4 + 2NaHCO 3 =
= CO 2 ↑ + Na 2 SO 4 + CuCO 3 + H 2 O. (4)
Таким образом, для снижения или полного устранения «передува» необходимо либо:
– следовать рекомендациям авторов [5, 9, 10, 13, 17] по продолжительности продувки в интервале 3–5 мин;
– рассчитывать оптимальное время продувки жидкостекольной формы относительно объема формовочной смеси, типа подачи углекислого газа и времени продува [17];
– наносить разделительное покрытие с солью, катионом которой является металл с положительным электродным потенциалом, а анионом является кислотный остаток, больший по силе, чем угольная кислота, при молекулярном соотношении жидкого стекла и соли 2 : 1.
Список литературы Возникновение "передува" на жидкостекольных смесях при отверждении углекислым газом
- Жилин А.И. Растворимое стекло, его свойства, получение и применение. Свердловск; М.: Гос. объединен. науч.-техн. изд-во, 1939. 100 с.
- Завьялов И.Н. Растворимое стекло // Строительная индустрия: справ. рук. по гражд. и пром. стр-ву / под общ. ред.: В.И. Вельман (гл. ред.) [и др.]. М.; Л.: ОНТИ-Госстройиздат, 1934. Т. 4. С. 184–194.
- Константинов Б.А., Пичета К.В., Филиппкин А.Т. Применение СО2 при изготовлении литейных форм: По материалам зарубежной печати. М.: Дом техники, 1957. 118 c.
- Мариенбах Л.М., Петров В.П., Фрадин Л.Р. Применение углекислого газа для химического твердения литейных форм и стержней. М.: Центр. бюро техн. информации трактор. и с.-х. машиностроения, 1958. 75 с.
- Вопросы теории литейных процессов / П.Н. Аксенов [и др.]. М.: Машгиз, 1960. 694 с.
- Лясс А.М., Куманин И.Б. Быстросохнущие смеси с жидким стеклом: Инструктивные материалы. М.: Машгиз, 1954. 49 с.
- Комаров Ф.В., Сысоев С.И. Химическая сушка литейных форм и стержней. М.: Машгиз, 1952. 36 с.
- Соколовский Л.О., Урин М.Н. Процесс химического твердения литейных форм и стержней. Л.: [б. и.], 1956. 11 с.
- Борсук П.А., Лясс А.М. Жидкие самотвердеющие смеси. М.: Машиностроение, 1979. 255 с.
- Жуковский С.С. Прочность литейной формы. М.: Машиностроение, 1989. 288 с.
- Лидин Р.А., Молочко В.А., Андреева Л.Л. Химические свойства неорганических веществ: учеб. пособие для вузов / под ред. Р.А. Лидина. 3-е изд., испр. М.: Химия, 2000. 480 с.
- Фирстов А.П. Дальнейшее применение СО2-процесса // Теория и технология металлургического производства. 2014. № 1 (14). С. 47–49.
- Илларионов И.Е., Петрова Н.В. Жидкостекольные смеси, отверждаемые продувкой углекислым газом // Труды Нижегородского государственного технического университета им. Р.Е. Алексеева. 2011. № 2 (87), С. 208–213.
- Фирстов А.П., Фирстова Н.Д. Преимущества применения кислот средней силы при от-верждении щелочных силикатов натрия // Литейные процессы. 2013. № 12. С. 161–165.
- Пат. RU 2764908 C1. Способ отверждения жидкостекольной смеси при изготовлении форм и стержней / А.П. Фирстов, Е.А. Лебедева, В.В. Мороз и др. № 2021122794; заявл. 30.07.2021; опубл. 24.01.2022.
- Можарин В.П. Литейное производство: учеб. пособие в двух книгах / В.П. Можарин; Юр-гинский технологический институт. Томск: Изд-во Томского политехн. ун-та, 2011. 408 с.
- Фирстов А.П. Расчет времени отверждения жидкостекольной формы на примере отливки «Корпус буксы» // Евразийское Научное Объединение. 2019. № 7-1 (53). С. 65–68.


