Выбор метода лечения послеоперационных вентральных грыж
Автор: Магомедов М.М., Топчиев А.М., Топчиев М.А., Абдулжалилов М.К., Магомедов А.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Абдоминальная хирургия
Статья в выпуске: 1 (95), 2026 года.
Бесплатный доступ
Введение. Устранение больших послеоперационных грыж является сложной задачей, а у пациентов с ожирением, диабетом и курением кратно возрастает риск послеоперационных осложнений. Цель исследования. Оценить результаты лечения послеоперационных вентральных грыж у больных с избыточной массой тела путем дифференцированного подхода к выбору метода герниопластики. Материал и методы исследования. Изучены результаты хирургического лечения 135 пациентов с послеоперационными вентральными грыжами в двух медицинских учреждениях. Первая группа (68 пациентов) оперирована с использованием эндопротезной сетки, вторая группа (67 пациентов) – с аутодермальным трансплантатом, подготовленным в оксигенированных препаратах. Результаты. Многофакторный логистический регрессионный анализ не выявил существенных различий в частоте возникновения нежелательных явлений между группами (ОШ = 0,834, 95 % ДИ [0,456–1,592], p = 0,687). Однако было отмечено значительное снижение частоты возникновения сером (7,35 % против 1,49 %, p = 0,004). Более того, аутотрансплантация кожи была связана со снижением частоты возникновения серомы (ОШ = 0,296, 95 % ДИ [0,097–0,931], p = 0,042). Заключение. Герниопластика с использованием деэпителизированной аутодермы, подготовленной предимплантационно в оксигенированных препаратах, подходит для лечения послеоперационных вентральных грыж у пациентов с ожирением (ИМТ ≥ 25 кг/м2), сахарным диабетом, а также у пациентов из группы высокого риска.
Послеоперационная вентральная грыжа, эндопротезирование передней брюшной стенки, аутопластика, дермальный трансплантат
Короткий адрес: https://sciup.org/142247237
IDR: 142247237 | УДК: 617-089.844 | DOI: 10.17238/2072-3180-2026-1-32-39
Choice of treatment method for postoperative ventral hernias
Introduction. Eliminating large postoperative hernias is a difficult task, and in patients with obesity, diabetes, and smoking, the risk of postoperative complications increases many times. Study objective. To evaluate the results of treatment of postoperative ventral hernias in overweight patients by using a differentiated approach to the choice of hernioplasty method. Materials and methods. The results of surgical treatment of 135 patients with postoperative ventral hernias in two medical institutions were studied. The first group (68 patients) underwent surgery using an endoprosthetic mesh, the second group (67 patients) underwent an autodermal transplant prepared in oxygenated preparations. Results. Multifactorial logistic regression analysis revealed no significant differences in the incidence of adverse events between the groups (OR = 0,834, 95 % CI [0,456–1,592], p = 0,687). However, there was a significant decrease in the incidence of seromas (7,35 % vs. 1,49 %, p = 0.004). Moreover, skin autotransplantation was associated with a decrease in the incidence of seroma (OR = 0,296, 95 % CI [0,097–0,931], p = 0,042). Conclusion. Hernioplasty using deepithelized autoderm prepared preimplantatively in oxygenated preparations is suitable for the treatment of postoperative ventral hernias in obese patients (BMI ≥ 25 kg/m2), diabetes mellitus, as well as in patients at high risk.
Текст научной статьи Выбор метода лечения послеоперационных вентральных грыж
После появления современных синтетических сетчатых материалов интерес к исследованиям в области аутотрансплантации кожи угас, особенно после смены парадигмы, произошедшей после исследований полипропиленовой сетки, проведённых Usher в 1958 году [1–3]. Использование сетки при стандартном лечении грыжи снижает риск рецидива примерно до 10 %, но при гигантских грыжах частота рецидивов составляет от 10 до 30 % [1]. Синтетическая сетка также может стать причиной хронической боли, инфекции и образования кишечно-кожного свища [4, 5], нарушению функции брюшной стенки с уменьшением мышечной силы и гибкости [5, 6]. Однако с ростом осведомленности о хронической послеоперационной боли и дискомфорте, а также о серьёзных осложнениях, связанных с имплантированным инородным материалом, в некоторых подгруппах пациентов с вентральной грыжей стала очевидной необходимость в альтернативных армирующих материалах [7–9]. Биологические трансплантаты были частично разработаны для устранения недостатков синтетической сетки, особенно в случаях инфицирования. В результате интерес к аутотрансплантации кожи возрос, и публикуется всё больше исследований [10, 11]. Результаты хирургических методов лечения сильно различаются. При герниопластике без сетки частота рецидивов высока, в то время как установка сетки может снизить риск рецидива [6]. При установке сетки одной из наиболее важных проблем является её расположение. Сообщается, что некоторые методы связаны с особенно высоким риском возникновения определённых осложнений, таких как рецидив, раневая инфекция и свищ [3]. В литературе проводится несколько исследований, в которых сравниваются методы пластики с использованием сетки и без неё, а также типы сеток и плоскости, в которых следует размещать сетку. Аутологичные одно- или двухслойные кожные трансплантаты в случае ожирения у пациентов высокого риска с рецидивирующими инфицированными грыжами могут быть успешно использованы при плановых реконструкциях брюшной стенки [12]. Использование двухслойного дер- мального трансплантата при сложных и рецидивирующих грыжах брюшной стенки описано в литературе как плановый хирургический метод [11]. Обоснование необходимости перфорации внешнего слоя трансплантата заключается в его более быстрой интеграции и ремоделировании. При интеграции аутодермального трансплантата были доказаны неоваскуляризация и ремоделирование коллагена даже в неоптимальных (инфицированных, некротических) условиях [6]. Такая реконструкция брюшной стенки не приводит к значительному повышению внутрибрюшного давления. С одной стороны, двухслойные дермальные аутотрансплантаты лучше противостоят внутрибрюшному давлению. Кроме того, укрепление брюшной стенки происходит более выраженно, чем в случае с однослойными трансплантатами [6]. Второе преимущество заключается в более интенсивной интеграции и перестройке внешнего кожного трансплантата, перфорированного описанным способом. Недостаток двухслойных кожных трансплантатов заключается в том, что трансплантат подходящего размера можно получить только у пациентов с ожирением. Если невозможно получить трансплантат подходящего размера, операция не проводится. Например, для реконструкции двухслойным дермальным трансплантатом дефекта брюшной полости площадью 100 см2 требуется дермальный трансплантат площадью около 300 см2. Перед применением этого метода во время физикального обследования брюшной полости можно оценить размер избыточного кожно-подкожного жирового комка и использовать этот метод только в том случае, если его размер достаточен [6]. Для правильной подготовки трансплантатов требуется практика. Не рекомендуется использовать этот метод в острых случаях, когда жировая ткань находится в замкнутом пространстве. Для более точной оценки влияния дермального трансплантата операций на частоту рецидивов грыж, продолжительность пребывания в стационаре и расходы на лечение в больнице на уровне сообщества потребуются дальнейшие исследования.
Цель исследования
Оценить результаты лечения послеоперационных вентральных грыж у больных с избыточной массой тела путем дифференцированного подхода к выбору метода герниопластики.
Материалы и методы
Это было ретроспективное исследование с участием 135 пациентов, которым была проведена пластика послеоперационных вентральных грыж. Настоящее исследование представляет данные из двух независимых учреждений. Были проанализированы хирургические карты 135 пациентов, перенёсших пластику послеоперационных грыж. 68 пациентов из отделения хирургии РКБСМП г. Махачкала (операции проводились в период с 1 января 2015 года по 31 декабря 2024 года) и 67 пациентов, оперированных с применением аутодермального деэпителизированного трансплантата, подготовленного предимплантационно в оксигенированных препаратах [патент на изобретение РФ 2465837 от 10.10.2012 г., № 2022103233 / 09.02.2022], из отделения хирургии больницы общего профиля г. Астрахань (операции проводились в период с 1 января 2012 года по 31 декабря 2024 года) соответствовали критериям включения. Все процедуры проводились в соответствии с этическими стандартами ответственного комитета по проведению экспериментов на людях и Хельсинкской декларацией 1975 года с поправками 2008 года. Пациенты с индексом массы тела (ИМТ) выше 35 кг/м2, оценкой Американского общества анестезиологов (ASA) 4 балла или тяжелыми заболеваниями легких или сердца не были включены в исследование. Остальные пациенты, согласившиеся на участие и подписавшие форму информированного согласия, были случайным образом распределены на две группы: первая группа – оперированные с применением эндопротезной полипропиленовой сетки, а вторая группа – с применением аутодермального лоскута. Характеристики пациентов, включая возраст и пол, индекс массы тела, детали операции, в том числе размер дефекта и размер сетки, продолжительность пребывания в больнице и состояние пациентов через 2 месяца после операции, были взяты из медицинских карт каждого пациента. Также были записаны данные о предоперационной компьютерной томографии брюшной полости, продолжительности пребывания в больнице, размере сетки и времени последующего наблюдения. После операции записанные случаи были проанализированы на предмет краткосрочных и долгосрочных осложнений. Ви- зуализация, то есть компьютерная томография или ультразвуковое исследование, проводилась при необходимости для подтверждения наличия или отсутствия осложнений. Для подтверждения или опровержения наличия рецидива проводилась компьютерная томография.
Пациенты были распределены на 3 категории по степени ожирения. Число пациентов с ожирением в основной и контрольной группах сравнимо (p >0,05).
Среди 135 проанализированных пациентов 97 (71,9 %) были женщины и 38 (28,1 %) – мужчины. Средний ИМТ составил 31 кг/м2. Распределение пациентов по классификации АSA отражено в таблице 1. Большинство грыж исходило от средней линии (88,1 %). Основные демографические показатели представлены в таблице 1.
Таблица 1 Основные демографические данные основной и контрольной группы
Table 1
Basic demographic data of the main and control groups
|
Пациенты / Patients |
Основная группа / Main group |
Контрольная группа / Control group |
Всего/ Total |
|
Всего |
68 (50,37 %) |
67 (49,63 %) |
135 |
|
Total |
|||
|
Пол : |
|||
|
Gender: |
|||
|
мужской |
19 (27,9 %) |
19 (28,4 %) |
38 (28,1 %) |
|
male |
|||
|
женский |
49 (72,1 %) |
48 (71,6 %) |
97 (71,9 %) |
|
female |
|||
|
ASA: |
|||
|
1 |
21 (30,9 %) |
21 (31,3 %) |
42 (31,1 %) |
|
2 |
33 (48,5 %) |
24 (35,8 %) |
57 (42,2 %) |
|
3 |
13 (19,1 %) |
19 (28,4 %) |
32 (23,7 %) |
|
4 |
1 (1,5 %) |
3 (4,5 %) |
4 (3,0 %) |
|
Отсутствуют |
1 (1,5 %) |
1 (1,5 %) |
2 (1,5 %) |
|
Missing |
|||
|
Медиана ИМТ (диапазон) |
36,4 (30,2-32,0) |
38,9 (32,5-35,5) |
31,7 (35,5-39,9) |
|
Median BMI (range) |
|||
|
Размер грыжи (мм) |
40 (10-100) |
60 (10-100) |
100 (10-200) |
|
Hernia size (mm) |
|||
|
Курильщики |
4 (5,9 %) |
5 (7,5 %) |
9 (6,7 %) |
|
Smokers |
В таблице 2 показаны размеры грыжевых ворот основной и контрольной группы.
Таблица 2
Размеры грыжевых ворот основной и контрольной группы
The sizes of the hernial gates of the main and control groups
Table 2
|
Показатель / Indicator |
Основная группа (n=68) / Main group (n=68) |
Группа контроля (n=67) / ontrol group (n=67) |
U |
Р |
|
Ме (25,75) |
Ме (25,75) |
|||
|
Грыжевой анамнез / Hernial history |
15,0 (11,0; 37,0) |
14,0 (12,0; 38,0) |
491,0 |
0,488 |
Окончание Таблицы 2 / End of Table 2
|
Показатель / Indicator |
Основная группа (n=68) / Main group (n=68) |
Группа контроля (n=67) / ontrol group (n=67) |
U |
Р |
|
Ме (25,75) |
Ме (25,75) |
|||
|
Ширина грыжевых ворот, см / The width of the hernial gate, cm |
12,0 (11,0; 16,1) |
12,0 (19,1; 145,0) |
369,6 |
0,019 |
|
Длина грыжевых ворот, см / The length of the hernial gate, cm |
133,1 (97,8; 176,1) |
134,0 (98,0; 141,0) |
418,0 |
0,086 |
|
Площадь грыжевых ворот, см2, The area of the hernial gate, сm2 |
135,1 (97,8; 176,1) |
130,0 (98,0; 141,0) |
418,1 |
0,099 |
Примечание: х2-критерий; х2- Пирсона; U- критерий Манна-Уитни.
Notes : x2-criterion; x2-Pearson; U- Mann-Whitney criterion.
По сравнению групп непосредственно по величине грыжевых ворот достоверных различий не выявлено (Mann-Whithey (U=981, p=0,499)) (табл. 3).
Таблица 3
Сравнение пациентов в группах по размеру грыжи и степени ожирения
Comparison of patients in groups by hernia size and degree of obesity
Table 3
|
Основная группа / Main group |
Контрольная группа / Control group |
р-значение / p-value |
|||
|
Размер грыжи / Hernia size |
n |
% |
n |
% |
|
|
W1 |
11 |
16,2 |
16 |
23,9 |
х2=6,102; р*=0,225 |
|
W2 |
38 |
55,9 |
32 |
47,8 |
х2=4,028; р=0,354 |
|
W3 |
19 |
27,9 |
19 |
28,4 |
х2=1,942; р=0,545 |
|
Всего: /Total: |
68 |
100 |
67 |
100 |
|
|
Степень ожирения / The degree of obesity |
|||||
|
I |
30 |
44,11 |
30 |
44,78 |
х2=15,044; р=0,352 |
|
II |
34 |
50,00 |
34 |
50,74 |
х2=1,800; р=0,749 |
|
III |
3 |
4,41 |
4 |
5,88 |
х2=1,600; р=0,839 |
|
Всего: / Total: |
67 |
100 |
68 |
100 |
|
Примечание: Расчет статистической значимости для р*-значения проводился с применением χ²Пирсона с поправкой Йейтса
Notes: The calculation of statistical significance for the p*-value was carried out using χ2 Pearson with the Yates correction
Все операции проводились под общим наркозом. У всех пациентов сетка располагалась таким образом, чтобы со всех сторон она перекрывала фасцию как минимум на 5 см. Всем пациентам над сеткой устанавливали вакуумный дренаж, а кожу и подкожную клетчатку закрывали рассасывающимися швами. Оперативное вмешательство второй группы проводилось с применением деэпителизированного аутодермального лоскута (ДАТ), выкроенного над местом грыжевого выпячивания во время операции. Деэпителизированный аутодермальный лоскут, подготовленный предимплантационно, моделировался по размеру дефекта и перекрывал его на 5 см от его края. Фиксация его осуществлялась узловыми швами к апоневрозу или ретромускулярно, рассасываю- щимся шовным материалом 2/0. Аутодерма размещалась в 21 случае – onlay, в 46 – sublay. Операция заняла в среднем 188–230 минут, из которых 50 минут ушло на подготовку кожных трансплантатов. Суть реконструкции брюшной стенки заключается в укреплении анатомических структур передней брюшной стенки аутодермой, которая после имплантации хорошо интегрируется в тканях, что подтвердили экспериментальные исследования на животных. Всем оперированным пациентам после операций показатели по визуальной аналоговой шкале (ВАШ) регистрировались на второй и 24-й час. Вакуумные дренажи удалялись, когда суточный дренаж составлял менее 50 мл. По завершении исследования все пациенты были приглашены на контрольный осмотр, в ходе которого их подвергли физикальному обследованию. Инфекция раны определялась как эритема и нагноение вокруг раны. Любой скопившийся в ране экссудат удалялся и исследовался на предмет бактериального посева. Эмпирическая терапия антибиотиками (4 × 1 г ципрофлоксацин в/в) была начата на операционном столе. Для профилактики тромбоза через 6 часов после окончания операции был назначен эноксапарин (1 × 0,6 мл п/к). Антибиотики вводили внутривенно еще в течение 2–5 суток с поправками в соответствии с результатами микробиологического посева. Всем пациентам проводилось измерение внутрибрюшного давления до, вовремя операции и после ее завершения.
Статистический анализ
Анализ проводился с помощью программного обеспечения Statistical Package for the Social Sciences 22.0 (IBM Corp.; Армонк, США). Для сравнения количественных параметрических данных использовался t-критерий Стьюдента, а для сравнения количественных непараметрических данных – U-критерий Манна-Уитни. Для сравнения качественных данных использовался критерий хи-квадрат. Статистическая значимость принималась при уровне 0,05.
Результаты
Средняя продолжительность операции составила 186 минут (в диапазоне от 130 до 262 минут) при наложении сетки и 188 минут (в диапазоне от 108 до 224 минут) при пересадке полнослойного кожного трансплантата. Дренажи в группе с полнослойным кожным трансплантатом были удалены через 2–5 дней. Ни один пациент не был выписан домой с дренажом. Дренажи были удалены, когда потеря жидкости составляла менее 50 мл в день или не позднее чем на 5-й день после операции. На вопрос «Испытываете ли вы какой-либо дискомфорт в области хирургического вмешательства?» 3 пациента ответили «да» в группе с деэпителизированным кожным трансплантатом и 12 – в группе с сеткой (p = 0,016). Пациенты в группе с кожным трансплантатом сообщали о меньшей боли по сравнению с группой с сеткой: 3 (4,5 %) против 15 (22,1 %). Пациенты, которым в качестве импланта применялась деэпителизированная аутодерма, подготовленная предимплантационно, отметили более высокую степень субъективного улучшения функции брюшной стенки по сравнению с теми, кому была пересажена синтетическая сетка (медиана 9 против 7; p = 0,038). Двое пациентов из группы с сеткой были прооперированы повторно из-за кровотечения. Ни один пациент из группы с деэпителизированным кожным трансплантатом не был прооперирован повторно. Многофакторный логистический регрессионный анализ не выявил существенных различий в частоте возникновения нежелательных явлений между группами (ОШ = 0,834, 95 % ДИ [0,456–1,592], p = 0,687). Однако было отмечено зна- чительное снижение частоты возникновения сером (7,35 % против 1,49 %, p = 0,004). Более того, аутотрансплантация кожи была связана со снижением частоты возникновения серомы (ОШ = 0,296, 95 % ДИ [0,097–0,931], p = 0,042). Инфекционные осложнения со стороны раны мы не наблюдали у пациентов в группе с кожным трансплантатом и у 7 (10,3 %) пациентов в группе с сеткой (p = 0,722). Это мы связываем с особенностью подготовки кожного импланта перед имплантацией. Отношение шансов развития послеоперационных осложнений увеличивалось на 5 % на каждую единицу ИМТ (р <0,01), в основном из-за роста числа поверхностных раневых инфекций (р <0,01) и образования сером (р = 0,07) у оперированных первой группы. Инфекция области хирургического вмешательства (ИОХВ) в группе пациентов с аутодермальным трансплантатом мы не наблюдали. Это мы связываем с особенностью предимплантационной подготовки аутодермы. С сетчатым имплантом эти осложнения наблюдались у 7 (10,3 %) пациентов (p = 0,722). Все инфекции, кроме одной, были поверхностными или ограничивались подкожной клетчаткой. У одного из пациентов в группе с установкой сетки возникла подкожная инфекция, потребовавшая хирургического вмешательства под общим наркозом. Все пациенты с инфекцией получали лечение клиндамицином. Между группами достоверная (p <0,05) разница в уходе за собой была обнаружена только на шестом месяце. Однако результаты по всем параметрам были сопоставимы при окончательном наблюдении. Кроме того, показатель EQ-VAS постепенно улучшался с каждым послеоперационным визитом. Хотя на шестом месяце была обнаружена достоверная (p <0,05) разница в показателях EQ-VAS между группами с кожным трансплантатом (87,13±18,15) и сеткой (81,98 ±11,92), средний результат был увеличен, и на 12 месяце было отмечено сопоставимое (89,89 ± 12,02 против 87,58 ±7,60) улучшение между группами. Средняя продолжительность пребывания в стационаре составила 5,16 ±1,9 дня в первой группе и 4,59±2,6 дня во второй группе. Средняя продолжительность пребывания в больнице была одинаковой в обеих группах (p = 0,834). Послеоперационную боль оценивали по ВАШ через два часа и через 24 часа. Через два часа средний показатель по ВАШ составил 7,38 ± 1 в первой группе и 6,9 ± 1 во второй. Средний показатель по ВАШ через два часа был значительно ниже во второй группе (p = 0,031). Аналогичным образом, через 24 часа средний показатель по ВАШ был значительно ниже в группе второй (2,5 ± 0,8 против 2,9 ± 1 соответственно) (p = 0,010). За период наблюдения, составивший в среднем 37,1 месяца, группы не различались по частоте рецидивов. Предикторами ИОХВ были наличие в анамнезе сетчатой инфекции (ОШ 4,8, 95% ДИ [1,9–12,1]; р <0,001) и повторные операции (ОШ 2,4, 95 % ДИ [1,1–5,6]; р <0,05). Единственным предиктором рецидива было наличие ИОХВ (ОШ 3,1, 95 % ДИ [1,5–6,3]; р <0,01). Необходимо подчеркнуть, что более 87 % пациентов, шедших на операцию, отмечали болевые ощущения не только при ходьбе, но и особенно при физической нагрузке, что приводило к ограничению в физической активности.
В процессе анкетирования по EuraHSQoL через 12 месяцев после хирургического вмешательства у пациентов первой группы жалобы на болевые ощущения и функциональный дискомфорт почти отсутствовали, тогда как во второй группе были зарегистрированы статистически значимые ограничения физической активности, особенно связанные с занятиями спортом и тяжелым физическим трудом (р ≤ 0,05) (рис. 1).
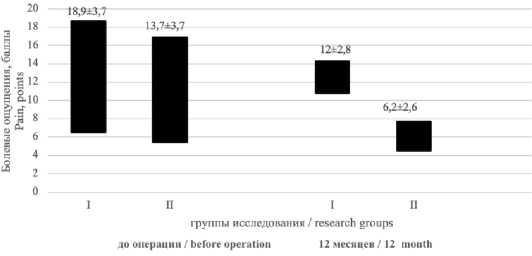
Рис.1. Болевые ощущения по EuraHSQoL в группах исследования до оперативного вмешательства и через 12 месяцев
Fig. 1 . Pain according to EuraHSQoL in the study groups before surgery and after 12 months
Через 12 месяцев после операции во второй группе (с применением ДАТ) отмечалось улучшение физической активности (р <0,05). Во второй группе зарегистрированы сравнительно худшие показатели, в то же время статистической разницы между группами не выявлено (рис. 2).
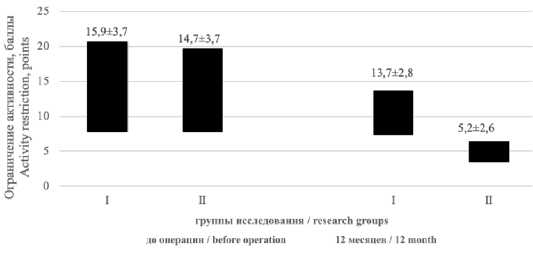
Рис. 2. Физическая активность по EuraHSQoL в группах исследования до оперативного вмешательства и через 12 месяцев
Fig. 2. EuraHSQoL physical activity in the study groups before surgery and after 12 months
Косметический дискомфорт спустя 12 месяцев сократился во всех группах (р ≥ 0,05) (рис. 3).
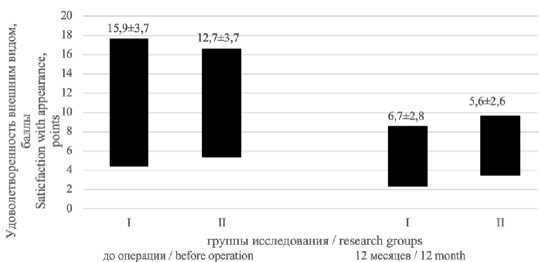
Рис. 3. Удовлетворенность внешним видом по EuraHSQoL в группах исследования до оперативного вмешательства и через 12 месяцев (р ≥ 0,05) Fig. 3. EuraHSQoL satisfaction with appearance in the study groups before and 12 months after surgery (p ≥ 0,05)
Отдаленные результаты лечения прослежены в сроки от 1 года до 10 лет (в среднем 5 лет ± 4 месяца) у 110 пациентов, повторно осмотрено 68 больных. Рецидив заболевания был выявлен в сроки от 6 месяцев до 1 года после операции у 2 пациентов из первой группы с осложненным течением послеоперационного периода (нагноение лапаротомной раны). Во второй группе зарегистрирован один рецидив спустя 2 года после операции.
Обсуждение
Первичная конечная точка этого исследования – меньше хирургических осложнений в раннем послеоперационном периоде – фиксировалась в группе пациентов, которым в качестве армирующего материала использовали деэпи-телизированную аутодерму. Особенно это касается сером и инфекционных осложнений со стороны раны. Одно из возможных объяснений этого заключается в том, что тяжесть осложнений может быть следствием не только хирургической травмы, качеством аллотрансплантата и его влиянием на ткани, в которые трансплантант имплантируется. Пациенты, которым была установлена сетка, испытывали больший дискомфорт и боль во время контрольного визита через 2 месяца и оценивали степень улучшения функции брюшной стенки по шкале ВАШ как более низкую. Этот дискомфорт ощущался в брюшной стенке и не был связан с какими-либо осложнениями в области хирургического вмешательства. Большинство сетчатых имплантатов были установлены по методике sublay, но у этих пациентов всё равно наблюдались симптомы дискомфорта, что подтверждается другими исследователями [12]. Использование дренажей, по-видимому, не предотвращало и не способствовало образованию сером. Это исследование не подтверждает такое мнение, поскольку частота дренирования в обеих группах была одинаковой (р <0,05). Кто-то может утверждать, что применяемый эндопротез стерилен, в отличие от собственной кожи пациента. Однако предлагаемые способы предимплантационной подготовки аутокожи не только не выявляют рост бактерий, но и подавляют его. Это мнение подтверждается исследованием некоторых авторов, которое проводилось с кожным трансплантатом, взятым непосредственно перед имплантацией [6]. Поскольку и синтетическая сетка, и аутотрансплантат кожи показали одинаковую эффективность, хотя в группах наблюдались некоторые различия в структуре осложнений, ожидаемого снижения нарушений заживления ран не произошло. Исходя из этого, аутокожа по-прежнему имеет потенциальные преимущества с точки зрения эластичности, меньшего количества инфекционных осложнений и очевидного экономического превосходства [11]. Ограничивающим фактором при использовании аутодермы в качестве пластического материала является наличие воспалительных заболеваний кожи [10]. У пациентов с гигантской вентральной грыжей обычно достаточно избыточной кожи, чтобы можно было иссечь кожный трансплантат достаточного размера. В заключение отметим, что аутотрансплантаты кожи являются надёжным материалом для укрепления брюшной стенки при лечении вентральных грыж. Они дают такие же результаты, вызывая меньше осложнений как в ранние сроки, так и в отдаленный период после вмешательства. Пациенты с ожирением, прооперированные с использованием кожного трансплантата, быстрее восстанавливаются после операции [6]. Использование аутодермы обходится дешевле, чем установка синтетической сетки. Кроме того, с гистологической и иммуногистохимической точек зрения кожный трансплантат предпочтительнее, поскольку он представляет собой имплантацию собственной ткани, хорошо в нее интегрируется, значительно снижает воспаление и стимулирует образование коллагена I. Эффективность использования аутокожи в отношении рецидива грыжи в долгосрочной перспективе еще предстоит определить в ходе дальнейшего наблюдения.
Заключение
Судя по результатам, герниопластика с использованием деэпителизированной аутодермы, подготовленной предимплантационно в оксигенированных препаратах, подходит для лечения послеоперационных вентральных грыж у пациентов с ожирением (ИМТ ≥ 25 кг/м2), сахарным диабетом, а также у пациентов из группы высокого риска. При соблюдении точной хирургической техники метод является безопасным, выполнимым и сопровождается меньшим количеством осложнений и рецидивов по сравнению с другими применяемыми и хорошо зарекомендовавшими себя методами. Для окончательной оценки этой операции в будущем необходимо провести дополнительные клинические испытания.


