Выбор растворителей для сольвотермального синтеза монокристаллов полициклических ароматических соединений
Автор: Жеребцов Дмитрий Анатольевич, Найферт Сергей Александрович, Полозов Максим Александрович, Живулин Дмитрий Евгеньевич, Живулин Владимир Евгеньевич, Мерзлов Сергей Владимирович, Авдин Вячеслав Викторович, Захаров Валерий Григорьевич, Кораблев Глеб Георгиевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 4 т.9, 2017 года.
Бесплатный доступ
Исследовано влияние температуры и типа растворителя на растворимость тяжелых полициклических ароматических соединений. Предложены перспективные пары растворитель - растворенное вещество. Определены растворители, непригодные для автоклавного метода выращивания кристаллов кубовых красителей.
Автоклав, монокристалл, ароматические полициклические соединения
Короткий адрес: https://sciup.org/147160404
IDR: 147160404 | УДК: 546.865+547.53.024+548.312.5 | DOI: 10.14529/chem170404
The choice of solvents for solvotermal synthesis of single-crystal polycyclic aromatic compounds
The effect of temperature and the solvent type on the solubility of heavy polycyclic aromatic compounds has been studied. Prospective solvent-solute pairs have been suggested. The solvents that are unsuitable for the autoclave method of growing crystals of vat dyes have been determined.
Текст научной статьи Выбор растворителей для сольвотермального синтеза монокристаллов полициклических ароматических соединений
Тяжелые полициклические ароматические соединения интересны для применения в составе жидких кристаллов, микропористых органических и металлоорганических структур, красителей, фотосенсибилизаторов солнечных элементов, органических полупроводников [1–3]. Крайне низкая растворимость тяжелых ароматических полициклических углеводородов в любых растворителях представляет собой экспериментальную сложность для получения их монокристаллов. Это объясняет крайне малое количество решенных кристаллических структур подобных соединений в кристаллографической базе данных CCSD. Получение монокристалла из раствора и решение структуры рентгеновскими методами позволит провести квантовохимические расчеты, описать электронную структуру и предсказать свойства такого соединения.
Экспериментальная часть
Для исследования возможности выращивания монокристаллов тяжелых полициклических ароматических соединений был применен автоклавный метод с использованием ряда раствори- телей. Для осуществления метода был разработан автоклав оригинальной конструкции (рис. 1).
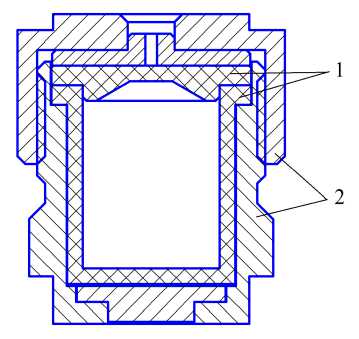
Рис. 1. Разрез автоклава: 1 – тефлоновый вкладыш, 2 – стальной корпус
В конструкции автоклава учтены наиболее удачные решения, доступные в открытых источниках. Корпус изготовлен из коррозионностойкой стали 12Х18Н10Т, вкладыш изготовлен из тетрафторэтилена. Рабочий объем автоклава составляет 40 мл. Расчётная прочность корпуса автоклава позволяет работать до температуры 200 °С при давлении до 150 атм. В верхней части автоклава предусмотрено отверстие, через которое осуществляется сброс избыточного газа при превышении расчётного давления, что предохраняет от разрыва стального корпуса. Уплотнение разъема автоклава осуществляется за счет применения сравнительно толстых крышки и заплечиков тефлонового вкладыша, которые имеют в 3 раза более высокий коэффициент расширения, чем сталь. Это приводит к автоуплотнению разъема при подъеме температуры .
В качестве растворителей были исследованы нафталин, 1,2-дихлорбензол (ОДХБ), 5,6-бензохинолин, 1-бромнафталин, изопропиловый, изоамиловый, н -бутиловый и этиловый спирты, трикрезилфосфат, динонилфталат, диметилсульфоксид (ДМСО), N,N-диметилформамид (ДМФА), толуол, моногидрат 4-толуолсульфокислоты, хинолин, γ-бутиролактон, бутилцелло-зольв, 1,4-диоксан, этилацетат. Кроме органических растворителей были исследованы концентрированные водные растворы NaOH, гидрохинона совместно с NaOH, растворы NaOH в бутиловом спирте, NaOH в изопропиловом спирте, водные растворы хлорида аммония, плавиковой кислоты, дитионита натрия (Na2S2O4) с NaOH. Большинство перечисленных веществ при комнатной температуре являются жидкостями, за исключением нафталина, 5,6-бензохинолина и 4-толуолсульфокислоты, имеющих температуры плавления соответственно 80, 90 и 103-106 °С. Растворители, способные растворять какой-либо краситель, были протестированы на большем числе красителей. Растворители, не растворявшие выбранный краситель, на других красителях не были протестированы.
В качестве труднорастворимых тяжелых полициклических ароматических соединений были использованы кубовые антроновые красители, имеющие в отечественной литературе названия: тиоиндиго ярко-розовый ЖД (1), кубовый ярко-зеленый СД (2), кубовый алый 2ЖД (3), кубовый бордо Д (4), кубовый ярко-оранжевый КХД (5), кубовый золотисто-желтый ЖХД (6), кубовый ярко-фиолетовый КД (7), кубовый оранжевый Д (8), кубовый ярко-голубой ЗД (9), кубовый бирюзовый 2ЗД (10). Основная примесь во всех красителях – до 15 масс. % Na 2 SO 4 , являющаяся побочным продуктом их производства. Структуры некоторых красителей приведены на рис. 2.
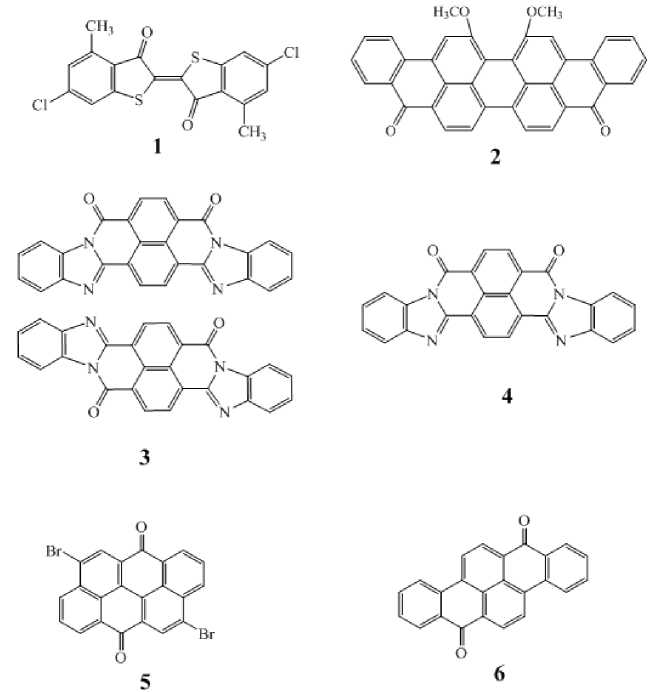
Рис. 2. Структуры некоторых использованных красителей
В автоклав помещалось 3 г красителя и 30 мл растворителя, что составляло около 80 % заполнения рабочего объёма. Типичный температурный режим проведения экспериментов состоял в нагреве до 200 °С в течение 5 ч, выдержке в течение 10 ч и охлаждении до 30 °С в течение 100 ч. Такой режим позволял получать насыщенный раствор, при охлаждении которого растворенное вещество вы- делялось в форме огранённых игольчатых кристаллов длиной от 0,001 до 1 мм, которые были исследованы с помощью оптического микроскопа Nikon 50, растрового электронного микроскопа Jeol JSM7001F с элементным анализатором Oxford INCA X-max 80, порошкового рентгеновского дифрактометра Rigaku Ultima IV. Это позволило идентифицировать сохранение состава и кристаллической структуры исходных веществ после кристаллизации, а также выяснить природу примесей. Количество и размер кристаллов позволили оценить перспективность того или иного растворителя для дальнейших экспериментов по выращиванию монокристаллов этих соединений. Растворимость оценивалась приближенно по наблюдаемому количеству перекристаллизованного вещества: к средней растворимости отнесены вещества, растворявшиеся в количестве 20–50 мг в 30 мл, к малой растворимости – в количестве 5–20 мг в 30 мл, к нерастворимым – менее 5 мг в 30 мл (визуально без признаков перекристаллизации). Ряд растворителей вступали в реакцию с растворенным веществом, что приводило к его частичному или полному разрушению. Сводная таблица растворимости кубовых красителей в автоклаве при 200 °С приведена в таблице. Растворители в таблице упорядочены сверху вниз, прежде всего по числу проведенных экспериментов и по их эффективности, а также по классам (спирты, ароматические соединения, водные растворы).
Растворимость кубовых красителей в автоклаве при 200 °С
|
Растворитель |
Краситель |
|||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
ОДХБ |
н |
– |
м |
– |
р* |
c* |
– |
н |
н |
м |
|
10 % Na 2 S 2 O 4 + + 10 % NaOH (водн) |
– |
н |
н |
н |
– |
– |
м |
с |
н |
м |
|
Нафталин |
– |
– |
– |
– |
м |
с |
– |
н |
н |
н |
|
н -Бутанол |
– |
н |
н |
– |
м |
– |
– |
– |
н |
– |
|
Изопропанол |
– |
– |
н |
– |
– |
– |
– |
– |
н |
м |
|
Изоамиловый спирт |
– |
– |
– |
– |
– |
– |
– |
н |
н |
н |
|
Этанол |
– |
– |
– |
– |
– |
– |
– |
– |
– |
н |
|
5,6-Бензохинолин |
– |
– |
– |
– |
– |
– |
н |
– |
н |
– |
|
1-Бромнафталин |
– |
– |
– |
– |
н |
– |
– |
– |
– |
н |
|
Толуол |
– |
н |
– |
– |
н |
– |
– |
– |
– |
– |
|
Хинолин |
– |
– |
н |
– |
– |
– |
– |
– |
– |
– |
|
4-Толуолсульфокислота |
– |
– |
– |
– |
– |
– |
– |
р |
– |
– |
|
ДМСО |
– |
р |
– |
– |
р |
– |
– |
– |
– |
– |
|
ДМФА |
– |
– |
– |
– |
– |
– |
р |
– |
н |
– |
|
40% HF |
– |
– |
– |
– |
– |
– |
– |
– |
– |
н |
|
20% NH 4 Cl (водн) |
– |
– |
м |
– |
– |
– |
– |
– |
н |
– |
|
20 % NaOH (водн) |
– |
– |
– |
– |
– |
– |
– |
с |
– |
– |
|
20 % NaOH (водн) + + 20 % ИПС |
– |
– |
– |
– |
– |
– |
– |
– |
н |
– |
|
20 % NaOH + Бутанол |
– |
– |
– |
– |
– |
– |
– |
– |
н |
– |
|
5 % Гидрохинон + +20 % NaOH |
н |
– |
– |
– |
– |
– |
– |
– |
– |
– |
|
Трикрезилфосфат |
– |
– |
– |
– |
– |
– |
– |
– |
– |
н |
|
Динонилфталат |
– |
– |
– |
– |
– |
– |
– |
– |
– |
м |
|
γ-Бутиролактон |
– |
– |
– |
– |
м |
– |
– |
– |
– |
– |
|
Бутилцеллозольв |
– |
– |
– |
– |
– |
– |
– |
– |
н |
– |
|
1,4-Диоксан |
– |
– |
– |
– |
м |
– |
– |
– |
– |
– |
|
Этилацетат |
– |
– |
– |
– |
н |
– |
– |
– |
– |
– |
|
Триэтиламин |
– |
– |
– |
– |
р |
– |
р |
– |
- |
– |
|
Малеиновый ангидрид |
– |
– |
– |
– |
н |
– |
– |
– |
р |
р |
Примечание . Обозначения: С – средне растворим, М – малорастворим, Н – нерастворим, Р – реагирует, * – 220 °С. Концентрация указана в массовых процентах.
Обсуждение результатов
Для анализа эффективности использования растворителей удобно упорядочить результаты по каждому из них:
-
1. Нафталин имеет определенный потенциал как растворитель. Красители 5, 6 были получены в виде игл размером до 0,2, 0,5 мм соответственно. Вместе с тем красители 8, 9 и 10 практически нерастворимы в нем при 200 °С. Относительно высокая температура плавления нафталина (80 °С) вносит неудобства при отделении его от кристаллов.
-
2. Бензохинолин, бромнафталин, толуол, хинолин, несмотря на близость по строению к кубовым красителям, не растворяют красители 2, 3, 5, 7, 8, 10 в заметных количествах.
-
3. ОДХБ позволил вырастить игольчатые кристаллы 3 и 10 размером до 0,1 и 0,8 мм соответственно. Вместе с тем красители 1, 8 и 9 практически не растворимы в ОДХБ при 200 °С. При 300 °С ОДХБ вступает с 5 в реакцию обмена, при которой бром частично (до 5 масс. %) обменивается на хлор, при этом параллельно протекают реакции разложения, приводящие к образованию нерастворимых углеродистых продуктов.
-
4. Бутиловый спирт позволил вырастить игольчатые кристаллы до 0,5 мм красителя 5, но красители 2, 3, 9 нерастворимы в бутиловом спирте. Другие спирты (изопропиловый, изоамиловый и этиловый) также не позволили вырастить кристаллы кубовых красителей 3, 8, 9, 10.
-
5. 1,4-диоксан и γ-бутиролактон позволили получить игольчатые кристаллы до 0,5 мм красителя 5.
-
6. Динонилфталат позволил получить мелкие кристаллы 10.
-
7. Раствор гидроксида натрия позволил получить прозрачные красные игольчатые кристаллы красителя 8.
-
8. Для 3 сравнительно успешным растворителем оказался насыщенный водный раствор хлорида аммония.
-
9. Плавиковая кислота показала себя как плохой растворитель 10.
-
10. Использование дитионита натрия со щелочью позволило получить мелкие кристаллы красителей 7, 8 и 10. Но для красителей 2, 3, 4 и 9 этого сделать не удалось.
-
11. Трикрезилфосфат и бутилцеллозольв позволили получить мелкие кристаллы красителей 10 и 9 соответственно.
-
12. Смеси растворов гидроксида натрия и изопропилового спирта, гидроксида натрия и бутилового спирта не позволили получить кристаллы красителя 9. Смесь гидрохинона и гидроксида натрия восстановила краситель 1 до фенолята, но не привела к росту кристаллов 1.
-
13. Диметилсульфоксид при 200 °С не является инертным растворителем по отношению к кубовым красителям. Краситель 2 претерпел преобразование, благодаря которому образовался растворимый продукт неизвестного состава. ДМСО при 200 °С реагирует с 5 с образованием углистого полимера и газов (вероятно, SO2 и HBr), которые разрушили тефлоновый вкладыш – выдавили его через выхлопное отверстие.
-
14. Диметилформамид при 200 °С реагирует с красителем 7 с образованием углистого полимера и газов. Для красителя 9 ДМФА является инертным растворителем, но вырастить его кристаллы не удалось.
-
15. Толуолсульфокислота не является инертным растворителем красителя 8 и при 200 °С реагирует с ним, разлагаясь на толуол и серную кислоту.
-
16. Триэтиламин прореагировал с 7 и 5 с образованием черной массы.
-
17. Малеиновый ангидрид прореагировал с образцом 10 с образованием чёрной пористой массы, которая вспучилась и выдавила выхлопное отверстие автоклава. Краситель 9 с МА дал чёрную пористую массу. Образец 5 с МА не реагировал, но растворения также не наблюдалось.
Выводы
Перспективными растворителями являются: 1) ОДХБ, 2) водный раствор 10 масс. % Na2S2O4+ + 10 масс. % NaOH, 3) бутанол, 4) концентрированные водные растворы NH 4 Cl или NaOH. Частично могут быть использованы динонилфталат, γ-бутиролактон, 1,4-диоксан. ДМСО, ДМФА, МА и толуолсульфокислота имеют мало перспектив в качестве растворителя, ввиду их реакций с исследуемыми веществами. Триэтиламин может представлять интерес как реагирующий растворитель, позволяющий получать растворимые производные красителей.
Список литературы Выбор растворителей для сольвотермального синтеза монокристаллов полициклических ароматических соединений
- Wu J. Chemistry of Functional π-Systems. Current Organic Chemistry, 2016, vol. 14, pp. 2016-2016 DOI: 10.2174/138527210793351625
- Guo J., Xu Y., Jin S., Chen L., Kaji T., Honsho Y., Addicoat M., Kim J., Saeki A., Ihee H., Seki S., Irle S., Hiramoto M., Gao J., Jiang D. Conjugated Organic Framework with Three-dimensionally Ordered Stable Structure and Delocalized π-Clouds. Nature Communications, 2013, vol. 4, pp. 1 -8 DOI: 10.1038/ncommc3736
- Chakraborty J.N. Fundamentals and Practices in Colouration of Textiles. Second Edition. Woodhead Publishing India Pvt. Ltd, 2014, P. 554.


