Выброс радиоактивных веществ в окружающую среду при тяжёлых авариях БН-1200М: радиологическая защита по международным стандартам
Автор: Иванов В.К., Меняйло А.Н., Пряхин Е.А., Чекин С.Ю., Соломатин В.М.
Рубрика: Научные статьи
Статья в выпуске: 1 т.35, 2026 года.
Бесплатный доступ
Рассматривается проблема радиологической защиты населения и персонала при возможных тяжёлых авариях реакторной установки БН1200М. Используется референтный уровень радиационно-обусловленного канцерогенного риска 103, соответствующий референтному уровню 20 мЗв для населения, рекомендованному Публикацией 146 МКРЗ в 2020 г. Применяется технология моделирования канцерогенного риска на основе поглощённых доз облучения в органах и тканях. Получены значения ожидаемых эффективных доз при достижении канцерогенного риска 103 для радионуклидов Cs, I и Na, дающих основной вклад в дозы облучения населения при запроектной аварии энергоблока с реакторной установкой БН1200М. Показано, что радиотоксичность изотопов 22Na и 24Na возрастает в 23 раза при их ингаляционном поступлении, по сравнению с пероральным поступлением, а радиотоксичность 131I в десятки раз меньше радиотоксичности радиоизотопов Na и Cs. При реализации принципа оптимизации радиологической защиты в ситуациях аварийного облучения необходимо принимать во внимание, что референтные уровни, установленные по показателю радиационного риска, в диапазоне от умеренного (103) до существенного (102), могут достигаться при существенно разных эффективных дозах, в зависимости от дозообразующего радионуклида, пути его поступления в организм человека, а также в зависимости от пола и возраста облучённых лиц.
Тяжёлая радиационная авария, реакторная установка БН-1200М, радионуклиды, Cs, I, Na, ожидаемая эффективная доза, поглощённая доза, референтный уровень дозы, референтный уровень риска, диспансеризация, охрана окружающей среды, здравоохранение
Короткий адрес: https://sciup.org/170211669
IDR: 170211669 | УДК: 621.039.586:539.163:539.1.074:504:05 | DOI: 10.21870/0131-3878-2026-35-1-5-17
Release of radioactive substances into the environment in severe accidents BN-1200M accidents: radiological protection according to international standards
The problem of radiological protection of the population and personnel in case of possible severe accidents of the BN-1200M reactor plant is considered. A reference level of radiation-induced car-cinogenic risk of 10-3 is used, corresponding to the reference level of 20 mSv for the population rec-ommended by ICRP Publication 146 in 2020. The technology of modeling carcinogenic risk based on absorbed radiation doses in organs and tissues is used. The values of the expected effective doses were obtained when the carcinogenic risk of 10-3 is reached for radionuclides Cs, I and Na, which make the main contribution to the radiation doses to the population in the event of a beyond design-basis accident of a power unit with a BN-1200M reactor plant. It has been shown that the radiotoxicity of the isotopes 22Na and 24Na increases by 2-3 times when they are inhaled, compared to oral intake, and the radiotoxicity of 131I is tens of times less than the radiotoxicity of radioisotopes Na and Cs. When implementing the principle of optimizing radiological protection in emergency ex-posure situations, it is necessary to consider that the reference levels, established in terms of radia-tion risk, ranging from moderate (10-3) to significant (10-2), can be achieved at significantly different effective doses, depending on the dose-forming radionuclide, the route of its entry into the human body, as well as depending on the sex and age of the exposed persons.
Текст научной статьи Выброс радиоактивных веществ в окружающую среду при тяжёлых авариях БН-1200М: радиологическая защита по международным стандартам
Как известно, тяжёлая авария или запроектная авария характеризуется нарушением работы АЭС, для которой в проектной документации не учтены причины её возникновения и этапы течения, но предусмотрены средства потенциальной защиты персонала, населения и окружающей среды.
В 2020 г. Международная комиссия по радиологической защите (МКРЗ) опубликовала документ № 146, который посвящён радиологической защите при тяжёлых авариях радиационной природы [1]. В этом документе внимательно изучены радиологические последствия аварий на Чернобыльской АЭС и на АЭС Фукусима-1, как на начальных стадиях аварий, так и долгосрочные последствия. Акцент в документе сделан на проблему оптимизации радиологической защиты при условии достижимости настолько низких уровней облучения, насколько это разумно, с учётом социально-экономических и экологических факторов (так называемый принцип оптимизации ALARA). Сделано
Иванов В.К. – науч. рук. НРЭР, гл. радиоэколог ПН «Прорыв», Председатель РНКРЗ, чл.-корр. РАН, д.т.н., проф.; Меняйло А.Н. – вед. науч. сотр., к.б.н.; Пряхин Е.А. – науч. сотр.; Чекин С.Ю.* – зав. лаб. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России. Соломатин В.М. – нач. отд. гл. радиоэколога, к.б.н. АО «Прорыв».
заключение принципиальной важности: дозовые нагрузки на население и персонал в ситуациях аварийного облучения не должны превышать 100 мЗв ожидаемой эффективной дозы (ОЭД), а для населения наиболее подходящий референтный уровень на ранней и промежуточной стадиях аварии, по возможности, может быть установлен на уровне 20 мЗв ([1], пар. 122). Чем было обосновано это заключение? Результатами долговременных исследований радиационных рисков в когортах лиц, переживших в 1945 г. атомные бомбардировки японских городов Хиросима и Нагасаки.
После атомных бомбардировок 1945 г. правительство Японии и США в 1954 г. создали регистр «хибакуси», т.е. лиц, переживших атомные бомбардировки (86,5 тыс. человек). Основной целью создания регистра была оценка частоты злокачественных новообразований (ЗНО) у облучённых контингентов. Регистр «хибакуси» существует до настоящего времени и является основой для получения радиационно-эпидемиологических зависимостей «доза-эффект», принятых на международном уровне [2]. В данном случае под эффектом действия ионизирующей радиации понимается повышение показателей частоты ЗНО (показателей онкозаболеваемости и онкосмертности).
В результате долгосрочных и крупномасштабных эпидемиологических исследований в Японии было установлено, что 7% выявленных смертей от солидных ЗНО обусловлены радиационным воздействием и 51% выявленных смертей от лейкозов также радиационно-обуслов-лены. Было также показано, что зависимость «доза-эффект» лучше всего описывается линейной беспороговой моделью. Вместе с тем, в дозовом интервале 0-100 мЗв имеет место очень высокая степень неопределённости в полученных рисковых коэффициентах.
Учитывая рекомендации Публикации 146 МКРЗ [1] по радиологической защите человека в ситуациях аварийного облучения (референтный уровень ОЭД в диапазоне 20-100 мЗв) и номинальные коэффициенты риска, приведённые в Публикации 103 МКРЗ [2] (около 5 х 10-2/Зв), соответствующий референтный уровень по показателю радиационного риска должен находиться в диапазоне 10-3-5 х 10-3.
Материалы и методы
Модели радиационного канцерогенеза
Под избыточным абсолютным риском (EAR) развития ЗНО или в случае смерти от ЗНО понимается приращение соответствующего фонового показателя риска А о после радиационного воздействия (1):
EAR = A-A0 . (1)
Кроме избыточного абсолютного риска в радиационной эпидемиологии применяется показатель избыточного относительного риска (ERR). Связь между этими двумя рисками представлена в (2):
EAR = ERR-A0 . (2)
В данной работе условимся рассматривать «однократное облучение» или «однократное поступление радионуклида» в организм как облучение или поступление радионуклида в организм в течение одного года.
Модели радиационных рисков, рекомендованные Публикацией 103 МКРЗ [2] для обоснования системы норм и правил радиационной защиты, основаны на исследованиях японской когорты лиц, переживших в 1945 г. атомные бомбардировки городов Хиросима и Нагасаки [3, 4]. Модель избыточного абсолютного риска (аддитивная модель) заболевания солидным ЗНО после однократного облучения представлена в формуле (3), а модель избыточного относительного риска после однократного облучения (мультипликативная модель) заболеваемости ЗНО – в формуле (4).
EAR M™p. (s,w = d • PEAR(s,c) ■ (^) "EARW ■ (1+2Ч^г) 0,1 ’ (Я - 30 ) , (3)
ERR^^s, c, g,a,d) = d^ P err (s, c) ■ (^f^ ) • (1 + ^ ERRr ) 0,1^ — 30 ) . (4)
Здесь s – пол; c – локализация опухоли; g – возраст при облучении; a – возраст, на который рассчитывается риск (возраст дожития); d – доза облучения; β EAR , ω EAR , γ EAR – параметры аддитивной модели; β ERR , ω ERR , γ ERR – параметры мультипликативной модели. Значения этих параметров представлены в табл. 1.
В моделях МКРЗ [2] минимальный латентный период (
T
LS
) для солидных ЗНО равен 10 годам, т.е. в течение 10 лет после облучения избыточные риски, рассчитанные как по мультипликативной, так и по аддитивной моделям, принимаются равными нулю. Другими словами:
ЕА'
МКРЗкр.
и
ERR0“
p3
K
p,
равны 0, если
a
Таблица 1
Параметры моделей риска заболеваемости для различных локализаций солидных ЗНО, модели Публикации 103 МКРЗ [2]
|
Локализация ЗНО |
Пол |
β ERR , Гр-1 |
γ ERR |
ω ERR |
β EAR , 10-4×Гр-1 |
γ EAR |
ω EAR |
|
Все солидные |
муж. жен. |
0,35 0,58 |
-17 |
-1,65 |
43,20 59,83 |
-24 |
2,22 |
|
Пищевод |
муж. жен. |
0,40 0,65 |
-17 |
-1,65 |
0,48 0,66 |
64 |
2,38 |
|
Желудок |
муж. жен. |
0,23 0,38 |
-17 |
-1,65 |
6,63 9,18 |
-24 |
2,38 |
|
Толстая кишка |
муж. жен. |
0,68 0,33 |
-17 |
-1,65 |
5,76 2,40 |
-24 |
2,38 |
|
Печень |
муж. жен. |
0,25 0,40 |
-17 |
-1,65 |
4,18 1,30 |
-24 |
2,38 |
|
Лёгкие |
муж. жен. |
0,29 1,36 |
+17 |
-1,65 |
6,47 8,97 |
1 |
4,25 |
|
Молочная железа |
жен. |
0,87 |
0 |
-2,26 |
10,9 |
-39 |
3,5* |
|
Яичник |
жен. |
0,32 |
-17 |
-1,65 |
1,47 |
-24 |
2,38 |
|
Мочевой пузырь |
муж. жен. |
0,67 1,10 |
-17 |
-1,65 |
2,00 2,77 |
-11 |
6,39 |
|
Щитовидная железа |
муж. жен. |
0,53 1,05 |
-56 |
0,00 |
0,69 2,33 |
-24 |
0,01 |
|
Другие ткани (солидные ЗНО) |
муж. жен. |
0,22 0,17 |
-34 |
-1,65 |
7,55 10,45 |
-24 |
2,38 |
Примечание: * – для ЗНО молочной железы ω EAR =1 при возрасте дожития больше 50 лет.
Согласно рекомендациям МКРЗ [2], для вычисления избыточного абсолютного риска заболеваемости солидными ЗНО в произвольной популяции (в популяции, для которой модели радиационного риска МКРЗ [2] не были идентифицированы по радиационно-эпидемиологическим данным) необходимо учитывать взвешивание мультипликативной и аддитивной моделей и связь (2) между избыточным относительным и абсолютным риском (5).
EAR™^ . (s, c, g, a, d) = p(c) ■ А 0 аб. (s, a, c) ■ ERR™™^ (s, c, g, a, d) +
+(1-p(c))^EARo™p{s,c,5,a,d) . (5)
Вычисление EAR заболеваемости лейкозами после однократного облучения красного костного мозга производится по формуле (6):
EAR ™*kKp. (.s,g,a,d) = p(s,g) ■ d ■ (1 + 0,79 ■ d) ■ exp\a(s,g) ■(a- g- 25)] . (6)
Здесь, так же как и в случае с риском для солидных типов ЗНО, s – пол; g – возраст при облучении; a – возраст, на который рассчитывается риск; d – доза однократного облучения в Гр; β и α – параметры модели избыточного абсолютно риска заболеваемости лейкозами. Их значения, зависящие от возраста на момент облучения, приведены в табл. 2.
Минимальный латентный период для заболеваемости лейкозами T LL равен 2 годам, и EAR ЛДHKо K р. (s,д,a,d) - 0 , если a < д + TLL .
Таблица 2 Параметры модели для вычисления избыточного абсолютного риска заболеваемости лейкозами после однократного облучения
|
Возраст при облучении |
β |
α |
||
|
мужчины |
женщины |
мужчины |
женщины |
|
|
0-19 лет |
3,3 |
6,6 |
-0,17 |
-0,07 |
|
20-39 лет |
4,8 |
9,7 |
-0,13 |
-0,03 |
|
> 40 лет |
13,1 |
26,4 |
-0,07 |
0,03 |
В итоге можно записать общее выражение (7) для вычисления избыточного абсолютного риска заболеваемости ЗНО различных локализаций после однократного облучения:
EAR однокр. (s, c, g,a, d)
(EAR 00H OKp . (s,c,g,a,d), для c — солидная локализация опухоли { EAR ЛеHKкр. (s, д, a, d), для c - лейкоз
, (7)
где c – одна из локализаций солидных ЗНО из табл. 1, или лейкоз.
Для вычисления радиационных рисков смертности МКРЗ рекомендует использовать риски заболеваемости ЗНО, умноженные на так называемую долю летальности. Доля летальности вычисляется следующим образом:
k(s, a, c) -
л ОГт:^
2 0 a6 ' (s,a,c)
■, А ( о'б (s, a, c) > 0 ,
где А™ ерт. - показатель смертности от ЗНО в год для заданного пола s , возраста а и локализации с ; А 0 аб. - показатель заболеваемости ЗНО в год для заданного пола s , возраста а и локализации с .
Таким образом, избыточный абсолютный риск смерти от ЗНО после однократного облучения вычисляется по формуле (9):
EAR O м H р Kр. (s,c,g,a,d) = k(s,a,c) ■ EAR 3оадHокр. (s,c,д, a, d) . (9)
Для вычисления прогноза радиационного риска используется так называемая функция здорового дожития (в случае вычислений рисков заболеваемости) или функция дожития (в случае вычисления рисков смертности).
Функция дожития S(s,e,a) характеризует вероятность для человека пола s и возраста е дожить до возраста a:
S(s,e,a) - exp [— S a— 1 ^ Общ смерт. (s,k)] , a> e .
При этом в возрасте e и ранее функция дожития по определению принимается равной единице, т.е. S(s,e,a) = 1 при a < e . Здесь Л общ CMepT. (s,k) - показатель общей фоновой смертности в год от всех причин для лиц пола s и в возрасте k .
S(s,e,a) может быть найдена при использовании формулы:
S(s , 0 , a) л Ч. л
S(s,e,a) - S^, a>e .
Эту формулу можно получить, исходя из теоремы Байеса.
Функция здорового дожития S’(s,c,e,a) характеризует вероятность для человека пола s и возраста e дожить до возраста a и не заболеть при этом ЗНО локализации c :
S'(s,c,e,a) = ехр[-Хк=е^о6Щ' смерт'^.Ю + ^S^c) - Л™^^^^ а> е.(12)
Так же как и S(s,e,a) , функция S'(s,c,e,a) = 1 при a< e . И, аналогично, S(s,e,a).
S ' (s,c,Q,a)
S (s,c,e,a') = s,, D ,, а> e.
S (s,c,V,eJ
Обозначим избыточный абсолютный риск с весом вероятности дожития (здорового дожития) как EARʹ . Тогда:
EAR^oKp. (s, c, g, a, d) = S' (s, c, e, a) ■ EARf^.(s, c,g,a,d)(14)
EAR^p.(s, c, g, a, d) = S(s, e, a) ■ EAR™^Kp.(s, c,g,a,d).(15)
Для вычисления избыточного абсолютного риска заболеваемости ЗНО или смертности от ЗНО с весом функции здорового дожития или функции дожития от многократного облучения требуется провести суммирование EARopHOKp по возрасту на момент облучения с соответствующей дозой облучения:
EAR’3a6-(s, c,a,g i ,...,gn,d i ,..., dn) = Z n=i EAR^^s, c, gt, a, dj , (16)
EAR’™epT(s,c,a,g i ,...,g n ,d i ,...,d n ) = ^lEART^s.c.g^^ (17)
Здесь n - количество облучений; gi,...,gn - возраст на момент облучения; di,...,dn -соответствующие дозы облучения, полученные органом или тканью с. В совокупности gi,...,gn, di,...,dn определяют дозовую историю облучения для данного органа или ткани.
Пожизненный радиационный риск применяют для расчёта риска возникновения ЗНО или риска смерти от ЗНО (в результате радиационного облучения) в течение всей жизни человека. Иными словами, это интегральный показатель риска, характеризующий радиационные послед- ствия в целом за период оставшейся жизни.
Пожизненный атрибутивный риск (LAR) характеризует число радиационно-индуцированных случаев заболеваний ЗНО или смертей от ЗНО, превышающих фоновое число, которые могут возникнуть в течение всей последующий жизни после облучения группы лиц, у которых оди- наковы модифицирующие риск-факторы (пол, возраст при облучении и др.).
Величина LAR вычисляется путём суммирования EAR с весом вероятности дожития (здорового дожития) по всем возможным возрастам дожития, начиная от текущего возраста (18), (19):
LAR3!>6-(s,c,e,g i ,...,g n ,d i ,...,dn) = ■ Т^ [EAR '3a6. (s,c,a,g i ,...,g n ,d i ,...,d n )] .
UUKEr
LARCMe?T(s, c, e,g i ,..., g n , d i ,..., d n ) = ^^ ■ Z^ [EAR ' CMepT . (s, c,a,g i ,...,g n ,d i ,..., d n )] .
Здесь DDREF – коэффициент эффективности дозы и мощности дозы, равный 2 для солидных типов опухолей и 1 - для лейкозов; EAR'336' - избыточный абсолютный риск заболеваемости ЗНО с весом вероятности здорового дожития от возраста е до a ; EAR'™epT' - избыточный абсолютный риск смертности от ЗНО с весом вероятности дожития от возраста e до a ; n – количество облучений; gi,...,gn- возраст на момент облучения; di,...,dn- соответствующие дозы облучения, полученные органом или тканью c ; e – текущий возраст человека, в котором он жив; a max – максимальный возраст дожития, равный 100 лет.
Согласно МКРЗ, DDREF – это «экспертно оценённый параметр, который объясняет обычно сниженную биологическую эффективность (на единицу дозы) радиационного воздействия низких доз и низких мощностей доз, если сравнивать её с эффективностью высоких доз и высоких мощностей доз» [2].
Различие в вычислении рисков для внешнего и внутреннего облучения заключается в том, что внешнее облучение по умолчанию распределяется на всё тело человека, поэтому в расчётах можно использовать значение эквивалентной дозы, применяя её в моделях риска для всех солидных ЗНО и лейкозов. Внутреннее облучение распределено неравномерно по телу человека. Для расчёта радиационных рисков от внутреннего облучения требуется учитывать эквивалентные дозы в отдельных органах и тканях. Если известна только ОЭД внутреннего облучения (и дозообразующие радионуклиды), значение ОЭД требуется перевести в набор эквивалентных доз в отдельных органах и тканях, используя для этого базу данных тканевых коэффициентов МКРЗ [5]. Если известна объёмная активность радионуклидов, она также переводится в набор эквивалентных доз по органам и тканям, с учётом возрастной зависимости годового объёма вдыхаемого человеком воздуха [6] в случае поступления радионуклидов ингаляционным путём.
Значения LAR для всех типов ЗНО в целом после внешнего облучения получают путём суммирования значений LAR для локализации «все солидные ЗНО» и «лейкозы». Этот подход является общим при расчёте рисков смертности и заболеваемости.
внешн. [L4K(s,c = все солидные^,#!д„,(1лdn)+l все зн°15,е,д1дп,а1dn) [ +LAg(s,c = лейкоз, е,д1дп,(dn) ]' (20)
Величина LAR для всех типов ЗНО в целом после внутреннего облучения определяется путём суммирования величин LAR по всем органам и тканям c из табл. 1, кроме локализации «все солидные ЗНО», плюс величина LAR для лейкозов.
LA^все 3H0 (s, е, д 1 , ■ ■ ■, д п , ( 1 , ■ ■ ■, ( п ) Е с^все солид. LA^(s, ^, е, д 1 , ■ ■ ■, д п , ( 1 , ■ ■ ■, ( п ) . (21)
Дозовая история д1,■ ■ ■,дп, d1,■■■,dn определяется, исходя из ОЭД внутреннего облучения или объёмной активности [5].
В Публикации 103 МКРЗ [2] подчёркивается: «дозы в органах и тканях, а не эффективные дозы, требуются для оценки вероятности индукции ЗНО у облучённых индивидуумов». Более подробно технология МКРЗ по оценке канцерогенных рисков на основе органных доз была описана ранее [6-8].
Тяжёлые аварии БН-1200М: радиологическая защита
В материалах Рабочей группы АО «Прорыв» отмечается, что основной вклад в дозы облучения при запроектных авариях на энергоблоке с реакторной установкой БН-1200М вносят летучие радиоактивные продукты, содержащие радиоизотопы Cs, I и Na, попадающие в окружающую среду через систему технической вентиляции.
На рис. 1-5 показаны распределения эквивалентных доз по органам и тканям, соответствующим локализациям ЗНО из табл. 1 и лейкозам (при облучении красного костного мозга), для радиоизотопов Na, I и Cs с ОЭД 1 мЗв при их поступлении в организм человека с водой и пищей, а также с воздухом. Приведены также значения пожизненного обусловленного канцерогенного риска (LAR) для мужчин и женщин.
Как видно из рис. 1-5, максимальное значение LAR при дозе в 1 мЗв достигается для 24Na, который имеет период полураспада 15 ч. Минимальное значение LAR при дозе 1 мЗв достигается для изотопа 1311 (мужчины - 1,31 x 10 —6 , женщины - 4,92 x 10 —6 ). Это связано с тем, что эквивалентная доза по данному изотопу полностью сконцентрирована в щитовидной железе, канцерогенный риск которой ограничен низкой спонтанной заболеваемостью.
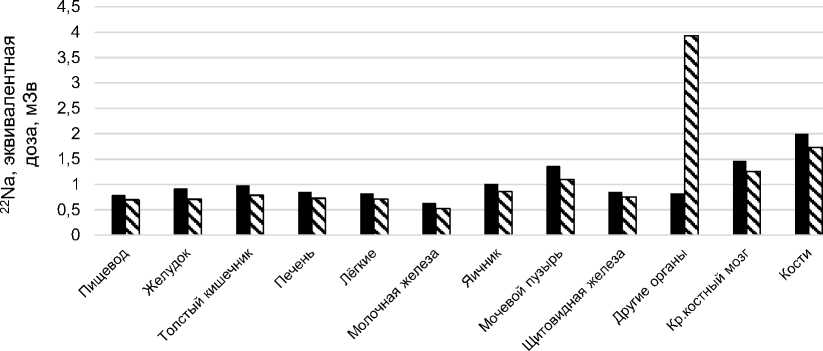
Поступление с пищей Поступление с воздухом
Рис. 1. Эквивалентная доза по органам и тканям от внутреннего облучения изотопами 22Na с ОЭД 1 мЗв (LAR: мужчины - 2,48 x 10 —5 , женщины - 2,99 x 10 —5 ).
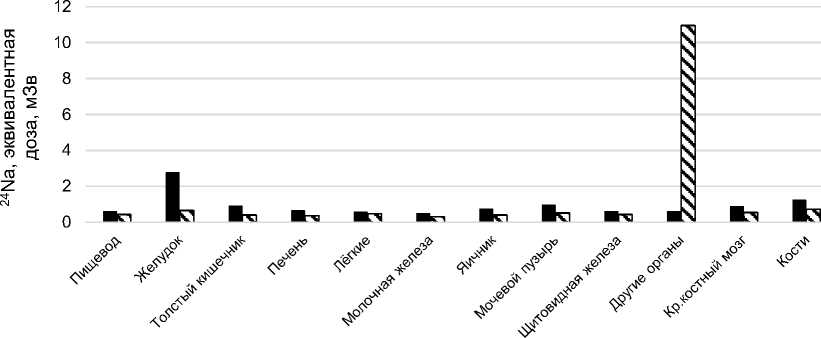
Поступление с пищей Поступление с воздухом
Рис. 2. Эквивалентная доза по органам и тканям от внутреннего облучения изотопами 24Na с ОЭД 1 мЗв (LAR: мужчины - 2,51 x 10 —5 , женщины - 3,26 x 10 —5 ).
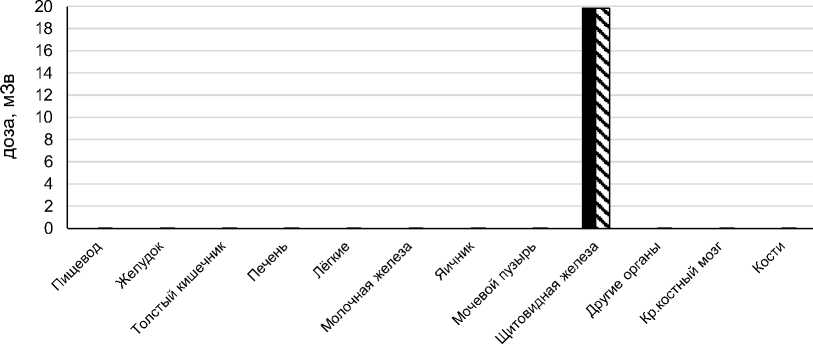
Поступление с пищей Поступление с воздухом
Рис. 3. Эквивалентная доза по органам и тканям от внутреннего облучения изотопами 131I с ОЭД 1 мЗв (LAR: мужчины - 1,31 x 10-6, женщины - 4,92 x 10-6).
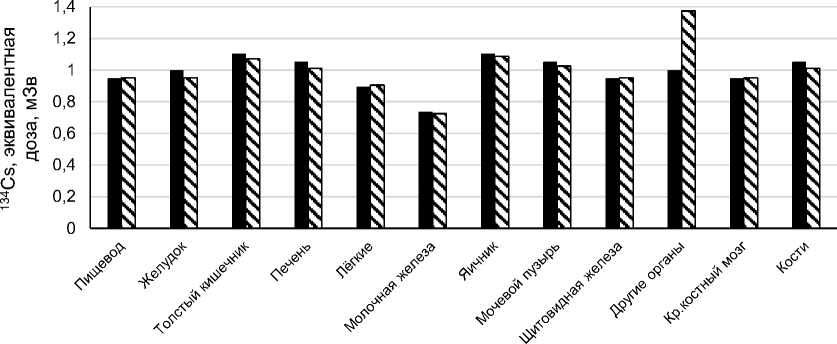
Поступление с пищей
Поступление с воздухом
Рис. 4. Эквивалентная доза по органам и тканям от внутреннего облучения изотопами 134Cs с ОЭД 1 мЗв (LAR: мужчины - 2,50 х 10-5, женщины - 3,11 х 10-5).
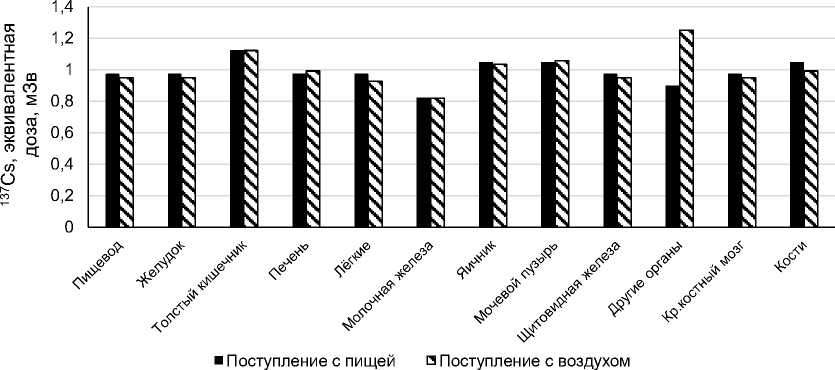
Рис. 5. Эквивалентная доза по органам и тканям от внутреннего облучения изотопами 137Cs с ОЭД 1 мЗв (LAR: мужчины - 2,50 х 10-5, женщины - 3,18 х 10-5).
Результаты и обсуждение
В табл. 3 для разных половозрастных групп приведены значения ОЭД при поступлении радионуклидов в организм человека с пищей и водой, при которых риск радиационно-обусловленного канцерогенеза достигает значения LAR=10-3. Для достижения уровня LAR=10-3 при поступлении радионуклидов с воздухом оценки ОЭД приведены в табл. 4. Для достижения такого риска максимальные значения ОЭД соответствуют радиоизотопу 131I, независимо от путей его поступления в организм человека.
Следует обратить внимание на то, что для радиоизотопов 22Na и 24Na ОЭД, соответствующие уровню риска 10-3, при ингаляционном поступлении в 2-3 раза меньше, чем при пероральном поступлении.
Согласно п. 3.2.3 НРБ-99/2009 [9], «облучение эффективной дозой свыше 200 мЗв в течение года должно рассматриваться как потенциально опасное. Лица, подвергшиеся такому облучению, должны немедленно выводиться из зоны облучения и направляться на медицинское обследование». С учётом номинального коэффициента риска около 5х10-2/Зв [2, 9], эффективной дозе 200 мЗв соответствует радиационный риск порядка 10-2, который следует принять в качестве верхнего референтного уровня риска при тяжёлых радиационных авариях. Тогда из табл. 3 следует, что для мужчин в возрасте 50 лет внутреннее облучение от 131I с ОЭД<21,1 Зв, при его поступлении с пищей и водой, лежит ниже верхнего референтного уровня 10-2, и для облучённых таким образом лиц не требуется дополнительного медицинского обследования. С другой стороны, медицинское обследование требуется для мужчин в возрасте 20 лет после внутреннего облучения 24Na, при его поступлении с воздухом, с ОЭД всего лишь 81,8 мЗв (табл. 4).
Таблица 3
Значение ОЭД (мЗв) внутреннего облучения от радионуклидов Na, I и Cs, при которых пожизненный атрибутивный риск (LAR) смертности от ЗНО равен 10-3, при поступлении радионуклидов в организм человека с пищей и водой
|
Радионуклид |
Мужчины, 20 лет |
Женщины, 20 лет |
Мужчины, 50 лет |
Женщины, 50 лет |
Мужчины, 18-64 года |
Женщины, 18-64 года |
|
22Na |
28,35 |
22,05 |
45,61 |
38,35 |
39,88 |
33,21 |
|
24Na |
26,21 |
18,86 |
48,3 |
37,62 |
39,61 |
30,61 |
|
131I |
246,59 |
56,83 |
2110,5 |
606,05 |
761,79 |
203,2 |
|
134Cs |
27,64 |
20,86 |
46,54 |
37,86 |
39,76 |
32,11 |
|
137Cs |
27,68 |
20,26 |
46,63 |
37,18 |
39,82 |
31,4 |
Таблица 4
Значение ОЭД (мЗв) внутреннего облучения от радионуклидов Na, I и Cs, при которых пожизненный атрибутивный риск (LAR) смертности от ЗНО равен 10-3, при поступлении радионуклидов в организм человека с воздухом
|
Радионуклид |
Мужчины, 20 лет |
Женщины, 20 лет |
Мужчины, 50 лет |
Женщины, 50 лет |
Мужчины, 18-64 года |
Женщины, 18-64 года |
|
22Na |
16,07 |
14 |
35,46 |
29,95 |
26,88 |
23,74 |
|
24Na |
8,18 |
7,44 |
23,86 |
19,63 |
15,6 |
14,05 |
|
131 |
240,79 |
56,29 |
1546,67 |
518,12 |
685,29 |
193,42 |
|
134Cs |
24,87 |
19,32 |
44,57 |
36,38 |
37,08 |
30,4 |
|
137Cs |
25,72 |
19,24 |
45,22 |
36,16 |
37,93 |
30,24 |
35%
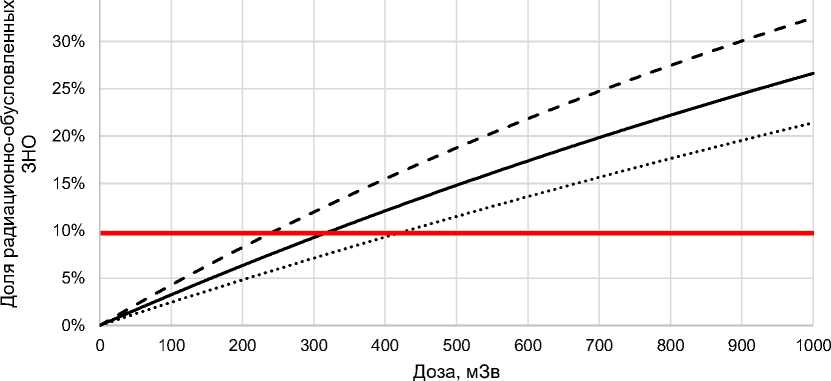
Мужчины Женщины Оба пола
Рис. 6. Доля радиационно-обусловленных ЗНО для возраста при облучении 20 лет.
В рамках международной шкалы канцерогенного риска [10] величина риска менее 10-3 относится к приемлемому для профессиональных групп уровню, не требующего специальной медицинской помощи. С другой стороны, опыт преодоления последствий тяжёлых радиационных аварий показал [11, 12], что если ежегодная доля потенциальных радиационно-обусловленных ЗНО превышает 10% (что примерно соответствует радиологическому риску 5 х 10 -3 -10-2 для всех ЗНО в совокупности), то необходима диспансеризация облучённых контингентов. Как видно из рис. 6, при внешнем облучении всего тела лиц в возрасте 20 лет, доля радиационно-обусловленных ЗНО может превысить 10% при дозах облучения для женщин более 250 мЗв, а для мужчин – более 400 мЗв.
Выводы
-
1. В Публикации 146 МКРЗ (2020 г.), на основе обзора долгосрочных эпидемиологических исследований последствий облучения населения японских городов Хиросима и Нагасаки в 1945 г., показано, что канцерогенный риск от радиационного воздействия при тяжёлых авариях не должен превышать значение 10-3, т.е. должен относиться к диапазону низкого радиологического риска по международной шкале.
-
2. В данной работе изложен метод оценки риска радиационно-обусловленного канцерогенеза (радиологического риска), в соответствии с рекомендациями МКРЗ [2], на основе доз облучения в органах и тканях, а не на основе эффективной дозы.
-
3. На основе этого метода показано, что одной и той же величине радиационного риска могут соответствовать ОЭД, различающиеся в десятки раз, в зависимости от дозообразующего радионуклида, пути его поступления в организм человека, а также в зависимости от пола и возраста облучённых лиц.
-
4. В частности, показано, что радиотоксичность изотопов 22Na и 24Na, определяемая по величине радиационного риска на единицу ОЭД, при их поступлении в организм человека с воздухом в 2-3 раза превышает их радиотоксичность при поступлении с пищей и водой, а радиотоксичность 131I в десятки раз меньше радиотоксичности радиоизотопов Na и Cs.
-
5. Для ситуации запроектной аварии на реакторной установке БН-1200М получены значения ОЭД при достижении умеренного референтного уровня риска 10-3 за счёт внутреннего облучения от радиоизотопов Na, I и Cs (табл. 3 и 4), дающих в этой ситуации основной вклад в дозы облучения персонала и населения.
-
6. При ОЭД, превышающих в 10 раз референтные уровни из табл. 3 или 4, а также при дозах внешнего облучения более 250 мЗв, требуется медицинское обследование (специализированная диспансеризация) облучённых лиц.
-
7. Таким образом, при реализации принципа оптимизации радиологической защиты в ситуациях аварийного облучения [2] необходимо принимать во внимание, что референтные уровни, установленные по показателю радиационного риска, в диапазоне от умеренного (10-3) до существенного (10-2), могут достигаться при существенно разных эффективных дозах, в зависимости от дозообразующего радионуклида, пути его поступления в организм человека, а также в зависимости от пола и возраста облучённых лиц.
Публикация подготовлена по результатам выполнения работ в Госкорпорации «Росатом» в рамках ПН «Прорыв.


