Высокоинтенсивная фокусированная ультразвуковая абляция в лечении гормонорезистентного локализованного и местнораспространенного рака предстательной железы
Автор: Шаплыгин Л.В., Соловов В.А., Воздвиженский М.О., Фесенко Д.В., Копылов А.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 2 (50), 2012 года.
Бесплатный доступ
Проведена оценка эффективности HIFU-терапии у 341 пациента с гормонорезистентным раком предстательной железы. Медиана гормонотерапии до возникновения гормонорезистентности составила 20 (3-48) мес. Пациенты были разделены на 2 группы в соот- ветствии с распространенностью и риском прогрессии. Трансуретральная резекция (ТУР) одновременно с процедурой HIFU была выполнена 238 пациентам, 69 - ТУР была выполнена за месяц до HIFU-терапии в связи с большим объемом простаты, 34 пациентам проведена только ультразвуковая абляция. Процедура HIFU выполнялась на роботизированной системе Ablatherm® (EDAP, Лион, Франция). Среднее время наблюдения после ультразвуковой абляции составило 36 (3-52) мес. Через 12 мес наблюдения в группе с низким риском прогрессии средней уровень ПСА - 0,04 нг/мл; в группе с высоким риском прогрессии - 0,05 нг/мл. Через 36 мес после HIFU в группе с низким риском прогрессии средний уровень ПСА составил 0,2 нг/мл; в группе с высоким риском прогрессии - 1,18 нг/мл. При анализе безрецидивной выживаемости по Каплан-Мееру у больных, которым проводилась HIFU- терапия, установлено, что она составила 95,5 % в группе с низким риском прогрессии (локализованный РПЖ) и 80 % в группе с высоким риском прогрессии (местнораспространенный РПЖ).
Гормонорезистентный рак предстательной железы, hifu-терапия, hifu-therapyтерапия
Короткий адрес: https://sciup.org/14056197
IDR: 14056197
High-intensity focused ultrasound ablation for the treatment of hormone-resistant localized and locally-advanced prostate cancer
Effectiveness of high-intensity focused ultrasound (HIFU) treatment was assessed for 341 patients with hormone-resistant prostate cancer. The median time before hormone-resistance was 20 (3-48) months. The patients were divided into 2 groups with respect to risk of progression. Two hundred thirty eight patients underwent transurethral resection of the prostate (TURP) in combination with HIFU, 69 patients underwent TURP one month before HIFU treatment due to the large prostate volume, and 34 patients received only ultrasound ablation. The HIFU procedure was carried out using the Ablatherm® HIFU device (EDAP, France). The median follow-up time after ultrasound ablation was 36 (3-52) months. The median PSA level 12 months after HIFU treatment was 0,04 ng∕ml in patients with localised PC, and 0,05 ng∕ml in patients with locally advanced disease. The medial PSA levels 36 months after HIFU treatment were 0,2 ng∕ml and 1,18 ng∕ml in patients with low and high risks of cancer progression, respectively. The Kaplan Meir analysis showed that the recurrence-free survival rate after HIFU therapy was 95,5 % in the group of patients with low risk of cancer progression (localized prostate cancer) and 80 % in the group of patients with high progression risk (locally-advanced prostate cancer).
Текст научной статьи Высокоинтенсивная фокусированная ультразвуковая абляция в лечении гормонорезистентного локализованного и местнораспространенного рака предстательной железы
Цель исследования – оценить клиническую эффективность HIFU терапии при лечении гормонорезистентного рака предстательной железы.
Материал и методы
Исследование было одобрено этическим комитетом ГУЗ СОКОД. От всех больных было получено информированное согласие на проведение исследования. С сентября 2007 г. по декабрь 2011 г. в Самарском областном клиническом онкологическом диспансере 341 пациенту с ГРРПЖ провели HIFU-терапию. Критерии включения в исследование: пациенты, не являющиеся кандидатами для
РПЭ и ДЛТ с локализованным и местнораспространенным ГРРПЖ. Медиана гормонотерапии до возникновения гормонорезистентности составила 20 (3–48) мес. Трехкратный рост ПСА на фоне проводимого лечения трактовался как развитие ГРРПЖ в соответствии с критериями ASTRO [4]. Критерии исключения из исследования: пациенты с метастатическим РПЖ, прорастание опухоли в прямую кишку или отсутствие прямой кишки.
Пациенты были разделены на 2 группы в соответствии с распространенностью и риском прогрессии:
– локализованный ГРРПЖ, низкий риск – 237 больных, Глисон ≤ 7, стадия T1–2N0M0, возраст – 69 (60–89) лет, ПСА перед HIFU – 40,0 (5,8–92,9) нг/мл, среднее значение объема простаты – 39,3 (28–92) см3;
– местнораспространенный ГРРПЖ, с высоким риском развития прогрессии – 104 пациента, Глисон ≤ 9, стадия T2–3N0M0, возраст – 72 (52–83) года, ПСА перед HIFU – 30,3 (20,1–60) нг/мл, среднее значение объема простаты – 41,2 (25–198) см3.
Лечение проводили под спинальной или эпидуральной анестезией. Процедура HIFU выполнялась на роботизированной системе Ablatherm® (EDAP, Лион, Франция). Среднее время наблюдения после ультразвуковой абляции – 36 (3–52) мес. После лечения определяли уровень ПСА каждые 3 мес, проводили МРТ и биопсию простаты в случае роста ПСА.
Результаты и обсуждение
Одновременно с процедурой HIFU трансуретральная резекция (ТУР) была выполнена 238 пациентам; 69 – ТУР была выполнена за 1 мес до HIFU терапии в связи с большим объемом простаты, 34 больным выполнена только ультразвуковая абляция. Средний объем резецированной ткани простаты во время ТУР составил – 30 (5–80) см3. Ультразвуковая абляция продолжалась 120 (60–245) мин. Среднее время госпитализации – 7 (2–19) дней. У пациентов, которым выполнялись ТУР + HIFU, уретральный катетер удаляли через 7 (3–21) дней. У пациентов, которым выполняли только процедуру HIFU, катетер удаляли через 14 (10–28) дней.
Через 12 мес наблюдения в группе с низким риском прогрессии медиана уровня ПСА составила 0,04 нг/мл; в группе с высоким риском прогрессии – 0,05 нг/мл. Через 36 мес после HIFU в группе с
Л.В. ШАПЛЫГИН, В.А. СОЛОВОВ, М.О. ВОЗДВИЖЕНСКИЙ И ДР.
Динамика уровня ПСА после HIFU-терапии
Таблица
В течение первых месяцев после процедуры отмечались следующие побочные эффекты: недержание мочи I ст. – 18 (5,3 %) пациентов, недержание мочи II ст. – 32 (9,4 %) пациента. Недержание купировалось у всех пациентов в течение 3–6 мес на фоне проводимой консервативной терапии. У 33 (9,7 %) пациентов в течение первых 12 мес после операции возникла стриктура простатического отдела уретры, что потребовало проведения ТУР. У 2 (0,6 %) пациентов в течение 1 мес после лечения развился ректоуретральный свищ, который потребовал наложения эпицистостомы и колостомы. Свищи закрылись самостоятельно в течение 6–12 мес.
Через 6 мес после лечения средний объем простаты составил 9,3 (2–18) см3. Объем был статистически значимо уменьшен по сравнению с начальным объемом (p<0,01). У 70 % пациентов отмечалось улучшение качества жизни по шкале
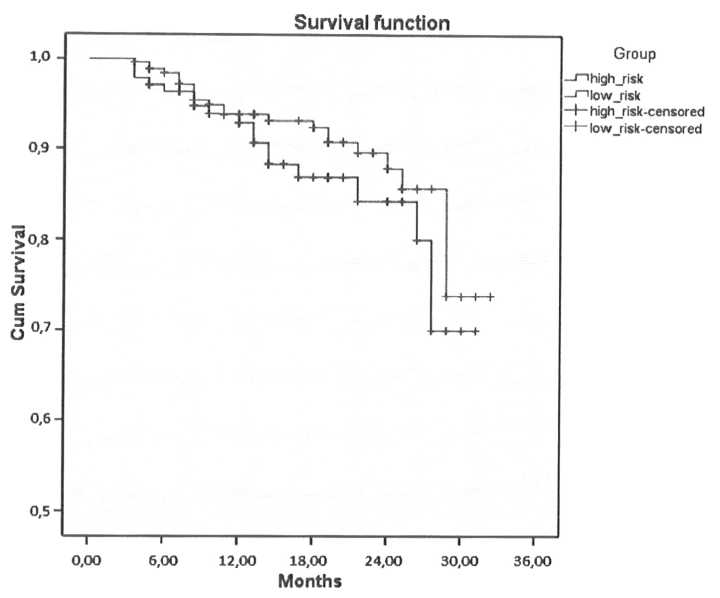
Рис. 1. Анализ безрецидивной выживаемости по Каплан-Майеру в соответствии с риском прогрессии в группах после HIFU
IPSS, у 30 % осталось без изменений. Одним из значимых преимуществ HIFU-терапии является возможность повторить лечение в случае продолженного роста опухоли или местного рецидива. Повторная HIFU-терапия была проведена 7 (2 %) пациентам при возникновении местного рецидива.
Таким образом, наши наблюдения показали, что HIFU-терапия была успешна у 90,9 % пролеченных пациентов. Был проведен анализ безрецидивной выживаемости по Каплан-Мееру, который показал 95,5 % эффективность HIFU-терапии в группе с низким риском прогрессии (локализованный РПЖ) и 80 % в группе с высоким риском прогрессии (местнораспространенный РПЖ) (рис. 1).
В России локализованный РПЖ, когда возможно радикальное лечение, выявляется только в 36,6 % [1]. При этом у больных I–II стадии после проведения радикальной простатэктомии или лучевой терапии в 25–50 % случаев развивается рецидив РПЖ [6]. Поэтому пациентам, не подходящим для хирургического или лучевого лечения, и с рецидивом РПЖ назначается гормональная абляция: билатеральная орхиэктомия или максимальная андрогеновая блокада. В настоящее время ни один из существующих антиандрогенных препаратов не превзошел результаты хирургической кастрации; показатели безрецидивной и общей выживаемости больных РПЖ остаются неизменными в течение нескольких десятилетий (12–24 и 24–36 мес соответственно) [8]. После начала гормонального лечения через 12–16 мес у 80–85 % пациентов развивается ГРРПЖ. Гормональная терапия второй и третьей линий, химиотерапия эффективна в 15–20 % случаев и не приводит к значительному увеличению продолжительности жизни пациентов, обладая при этом существенными побочными эффектами [10, 12, 13].
Тактика и стратегия ведения пациентов с ГРРПЖ не разработана, не существует клинически обоснованных рекомендаций. Публикации о фокальной терапии данной категории больных малочисленны,
СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2012. № 2 (50)
основаны на малом клиническом материале и имеют непродолжительный период наблюдений. На сегодняшний день опубликованы долгосрочные [5] и среднесрочные результаты [7, 14] HIFU-терапии РПЖ. По данным европейского многоцентрового исследования, включавшего 559 пациентов с РПЖ группы низкого и умеренного риска, S. Thuroff et al. [14] сообщили об отрицательном результате биопсии после HIFU-терапии у 87,2 % из 288 пациентов с периодом наблюдения не менее 6 мес. A. Blana et al. оценили результаты HIFU у 146 пациентов со средним периодом наблюдения 22,5 мес [5]. Средний дооперационный уровень ПСА составил 7,6 нг/мл, в то время как средний уровень ПСА через 3 мес после терапии составил 0,07 нг/мл. У 93,4 % из 137 больных, доступных для наблюдения, не обнаружено опухоли при биопсии зоны воздействия. В другом исследовании HIFU проводили 517 пациентам с локализированным или местнораспространенным РПЖ [15]. При медиане наблюдения 5 лет безрецидивная выживаемость составила 72 % для всех пациентов (р<0,0001). В среднем безрецидивная выживаемость, по данным зарубежных авторов, составляет от 66 до 84 % при сроке наблюдения от 5 до 14 лет.
В данном исследовании мы предприняли попытку оценить возможности HIFU-терапии у пациентов ГРРПЖ. Полученные нами данные свидетельствуют о том, что HIFU-терапия ГРРПЖ клинически эффективна. Результаты лечения показали, что при 3-летнем наблюдении HIFU-терапия была в целом успешна у 90,9 % пациентов. Анализ безрецидивной выживаемости по Каплан-Мееру показал 95,5 % эффективность HIFU-терапии в группе с низким риском прогрессии (локализованный РПЖ) и 80 % в группе с высоким риском прогрессии (местнораспространенный РПЖ) При этом отмечались умеренные краткосрочные побочные эффекты, у большинства пациентов улучшилось качество жизни. Тем не менее наши исследования остаются незавершенными, очевидно, что требуются более длительные наблюдения для оценки эффективности HIFU-терапии у пациентов с ГРРПЖ.


