Взаимодействие Гексахлороплатиноводородной кислоты с 2,2'-бипиридином и 1,2,3,4-тетрагидроакридин-9-карбоновой кислотой
Автор: Шарутина О.К., Беляев И.Е., Шевченко Д.П., Шарутин В.В., Доценко В.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Неорганическая химия
Статья в выпуске: 1 т.17, 2025 года.
Бесплатный доступ
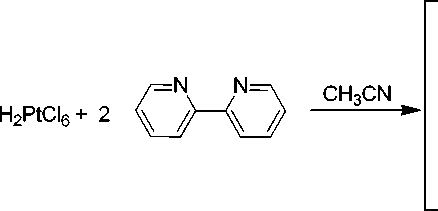
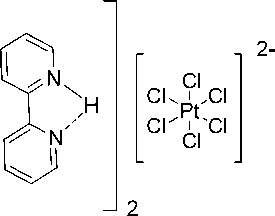
Продуктом реакции гексахлороплатиноводородной кислоты с 2,2¢-бипиридином в смеси вода-ацетонитрил при комнатной температуре является гексахлороплатинат(IV) 2,2`-бипиридиния [C10N2H8∙H]+2[PtCl6]2- (I). В тех же условиях гексахлороплатиноводородная кислота протонирует 1,2,3,4-тетрагидроакридин-9-карбоновую кислоту по атому азота с образованием кристаллогидрата [C28N2О4H30∙H]+2[PtCl6]2-×2Н2О (II). Новые комплексы с гексахлороплатинат-анионами охарактеризованы методом рентгеноструктурного анализа, проведенного на монокристальном дифрактометре D8 Quest фирмы Bruker (MoKα-излучение, λ = 0,71073 Å, графитовый монохроматор) при 293(2)К. Центросимметричные анионы [PtCl6]2- в комплексах I и II по геометрическим характеристикам мало отличаются друг от друга (связи Pt-Cl 2,3211(9)-2,3340(8) Å, углы ClPtCl 89,71(3)°-90,31(3)°). Катионом I является протонированная по одному из атомов азота молекула 2,2¢-бипиридина со слабой внутримолекулярной водородной связью N-H×××N (2,20 Å). В комплексе II катион представляет собой протонированную по атому азота гетероцикла 1,2,3,4-тетрагидро-акридин-9-карбоновую кислоту. В кристалле I наблюдаются короткие контакты, которые обусловлены слабыми межмолекулярными связями типа N-H×××Cl (2,69 Å) и C-H×××Cl (2,85-2,94 Å), при этом каждый анион имеет в ближнем окружении восемь катионов, а каждый катион - четыре аниона. В кристалле II можно выделить структурные единицы в виде цепочек, в которых анион образует водородные связи О-Н×××Cl (2,34 Å) через карбоксильные группы с двумя катионами, связанными с молекулами воды через протонированный атом азота N-H×××O (1,91 Å). Между собой цепочки связаны более слабыми взаимодействиями, среди которых можно выделить водородные связи О-Н×××Cl (2,54 и 2,77 Å) между молекулами воды и анионами.
Гексахлороплатиноводородная кислота, 2, 2'-бипиридин, 1, 2, 3, 4-тетрагидроакридин-9-карбоновая кислота, протонирование, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147248049
IDR: 147248049 | УДК: 546.17/.19+546.924+547.821.2+547.835.2+547.835.8+548.312 | DOI: 10.14529/chem250109
Interaction of hexachloroplatinum hydrocacid with 2,2'-bipyridine and 1,2,3,4-tetrahydroacridine-9-carboxylic acid: structure of reaction products
The product of the reaction of hexachloroplatinic acid with 2,2'-bipyridine in a water-acetonitrile mixture at room temperature is 2,2'-bipyridinium hexachloroplatinate(IV) [C10N2H8∙H]+2[PtCl6]2- (I). Under the same conditions, hexachloroplatinic acid protonates 1,2,3,4-tetrahydroacridine-9-carboxylic aсid at the nitrogen atom to form the dihydrate [C28N2О4H30∙H]+2[PtCl6]2-×2Н2О (II). New complexes with hexachloroplatinate anions were characterized by X-ray diffraction analysis at 293(2) K (Bruker D8 Quest, MoKα radiation, λ = 0.71073 Å, graphite monochromator). Centrosymmetric [PtCl6]2- anions in complexes I and II have similar geometric characteristics (the Pt-Cl bonds are 2.3211(9)-2.3340(8) Å, the ClPtCl angles are 89.71(3)°-90.31(3)°). Cation I is 2,2'-bipyridine molecule protonated at one of the nitrogen atoms with a weak intramolecular hydrogen bond N-H×××N (2.20 Å). In complex II, the cation is 1,2,3,4-tetrahydroacridine-9-carboxylic acid protonated at the nitrogen atom of the heterocycle. The short contacts observed in crystal I are caused by weak intermolecular bonds of the N-H×××Cl (2.69 Å) and C-H×××Cl (2.85-2.94 Å) types, with each anion surrounded by eight cations and each cation surrounded by four anions. In crystal II chain-like structural units can be distinguished. In these chains the anion forms hydrogen bonds О-Н×××Cl (2.34 Å) through the carboxyl groups with two cations, which are bound to water molecules through the protonated nitrogen atom N-H×××O (1.91 Å). The chains are connected to each other by weaker interactions, among which are the hydrogen bonds О-Н×××Cl (2.54 and 2.77 Å) between water molecules and anions.
Текст научной статьи Взаимодействие Гексахлороплатиноводородной кислоты с 2,2'-бипиридином и 1,2,3,4-тетрагидроакридин-9-карбоновой кислотой
Основные области применения разнообразных комплексов платины, как ионных, так и молекулярных, обусловлены их каталитическими свойствами и биологической активностью. В настоящее время достаточно большое количество работ посвящено комплексам с гексахлороплати-натными анионами [1], среди которых найдены соединения, демонстрирующие противоопухолевую активность и противовоспалительные, противомикробные, противогрибковые свойства [2, 3].
Катионами в гексахлороплатинатных комплексах часто являются производные N-гетероциклов, таких как: пуриновые и пиримидиновые основания, имидазол, пиридин, пирролидин, фенантролин и др., которые выступают в роли акцепторов, образуя с гексахлороплатиноводородной кислотой системы переноса протонов.
Так, взаимодействие гексахлороплатиноводородной кислоты с метиладенином, приводит к образованию гексахлороплатината(IV) метиладениния [4], пирролидин с гексахлороплатиноводородной кислотой в водном растворе соляной кислоты при комнатной температуре образует гексахлороплатинат(IV) бис(пирролидиния) [5]. В качестве акцепторов протона могут выступать имидазолы и бензидазолы, которые при кипячении в воде с гексахлороплатиноводородной кислотой дают с высоким выходом гексахлороплатинаты(IV) замещенных имидазолия [3, 6-9]; из- вестны аналогичные комплексы с катионами замещенного пиридиния [10-12] и фенантриди-ния [13], полученные в смеси метанол-ацетонитрил или в этаноле. Хорошими рецепторами для гексахлороплатинат-аниона [PtCl6]2– являются протонированные формы аминов, амидоаминов и амидоэфиров [14-19].
Были проведены исследования [20], показывающие, что строение продуктов взаимодействия гексахлороплатиноводородной кислоты с азотсодержащими гетероциклическими соединениями может зависеть от растворителя. Так, ионный комплекс с катионом бипиридиния в реакции с 6,6`-диметил-2,2`-бипиридином (1 : 2 мольн.) образуется только в ацетонитриле, тогда как в диметилсульфоксиде и смеси диметилформамид - диметилсульфоксид - вода продуктами являются молекулярные комплексы платины(II) и платины(IV) соответственно, которые получаются в результате лигандного обмена при атомах платины. В комплексе платины(IV) азотсодержащий лиганд образует с центральным атомом ковалентную связь Pt - C (валентное взаимодействие) и донорно-акцепторную Pt ⋅⋅⋅ N (невалентное взаимодействие). В других работах показано, что при проведении реакций гексахлороплатиноводородной кислоты с 5,5`-диметил-2,2`-бипиридином, 6-метил-2,2`-бипиридином и 4,4`-ди- трет -бутил-2,2`-бипиридином в метаноле протонирования гетероциклов не наблюдается, а выделяются молекулярные комплексы, в которых лиганды координируется как N,N-бидентатные [21, 22]. Молекулярный комплекс дает реакция гексахлороплатиноводородной кислоты с монодентатным лигандом 3-фенилпиридином в метаноле [22].
Получение новых комплексов платины с азотсодержащими гетероциклическими соединениями представляет значительный научный и практический интерес.
Экспериментальная часть
Синтез комплекса [C 10 N 2 H 8 ∙H]+ 2 [PtCl 6 ]2– (I) . К 20%-ному водному раствору H 2 PtCl 6 (0,5 мл, 0,24 ммоль) приливали раствор 2,2`-бипиридина (0,076 г, 0,5 ммоль) в 10 мл CH 3 CN при комнатной температуре и перемешивали. Цвет раствора менялся с жёлтого на оранжевый. Через сутки наблюдали образование оранжевых кристаллов I , которые фильтровали и сушили. Выход 0,158 г, 90 %, Т разл 208 °С.
ИК-спектр (ν, см–1): 3061, 3088, 3152, 1472, 1457, 1431, 1358, 1317, 1306, 1281, 1250, 1223, 1167, 1153, 1088, 1070, 1011, 975, 993, 922, 860, 767, 745, 725, 611, 544, 469, 407.
Синтез комплекса [C 28 N 2 О 4 H 30 ∙H]+ 2 [PtCl 6 ]2– ⋅ 2Н 2 О (II). К 20%-ному водному раствору H 2 PtCl 6 (0,25 мл, 0,12 ммоль) приливали раствор 1,2,3,4-тетрагидро-9-акридинкарбоновой кислоты (0,055 г, 0,24 ммоль) в 20 мл CH 3 CN при комнатной температуре и перемешивали, наблюдали появление ярко-жёлтого цвета раствора. При медленном испарении растворителя выпадали светло-оранжевые кристаллы, которые сушили при комнатной температуре. Выход 0,074 г, 69 %. Т разл 170 °С.
ИК-спектр (ν, см–1): 3289, 3169, 3032,2957, 2870, 2718, 2698, 1884, 1756, 1719, 1705, 1651,1637, 1597, 1531, 1495, 1460, 1450, 1425, 1416, 1365, 1335, 1304, 1259, 1242, 1188, 1171, 1153, 1084, 1005, 964, 947, 895, 854, 839, 826, 785, 766, 756, 682, 669, 631, 613, 569, 534, 499, 467, 418.
ИК-спектры соединения 1 и 2 записывали на ИК-спектрометре Shimadzu IRAffinity-1S в таблетках KBr в области 4000–400 см–1.
РСА кристаллов 1 и 2 проведен на дифрактометре D8 Quest фирмы Bruker (MoKα-излучение, λ = 0,71073 Å, графитовый монохроматор) при 296(2) К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [23]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [24] и OLEX2 [25]. Структура определена прямым методом и уточнена методом наименьших квадратов в анизотропном приближении для неводородных атомов. Положение атомов водорода уточняли по модели наездника (Uизо(H) = 1,2Uэкв(C)). Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2224721 (I); № 2336726 (II) ; . Основные кристаллографические данные и результаты уточнения структур I и II приведены в табл. 1, длины связей и валентные углы – в табл. 2.
Таблица 1
|
Параметр |
I |
II |
|
Стехиометрическая формула |
C 20 H 18 N 4 Cl 6 Pt |
C 28 H 32 N 2 O 6 Cl 6 Pt |
|
М |
722.17 |
900.35 |
|
Сингония |
Триклинная |
Триклинная |
|
Пространственная группа |
P– 1 |
P– 1 |
|
a , Å |
8,535(3) |
8,590(2) |
|
b , Å |
9,289(4) |
9,464(3) |
|
c, Å |
9,327(4) |
10,209(3) |
|
α , град. |
63,90(2) |
94,565(13) |
|
β, град. |
89,013(18) |
99,188(16) |
|
γ , град. |
66,571(17) |
96,496(15) |
|
V , Å3 |
598,0(4) |
810,0(4) |
|
Z |
1 |
1 |
|
ρ выч, г/см |
2,005 |
1,846 |
|
µ , мм–1 |
6,553 |
4,870 |
|
F (000) |
346,0 |
442,0 |
|
Размер кристалла, мм |
0,41 × 0,36 × 0,23 |
0,53 × 0,5 × 0,19 |
|
Диапазон сбора данных по 2 θ , град. |
5,7–96,3 |
6,08 - 54,28 |
|
Диапазон индексов |
–17 ≤ h ≤ 17, –19 ≤ k ≤ 19, –19 ≤ l ≤ 19 |
- 10 ≤ h ≤ 10, - 12 ≤ k ≤ 12, - 13 ≤ l ≤ 13 |
|
Число измеренных рефлексов |
81064 |
18908 |
|
Число независимых рефлексов |
11422 |
|
|
R int |
0,1223 |
0,0410 |
|
GOOF |
1,082 |
1,127 |
|
Число параметров |
146 |
200 |
|
R -факторы по I > 2 σ ( I ) |
R 1 = 0,0288, wR 2 = 0,0589 |
R 1 = 0,0249, wR 2 = 0,0629 |
|
R -факторы по всем рефлексам |
R 1 = 0,0341, wR 2 = 0,0611 |
R 1 = 0,0249, wR 2 = 0,0629 |
|
Остаточная электронная плотность (max/min), e/A3 |
0,63/–3,02 |
0,88/ - 2,34 |
Таблица 2
|
Связь \ |
d , Å 1 |
Угол 1 |
ω, град. |
|
I |
|||
|
Pt(1)–Cl(1) |
2,3280(9) |
Cl1 - Pt1–Cl11 |
179,999(2) |
|
Pt(1)–Cl(11) |
2,3280(9) |
Cl2 - Pt1–Cl21 |
180,0 |
|
Pt(1)–Cl(2) |
2,3340(8) |
Cl3 - Pt1–Cl31 |
180,0 |
|
Pt(1)–Cl(21) |
2,3340(8) |
Cl1 - Pt1–Cl2 |
90,31(3) |
|
Pt(1)–Cl(3) |
2,3231(11) |
Cl11‒ Pt1–Cl2 |
89,68(3) |
|
Pt(1)–Cl(31) |
2,3231(11) |
Cl1‒Pt1–Cl21 |
89,69(3) |
|
N(1)–C(1) |
1,343(3) |
Cl11‒Pt1–Cl21 |
90,31(3) |
|
N(1)–C(5) |
1,350(2) |
Cl3 - Pt1–Cl11 |
90,03(3) |
|
N(2)–C(6) |
1,336(2) |
Cl31‒Pt1–Cl11 |
89,97(3) |
|
N(2)–C(10) |
1,340(3) |
Cl3 - Pt1–Cl1 |
89,97(3) |
|
Преобразования симметрии: 1 - X, 2 - Y, 1 - Z |
|||
|
II |
|||
|
Pt(1)–Cl(1) |
2,3211(9) |
Cl1 - Pt1–Cl11 |
180,0 |
|
Pt(1)–Cl(11) |
2,3211(9) |
Cl2 - Pt1–Cl21 |
180,0 |
|
Pt(1)–Cl(2) |
2,3260(10) |
Cl3 - Pt1–Cl31 |
180,0 |
|
Pt(1)–Cl(21) |
2,3260(10) |
Cl1 - Pt1–Cl2 |
89,71(3) |
|
Pt(1)–Cl(3) |
2,3303(10) |
Cl11‒ Pt1–Cl2 |
90,29(3) |
Окончание табл. 2
|
Связь |
d , Å |
Угол |
ω, град. |
|
Pt(1)–Cl(31) |
2,3303(10) |
Cl1‒Pt1–Cl21 |
90,29(3) |
|
N(1)–C(6) |
1,370(4) |
Cl11‒Pt1–Cl21 |
89,71(3) |
|
N(1)–C(11) |
1,327(4) |
Cl3 - Pt1-Cl1 1 |
89,88(3) |
|
Преобразования симметрии: 1 1 - X, - Y ,1 - Z |
|||
Обсуждение результатов
Установлено, что гексахлороплатиноводородная кислота взаимодействует с 2,2 ' -бипиридином в смеси вода – ацетонитрил при комнатной температуре с образованием комплексной соли гексахлороплатината 2,2 ' -бипиридиния ( I ), выход которой составил 90 %.
Кристаллографические данные, параметры эксперимента и уточнения структур I и II
Длины связей и валентные углы в структурах I и II
I
Соединение I представляет собой оранжевые кристаллы, разлагающиеся при 208 °С.
Ранее было показано, что аналогично протекает реакция с 6,6`-диметил-2,2`-бипиридином [20].
Гексахлороплатиноводородная кислота протонирует 1,2,3,4-тетрагидроакридин-9-карбоновую кислоту по атому азота гетероцикла в растворе вода-ацетонитрил с образованием ионного комплекса II .
OH
H 2 PtCl 6(aq.) +
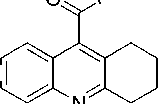
CH 3 CN
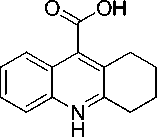
Cl ClCl
Cl PCtl Cl
2-
2H 2 O
II
Комплекс кристаллизуется из смеси растворителей в форме гидрата на две молекулы воды. Выход составил 69 %. Кристаллы светло-оранжевого цвета начинают разлагаться при 170 °С.
Строение комплексов I и II было установлено методом рентгеноструктурного анализа.
Катион 2,2 ' -бипиридиния комплекса I образован протонированной формой 2,2 ' -бипиридина (водород присоединяется к одному из эндоциклических атомов азота) (рис. 1). Плоскости гетероциклов [C(1)C(2)C(3)C(4)C(5)N(1)] и [C(6)C(7)C(8)C(9)C(10)N(2)] составляют угол 20,53 ° . Связи N - C в протонированном гетероцикле (1,343(3) и 1,350(2) А) несколько длиннее аналогичных связей в пиридиновом фрагменте (1,336(2) и 1,340(3) Å). Внутримолекулярную водородную связь N(1) - H—N(2) в катионе можно оценить как слабую, поскольку расстояние H—N составляет 2,20 Å.
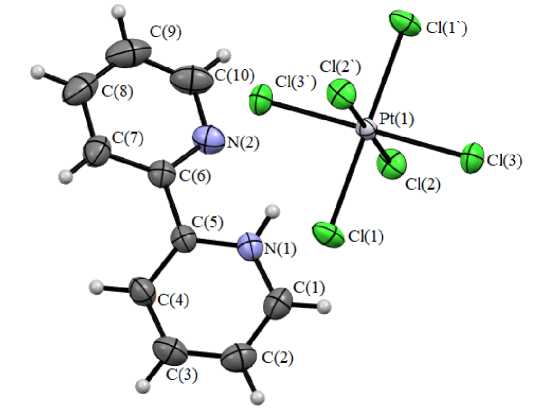
Рис. 1. Строение комплекса I (эллипсоиды смещения с вероятностью 50 %)
В II ка ти он п редс та в ля ет собой протонированную по атому азота 1,2,3,4-тетрагидро-акридин-9-карбоновую ки с л оту (рис. 2). Угол между плоскостями конденси ров а н н ых а ром а ти ч еских циклов составляет 1,41 ° , в ыхо д атомов углерода из средней плоскости двух циклов варьирует от 0,005 до 0,022 Å, атом а зот а в ыхо д и т и з э той п лоск о сти на 0,014 Å. Карбоксильная группа п рак тическ и перп е н д ик у лярн а плоскости ароматического кольца (угол раве н 83, 58 ° ). Конформация кресло ц и к л огек са н ов ого фрагмента искажена: атомы С(4)С(5)С(6)С(1) об раз у ю т п л оск ост ь , и з к оторой пере чис ле н ные а т омы отк лон я ются на 0,006 - 0,014 А, в то время как атомы С(2) и С (3) в ыхо д ят и з п л ос кос т и в п роти в оп оложн ы е с то рон ы н а 0, 4 38 и 0, 26 7 Å соответственно.
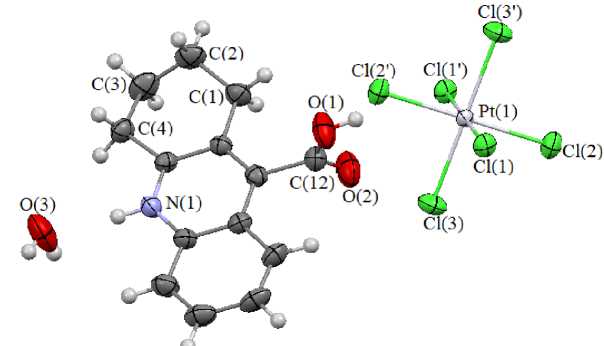
Рис. 2. Строение комплекса II (эллипсоиды смещения с вероятностью 50 %)
Связи С(12) - О(1) и С(12) - О(2) в карбоксильной группе существенно различаются (1,313(5) и 1,190(5) Å), чт о с оотв е т с тв у ет одинарной и двойной связи соответственно и с в и д е те льс тв у е т об о т сутст в и и д елок а ли за ц ии э ле к трон н ой п лотн ос т и . У гол О( 1) - С(12) - О(2) равен 126,3(4) ° . Расстояния N - C в протон иров а н ном гетероцикле составляют 1,327(4) и 1,3 70( 4) А). Связи С - С в ц и к л огек с а н ов ом фр а гм е н те ( 1 , 499 ( 7) - 1,534(6) А), как и следовало ожидать, превосходят анал оги чн ые с в язи в а рома т и че с к и х ц ик ла х ( 1, 36 3( 6 ) - 1,423(5) А), что соответствует sp 3- и sp 2-типам г ибри д и з ац ии ат ом ов у гле рода .
Геометрия анионов [PtCl6]2– в I и II практически одинакова и мало отличается от строения анионов в других комплексах с гексахлороплатинатными анионами [1]. Анионы центросиммет- ричны. В I и II связи Pt–Cl равны 2,3231(11), 2,3280(9), 2,3340(8) Å и 2,3211(9), 2,3260(10), 2,3303(10) А; углы ClPtCl составляют 89,68(3)°, 89,97(3)°, 90,09(3)°, 90,31(3)° и 89,71(3)°, 89,88(3)°, 90,12(3)°, 90,29(3)°.
Пространственная структура I сформирована таким образом, что каждый анион имеет в ближнем окружении восемь катионов, а каждый катион – четыре аниона; короткие контакты обусловлены слабыми межмолекулярными связями типа N - H --- C1 (2,69 А) и C - H—C1 (2,85 - 2,94 А) (рис. 3).
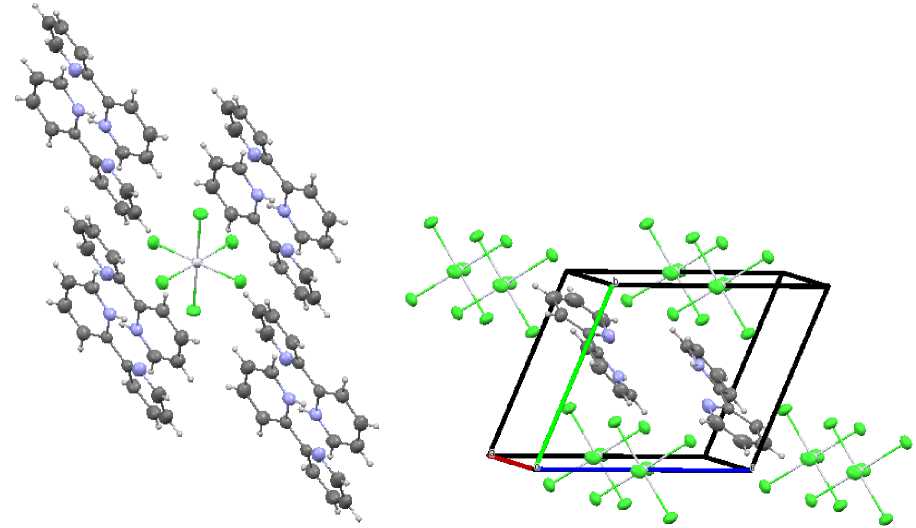
а)
б)
Рис. 3. Окружение аниона (а) и катиона (б) в кристалле I
В кристалле II участие в формировании структуры принимают молекулы воды. Можно выделить цепочки, в которых два катиона, анион и две молекулы воды связаны посредством водородных связей О - Н --- С1 (2,34 А), N - H --- O (1,91 А) (рис. 4). Расположение цепочек относительно кристаллографической оси а показано на рис. 5.
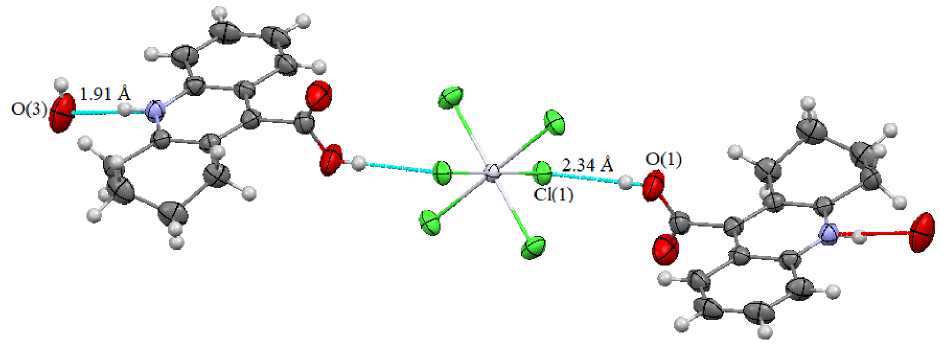
Рис. 4. Система водородных связей в кристалле комплекса II
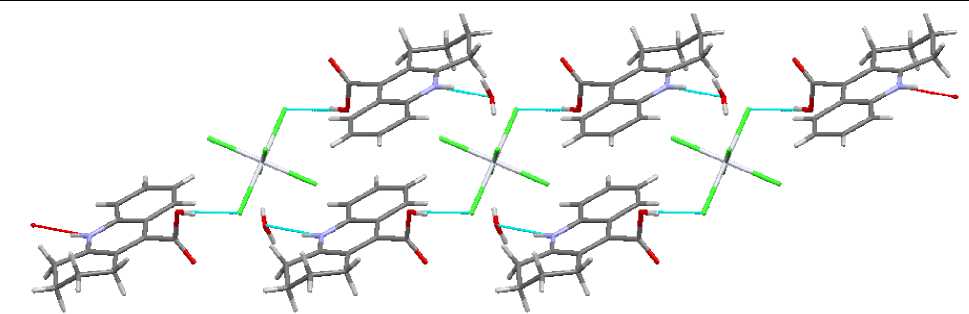
Рис. 5. Расположение структурных единиц в кристалле II относительно кристаллографической оси а
Между собой цепочки связаны более слабыми взаимодействиями, среди которых можно выделить водородные связи О - Н ⋅⋅⋅ Cl (2,54 и 2,77 Å) между молекулами воды и анионами.
Выводы
Таким образом, в результате реакций гексахлороплатиноводородной кислоты с органическими соединениями, включающими азотсодержащие гетероциклы, протекающих в водно-ацетонитрильных растворах, наблюдается образование гексахлороплатинатных комплексов с катионами, представляющими собой протонированную по азоту форму исходных молекул. Кристаллическая и молекулярная структуры двух неизвестных ранее комплексов установлены методом рентгеноструктурного анализа.


