Взаимодействие треонина с хлоридами биометаллов в водной среде при 25°C
Автор: Бекташева У.К., Алтыбаева Д.Т., Абдуллаева Ж.Д., Матаипова А.К.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Химические науки
Статья в выпуске: 4 т.10, 2024 года.
Бесплатный доступ
Метод синтеза комплексов с солями биометаллов переходных групп с аминокислотой треонин включает в себя улучшение реакционных условий, выбор реагентов и методов анализа для подтверждения образования комплексов . Цели исследования: получение комплексных соединений биометаллов, хлорида кобальта, хлорида никеля и хлорида марганца с аминокислотой треонин, а также изучение их физико-химических и биологических свойств. При синтезе комплексных соединений был применен препаративный метод. Состав образованных кристаллов был проанализирован ИК спектроскопией. Строение и форма кристаллов кобальта, никеля и марганца были определены микроскопом. Индивидуальность полученных соединений подтверждена методом ИК спектроскопии и микроскопическим анализами. Можно сделать вывод о том, что треонин в комплексе координирован к ионам металла через атомы кислорода карбоксильной и азота аминной групп.
Треонин, хлориды биометаллов, растворимость, ик-спектры, лиганд
Короткий адрес: https://sciup.org/14129767
IDR: 14129767 | УДК: 546.212:546.47 | DOI: 10.33619/2414-2948/101/04
Interaction of threonine with biometal chlorides in an aqueous environment at 25°C
The method for the synthesis of complexes with transition group biometal salts with the amino acid threonine includes improvement of reaction conditions, selection of reagents and analytical methods to confirm the formation of complexes. Research purpose: obtaining complex compounds of biometals, cobalt chloride, nickel chloride and manganese chloride with the amino acid threonine, as well as the study of their physicochemical and biological properties. In the synthesis of complex compounds, the preparative method was used. Compositions of the formed crystals were analyzed by IR spectroscopy. The structure and shape of cobalt, nickel and manganese crystals were determined using a microscope. The identity of the obtained compounds was confirmed by IR spectroscopy and microscopic analyses. We can conclude that threonine in the complex is coordinated to metal ions through the oxygen atoms of the carboxyl and nitrogen groups of the amine groups.
Текст научной статьи Взаимодействие треонина с хлоридами биометаллов в водной среде при 25°C
Бюллетень науки и практики / Bulletin of Science and Practice
УДК 546.212:546.47
Среди биологически активных веществ значительное место занимают аминокислоты и их производные, нуклеиновые кислоты. Интерес к комплексным соединениям, содержащим природные аминокислоты и их производные в качестве лигандов, сохраняется на протяжении десятилетий. Структура аминокислот предопределяет возможность образования разнообразных комплексных соединений с металлическими ионами, варьирующихся в зависимости от наличия карбоксильной, аминогруппы и дополнительных донорных групп [1–4]. Также была исследована тройная система хлорид гольмия – глицин – вода [5].
Аминокислоты представляют собой гетерофункциональные соединения, включающие карбоксильную группу и аминогруппу в их молекуле. Они проявляют кристаллические свойства и растворимы в воде, однако оказываются малорастворимыми в органических растворителях и подвержены плавлению при повышенных температурах, при этом распадаясь. Интересно, что многие из них обладают сладким вкусом.
Цель исследования : разработать экономически эффективные методики синтеза комплексных соединений металлов с аминокислотой треонин. Это включает в себя выбор оптимальных реакционных условий, реагентов и методов анализа продуктов реакции.
Синтезировать комплексы биометаллов, таких как кобальт, никель и марганец с использованием аминокислоты треонин в качестве лиганда. Это позволит изучить, какие металлы образуют стабильные комплексы с данной аминокислотой.
Материалы и методы исследования
Для обеспечения достоверности полученных результатов проводились комплексные анализы данных при использовании наиболее современных и актуальных научноисследовательских методов, и инструментов.
Все эксперименты выполнялись с повторяемостью не менее 5 раз, чтобы обеспечить надежность данных. Состав и строение образованных кристаллов были анализированы ИК спектроскопией и микроскопом.
Результаты и обсуждение
Состав полученных комплексных соединений идентифицирован ИК спектроскопией после чего были выделены спектры поглощения комплексных соединений (Рисунок 1).
Колебательные частоты ИК спектроскопии комплексных соединений хлорида кобальта с треонином СоСl 2 ×C 4 H 9 NO 3 , хлорида никеля с треонином NiСl 2 ×C 4 H 9 NO 3 и хлорида марганца с треонином MnСl 2 ×C 4 H 9 NO 3 даны в Таблице.
Микроскопическое строение кристаллов комплексного соединения хлорида кобальта с треонином СоСl 2 ×2C 5 H 11 O 2 N представлено на Рисунке 2. В ИК-спектре нового комплексных соединений СоСl 2 ×2C 5 H 11 O 2 N, NiСl 2 ×2C 5 H 11 O 2 N и MnСl 2 ×2C 5 H 11 O 2 N в длинноволновой области проявляющиеся пики 3212, 3220, 2931 см-1 соответствуют валентному колебанию аминогруппы, что свидетельствует о комплексообразовании, в котором принимает участие аминогруппа.
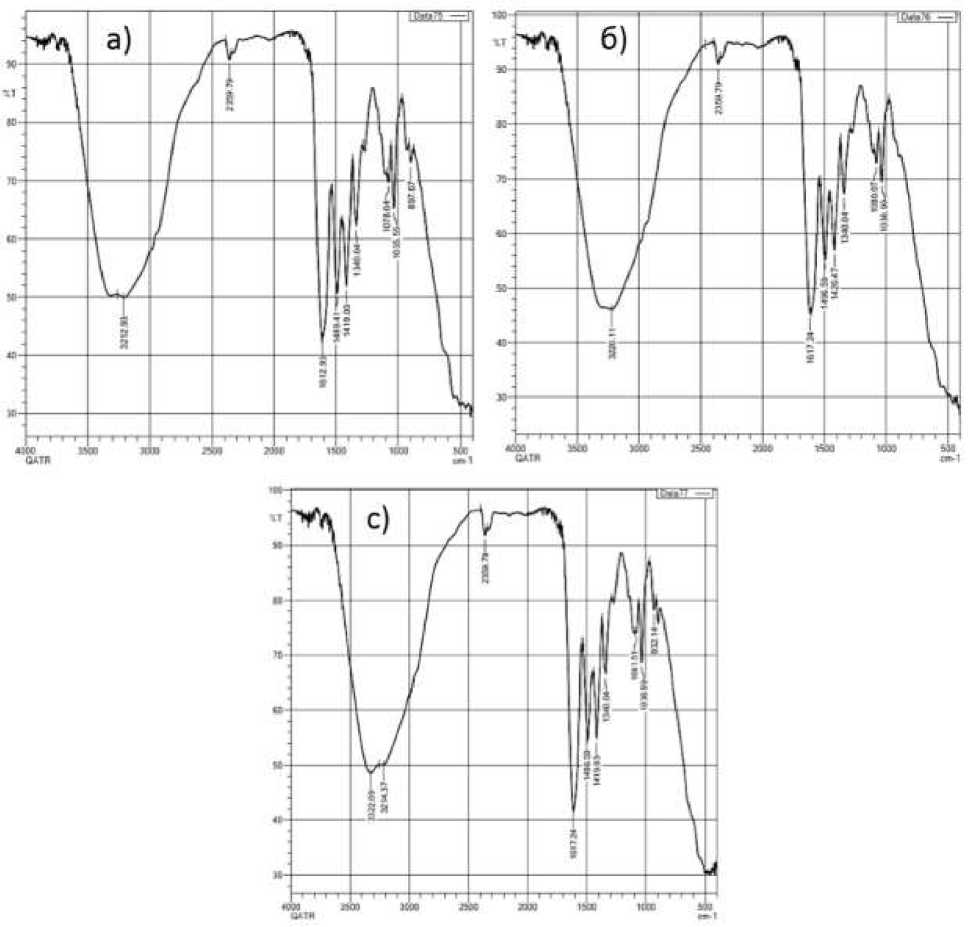
Рисунок 1. ИК-спектры поглощения комплексных соединений: а) хлорида кобальта с треонином СоСl 2 ×C 4 H 9 NO 3 ; б) хлорида никеля с треонином NiСl 2 ×C 4 H 9 NO 3 ; в) хлорида марганца с треонином MnСl 2 ×C 4 H 9 NO 3
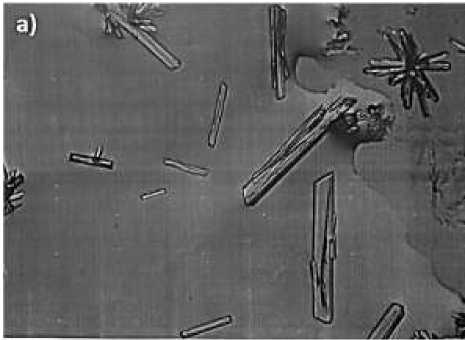
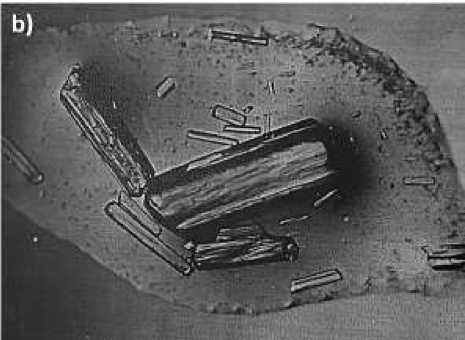
Рисунок 2. Строение кристаллов: a) аминокислоты треонин; b) комплексного соединения хлорида кобальта с валином СоСl 2 ×2C 5 H 11 O 2 N
Наблюдается сдвиг полосы поглощения валентного колебания карбоксильной группы (νasСОО-) на 60 см-1, т. е. смещена в низкочастотную область от 1620 см-1 до 1585 и 1617 см-1, что подтверждает возможность комплексообразования через атом кислорода карбоксильной группы.
Таблица
ОСНОВНЫЕ КОЛЕБАТЕЛЬНЫЕ ЧАСТОТЫ (см-1) в ИК-спектрах треонина и новых комплексных соединений СоСl 2 ×C 4 H 9 NO 3 , NiСl 2 ×C 4 H 9 NO 3 и MnСl 2 ×C 4 H 9 NO 3
|
Отнесение |
C 4 H 9 NO 3 |
СоСl 2 ×C 4 H 9 NO 3 |
|
v as (NH 2 ) |
— |
3212,93 |
|
v s (NH 2 ) |
2974,51 |
2359,79 |
|
v as (COO-) |
1620,11 |
1612,93 |
|
v s (COO-) |
1413,29 |
1419,03 |
|
δ as (NH 2 ) |
— |
1078,64 |
|
δ s (NH 2 ) |
1028,37 |
1035,55 |
|
Отнесение |
C 4 H 9 NO 3 |
NiСl 2 ×C 4 H 9 NO 3 |
|
v as (NH 2 ) |
— |
3220,11 |
|
v s (NH 2 ) |
2974,51 |
2359,79 |
|
v as (COO-) |
1620,11 |
1617,24 |
|
v s (COO-) |
1413,29 |
1420,47 |
|
δ as (NH 2 ) |
— |
1080,07 |
|
δ s (NH 2 ) |
1028,37 |
1036,99 |
|
Отнесение |
C 4 H 9 NO 3 |
MnСl 2 ×C 4 H 9 NO 3 |
|
v as (NH 2 ) |
— |
2931,42 |
|
v s (NH 2 ) |
2974,51 |
2595,34 |
|
v as (COO-) |
1620,11 |
1585,64 |
|
v s (COO-) |
1413,29 |
1394,64 |
|
δ as (NH 2 ) |
— |
1028,3 |
|
δ s (NH 2 ) |
1028,37 |
715,26 |
Выводы
ИК-спектры синтезированных комплексных соединений металлов с треонином свидетельствуют о том, что химическая связь между металлом и лигандом осуществляется через атомы кислорода карбоксильной и азота аминной групп.
Определены оптимальные условия синтеза координационных соединений кобальта, никеля и марганца с аминокислотой треонин, обеспечивающие формирование однородных продуктов с выходом от 86% до 92% что важно для обеспечения высокой эффективности синтеза.
Список литературы Взаимодействие треонина с хлоридами биометаллов в водной среде при 25°C
- Болотин С. Н. Координационная химия природных аминокислот. М.: URSS, 2008. 238 с. EDN: SZLWUX
- Дятлова Н. М., Фридман А. Я., Барханова Н. Н. Влияние дентатности и основности лигандов на устойчивость в растворе смешанных двуядерных соединений этилендиаминтетраацетатов меди (И) // Журнал неорганической химии. 1974. Т. 19. №4-5. С. 1318.
- Есина Н. Я., Молодкин А. К., Тараканова Е. В. Разнолигандные комплексные соединения меди (II), никеля (II) и кобальта (II) с L-аспарагиновой кислотой и L-треонином // Журнал неорганической химии. 1996. Т. 41. №11. С. 1874-1879.
- Кайгородова Е. А., Косянок Н. Е., Яблонская Е. К., Пушкарева К. С. Синтез и исследование спектральных характеристик координационных соединений метионина и пантотеновой кислоты с d-элементами // Спектроскопия координационных соединений: Сборник тезисов VII Международной конференции. 2010. С. 126.
- Осмонова С. С., Орозбаева Н. О., Дубанаева К. Д., Саркелов Ж. С., Байдинов Т. Б. Комплексообразующая способность хлорида гольмия с глицином в водной среде при 25°C // Международный журнал прикладных и фундаментальных исследований. 2021. №3. С. 78-84. EDN: BFWQUY


