Взаимодействие ZrO2 в расплавах системы А1203- ZrO2 с добавками оксидов подгруппы лантана
Автор: Пашкеев И.Ю.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 3 (43), 2005 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/147156528
IDR: 147156528 | УДК: 549.5:546.831
Текст обзорной статьи Взаимодействие ZrO2 в расплавах системы А1203- ZrO2 с добавками оксидов подгруппы лантана
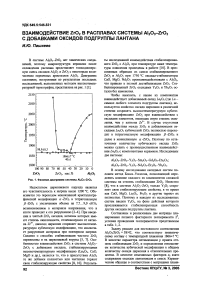
В системе AI2O3-Z102 нет химических соединений, поэтому микроструктура керамики после охлаждения расплава представляет тонкодисперсную смесь оксидов А12О3 и ZrO2 с некоторым количеством первичных кристаллов А12О3. Диаграмма состояния, построенная по результатам последних исследований, выполненных методом высокотемпературной термографии, представлена на рис. 1 [1].
ZrO2 ZrO2, мае.% AI2O3
Рис. 1. Фазовая диаграмма системы AI2O3-ZrO2
Недостатком циркониевого корунда является его чувствительность к нагреву выше 1200 °C. Объясняется это переходом моноклинной кристаллографической модификации a-ZrO2 в тетрагональную /?-ZrO2 с увеличением объема на 7,7...9,0 об.%, возникновением в материале напряжения, что в итоге приводит к его разрушению [2-4]. При введении в чистый ZrO2 оксидов, катионы которых имеют степень окисленности, отличающуюся от катиона Zr4+, диоксид циркония сохраняет высокотемпературную кубическую модификацию, что исключает разрушение материала при повторном нагреве. Сведеня о способах стабиилизации чистого ZrO2 перенесены и на циркониевый корунд [5, 7]. Особенностью взаимодействия ZrO2 в системе А12О3-ZrO2 с добавками оксидов, стабилизирующими высокотемпературную модификацию (Ln2O3, СаО, MgO и др.), является то, что в присутствии А12О3 те же добавки полностью или частично теряют свои стабилизирующие свойства [8, 10]. Результа ты исследований взаимодействия стабилизированного ZrO2 с А12О3 при температуре ниже температуры плавления приведены в работе [10]. В прессованных образцах из смеси стабилизированного ZrO2 и А12О3 при 1750 °C оксиды-стабилизаторы СаО, MgO, Nd2O3 провзаимодействовали с А12О3, что привело к полной дестабилизации ZrO2. Стабилизированный ZrO2 оксидами У2О3 и УЬ2О3 остался без изменения.
Чтобы выяснить, с каким из компонентов взаимодействует добавляемый оксид LnjO3 (где Ln - символ любого элемента подгруппы лантана), используется свойство оксида циркония в различной степени сохранять высокотемпературную кубическую модификацию ZrO2 при взаимодействии с оксидами элементов, имеющих иную степень окисления, чем у катиона Zr4+. В случае отсутствия взаимодействия между ZrO2 и добавляемыми оксидами ЬпгО3 кубический ZrO2 полностью переходит в тетрагональную модификацию Р -ZrO2 и далее в моноклинную a-ZrO2. Поэтому по остаточному количеству кубического оксида ZrO2 можно судить о преимущественном взаимодействии £и2О3 с компонентами керамики. Исследованы две системы:
А12О3—ZrO2—У 2O3—Sm2O3—Gd2O3—Пу2О3;
AI2O3—ZrO2- У 3О3—Nd2O3—ЕГ2О3—УЪ2О3.
В основу исследования оксидных систем положен метод Бокса-Уилсона, позволяющий определить влияние каждого из компонентов сложной системы на степень стабилизации ZrO2. Известно [8], что в системе Al2O3-ZrO2 только У2О3 сохраняет свои стабилизирующие свойства, в то время как СаО, MgO, La2O3, Рг2О3 и другие теряют их полностью. Поэтому в каждую из исследованных систем введен У2О3, на фоне действия которого прослеживается стабилизирующая способность других оксидов подгруппы лантана.
Составлены и реализованы две матрицы планирования полного факторного эксперимента 24, условия проведения экспериментов представлены в табл. 1,2.
Задачу решали для постоянного соотношения Al2O3/Zro2 = 58/42, что соответствует эвтектическому составу с температурой плавления 1866±7 °C. В качестве параметра оптимизации у прията степень стабилизации ZrO2 и определяемая отношением количества кубической модификации к общему количеству оксида циркония в относительных процентах. В качестве изменяемых факторов х,- взято содержание оксидов лантаноидов в смеси. Керамические образцы в соответствии с матрицами плани-
Таблица 1
Условия проведения эксперимента в системе AhOa-ZrOr-YjOj-SmjOa-GdjOr-DyjOa
|
Факторы, параметр оптимизации |
y2o3, мол.% |
Sm2O3, мол.% |
Dy2O3, мол.% |
Gd2O3, мол.% |
а, отн,% |
|
Код |
*1 |
*2 |
*3 |
*4 |
У |
|
Нулевой уровень |
1,5 |
1,5 |
1,0 |
1,0 |
|
|
Интервал варьирования, А*, |
0,5 |
0,5 |
1,0 |
1,0 |
|
|
Верхний уровень, +1 |
2,0 |
2,0 |
2,0 |
2,0 |
|
|
Нижний уровень, -1 |
1,0 |
1,0 |
0 |
0 |
Таблица 2
Условия проведения эксперимента в системе AUOa-ZrOz-YzOa-NdaOs-EriCb-YbzCb
гШ
[%2Ю2(ку6)] = —^—„-ЮО, (1)
где /Р1 - интегральная интенсивность пика кубической фазы, 4)1 - интегральная интенсивность пика моноклинной фазы. Результаты количественного анализа образцов исследованных систем приведены в табл. 3,4.
Связь степени стабилизации ZrO2 в циркониевом корунде у и количеством стабилизирующих добавок описывается полиномом к к к y = b0+y,bixi+ ^ ЬуХ,х3+уЬ„х^ +..., (2) м ,=i j*\ ,=1
в котором коэффициенты Ьь by определяются по экспериментальным результатам:
b, =^:'$lxiny„ , (3)
Л И=1
где xin - значение z-го фактора в и-й строке матрицы планирования в кодовом значении; у„ - экспериментальное значение степени стабилизации и-й строки матрицы планирования; N - число опытов матрицы планирования.
Оценка статистической значимости коэффициентов и адекватности математической модели по критериям Стьюдента и Фишера показали, что можно ограничиться линейной моделью для описания функции отклика:
для системы
А120з- 2Юг- Y2O3(*i)--Sm2O3(x2)---Dy2O3(x3)--Gd2O3(x4):
у = 80,5 + 4,9*1 + 2,7*2 + 9,6х3 + 5,7*4; (4)
для системы
AbO^ZrtVYAte^dzQK^^
у = 80,6 + 5,97*5 + 0,531*6 + 8,65*7 + 9,94*8. (5)
Коэффициенты уравнений (4), (5) отражают влияние факторов на степень стабилизации высокотемпературной модификации ZrO2 или, иными словами, склонность оксидов подгруппы лантана к взаимодействию с ZrO2 в сложных системах, содержащих А12О3. Если в уравнениях (4), (5) принять за единицу сравнения действие Y2O3 в качестве стабилизатора высокотемпературной модификации ZrO2, то можно оценить суммарное стабилизирующее действие D смеси оксидов лантаноидов, эквивалентное действию чистого Y2O3:
D = 1,0(мас.% Y2O3) + 0,10(мас.% Nd2O3) +
+ 0,55(мас.% Sm2O3) + 0,60(мас.% Gd2O3) +
+ 0,98(мас.% Dy2O3) + 1,45(мас.% Ег2О3) +
+ l,67(Mac.%Yb2O3), (6)
где D - суммарное содержание компонентов добавки, эквивалентное по действию чистому Y2O3, мол.%; символы в скобках - содержание оксидов в смеси, мас.%.
Полученные результаты позволяют рассчитать количество добавки, необходимой для стабилизации ZrO2 в системе Al2O3-ZrO2 с учетом состава смеси оксидов РЗМ, представленных обычно различными концентратами. Количество стабилизирующей добавки вычисляется по формуле:
100 • А • • А/у п
Д06 М^ (100 - A). D ’ где Сдоб - масса стабилизирующей добавки, кг; А - назначаемое количество стабилизирующей добавки, мол.%; тиао2 - количество ZrO2 в шихте, кг; A^y2o3 > -^Zro2 ~ молярная масса Y2O3 и ZrO2 соответственно; D - суммарное содержание оксидов в стабилизирующей добавке, эквивалентное по дей- U^-Am^y
ствию чистому У20з, мол.%. Сдоб =
После преобразования уравнение (7) прини- vluu А)и мает окончательный вид:
Таблица 3
Матрица планирования в кодовом и натуральном масштабах для исследования системы AhOs-ZrOr-YiOs-SmzOr-DyzOs-GdzOj и результаты ее реализации
|
№ опыта |
. . Концентрация стабилизатора |
а, отн.% |
|||||||
|
У2Оз |
Sm2O3 |
Оу2Оз |
Gd2O3 |
||||||
|
Хз |
мол.% |
х2 |
мол.% |
*3 |
мол.% |
х4 |
мол.% |
У |
|
|
1 |
+ |
2 |
+ |
2 |
+ |
2 |
+ |
2 |
95,0 |
|
2 |
— |
1 |
+ |
2 |
+ |
2 |
+ |
2 |
94,0 |
|
3 |
+ |
2 |
— |
1 |
+ |
2 |
+ |
2 |
97,0 |
|
4 |
— |
1 |
— |
1 |
+ |
2 |
+ |
2 |
95,0 |
|
5 |
+ |
2 |
+ |
2 |
— |
0 |
+ |
2 |
87,0 |
|
6 |
— |
1 |
+ |
2 |
— |
0 |
+ |
2 |
76,0 |
|
7 |
+ |
2 |
— |
1 |
— |
0 |
+ |
2 |
83,0 |
|
8 |
— |
1 |
— |
1 |
— |
0 |
+ |
2 |
63,0 |
|
9 |
+ |
2 |
+ |
2 |
+ |
2 |
0 |
91,0 |
|
|
10 |
1 |
+ |
2 |
■ + |
2 |
— |
0 |
79,0 |
|
|
11 |
+ |
2 |
— |
1 |
+ |
2 |
— |
0 |
91,5 |
|
12 |
— |
1 |
— |
1 |
+ |
2 |
— |
0 |
78,5 |
|
13 |
+ |
2 |
+ |
2 |
0 |
0 |
71,5 |
||
|
14 |
— |
1 |
+ |
2 |
— |
0 |
— |
0 |
72,0 |
|
15 |
+ |
2 |
1 |
— |
0 |
— |
0 |
67,5 |
|
|
16 |
— |
1 |
— |
1 |
— |
0 |
— |
0 |
47,5 |
|
17 |
84,5 |
||||||||
|
18 |
0 |
1,5 |
0 |
1,5 |
0 |
1 |
0 |
1 |
82,0 |
|
19 |
82,0 |
||||||||
|
20 |
81,0 |
||||||||
Таблица 4
Матрица планирования в кодовом и натуральном масштабах для исследования системы AliOa-ZrOr-YzOa-NekOa-E^Oy-YbzOs и результаты ее реализации.
|
№ опыта |
Концентрация стабилизатора |
а, отн.% |
|||||||
|
У2О3 |
NdA |
Ег20з |
УЬ20з |
||||||
|
Xi |
мол.% |
^2 |
мОл.% |
х3 |
мол.% |
х4 |
мол.% |
У |
|
|
1 |
+ |
2,0 |
+ |
2,5 |
+ |
1 |
+ |
1 |
98,0 |
|
2 |
— |
1,0 |
+ |
2,5 |
+ |
1 |
+ ' |
1 |
98,5 |
|
3 |
+ |
2,0 |
1,5 |
+ |
1 |
+ |
1 |
98,0 |
|
|
4 |
— |
1,0 |
— |
1,5 |
+ |
1 |
+ |
1 |
93,5 |
|
5 |
+ |
2,0 |
+ |
2,5 |
— |
0 |
+ |
1 |
91,0 |
|
6 |
1,0 |
+ |
2,5 |
— |
0 |
+ |
1 |
76,0 |
|
|
7 |
+ |
2,0 |
— |
1,5 |
— |
0 |
+ |
1 |
95,0 |
|
8 |
— |
1,0 |
1,5 |
— |
0 |
+ |
1 |
74,5 |
|
|
9 |
+ |
2,0 |
+ |
2,5 |
+ |
1 |
— |
0 |
88,5 |
|
10 |
— |
1,0 |
+ |
2,5 |
+ |
1 |
— |
0 |
76,0 |
|
11 . |
+ |
2,0 |
— |
1,5 |
+ |
1 |
— |
0 |
88,0 |
|
12 |
— |
1,0 |
— |
1,5 |
+ |
1 |
— |
0 |
73,0 |
|
13 |
+ |
2,0 |
+ |
2,5 |
— |
0 |
— |
0 |
66,5 |
|
14 |
— |
1,0 |
+ |
2,5 |
— |
0 |
— |
0 |
54,5 |
|
15 |
+ |
2,0 |
— |
1,5 |
0 |
— |
0 |
69,0 |
|
|
16 |
— |
1,0 |
— |
1,5 |
— |
0 |
0 |
49,5 |
|
|
17 18 19 |
0 |
1,5 |
0 |
2,0 |
0 |
0,5 |
0 |
0,5 |
83,0 83,0 79,5 |
|
20 21 |
91,7 89,0 |
||||||||
Дальнейшая проверка уравнения (7) показала полное соответствие расчетного количества стабилизирующей добавки сложного стабилизатора, определенного по уравнению (6), фактически необходимому, экспериментально установленному по степени стабилизации циркониевого корунда.
Способность оксидов подгруппы лантана стабилизировать высокотемпературную модификацию ZrO2 в присутствии А12О3 приведена на рис. 2.

La Се Pr Nd PmSm EuGd TbDy Ho Er Tm YbLu
Рис. 2. Способность оксидов элементов подгруппы лантана стабилизировать высокотемпературную модификацию ZrO2 в системе А12Оз-2Юз-кп2Оз в сравнении с Y2O3:
о - данные настоящей работы;
• - данные работы [8]
Сопоставляя результаты наших исследований с литературными данными, можно сделать вывод о том, что оксиды элементов с 57 по 71 по своему взаимодействию с ZrO2 делятся на три подгруппы. В системе Al2O3-ZrO2 оксиды элементов 57-59
образуют алюминаты, оксиды элементов 60-65 частично соединяются с А12О3 и частично с ZrO2, а оксиды элементов 66-71 преимущественно образуют цирконаты. -
Список литературы Взаимодействие ZrO2 в расплавах системы А1203- ZrO2 с добавками оксидов подгруппы лантана
- Jerebtsov D.A., Mikhailov G.G., Sverdina S. V. Phase diagram of the system: Al2O3-ZrO2/Ceramics International. -2000. -N26. -P. 821-823.
- Керамика из высокоогнеупорных окислов/И.С. Бакунов, В.Л. Балкевич, A.C. Власов и др.; Под ред. Д.Н. Полубояринова и Р.Я. Попильского. -М.: Металлургия, 1977. -304 с.
- Тонкая техническая керамика/Под ред. X. Янагида. -М.: Металлургия, 1986. -279 с.
- Производство и применение плавленолитых огнеупоров/О.Н. Попов, П.Т. Рыбалкин, В.А. Соколов, С.Д. Иванов. -М.: Металлургия, 1985. -256 с.
- Способ изготовления керамического материала для режущего инструмента/Япония, заявка. Кл. С 04 В 35/10, N 56-26767, опубл. 14.03.81.
- Высокопрочная и высокотвердая керамика на основе Al2O3/Япония, заявка. Кл. С 04 В 35/10, N 57-38370, опубл. 03.03.82.
- Абразивные зерна из плавленной смеси Al2O3-ZrO2-Ce2O3/Патент США, Кл. С 04 С 1/68, С 04 В 31/16, N 3881282, опубл. 6.05.75.
- Исследование процесса стабилизации ZrO2 в циркониевом электрокорунде/Ю.С. Кузнецов,Т. Ивашинников, Г.Г. Михайлов, В.А. Квитко и др.//Вопросы производства и обработки стали: Сб. научн. тр. -Челябинск: ЧПИ. -1979. -№ 229. -122-128.
- Умайский Я.С., Скаков Ю.А. Кристаллография, рентгенография и электронная микроскопия. -М.: Металлургия, 1982. -632 с.
- Фазовые преобразования в композициях стабилизированный ZrO2-Al2O3 и свойства циркониевых огнеупоров/В.И. Страхов, Е.А. Павлова, С.И. Гершкович//Огнеупоры. -1995. -№ 12. -С. 5-8.