Взаимосвязь структурных и энтальпийных характеристик мета- и ортосиликатов щелочных и щелочноземельных металлов
Автор: Груба Оксана Николаевна, Германюк Нина Васильевна, Рябухин Александр Григорьевич
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Химия твёрдого тела
Статья в выпуске: 1 (260), 2012 года.
Бесплатный доступ
С использованием модели эффективных ионных радиусов, принципа метаморфозы кристаллических структур в квазикубические и авторской методики расчета энтальпии кристаллической решетки впервые рассчитана стандартная энтальпия образования газообразного аниона SiO 2- 3, составившая 715,648 ± 0,067 кДж-моль -1. В качестве исходных данных для расчетов использованы справочные сведения о рентгеновских и термодинамических (стандартные энтальпии образования) характеристиках метасиликатов щелочных Na, K и щелочноземельных Ca, Sr, Ba металлов, а также ортосиликатов Ca, Sr, Ba. Для метасиликатов Rb, Cs, Fr, Ra и ортосилика тов Ra сделаны предсказательные вычисления энтальпий межструктурных взаимодействий, энтальпий кристаллических решеток и стандартных энтальпий образования кристаллических соединений.
Ортосиликаты, метасиликаты, силикат-ион, щелочные металлы, щелочноземельные металлы, стандартная энтальпия образования
Короткий адрес: https://sciup.org/147160217
IDR: 147160217 | УДК: 548.3+548.314+348.314.5+536.75
Correlation between structure and enthalpy properties of alkaline and alkali-earth metals mеtа- and orthosilicates
Using equations of model of effective ionic radii, metamorphosis of crystalline structures into cubic ones and enthalpies of a crystal lattice on the basis of X-ray and thermodynamic data of alkaline (Na, K), alkaline-earth (Ca, Sr, Ba) metasilicates and alkaline-earth (Ca, Sr, Ba) orthosilicates for the first time calculated standart energy of formation (SiO 2- 3, g), namely 715,65±0,07 kJ·mole -1. For Rb, Cs, Fr, Ra metasilicates and Ra orthosilicates it is estimated their enthalpies of interstructural interactions, enthalpies of crystal lattices and standart energy of formation.
Текст научной статьи Взаимосвязь структурных и энтальпийных характеристик мета- и ортосиликатов щелочных и щелочноземельных металлов
Мантия Земли основана на изверженных силикатных (базальты ~50 % SiO 2 ) и алюмосиликатных (граниты ~70 % SiO 2 , ~15 % Al 2 O 3 ), породах, содержащих их различные минералы, продукты превращений, разрушений до осадочных пород. Это главные источники рудных масс.
Силикаты кристаллизуются во всех семи сингониях в разнообразных структурах. Поэтому возникла необходимость расчета минимального радиуса SiO 2 - как основной анионной структурной единицы. Хотя газообразный силикат-ион – редкость в обычных условиях, но он и его свойства являются ключевым и связующим звеном в цепочке расчетов авторской модели: близкие значения A f H ° ( siO 2 - , г ) , полученные для однотипных силикатов щелочных и щелочноземельных металлов, кристаллизующихся в одинаковых структурах, подтверждают адекватность модели в целом. Проведение подобных расчетов стало возможным в результате использования моделей эффективных ионных радиусов [1] и метаморфозы кристаллических структур в квази-кубическую [2], что показано в работе [3]. Полученные результаты открыли возможность решения интересной и актуальной задачи – расчетов ряда энтальпийных характеристик (энтальпии межструктурного электромагнитного взаимодействия, энтальпии кристаллической решетки, стандартных энтальпий образования (СЭО) веществ и их составляющих) экспериментальное определение которых или затруднено, или невозможно. В свое время это уже было показано на примерах вычислений СЭО 24 однозарядных простых и сложных анионов халькогенов, первого и второго сродства к электрону, уточнений третьего и четвертого потенциалов ионизации редкоземельных металлов и Th–Pu [1]. В соответствии с моделью [1] были выполнены расчеты энтальпии кристаллической решетки для веществ, кристаллизующихся в различных вариантах кубической сингонии. Следующая задача, которая может быть решена – установление взаимосвязи структурных и термических характеристик в веществах, кристаллизующихся в других сингониях.
Результаты расчетов и их обсуждение
По определению энтальпия (разрушения) кристаллической решетки
A р Н ( К y A z ) = y A f H ° ( К z + , г ) + z A f H ° ( A y - , г ) -A f H ° ( К y A z , к ) . (1)
С другой стороны, в соответствии с моделью [1]
А р Н ( К y A z ) = A H о + A H вз . (2)
Здесь АН о = 114,174 z к z а f — энтальпия нуля отсчета, АН вз = 103,7074 А м z к z а Kf 2 Гр1 — энтальпия электромагнитного взаимодействия. Числовые коэффициенты (кДж·моль–1) представляют собой комбинацию фундаментальных физических констант [1]; z К , z А – формальные заряды катиона и аниона соответственно (степень окисления с учетом числа частиц) ; АМ – число Маделунга конечной структуры (квазикубической); K – координационное число катиона; f 1 и f 2 – функции структуры, представляющие собой комбинацию структурных констант исходной ( f исх , «память») и конечной ( f кк , квазикуба) структур; rр – межструктурное расстояние в ячейке квазикуба. Математический аппарат модели, по сути, сводится к совместному решению уравнений (1) и (2). Проиллюстрируем применение модели.
Энтальпийные характеристики метасиликатов щелочных металлов Ме 2 SiO 3 . Силикаты щелочных металлов кристаллизуются в ромбической (Р) сингонии. Исходные данные:
z К = z Me + • n Me + = 1 2 2- z А = z SiO2 - * n SiO2 - 2 1 2'
АМ = АМ (CaF 2 *) = 1,259695; K =6;
f 1 = f p f кк = 73^22- = 1,224745 ** , f 2 = f прим
+ fK = 1 + кк
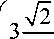
I 2
= 2,5;
А Н 0 = 114,174 * (12 • 2) • (22 * 1) • 1,224745 = 1118,672;
А Н3 = 103,7074 • 1,259695 • 2 • 2 • 6 • 2,5 r - 1 = 7838,3815 r „-1.
вз рр
Тогда окончательно уравнение (2) для соединений типа Me2SiO3 будет выглядеть следующим образом:
А рН = 1118,672 + 7838,3815 rp1.(3)
Для метасиликатов щелочных металлов уравнение (1) примет вид:
А рН (Ме2SiO3 ) = 2 А fH ° (Me+, г)+ А fH ° (siO2-, г )-А fH ° (Ме2SiO3, к).(4)
Решим это уравнение относительно неизвестной величины А f H ° ( siO 2 - , г ) :
АfH° (SiO2-, г)=АрН (Ме2SiO3) - 2 АfH° (Me+, г) + АfH° (Ме2SiO3, к).(5)
Тогда, для метасиликата калия K 2 SiO 3
А fH ° ( SiO 2 - , г ) =А рН ( K2SiO3 ) - 2 А fH ° ( K+, г ) + А fH ° ( K2SiO3, к ) .
Или, используя уравнение (3)
А fH ° ( SiO 2 - , г ) = (1118,672 + 7838,3815 r p -1) - 2 А fH ° ( K + , г ) + А fH ° ( K2SiO3, к ) .
После подставки в уравнение известных справочных данных по K2SiO3 (rр = 3,53796 Å [1]; АfH° (K+, г) = 514,007 Дж молы К [4]; АfH° (K2SiO3, к) = 1590,338 Дж молы К [5]) получим АfH° (SiO2-, г) = 715,831 Дж7молыК. Аналогичные вычисления по данным для метасиликата натрия Na2SiO3 дают значение АfH° (SiO2 , г) = 715,619 Дж/молыК. Средняя величина стандартной энтальпии образования газообразного силикат-иона по результатам двух расчетов составляет 715,725±0,106 Дж/моль·К.
Хорошая согласованность величины A f H ° ( siO 2 - , г ) позволяет использовать ее для других расчетов. В справочной литературе не найдены значения A f H ° ( Ме2SiO з , к ) для метасиликатов рубидия, цезия и франция. Поэтому уравнение (4) для этих соединений решается относительно A fH ° ( Ме2SiO3, к ) :
A fH ° ( Ме2SiO3, к ) = 2 A fH ° ( Me+, г ) + A fH ° ( SiO 2 - , г ) - A рН ( Ме^Ю3 )
с использованием полученного ранее среднего значения A f H ° ( S1O 3 , г ) .
Исходные данные и результаты некоторых расчетов представлены в табл. 1.
Таблица 1
Энтальпийные характеристики метасиликатов щелочных металлов Me 2 SiO 3
|
Ме r (Me+), [1] |
r rр , [1] |
A f H °(Me+, г ), [4] |
- A H °(Me2SiO 3, к ), [5] - A f H °(Me2SiO 3, к ), ур. (4) |
A р Н , ур. (3) |
A f H °(SiO 3 2 - , г ), ур. (5) |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
Na 0,94880 |
3,29400 |
609,542 |
1563,561±5,021 1563,453 |
3498,264 |
715,619 |
|
K 1,33053 |
3,53796 |
514,007 |
1590,338±5,021 1590,444 |
333,183 |
715,831 |
|
Rb 1,48148 |
3,65655 |
490,129 |
– 1566,345 |
3262,328 |
(715,725±0,106) |
|
Cs 1,68161 |
3,82375 |
458,402 |
– 1535,060 |
3168,589 |
(715,725±0,106) |
|
Fr 1,71438 |
3,85194 |
455,235 |
– 1527,395 |
3153,590 |
(715,725±0,106) |
Таким образом, с использованием модели расчета энтальпии кристаллической решетки [1] впервые определена стандартная энтальпия образования частицы SiO 2 - в газообразном состоянии. Вычислены энтальпии электромагнитного взаимодействия A H вз и энтальпии кристаллических решеток A р Н метасиликатов щелочных металлов. Для соединений Me2SiO3, где Ме - это Rb, Cs и Fr, полученные значения A H вз, A р Н и A f H ° ( Ме2SiO3, к ) имеют предсказательный характер.
Энтальпийные характеристики метасиликатов щелочноземельных металлов МеSiO 3 . Метасиликаты щелочноземельных металлов кристаллизуются в различных сингониях. Для исследования выбрана одна из структур моноклинной сингонии, для которой в справочной литературе приведены наиболее полные данные. Методика расчетов необходимых структурных характеристик силикатов подробно изложена в [3]. В расчетах были использованы следующие констан-333
ты: структурная постоянная а =---= 0,487139; за базовую структуру при определении де- баевского радиуса экранирования принята структура сфалерита rD = rD (ZnS) = 17,418081 [1], тогда окончательно дебаевский радиус экранирования rD = 19,051525; функция заряда f (z) = (1 + ^2 • 2 -1) = 2,732051; структурная функция f (c) =
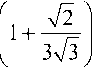
• 2 ( V2 - 1 ) = 0,396631.
Результаты вычислений межструктурных расстояний rр этих силикатов представлены в табл. 2 (колонка 2).
Таблица 2
Энтальпийные характеристики метасиликатов щелочноземельных металлов MeSiO 3
|
Ме r (Me2+), [1] |
rр , [3] |
A H °(Me2+, г ), [6] |
- A H °(MeSiO 3, к ), [6] - A H °(MeSiO 3, к ), ур. (7) |
A p H , ур. (6) |
A H °( 5 iO 2 - , г ), ур. (7) |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
Сa 1,01202 |
3,39721 |
1919,167± ±0,837 |
1633,559±1,674 1633,512 |
4268,282 |
715,556 |
|
Sr 1,15779 |
3,47351 |
1780,677± ±2,092 |
1666,613±2,052 1666,660 |
4162,940 |
715,650 |
|
Ba 1,36361 |
3,61074 |
1653,140± ±1,255 |
1615,948±2,636 1615,948 |
3984,691 |
715,603 |
|
Ra 1,38269 |
3,62467 |
1521,023± ±8,368 |
– 1630,715 |
3967,341 |
(715,603±0,030) |
Для метасиликатов щелочноземельных металлов характерны следующие исходные данные. zК = zА = 2;
А М = А М (CaF 2 ) = 1,259695; K = 6;
f i = Л Л к = • т= 0,288675, f 2 = f ‘ f « = 3V3 • 1 = 5,196152.
1 мкк 2 мкк
Слагаемые уравнения (2) после подстановки:
A H 0 = - 114,174 • (22 • I) • (22 • I) • 0,288675 = -527,347;
AH, = 103,7074 • 1,259695 • 2 • 2 • 6 • 5,196152 rn-1 = 16291,770 r„-1. вз рр
Окончательно уравнение (2) для МеSiO 3 (Ме – щелочноземельные металлы) выглядит:
AрН = -527,347 +16291,770 r-1.(6)
Уравнение (1) применительно к метасиликатам щелочноземельных металлов примет вид:
AрН(МеSiO3)= AfH0(Me2+, г)+ AfH0(SiO32-,г)-AfH0(МеSiO3, к).(7)
С помощью уравнений (6) и (7), используя справочные данные, может быть рассчитана стандартная энтальпия образования СЭО газообразного силикат-иона A f H ° ( siO 2 - , г ) .
Необходимые исходные данные и результаты расчетов по метасиликатам кальция, стронция и бария помещены в табл. 2. По результатам трех вычислении среднее значение A f H ° ( SiO 2 - , г ) составило 715,603±0,030, что хорошо согласуется с величиной, полученной ранее для метасиликатов щелочных металлов (см. табл. 1). Обратным ходом расчета с использованием среднего значения A f H ° ( siO 2 - , г ) получены предсказательные значения СЭО кристаллического метасиликата радия.
Энтальпийные характеристики ортосиликатов щелочноземельных металлов Ме 2 SiO 4 (2МеО·SiO 2 ). Ортосиликаты щелочноземельных металлов кристаллизуются в ромбической сингонии (структура K2SO4, Pnam - 4). Структурные характеристики, необходимые при определении термических констант, получены по методике, изложенной в работе [3]. При проведении 333
расчетов использованы следующие константы. Структурная постоянная а = а р а кк = 8 • —--
= 0,487139. Дебаевский радиус экранирования r D = r°D f ( z ) f ( c )= 14,892723. При этом в качестве базовой принята структура флюорита r°D = r D (CaF2) = 15,418081, что следует из общей формулы К2А. Функция заряда f ( z ) = ( 1 + z К z А - 1 ) = ( 1 + 2 • 2 - 1 ) = 2,732051. Структурная функция f ( c ) = fpf^ = — • ^^ = 0,3535534. Результаты вычислений межструктурных расстояний r 83
ортосиликатов щелочноземельных металлов представлены в табл. 3 (колонка 2).
Таблица 3
Энтальпийные характеристики ортосиликатов щелочноземельных металлов Me 2 SiO 4
|
Ме r (Me2+), [1] |
r р , [3] |
A. / /«Me + г ), [6] |
- A H °(Me2SiO 4, к ), [6] - A H °(Me2SiO 4, к ), ур. (9) |
A р Н, ур. (8) |
A H °( A iO 2 - , г ), ур. (9) |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
Сa 1,01202 |
3,56726 |
1919,167± ±0,837 |
2316,681±4,184 2316,917 |
7939,979 |
715,836 |
|
Sr 1,15779 |
3,61209 |
1780,677± ±2,092 |
2421,156±2,510 2421,143 |
7767,242 |
715,479 |
|
Ba 1,36361 |
3,72040 |
1653,140± ±1,255 |
2275,678±4,602 2276,042 |
7367,054 |
715,968 |
|
Ra 1,38269 |
3,73223 |
1521,023± ±8,368 |
– 2297,974 |
7324,752 |
(715,617±0,236) |
Исходные данные для ортосиликатов щелочноземельных металлов: z К = z А = 2;
АМ = АМ (CaF 2 ) = 1,259695; K = 6;
кк
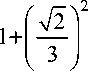
- 1
( SA 1 8
1+- —= 7,917947.
I 9 ) з7з
• 2 = 1,636364, f = f ‘ f ^ = f ‘ f'
2 p кк p тетр
Слагаемые уравнения (2) после подстановки исходных данных:
AH 0 = - 114,174 • (22 • 2) • (22 • 1) • 1,636364 = --978,-67;
A H, = 103,7074 • 1,2-969- • 2 • 2 • 2 • 1 • 6 • 7,917947 r - 1 = 496-1,106 r - 1. вз р р
Окончательно уравнение (2) для Ме 2 SiO 4 (Ме – щелочноземельные металлы):
A pH = - -978,-67 + 496-1,106 r A (8)
Уравнение (1) для ортосиликатов щелочноземельных металлов примет вид:
A pH ( Ме2SiO4 ) = 2 A fH ° ( Me2 + , г ) + A fH ° ( SiO32 - , г ) + A fH ° ( O2 - , г ) - A fH ° ( Ме2SiO4, к ) . (9)
Порядок расчетов рассмотрим на примере Са 2 SiO 4 . Для него r р = 3,56726;
A fH ° ( Са2 + , г ) = 1919,167 [6]; A fH ° ( Са2SiO4, к ) = -2316,681 [6]; A fH ° ( O2 - , г ) = 1069,128 [1].
По уравнению (8) вычислим энтальпию кристаллической решетки:
A pH = - -978,-67 + 496-1,106 • 3,-6726 = 7939,979.
Решим уравнение (9) относительно A f H ° ( S1O 3 , г ) :
A fH ° ( SiO 2 - , г ) =A рН ( Са2SiO4 ) - 2 A fH ° ( Са2 + , г ) - A fH ° ( о2 - , г ) + A fH ° ( Са2SiO4, к ) =
= 7939,979 – 2·1919,167 – 1069,128 – 2316,681 = 715,836.
Аналогичные расчеты проведены для ортосиликатов стронция и бария. Справочные данные и результаты расчетов приведены в табл. 3. По данным колонки 6 получено среднее значение стандартной энтальпии газообразного силикат-иона A f H ° ( siO 2 - , г ) = 71-,617±0,236.
Таким образом, результаты расчетов энтальпийных характеристик ортосиликатов щелочноземельных металлов (см. табл. 3) обнаруживают хорошее согласие величины СЭО силикат-иона в газообразном состоянии с данными, полученными для метасиликатов щелочных и щелочноземельных металлов (см. табл. 1, 2).
Заключение
-
1. Использование уравнений трех моделей: эффективных ионных радиусов, метаморфозы кристаллических структур в квазикубическую и энтальпии кристаллической решетки – позволило впервые рассчитать энтальпийные характеристики метасиликатов щелочных и щелочнозе-
- мельных металлов, ортосиликатов щелочноземельных металлов. Расчеты проведены, опираясь на сведения справочных (академических) изданий по термодинамическим константам и рентгеновским данным по сингониям и структурам веществ.
-
2. По данным для восьми рассмотренных соединений вычислена стандартная энтальпия образования газообразного силикат-иона A f H ° ( siO 2 - , г ) , составившая 715,648±0,067 кДж/моль^К. Это подтверждает предположение о том, что основная анионная составляющая в силикатах находится в форме SiO 2 - .
-
3. Комплексная модель обладает предсказательностью, что позволило вычислить энтальпийные характеристики (энтальпии электромагнитного взаимодействия и энтальпии разрушения кристаллической решетки) и стандартные энтальпии образования метасиликатов рубидия, цезия, франция и радия, а так же ортосиликата радия.
Список литературы Взаимосвязь структурных и энтальпийных характеристик мета- и ортосиликатов щелочных и щелочноземельных металлов
- Рябухин, А.Г. Эффективные ионные радиусы. Энтальпия кристаллической решетки. Энтальпия гидратации ионов: моногр./А.Г. Рябухин. -Челябинск: Изд-во ЮУрГУ, 2000. -115 с.
- Рябухин, А.Г. Математическая модель метаморфизма кристаллических структур в кубическую/А.Г. Рябухин//Вестник ЮУрГУ. Серия «Металлургия». -2007. -Вып. 9. -№ 21(93) -С. 3-6.
- Груба, О.Н. Структурные фрагменты силикатов на основе sp-элементов/О.Н. Груба, Н.В. Германюк, А.Г. Рябухин//Вестник ЮУрГУ. Серия «Химия». -2010. -Вып. 4. -№ 31(207). -С. 90-96.
- Термодинамические свойства индивидуальных веществ: справ. изд. в 4 т./под ред. В.П. Глушко. -М.: Наука, 1982. -Т. IV, кн. 2. -559 с.
- Термические константы веществ: справ: в 10 вып./под ред. В.П. Глушко. -М.: ВИНИТИ АН СССР, 1978. -Вып. 8. -Ч. I. -527 с.
- Термические константы веществ: спр. в 10 вып./под ред. В.П. Глушко. -М.: ВИНИТИ АН СССР, 1979. -Вып. 9. -Ч. I. -574 с.
- Справочник химика/под ред. Б.П. Никольского. -Л.: Химия. -1971. -Т. 1. -1071 с.


