Закономерности сорбции катионов металлов модифицированной корой хвойных древесных пород Сибири
Автор: Семенович А.В., Лоскутов С.Р.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Лесное хозяйство
Статья в выпуске: 1, 2015 года.
Бесплатный доступ
В статье рассматриваются сорбционные свойства модифицированной коры хвойных древесных пород, произрастающих на территории Сибири. Предложен способ утилизации отхода деревообработки (коры), позволяющий получать эффективные сорбенты.
Утилизация коры, модифицирование, сорбция катионов металлов
Короткий адрес: https://sciup.org/14083968
IDR: 14083968 | УДК: 581.6:582.47:674.8
The regularity of the metal cation sorption by the modified bark of Siberian coniferous tree species
The sorption properties of the modified bark of the coniferous tree species growing in the territory of Siberia are considered in the article. The way of the utilization of the woodworking waste(bark) allowing to receive the effective sorbents is offered.
Текст научной статьи Закономерности сорбции катионов металлов модифицированной корой хвойных древесных пород Сибири
|
Номер способа |
Особенности модифицирования |
Образец |
|
1 |
Продолжительность 15 мин, катализатор 0,2 N H 2 SO 4 , температура 50°С |
МКЛ №1, МКС №1, МКП № 1 |
|
2 |
Продолжительность 2 ч, катализатор 0,2 N H 2 SO 4 , температура 50°С |
МКЛ №2, МКС №2, МКП №2 |
|
3 |
Продолжительность 15 мин, катализатор 3 % HNO 3 , температура 50°С |
МКЛ №3, МКС №3, МКП №3 |
|
4 |
Продолжительность 2 ч, катализатор 3 % HNO 3 , температура 50°С |
МКЛ №4, МКС №4, МКП №4 |
Примечание. МКЛ, МКС, МКП – соответственно модифицированная кора лиственницы, сосны и пихты.
Изучение сорбентов проводилось с помощью растровой электронной микроскопии, р ентгенофлуоресцентной спектрометрии, инфракрасной спектроскопии, потенциометрического титрования. Равновесную концентрацию катионов в растворах определяли фотометрическим методом анализа.
Результаты исследований и их обсуждение. Сорбционная способность модифицированной коры по отношению к катионам Cu2+, Zn2+, Co2+, Ca2+ в статических условиях при исходной концентрации катионов в водных растворах 100 и 200 мг/дм3 и отношении «масса сорбента:объём раствора» 1:77, г:см3 варьирует от 1,70 до 21,30 мг/г, степень извлечения достигает 100 % (табл. 2).
Таблица 2
Величина сорбции и степень извлечения катионов металла сорбентами из водно-солевых растворов1
|
Образец |
S e 2, мг/г |
Q, % |
S e , мг/г |
Q, % |
S e , мг/г |
Q, % |
S e , мг/г |
Q , % |
|
Zn (CH 3 COO) 2 |
Ca(CH 3 COO) 2 ⋅ H 2 O |
CuSO 4 |
CoSO 4 ⋅ 7H 2 O |
|||||
|
Модифицированная кора лиственницы |
||||||||
|
МКЛ №1 |
13,4 |
87,1 |
4,2 |
27,3 |
2,2 |
14,3 |
3,7 |
24,0 |
|
МКЛ №2 |
8,4 |
54,6 |
5,1 |
33,1 |
4,1 |
26,6 |
2,6 |
16,9 |
|
МКЛ №3 |
5,8 |
37,7 |
4,4 |
28,6 |
2,7 |
17,5 |
3,2 |
20,8 |
|
МКЛ №4 |
7,7 |
50,0 |
5,3 |
34,4 |
3,1 |
20,1 |
2,7 |
17,5 |
|
Модифицированная кора сосны |
||||||||
|
МКC №1 |
10,1 |
65,5 |
5,3 |
34,4 |
4,2 |
27,3 |
4,3 |
27,9 |
|
МКC №2 |
11,8 |
76,7 |
6,9 |
44,8 |
4,7 |
30,5 |
3,6 |
23,4 |
|
МКC №3 |
10,7 |
69,5 |
3,4 |
22,1 |
4,9 |
31,8 |
4,9 |
31,8 |
|
МКC №4 |
11,3 |
73,4 |
4,6 |
29,9 |
3,9 |
25,3 |
4,4 |
28,6 |
|
Модифицированная кора пихты |
||||||||
|
МКП №1 |
14,7 |
100,0 |
7,9 |
51,3 |
8,0 |
52,0 |
5,3 |
34,4 |
|
МКП №2 |
21,3 |
100,0 |
7,5 |
48,7 |
8,2 |
53,3 |
4,2 |
27,3 |
|
МКП №3 |
14,1 |
100,0 |
7,9 |
51,3 |
9,9 |
64,3 |
5,6 |
36,4 |
|
МКП №4 |
20,4 |
100,0 |
4,9 |
31,8 |
6,5 |
42,2 |
5,5 |
35,7 |
1Приведены результаты, полученные при концентрации катионов металла (Ме2+) в растворе 200 мг/дм3, отношении «масса сорбента:объём раствора» 1:77, г:см3;
Из анализа экспериментальных данных установлено следующее. Модифицированная кора пихты извлекает из водного раствора солей катионы металлов в больших количествах по сравнению с модифицированной корой сосны и лиственницы.
Свойства поверхности коры изменяются и в зависимости от характера обработки. Увеличение продолжительности химического воздействия и последующая термообработка образцов приводит к разным изменениям в структуре сорбентов, что объясняется неоднородностью поверхности модифицированной коры. По влиянию продолжительности модифицирования полученные сорбенты можно разделить на две группы. К первой группе относятся образцы, для которых с увеличением продолжительности модифицирования при использовании одного типа катализатора сорбционная способность возрастает. При сорбции препаратами этой группы катионы сорбируются на активных центрах сорбента, расположенных как на гладких участках, вершинах, так и в порах и углублениях различной формы и размеров. Вторую группу образуют препараты, для которых с увеличением продолжительности модифицирования при использовании одного типа катализатора сорбционная способность, напротив, снижается. При сорбции катионов препаратами данной группы, участки, находящиеся в углублениях поверхности сорбентов, становятся неактивными в отношении сорбции, доступ катионов в глубь материала затрудняется, сорбционная способность сорбентов снижается.
По влиянию типа катализатора, используемого при модифицировании коры на сорбционную способность, сорбенты можно разделить на две группы. В первую группу входят препараты, сорбционная способность которых возрастает при использовании в качестве катализатора азотной кислоты по сравнению с сорбционной способностью препаратов, полученных в присутствии серной кислоты. Во вторую группу входят сорбенты, сорбционная способность которых, напротив, снижается при применении азотной кислоты в качестве катализатора. Мнение зарубежных исследователей по данному вопросу также разделились: использование азотной кислоты приводит к повышению сорбционной способности сорбентов [4] или к ее снижению [1]. Повышенная сорбционная способность модифицированной в присутствии азотной кислоты коры связана с увеличением содержания карбоксильных групп в составе коры после ее модифицирования [5]. Снижение сорбционной способности сорбентов объясняют особенностями взаимодействия серной кислоты с лигнином [6].
Отмечены различия в сорбционной способности сорбентов в зависимости от типа катиона металла. Из водных растворов ацетатов модифицированной корой лучше извлекаются катионы Zn2+, чем катионы Са2+, из сульфатов - катионы Cu2+, чем катионы Со2+, что объясняется физико-химическими характеристиками катионов [7 - 9].
Изотермы сорбции катионов Cu2+ образцами МКЛ №2 и МКС №2 относятся к изотермам L -типа [10] (рис. 1), что позволяет сделать заключение о неспецифическом характере взаимодействия «сорбат-сорбент». Изотерма сорбции образцом МКП №2 имеет S -форму, что указывает на поверхностную адсорбцию катионов в виде цепей и агрегатов.
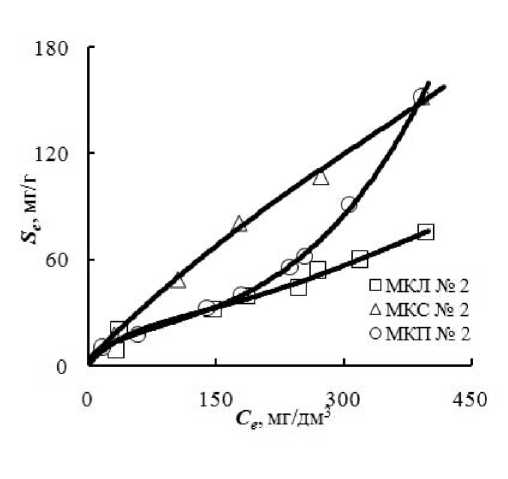
Рис. 1. Изотермы сорбции катионов Cu2+ из раствора модифицированной корой (отношение «масса сорбента:объём раствора» 1:250, г:см3)
Описание изотерм сорбции уравнениями, которым соответствуют модели сорбции, позволило получить информацию о межмолекулярных взаимодействиях «сорбат-сорбент», термодинамических характеристиках сорбционного равновесия, геометрических параметрах сорбента. Оценка пригодности моделей для описания изотерм сорбции и значения сорбционных параметров приведена в табл. 3.
Параметры сорбции катионов Cu2+ модифицированной корой
Таблица 3
|
Уравнение |
Параметр |
МКЛ №2 |
МКС №2 |
МКП №2 |
|
S е , мг/г |
53,74 |
106,70 |
61,53 |
|
|
S уд , м2/г |
280,68 |
557,28 |
321,36 |
|
|
Ленгмюра |
S max , мг/г |
55,25 |
370,37 |
74,62 |
|
b , дм3/мг |
0,01 |
0,001 |
0,009 |
|
|
-AG , кДж/моль |
10,78 |
16,83 |
11,48 |
|
|
R2 |
0,93 |
0,99 |
0,91 |
|
|
R |
0,98 |
0,96 |
0,71 |
|
|
ARS |
0,06 |
0,28 |
0,35 |
|
|
Фрейндлиха |
n |
1,43 |
1,18 |
1,26 |
|
К F , мг/г |
1,06 |
0,96 |
0,83 |
|
|
R2 |
0,89 |
0,99 |
0,90 |
|
|
R |
0,99 |
0,99 |
0,90 |
|
|
ARS |
0,05 |
0,11 |
0,27 |
|
|
Дубинина-Радушкевича |
S D , мг/г |
53,68 |
144,21 |
59,96 |
|
Е , кДж/моль |
3,60 |
3,18 |
4,67 |
|
|
в , моль2кДж -2 |
0,04 |
0,05 |
0,03 |
|
|
Х, нм |
2,78 |
3,14 |
2,14 |
|
|
R2 |
0,83 |
0,78 |
0,59 |
|
|
R |
0,84 |
0,88 |
0,56 |
|
|
ARS |
0,23 |
0,41 |
0,48 |
|
|
Темкина |
A T , дм3/мг |
0,05 |
0,02 |
0,04 |
|
RT/b Т , кДж/моль |
20,99 |
69,17 |
33,56 |
|
|
R2 |
0,86 |
0,87 |
0,58 |
|
|
R |
0,95 |
0,94 |
0,93 |
|
|
ARS |
0,59 |
0,59 |
0,56 |
Примечание. S е – при концентрации Cu2+ в водном растворе 700 мг/дм3 и отношении «масса сорбента:объём раствора» 1:250, г:см3; S уд – удельная поверхность; R2– коэффициент детерминации; R – коэффициент корреляции; ARS – относительная стандартная ошибка среднего; S max – предельная величина адсорбции, мг/г; b - константа равновесия, дм3/мг; AG - энергия Гиббса, кДж/моль [11]; n – коэффициент, отражающий интенсивность адсорбции; K f – константа, представляющая величину адсорбции при С е =1 мг/дм3, мг/г; S D – предельная адсорбция, мг/г; Е – характеристическая энергия адсорбции, кДж/моль; β D – потенциал взаимодействия с адсорбированными катионами, моль2кДж-2; Х – полуширина щелевидной микропоры, нм [12]; A T – константа, дм3/мг; RT/b T – константа, отвечающая максимальной теплоте адсорбции, кДж/моль.
Уравнение Ленгмюра хорошо применимо в области малых и средних степеней заполнения поверхности сорбентов катионами, что позволило вычислить значения предельной адсорбции образцов. Применимость уравнений к приведенным адсорбционным системам снижается в ряду уравнений: Ленгмюра>Фрейндлиха>Темкина>Д-Р. На основании значений параметра b, характеризующего энергию взаимодействия сорбата с поверхностью сорбента получен ряд, показывающий снижение устойчивости сформированных комплексов в зависимости от породы дерева: МКЛ №2 > МКП №2 > МКС №2.
Согласно данным литературы [13], в структуре модифицированной коры (например, в таких соединениях, как флавоноиды, катехины, танниды, антоцианы) присутствуют полидентантные центры сорбции, способные связывать Cu2+ с образованием устойчивых хелатных комплексов. Относительно слабая устойчивость комплексов может быть обусловлена преимущественным взаимодействием катионов с монодентант-ными лигандами сорбента. Подобный тип взаимодействия возможен с карбоксильнокислыми группами уроновых кислот, входящих в состав полисахаридов.
Значения параметра n уравнения Фрейндлиха ( n > 1) при сорбции катионов Cu2+ образцами свидетельствуют о том, что условия для адсорбции более благоприятны при высоких концентрациях катионов Cu2+ в растворе и о слабом взаимодействии между сорбатом и сорбентами. Сравнение величин констант Фрейндлиха K f позволило установить наибольшее сродство катионов Cu2+ к поверхности МКЛ №2.
Удельная поверхность сорбентов S yg для монослойного заполнения катионами Cu2+, рассчитанная с учетом гидратации Cu2+, свидетельствует о развитой поверхности сорбентов. Отрицательные значения энергии Гиббса для всех систем говорят о самопроизвольности протекания извлечения катионов Cu2+ модифицированной корой из водного раствора.
Проверка соответствия изотерм сорбции уравнению Д-Р показала, что в области высоких степеней заполнения сорбентов уравнение хорошо применимо, что свидетельствует о том, что процесс сорбции может протекать в объёме доступных микропор. Отклонение от линейности изотерм сорбции в области малых и средних заполнений может быть обусловлено влиянием малых размеров микропор сорбентов на конкурентную сорбцию Cu2+ и молекул воды.
Механизм взаимодействия катионов Cu2+ с поверхностными группами сорбентов сложен. Результаты определения рН раствора в зависимости от продолжительности контактирования сорбента с сорбатом (рис. 2) свидетельствуют о преобладании ионообменного механизма сорбции в статических условиях.
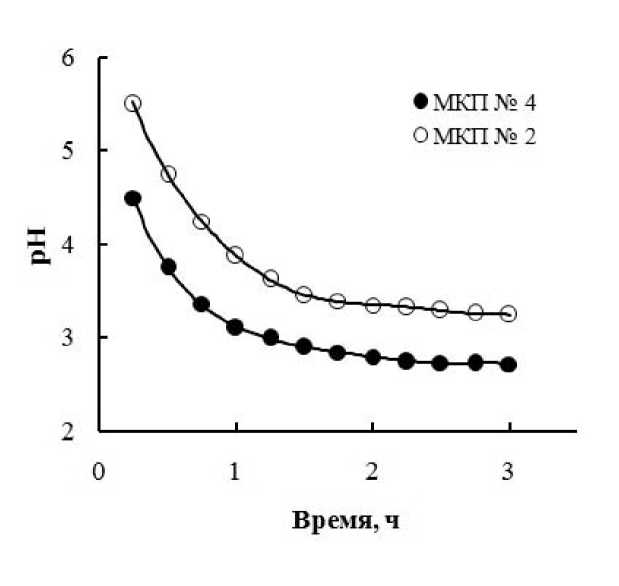
Рис. 2. Изменение рН раствора в процессе сорбции катионов Cu2+ модифицированной корой (концентрация катионов Cu2+ в водном растворе 100 мг/дм3)
Анализ значений теплоты адсорбции, рассчитанной по уравнениям (Е, RT/Ьт, A G), свидетельствует о влиянии на ионный обмен физической адсорбции катионов на поверхности сорбентов, специфического меж- молекулярного взаимодействия за счет образования водородных и ионных связей и неспецифического межмолекулярного взаимодействия.
Заключение . Модифицированная кора лиственницы сибирской, сосны обыкновенной и пихты сибирской - эффективный сорбент для извлечения катионов Cu2+, Zn2+, Co2+, Ca2+ из водных растворов. Степень извлечения катионов металлов модифицированной корой может достигать 100 %. Существенное влияние на сорбционную способность сорбентов оказывают продолжительность химического воздействия, тип катализатора, физико-химические характеристики катиона металла, концентрация катионов в растворе, отношение «масса сорбента:объём раствора». Максимальная сорбционная способность сорбента по отношению к катионам Zn2+ (до 21,30 мг/г) проявляется при применении к коре способа обработки №2, по отношению к катионам Cu2+, Co2+, Ca2+ - № 3 (до 9,90 мг/г).
Механизм взаимодействия Cu2+ с поверхностными группами сорбентов включает ионный обмен, физическую адсорбцию на поверхности сорбентов, специфическое межмолекулярное взаимодействие за счет образования водородных, ионных связей и неспецифического межмолекулярного взаимодействия. Выявленные закономерности сорбции катионов металлов модифицированной корой хвойных пород Сибири могут служить основой для разработки технологических процессов очистки сточных вод от катионов металлов при помощи полученных сорбентов.


