Защита миокарда от ишемически-реперфузионного повреждения посредством подачи оксида азота в контур экстракорпоральной циркуляции при проведении искусственного кровообращения
Автор: Каменщиков Николай Олегович, Мандель И.А., Подоксенов Ю.К., Михеев С.Л., Семенцов А.С., Маслов Л.Н., Козлов Б.Н., Шипулин В.М.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Экспериментальные статьи
Статья в выпуске: 4 т.21, 2017 года.
Бесплатный доступ
Цель Изучение эффективности подачи оксида азота в контур экстракорпоральной циркуляции для защиты миокарда от ишемически-реперфузионного повреждения при моделировании острого инфаркта миокарда в условиях нормотермического искусственного кровообращения в эксперименте. Методы В условиях сбалансированной анестезии, искусственных вентиляции легких и кровообращения была смоделирована острая ишемия с последующей реперфузией миокарда у кроликов (n = 20). Эксперимент включал окклюзию левой коронарной артерии путем пережатия лигатурой на 45 мин с последующей реперфузией в течение 120 мин на фоне искусственного кровообращения. Все животные были разделены на 2 равные группы: 10 кроликам проводилась подача оксида азота в контур экстракорпоральной циркуляции в дозе 40 ppm (основная группа); 10 кроликов составили контрольную группу, доставка оксида азота им не выполнялась. Определяли отношение зоны инфаркта к области риска, оценивали количество и характер желудочковых аритмий, темп диуреза. Результаты Подача оксида азота в контур экстракорпоральной циркуляции при искусственном кровообращении оказывает выраженное инфаркт-лимитирующее действие, проявляющееся в снижении отношения зоны инфаркта к области риска на 15%, р = 0,0002. В периоды ишемии и реперфузии статистически значимое меньшее количество политопных и полиморфных желудочковых экстрасистол наблюдали в основной группе (р = 0,003 и р = 0,012). Выявлено статистически значимое снижение веноартериального градиента парциального давления углекислого газа в основной группе. снижение веноартериального градиента pCO2 в основной группе было ассоциировано со значимым повышением темпа мочеотделения во время искусственного кровообращения, который составил 1,4 [1,3; 1,5] мл/кг/ч в основной группе и 1,15 [1; 1,3] мл/кг/ч в контрольной группе, p = 0,013. Выводы Полученные в ходе эксперимента данные свидетельствуют о кардиопротективных свойствах оксида азота при его подаче в контур экстракорпоральной циркуляции при моделировании ишемически-реперфузионного повреждения миокарда в виде снижения отношения зоны инфаркта к области риска на 15%, меньшего количества аритмий, а также улучшения тканевой перфузии во время искусственного кровообращения. Интраоперационная органопротекция миокарда оксидом азота у больных, оперированных в условиях искусственного кровообращения, должна стать объектом дальнейших клинических исследований.
Защита миокарда, прекондиционирование, ишемически-реперфузионное повреждение, оксид азота
Короткий адрес: https://sciup.org/142230641
IDR: 142230641
Myocardium protection against ischemic-reperfusion injury by nitric oxide supplied to the extracorporeal circulation line during cardiopulmonary bypass (experimental study)
Aim. The study was designed to assess the efficiency of exogenous nitric oxide supply to the extracorporeal circulation line for myocardial protection against ischemic-reperfusion injury in acute myocardial infarction simulation during cardiopulmonary bypass (CPB) in the experiment. Methods. Acute ischemia was simulated in rabbits (n = 20) with subsequent myocardial reperfusion. All animals were anesthetized and mechanically ventilated through a nasotracheal tube. The experiment included occlusion of the left coronary artery by its clamping with a ligature for 45 min with subsequent reperfusion for 120 min during CPB. All animals were divided into 2 equal groups: 10 rabbits received nitric oxide supply to the extracorporeal circulation line in a dose of 40 ppm throughout the entire CPB period (the main group); 10 rabbits made up the control group. The ratio of the infarction area to the risk area was determined, and the quantity and nature of ventricular arrhythmias were accessed. results. It was established that nitric oxide supply through the extracorporeal circulation line during CPB had a pronounced infarct-limiting effect, the infarct area to the risk area ratio decreased by 15% as compared to the control group, p = 0.0002. There was also a significant antiarrhythmic effect. A lesser quantity of polytopic and polymorphic ventricular extrasystoles were observed in the main group during periods of ischemia and reperfusion (p = 0.003 and p = 0.012). A statistically significant decrease in the venoarterial gradient of the partial pressure of carbon dioxide in the main group was associated with an increase in the urine flow rate amounting to 1.4 [1.3; 1.5] ml/kg/h in the main group and 1.15 [1; 1.3] ml/kg/h in the control group, p = 0.013. Conclusion. The data obtained during the experiment demonstrate the presence of cardioprotective properties of nitric oxide delivered to the extracorporeal circulation line when simulating myocardial ischemic-reperfusion injury. These properties manifest themselves as a 15% decrease of the infarction zone-risk area ratio, a fewer number of arrhythmias and improvement of tissue perfusion during CPB. Intraoperative myocardial protection by nitric oxide in patients operated with CPB should be the object of further clinical research.
Текст научной статьи Защита миокарда от ишемически-реперфузионного повреждения посредством подачи оксида азота в контур экстракорпоральной циркуляции при проведении искусственного кровообращения
Кардиохирургическое вмешательство, выполненное в условиях искусственного кровообращения (ИК), сопровождается разнонаправленными изменениями на всех уровнях нервно-рефлекторной регуляции, гуморальной активности и метаболического статуса [1]. Интраоперационная защита органов и тканей, в частности миокарда, по-прежнему остается одним из нерешенных вопросов кардиоанестезиологии. Частота миокардиальной дисфункции в раннем послеоперационном периоде колеблется от 3 до 30% случаев [3] и обусловлена сложным взаимодействием разнообразных механизмов, включающих особый режим обменных процессов в миокарде, свободно-радикальное повреждение, ионный парадокс и эндотелиальную дисфункцию [4].
Одним из перспективных направлений является реализация клинических эффектов феномена прекондиционирования [5, 6]. Ишемическое и фармакологическое прекондиционирование представляет собой эффективный способ повышения резистентности организма к повреждающим воздействиям [7–11]. Однако у больных кардиологического профиля, ввиду возможного усугубления симптомов и сниженных резервов миокарда для защиты сердца от интраоперационной ишемии и реперфузии, наиболее подходящим и безопасным считается фармакологически индуцированное прекондиционирование [12]. При этом в качестве триггера адаптации сердца к ишемически-реперфузионно-му повреждению может выступать оксид азота (NO), запускающий инфаркт-лимитирующее действие через активацию сGMP (циклический гуанозинмонофосфат)-зависимой протеинкиназы G и образование свободных радикалов [13–16]. Стимуляция синтеза NO также играет ключевую роль и в опосредовании феномена эндогенной органопротекции, выступая медиатором поздней фазы цитопротективных эффектов [17].
Цель исследования: изучить эффективность подачи NO в контур экстракорпоральной циркуляции для защиты миокарда от ишемически-реперфузионного повреждения при моделировании острого инфаркта миокарда в условиях искусственного кровообращения.
Методы
Проспективное экспериментальное исследование проводили на 20 кроликах-самцах породы «Советская шиншилла» массой 3–3,5 кг. Все животные были разделены на 2 равные группы: 10 кроликам проводилась подача NO в контур экстракорпоральной циркуляции в дозе 40
ppm на протяжении всего периода ИК (основная группа); 10 кроликов составили контрольную группу. Животных содержали в условиях конвенционального вивария. Все болезненные процедуры и выведение животных из эксперимента осуществляли на наркотизированных животных согласно приказу Минздрава №199н «Об утверждении правил надлежащей лабораторной практики» от 1 апреля 2016 г., Принципам надлежащей лабораторной практики ГОСТ 33044-2014 и руководству Janet C. Garber, Guide for the Care and Use of Laboratory Animals: Eighth Edition National Research Council, 2011.
Эксперимент начинали с масочной индукции анестезии севофлураном. По достижении целевого уровня анестезии выполняли ретроградную интубацию трахеи по разработанной нами методике эндотрахеаль-ной трубкой № 2,5 (патент № 2611955 от 1 марта 2017 г.), животное фиксировали в положении лежа на спине. Искусственную вентиляцию легких проводили с помощью аппарата искусственной вентиляции легких Puritan Bennett 760 (США) с дыхательным объемом 30–40 мл, частотой дыхательных движений 50–55 в минуту в режиме Controlled Mandatory Ventilation (CMV) с управляемым объемом. Поддержание анестезии обеспечивали севофлураном 1,2–1,5 об% через испаритель Vapor 2000 (Drager, Германия). Использовали стандартный мониторинг анестезии, включавший непрерывный анализ электрокардиографии, инвазивный мониторинг артериального давления, пульсоксиметрию, термометрию с помощью монитора Siemens 7000 (Германия), учет темпа мочеотделения. Для инвазивного измерения артериального давления и забора крови для лабораторного анализа канюлировали бедренную артерию катетером 20G. Для инфузионной терапии канюлировали бедренную вену катетером 20G. Температурный датчик устанавливали в пищевод. Мониторировали показатели сатурации артериальной крови SаО2, сатурации венозной крови из контура искусственного кровообращения SvO2, веноартериальный градиент pCO2, уровень лактата, рассчитывали индекс экстракции кислорода O2EI, а также контролировали кислотно-щелочное состояние крови. Газовый состав крови определяли на приборе STAT PROFILE Critical Care Xpress (Nova Biomedical, США). Забор крови проводили на этапах: до ИК, начало ИК, 45 мин ишемии миокарда, 45 мин реперфузии миокарда, 90 мин реперфузии, 120 мин реперфузии. Также с помощью данного газоанализатора методом отражающей фотометрии контролировали уровень метгемоглобина. Для проведения ИК использовали роликовый насос НПМ-1, неонаталь-
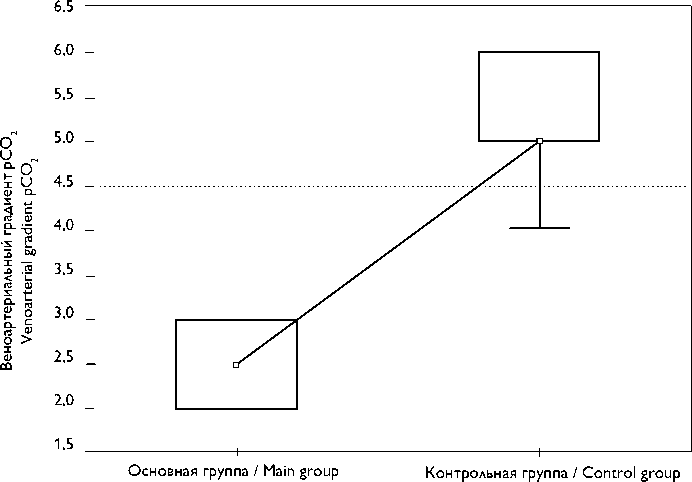
Рис. 1. Веноартериальный градиент pCO2, 45 мин ишемии, данные представлены как Ме [25; 75]; p = 0,0001
Fig. 1. Venoarterial gradient pCO2, 45 min ischemia, data are presented as Me [25; 75]; p = 0.0001
ный оксигенатор Kids D100 (Dideco, Италия). Площадь поверхности тела кролика считали равной 0,25 м2. ИК осуществляли в непульсирующем режиме, в условиях нормотермии. Подключение аппарата искусственного кровообращения осуществляли по принятой методике по схеме «аорта – правое предсердие». Перфузионный индекс составлял 1,8 л/мин/м2. Вазоактивные препараты в обеих группах не применяли. В исследуемой группе в магистраль подачи газо-воздушной смеси в асептических условиях встраивали дополнительную линию для доставки NO. Коннектор линии доставки NO был максимально приближен к оксигенатору аппарата ИК и имел бактериальный фильтр. После достижения расчетной объемной скорости перфузии осуществляли подачу NO в контур экстракорпоральной циркуляции в дозе 40 ppm. Дозирование NO осуществляли с помощью анализатора PrinterNOX (CareFusion, США). Затем проводили окклюзию левой коронарной артерии путем пережатия лигатурой на 45 мин с последующей реперфузией в течение 120 мин на фоне ИК. При этом протокол инсуффляции NO сохраняли без изменений на протяжении всего периода искусственного кровообращения.
В группе контроля подачу NO в контур аппарата ИК не проводили. Эксперимент включал окклюзию левой коронарной артерии в течение 45 мин с последующей реперфузией в течение 120 мин в условиях искусственного кровообращения.
Нарушения ритма за период коронароокклюзии регистрировали в первые 10 мин (фаза 1) и последующие 35 мин (фаза 2), поскольку механизмы возникновения аритмий в эти периоды различаются. Фаза 3 — первые 45 мин реперфузии. В фазу 1 нарушения ритма возникают по механизму reentry, в фазу ишемии 2 и при реперфузии — как по механизму reentry, так и при участии эктопического автоматизма [2].
Измерение отношения зоны инфаркта (ЗИ) к области риска (ОР) проводили с помощью модифицированного метода, предложенного J. Neckar [18]. Для определения области риска (гипоперфузии) лигатуру повторно затягивали, сердце окрашивали 5% раствором перманганата калия, который вводили через аортальную канюлю. Сердце извлекали из грудной полости, удаляли правый желудочек и готовили срезы толщиной 1 мм, которые делали строго перпендикулярно продольной оси сердца, используя слайсер HSRABBIT002-1 (Zivic Instruments, Pittsburgh, США)). Срезы сканировали с обеих сторон с помощью HP Scanjet G4050 (Hewlett-Packard, Palo Alto, США) с высоким разрешением (2400 dpi). В области гипоперфузии разграничивали зоны, в которых ткани миокарда подверглись некрозу. Величину ЗИ и ОР определяли
Основная группа / Main group
Контрольная группа / Control group
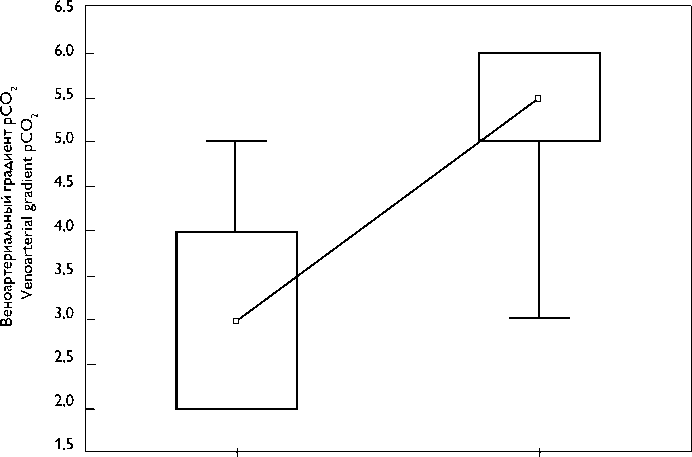
Рис. 2. Веноартериальный градиент pCO2, 45 мин реперфузии, p = 0,0016; данные представлены как Ме [25; 75]
Fig. 2. Venoarterial gradient pCO2, 45 min reperfusion, p = 0.0016; data are presented as Me [25; 75]
компьютеризированным планиметрическим методом, используя оригинальное программное обеспечение. Метод компьютерной планиметрии применяли для измерения общей площади срезов, суммарной площади зоны инфаркта и области риска для каждого сердца в отдельности. Измерение осуществляли с помощью программного обеспечения для анализа изображений ImageJ2 [19]. Величину очага инфаркта выражали в виде процентного соотношения зоны инфаркта к размеру области риска (ЗИ/ОР).
Статистический анализ
Статистический анализ полученных данных был проведен в программе Statistica 10.0 (StatSoft). Количественные значения выражали как медиану 25-го и 75-го процентилей (Me [25; 75]). Сравнение количественных характеристик проводили с помощью U-критерия Манна – Уитни (для независимых переменных) и T-критерия Уилкоксона (для зависимых переменных). Различия между группами в частоте возникновения желудочковых аритмий оценивали с помощью критерия хи-квадрат. Различия считали статистически значимыми при p<0,05.
Результаты
У животных обеих групп в течение эксперимента были стабильные показатели метаболизма, кислотноосновной состав крови и ионнограмма: рН, уровни бу- ферных оснований, концентрация лактата, глюкозы, ионов натрия, калия и кальция — находились в пределах референтных значений. При анализе межгрупповых различий отмечено значимое снижение веноартериального градиента pCO2 на этапе 45 мин ишемии (рис. 1), р = 0,0001, и на этапе 45 мин реперфузии, p = 0,0016 (рис. 2).
Снижение веноартериального градиента pCO2 в основной группе было ассоциировано со значимым повышением темпа мочеотделения во время ИК, который составил 1,4 [1,3; 1,5] мл/кг/ч в основной группе и 1,15 [1; 1,3] мл/кг/ч в контрольной, p = 0,013 (рис. 3).
В первые 10 мин ишемии миокарда в основной группе политопные и полиморфные желудочковые экстрасистолы (ЖЭС) наблюдали значимо реже, р = 0,003. В группе контроля чаще отмечены политопные и полиморфные ЖЭС; фибрилляция желудочков развилась у одного животного. В последующие 35 мин ишемии в основной группе животных наблюдали большую электрическую стабильность миокарда, по сравнению с контрольной, р = 0,001. В период реперфузии наблюдали различные виды желудочковых аритмий, статистически значимо меньшее количество политопных и полиморфных ЖЭС наблюдалось в группе NO-протекции, р = 0,012. Фибрилляция желудочков на этапе реперфузии развилась у 4 животных контрольной группы, в основ-
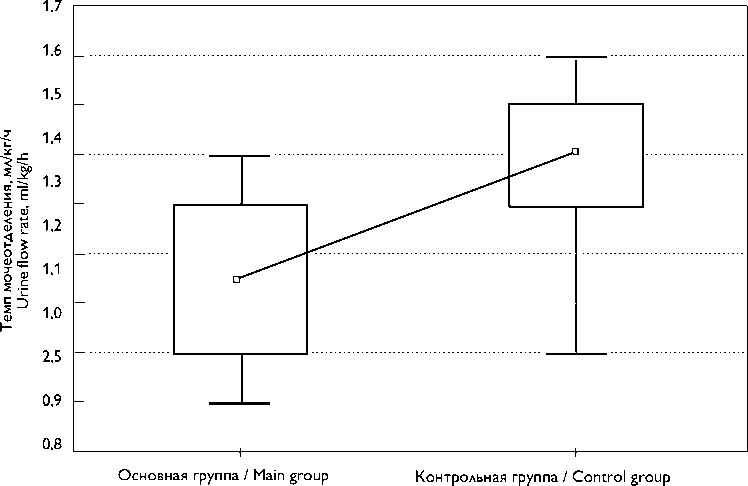
Рис. 3. Темп мочеотделения, мл/кг/ч; p = 0,013
Fig. 3. Urine flow rate, ml/kg/h; p = 0.013
ной группе фибрилляция желудочков не зарегистрирована, р = 0,04 ( таблица ).
Соотношение ЗИ/ОР в основной группе составило 55,6 [50; 61] %, что меньше на 15%, чем у животных контрольной группы — 69,9 [68; 73] %, p = 0,0002 (рис. 4).
Обсуждение
Известно, что NO участвует в реализации различных защитных эффектов адаптации через изменение функционального состояния митохондрий. Возможные механизмы органопротективного действия включают каскады внутриклеточных трансмиттеров с активацией КАТФ-каналов и ингибированием митохондриальных проводящих пор как конечных эффекторов прекондиционирования и снижения повреждения митохондрий при гипоксии/аноксии. Опосредованное NO-угнетение адренергической стимуляции и сократимости с сохранением эндотелий-зависимой вазодилатации и снижением кальциевой перегрузки клеток ведет к уменьшению феномена no-reflow. В исследовании у грызунов установлено, что ингаляция оксида азота приводит к быстрому накоплению метаболитов NO в крови и тканях, способс-
Влияние доставки NO в контур искусственного кровообращения на частоту возникновения аритмий на этапах ишемии и реперфузии
|
Фаза |
Вид нарушения сердечного ритма |
Основная группа, n (%) |
Контрольная группа, n (%) |
p |
|
10 мин ишемии |
нет аритмий либо редкие монотопные ЖЭС |
5 (50) |
6 (60) |
0,5 |
|
10 мин ишемии |
политопные и полиморфные ЖЭС |
2 (20) |
9 (90) |
0,003 |
|
10 мин ишемии |
фибрилляция желудочков |
0 |
1 (10) |
0,5 |
|
35 мин ишемии |
нет аритмий либо редкие монотопные ЖЭС |
5 (50) |
6 (60) |
0,5 |
|
35 мин ишемии |
политопные и полиморфные ЖЭС |
1 (10) |
7 (70) |
0,001 |
|
35 мин ишемии |
фибрилляция желудочков |
1 (10) |
1 (10) |
1 |
|
45 мин реперфузии |
нет аритмий либо редкие монотопные ЖЭС |
5 (50) |
4 (40) |
0,5 |
|
45 мин реперфузии |
политопные и полиморфные ЖЭС |
2 (20) |
8 (80) |
0,012 |
|
45 мин реперфузии |
фибрилляция желудочков |
0 |
4 (40) |
0,04 |
Примечание. ЖЭС — желудочковые экстрасистолы, применен критерий χ 2 Пирсона
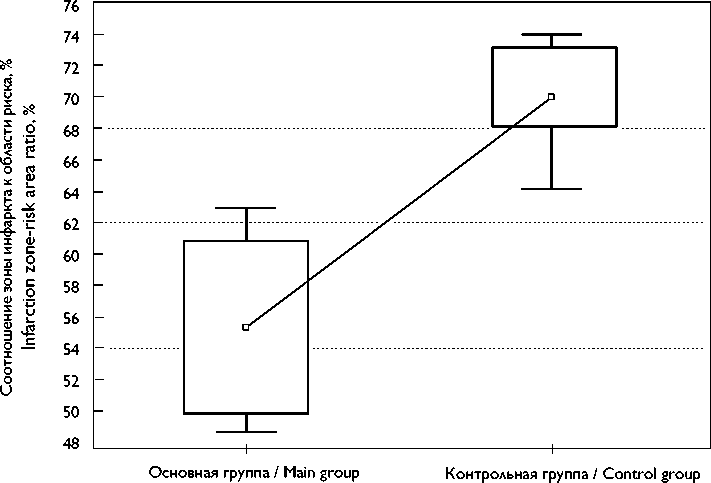
Рис. 4. Соотношение зоны инфаркта к области риска, данные представлены в % как Ме [25; 75], использован критерий Манна – Уитни; p = 0,0002
Fig. 4. Infarction zone-risk area ratio, the data are presented in % as Me [25; 75], Mann – Whitney test was used; p = 0.0002
твуя кардиопротекции при ишемически-реперфузион-ном повреждении и уменьшению ЗИ/ОР на 31% [20, 21].
Полученные нами данные также свидетельствуют о кардиопротективных свойствах NO при его подаче в контур экстракорпоральной циркуляции при моделировании ишемически-реперфузионного повреждения миокарда. Выявлен инфаркт-лимитирующий эффект со снижением ЗИ/ОР на 15% по сравнению с контрольной группой, а также антиаритмическое действие.
Кардиохирургические пациенты имеют повышенный риск острого повреждения почек и желудочно-кишечного тракта, особенно при необходимости сочетанной операции [22]. Развитие гемолиза вследствие длительного ИК и применения компонентов донорской крови, а также ограничение NO-биодоступности приводят к расстройствам микроциркуляции и системным аберрациям органного кровотока [23].
В исследованиях последних лет доказана безопасность применения оксида азота в течение 24 ч, а также не-фропротективное действие оксида азота, примененного во время ИК и в течение 24 ч после ИК в виде ингаляции, которое проявлялось в снижении развития острого почечного повреждения после кардиохирургических операций в условиях длительного перфузионного периода [24].
По нашим данным, снижение веноартериального градиента pCO2 в основной группе было ассоциировано со значимым повышением темпа мочеотделения во время ИК, что указывает на более выгодный режим кровообращения в органах спланхнического бассейна, в том числе почек во время ИК. Определение оптимального режима дозирования требует дальнейшего изучения.
Выводы
Полученные в ходе эксперимента данные свидетельствуют о кардиопротективных свойствах оксида азота при его подаче в контур экстракорпоральной циркуляции при моделировании ишемически-реперфузионно-го повреждения миокарда в виде снижения ЗИ/ОР на 15%, меньшего количества аритмий. Доставка оксида азота в контур экстракорпоральной циркуляции также приводит к улучшению тканевой перфузии во время искусственного кровообращения. Интраоперационная органопротекция миокарда оксидом азота у больных, оперированных в условиях ИК, должна стать объектом дальнейших клинических исследований.
Финансирование
Исследование не имело спонсорской поддержки.
Список литературы Защита миокарда от ишемически-реперфузионного повреждения посредством подачи оксида азота в контур экстракорпоральной циркуляции при проведении искусственного кровообращения
- Караськов А.М., Аомиворотов В.В. Биохимическая адаптация организма после кардиохирургических вмешательств. Новосибирск: Академическое издательство «Гео», 2004. 288 c.
- Маслов А.Н., Аишманов Ю.Б., Крылатов А.В., Семенцов А.С., Портниченко А.Г., Подоксёнов Ю.К., Халиулин И.Г. Сравнительный анализ кардиопротекторной и антиаритмической эффективности раннего и позднего гипоксического прекондиционирования. Бюллетень экспериментальной биологии и медицины. 2013;156(12):705-708. Режим доступа: http://www. iramn.ru/journal/bebm/2013/bbm1312.htm
- Yau J.M., Alexander J.H., Hafley G., Mahaffey K.W., Mack M.J., Kouchoukos N., Goyal A., Peterson E.D., Gibson C.M., Califf R.M., Harrington R.A., Ferguson T.B.; PREVENT IV Investigators. Impact of perioperative myocardial infarction on angiographic and clinical outcomes following coronary artery bypass grafting (from PRoject of Ex-vivo Vein graft ENgineering via Transfection [PREVENT] IV). Am J Cardiol. 2008;102(5):546-51. PMID: 18721510. https://doi. org/ DOI: 10.1016/j.amjcard.2008.04.069
- Carden D.L, Granger D.N. Pathophysiology of ischaemia- reperfusion injury. J Pathol. 2000;190(3):255-66. PMID: 10685060. - PATH526>3.0.CO;2-6 DOI: 10.1002/(SICI)1096-9896(200002)190:3
- Murry C.E., Jennings R.B., Reimer K.A. Preconditioning with ischemia: a delay of lethal cell injury in ischemic myocardium. Circulation. 1986;74(5):1124-36. PMID: 3769170. https://doi. org/ DOI: 10.1161/01.CIR.74.5.1124


