Зависимость ангиогенного эффекта амниотической мембраны от способа ее обработки
Автор: Кучук К.Е., Новиков И.В., Волова Л.Т., Милюдин Е.С., Колсанов А.В.
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 1 т.34, 2026 года.
Бесплатный доступ
ЦЕЛЬ: изучение влияния физических методов децеллюляризации и предварительной обработки глицерином на морфологическую структуру и биологические свойства лиофилизированной амниотической мембраны. МАТЕРИАЛЫ И МЕТОДЫ. Исследованию подвергнуты две группы фрагментов человеческой амниотической мембраны. В ходе предварительной обработки первая группа фрагментов биоматериала помещалась на 20 минут в 10% раствор глицерина, фрагменты второй группы не обрабатывались глицерином. Далее производилась обработка в течение 15 минут ультразвуком с частотой 35±10% кГц и лиофилизация.Биологические свойства оценивались по результатам изучения протеомного состава консервированной амниотической мембраны и экспериментального исследования на лабораторных животных. Морфологические исследования выполнялись с использованием светового микроскопа и растрового электронного микроскопа JEOLJSM-6390 A Analysis Station (Япония). РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ. Определена деструкция эпителиальных клеток и слущивание эпителиального слоя, более выраженного на препаратах амниотической мембраны, не обработанной глицерином, стромальные слои уплощены. Разнонаправленные волокна придают объемную структуру. На препаратах амниотической мембраны лиофилизированной после предварительного пропитывания глицерином определяются гомогенные бесструктурные субстраты, прикрепленные гроздями и формирующие древовидную форму. При изучении результатов протеомного состава определено большее количество индукторов ангиогенеза во фрагментах амниотической мембраны не обработанной глицерином. В области имплантации фрагментов биоматериала, не обработанного глицерином, отмечается большее количество тучных клеток, выраженный неоангиогенез. ЗАКЛЮЧЕНИЕ. Физические методы децеллюляризации и консервации позволяют сохранить анатомическую структуру и белковые соединения, определяющие биологическую активность амниотической мембраны. Обработка биоматериала глицерином децеллюляризованной лиофилизированной амниотической мембраны способствует сохранению в структуре ткани разных по составу белковых соединений, определяющих биологическую активность. Биоматериал, не пропитанный глицерином, имеет в составе большее количество протеинов, способствует большей клеточной инфильтрации и активизирует неоангиогенез. Напротив, амниотическая мембрана, предварительно обработанная глицерином, не вызывает выраженной воспалительной реакции и не приводит к развитию вновь образованных сосудов.
Амниотическая мембрана, децеллюляризация, обработка глицерином, обработка ультразвуком, лио-филизация, протеомное исследование, морфологическое исследование, ангиогенный эффект
Короткий адрес: https://sciup.org/143185637
IDR: 143185637 | УДК: 611.013.85+615.361+616-089.843 | DOI: 10.20340/mv-mn.2026.34(1).999
Dependence of the angiogenic effect of the amniotic membrane on the method of its processing
AIM: to investigate the effect of physical decellularization methods and glycerol pretreatment on the morphological structure and biological properties of lyophilized amniotic membrane. MATERIALS AND METHODS. Two groups of human amniotic membrane fragments were studied. During pretreatment, fragments of the first group were immersed for 20 minutes in a 10% glycerol solution, while fragments of the second group received no glycerol treatment. Both groups were subsequently subjected to ultrasonic processing at a frequency of 35±10% kHz for 15 minutes, followed by lyophilization. Biological properties were assessed based on proteomic analysis of the preserved amniotic membrane and experimental studies in laboratory animals. Morphological examination was performed using light microscopy and a JEOL JSM-6390A Analysis Station scanning electron microscope (Japan). RESULTS AND DISCUSSION. Destruction of epithelial cells and desquamation of the epithelial layer were identified, both more pronounced in amniotic membrane specimens not pretreated with glycerol; the stromal layers were flattened. Multidirectional fibers confer a three-dimensional architecture. In specimens of amniotic membrane lyophilized after glycerol impregnation, homogeneous, structureless substrates attached in clusters and forming a tree-like configuration were observed. Proteomic analysis revealed a greater number of angiogenesis inducers in amniotic membrane fragments not pretreated with glycerol. At the implantation site of biomaterial fragments not treated with glycerol, a greater number of mast cells and pronounced neoangiogenesis were noted. CONCLUSION. Physical decellularization and preservation methods allow the anatomical structure and protein compounds that determine the biological activity of the amniotic membrane to be maintained. Glycerol treatment of decellularized lyophilized amniotic membrane promotes the retention of diverse protein compounds within the tissue structure, thereby sustaining its biological activity. Biomaterial not impregnated with glycerol contains a greater number of proteins, promotes greater cellular infiltration, and activates neoangiogenesis. By contrast, amniotic membrane pretreated with glycerol does not elicit a pronounced inflammatory response and does not lead to the formation of newly formed vessels.
Текст научной статьи Зависимость ангиогенного эффекта амниотической мембраны от способа ее обработки
(1).999
(1).999
Kuchuk KE, Novikov IV, Volova LT, Milyudin ES, Kolsanov AV. Dependence of the angiogenic effect of the amniotic membrane on the method of its processing. Morfologicheskie Vedomosti – Morphological newsletter. 2026;34(1):999. (1).999
В регенеративной медицине широко применяется один из уникальнейших биоматериалов – амниотическая мембрана, образованная монослоем эпителиальных клеток на базальной мембране и стромы, состоящей из трех слоев. Содержащиеся во всех слоях амниотической мембраны биологически активные вещества обеспечивают активацию регенераторных процессов, пролифе- рацию клеток и ускоряют их миграцию [1, 2]. При создании тканеинженерных комплексов исследователи предпочитают децеллюляризованную амниотическую мембрану в качестве биологической подложки для культивированных клеток. Децеллюляризация – это процесс, направленный на удаление клеток из ткани с сохранением в ней матрикса и трехмерности структуры [3], с использованием различных методов воздействия.
Все методы можно разделить на три типа – физические, химические и биологические.
Физический метод присутствует в большинстве протоколов. Это в основном ротаторы, шейкеры или камеры прямой перфузии, позволяющие ускорить процесс обмена жидкости, воздействующей на клеточные мембраны и разрушающей ядра клеток. Но чаще всего используются химические методы, в частности, анионное поверхностно-активное вещество додецилсульфат натрия, характеризующейся способностью денатурировать белки и растворять клеточные мембраны. Также используются и органические кислоты, в частности, периуксусная кислота, которая разрушает и удаляет нуклеиновые кислоты. Возможно использование для де-целлюляризации биоматериала спиртов и хелатирующих агентов [4, 5, 6].
Наиболее простым физическим методом де-целлюляризации является метод многократного замораживания и оттаивания, при котором происходит разрушение мембран кристаллами льда, и соответственно потеря жизнеспособности клеток. К физическим методам можно также отнести погружение в гипертонический раствор, что приводит к осмотическому стрессу и соответственно повреждению мембран клеток [5, 6]. Наиболее эффективным физическим методом децеллюля-ризации является метод ультразвукового воздействия, поскольку высокая эффективность повреждения клеточных структур дополняется еще и очищением от клеточного мусора [7].
Однако исследователи, предпочитающие использовать децеллюляризованную консервированную амниотическую мембрану высказывают сомнение в отношении сохранности в ней биологически активных свойств и считают необходимым проведение дополнительных исследований [8, 9, 10].
Основываясь на опыте Самарского тканевого банка нами разработан метод обработки и лиофилизации амниотической мембраны, в котором используются физические методы децел-люляризации и особый режим сублимационной сушки [11].
ЦЕЛЬ ИССЛЕДОВАНИЯ: изучение влияния физических методов децеллюляризации и предварительной обработки глицерином на морфологическую структуру и биологические свойства лиофилизированной амниотической мембраны.
МАТЕРИАЛ И МЕТОДЫ
Исследованию подвергнута человеческая амниотическая мембрана, поступившая в тканевой банк от одного донора. Она была механически отделена от хориона и отмывалась от сгустков крови в физиологическом растворе (0,9% раствор NaCl, pH 5–7,5) не менее 30 минут. Далее фрагменты донорского биоматериалабыли распределены на две группы. В ходе предварительной обработки первая группа фрагментов биоматериала помещалась на 20 минут в 10% раствор глицерина, в последующем обрабатывалась в течение 15 минут ультразвуком с частотой 35±10% кГц. После чего фрагменты помещались на 15 минут в камеру, в которой создавался вакуум с остаточным давлением 1–2 Па. После извлечения из камеры биоматериал повторно промывался в растворе 0,9% NaCl, замораживался при температуре от –20°С до –60°С, лиофилизировался, герметично упаковывался и стерилизовался радиационным методом (гамма-лучами или быстрыми электронами).
Вторая группа фрагментов биоматериала, без предварительной обработки глицерином, также подвергалась воздействию низкочастотного ультразвука, помещалась в вакуумную камеру и после повторной промывки и замораживания подвергалась лиофилизации. Лиофилизацию материала (вакуумную сушку сублимацией) проводили с использованием сублимационной установки ALPHA2-4LSC (Martin Christ Gefriertrocknungsanlagen GmbH, Остероде-ам-Харц, Германия). Лиофилизированный биоматериал после упаковки в герметичные пакеты стерилизовался радиационным методом.
Морфологические исследования были проведены после фиксации биоматериала в 12% нейтральном растворе формалина, проводки через батарею спиртов и заливки в целлоидин. Вы- полнено не менее 500 срезов с разных образцов биоматериала. Срезы окрашивались гематокси-лин-эозином или пикрофуксином по Ван Гизону.
Сканирующая электронная микроскопия (СЭМ) амниотической мембраны после консервации выполнялась с использованием растрового электронного микроскопа JEOLJSM-6390 A Analysis Station (Япония). Для данного исследования фрагменты биоматериала фиксировали 2,5% водным раствором глутарового альдегида, далее осуществляли проводку через батарею спиртов. После проведения через раствор этанола в возрастающей концентрации и сушки при комнатной температуре в течение 24 часов на биоматериал напылялось золото или углерод для улучшения требуемой поверхностной электропроводности при выполнении сканирующей электронной микроскопии.
Биологически активные свойства децеллюля-ризированной лиофилизированной амниотической мембраны исследовались в эксперименте на лабораторных животных. Исследование выполнено на 28 лабораторных крысах обоего пола сток Wistar, которые были разделены на две группы. При выполнении оперативных вмешательств на животных, а также их содержании в виварии НИИ БиоТех ФГБОУ ВО СамГМУ Минздрава России, руководствовались Европейской конвенцией о защите позвоночных животных, используемых для экспериментов или в иных научных целях (ETS № 123, Страсбург, 18.03.1986г.); «Принципами надлежащей лабораторной практики» национальный стандарт Российской Федерации ГОСТ № 33044-2014, введен с 1.08.2015г.; «Санитарноэпидемиологическими требованиями к устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев)» (СП 2.2.1.3218-14). Все оперативные вмешательства на животных проводились под внутримышечным наркозом смеси анестетиков «Zoletil 100» (Virbac C.A., Франция) в дозировке 0,5 мг/100 гр. веса и «Solutionis rometarum 20 mg/ml» (Bioveta, Чехия) в дозировке 0,6 мг/100 гр. веса. Эксперименты производили с соблюдением правил асептики и антисептики. Операционное поле после удаления шерсти обрабатывали антисептиком, изолировали стерильными салфетками. Скальпелем производили разрез кожи длиной 1–1,5 см в области холки. Тупым методом формировали карман, в который помещали фрагмент (2x2 см) лиофилизированной амниотической мембраны. Рану ушивали наглухо. По истечении срока эксперимента животное выводили из эксперимента путем передозировки наркоза внутрисердечной инъекцией. Иссеченный фрагмент тканей из области имплантации помещали на 24–48 часов в фиксирующую жидкость (10% забуференный формалин) при комнатной температуре. Далее изготавливали гистологические препараты по стандартной методике и окрашивали гематоксилином и эозином; гематоксилином и пикрофуксином.
Анализ изображений окрашенных препаратов производили с помощью системы визуализации на основе исследовательского микроскопа Olympus ВX41 («Olympus», Япония), цветной цифровой камеры «ProgRes CF» и стационарного компьютера, с программным обеспечением «Морфология 5.2» («ВидеоТесТ», Россия).
Полученные результаты обрабатывались статистическими методами пакета SPSS_Statistics.
Работа была выполнена с разрешения Комитета по биоэтике Самарского государственного медицинского университета (Выписка из протокола № 206 от 18 марта 2020 г.).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Используемый в нашем тканевом банке оригинальный метод консервации амниотической мембраны путем сублимационной сушки с предварительной децеллюляризацией путем физических воздействий позволяет хранить консервированный биоматериал при комнатных условиях. В свою очередь, децеллюляризация и сублимационная сушка приводят к структурным изменениям и даже, возможно, денатурации белков, обеспечивающих биологическую активность нативной амниотической мембраны [5, 12, 13]. Ультразвуковое воздействие способствует удалению элементов крови и в тоже время гарантированно разрушает клеточные структуры биоматериала. После лиофилизации и стерилизации радиационным методом фрагменты, амниотической мембраны, обработанные на предварительном этапе глицерином, внешне незначительно отличались от фрагментов, не обработанных глицерином. Обработанная глицерином амниотическая мембрана выглядела более матовой, чем фрагменты без обработки глицерином.
При детальном исследовании гистологических препаратов I группычетко визуализируется эпителиальный слой (рис. 1).
Но при этом наблюдается деструкция эпителиальных клеток, а в сохранившихся клетках – пикноз ядер. Компактный же слой выглядит как гомогенная бесклеточная оксифильная полоса, а местами в нем визуализируются волокна. Спон-гиозный слой также сохранен, но уплотнен, а структурная организация его потеряна. Толщина препаратов лиофилизированной амниотической мембраны с предварительным пропитыванием глицерином имеет среднее значение измерений (n=48) – 10,236 мкм.
Эпителио-эпителиальный слой на гистологических препаратах II группы образцов замещен уплощенной гомогенной оксифильной структурой (рис. 2). В единичных сохранившихся эпителиоцитах наблюдается кариолизис и концентрация хроматина в виде конгломератов.
Компактный слой мембраны уплощен и гомогенно изменен. Количество фибробластов резко уменьшено, ядра сохранившихся из них имеют палочковидную форму или видны только как тени. Спонгиозный слой уплощен. Толщина препаратов лиофилизированной амниотической мембраны без обработки глицерином имеет среднее значение измерений (n=44) – 10,026 мкм.
Для более детального исследования плоских препаратов децеллюляризованной лиофилизированной амниотической мембраны былапро-ведена растровая электронная микроскопия.

Рисунок 1. Гистологический препарат амниотической мембраны, консервированной путем лиофилизации после предварительной обработки глицерином. Окраска ге-матоксилин-эозином. Ув. 400
Figure 1. Histological section of amniotic membrane preserved by lyophilization following glycerol pretreatment. Hematoxylin and eosin stain. Mag. 400
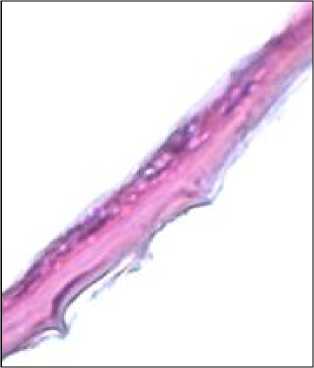
Рисунок 2. Гистологический препарат амниотической мембраны, консервированной путем лиофильной сушки без обработки глицерином. Окраска гематоксилин-эозином. Ув. 400
Figure 2. Histological section of amniotic membrane preserved by lyophilization without glycerol pretreatment. Hematoxylin and eosin stain. Mag. 400
При исследовании лиофилизированных образцов, предварительно обработанных глицерином, наблюдаются выраженные повреждения эпителиального слоя, в котором большая часть нежизнеспособных эпителиоцитов были десква-мированы (рис. 3). Базальная мембрана была повреждена и частично отслоена от подлежащих слоев амниотической мембраны. На сохранившихся ее участках поверхность складчатая, с единичными поврежденными эпителиоцитами. Цитоплазматические тяжи и межклеточные каналы в образцах I группы не обнаружены.
Сканирующая электронная микроскопия образцов II группы амниотической мембраны де-целлюляризованных и лиофилизированных без предварительной обработки глицерином выявила значительно более выраженные морфологические изменения (рис. 4).

Рисунок 3. Эпителиальная поверхность препарата лиофилизированной амниотической мембраны, предварительно обработанной глицерином. Сканирующая электронограм-ма. Ув. 1000
Figure 3. Epithelial surface of a lyophilized amniotic membrane preparation pre-treated with glycerol. Scanning electron diffraction. Mag. 1000
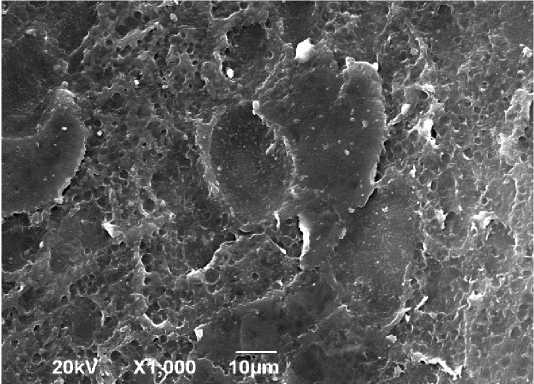
Рисунок 4. Эпителиальная поверхность препарата децел-люляризированной и лиофилизированной амниотической мембраны, не обрабоанного глицерином. Сканирующая электронограмма. Ув. 1000
Figure 4. Epithelial surface of a decellularized and lyophilized amniotic membrane preparation without glycerol treatment. Scanning electron diffraction. Mag. 1000
Так, наблюдается практически полая десква-мация эпителиоцитов с поверхности базальной мембраны. В незначительных сохраненных участках эпителиального слоя формировались кратеры разной величины на месте разрушенных эпителиоцитов. Базальная мембрана в образцах II группы также на значительных участках была десквамирована. На сохранившихся ее участках эпителий плотно прилежит к подлежащим слоям, но в нем образуется наблюдается множество округлых, разного диаметра дефектов мозаичной структуры.
Результаты сканирующей электронной микроскопии спонгиозного слоя образцов амниотической мембраны, обработанных разными методами, также показали значительные морфологические изменения. Спонгиозный слой амниотической мембраны лиофилизированной после предварительной обработки глицерином сохраняет структуру рыхлой ретикулярной соединительной ткани. Разнонаправленные соединительнотканные волокна придают биоматериалу объемную структуру. Однако некоторые соединитель-но-тканные волокна соединены друг с другом гомогенными бесструктурными образованиями, прикрепленными к ним в виде гроздей древовидной формы (рис. 5).
Спонгиозный слой образцов амниотической мембраны лиофилизированных без предварительной обработки глицерином выглядит менее всего поврежденным. В них сохраняется рыхлая структура ретикулярной соединительной ткани, некоторые волокна которой соединены друг с другом и на которых фиксированы единичные бесструктурные субстраты. На этих препаратах четко прослеживается сквозная пористость биоматериала. Необходимо так же отметить и наличие только единичных гомогенных образований, прикрепленных к коллагеновым волокнам (рис. 6).

Рисунок 5. Спонгиозный слой препарата амниотической мембраны лиофилизированной с предварительным пропитыванием глицерином. Сканирующая электронограмма. Ув. 1000
Figure 5. Spongy layer of a lyophilized amniotic membrane specimen pretreated with glycerol impregnation. Scanning electron diffraction. Mag. 1000

Рисунок 6. Спонгиозный слой препарата амниотической мембраны лиофилизированной без предварительного пропитывания глицерином. Сканирующая электронограмма. Ув. 1000 Figure 6. Spongy layer of a lyophilized amniotic membrane specimen without glycerol pretreatment. Scanning electron diffraction. Mag. 1000
Содержание и сохранность биологически активных веществ в децеллюляризованной амниотической мембране, изготовленной по специальной технологии с предварительной обработкой глицерином и без нами изучено путем определения протеомного состава. В составе человеческой амниотической мембраны, не обработанной глицерином перед лиофилизацией идентифицированы с высокой достоверностью 153 белка с молекулярным весом от 8,4 кДа до 628,7 кДа. Тогда как в составе амниотической мембраны обработанной перед лиофилизацией глицерином выявлен 121 белок с молекулярным весом от 11,4 кДа до 628,7 кДа. Необходимо отметить, что состав белков в образцах обработанных и не обработанных глицерином значительно отличается. В I группе фрагментов биоматериала 88 белковых структур не определены из имеющихся во II группе фрагментов биоматериала. Соответственно в образцах лиофилизированной амниотической мембраны, не обработанной глицерином отсутствует 28 белков, имеющихся во фрагментах, пропитанных глицерином перед лиофилизацией. Меньшее количество идентифицированных белков в структуре образцов лиофилизированной амниотической мембраны, обработанной глицерином, объясняется стабилизирующей функцией глицерина, который взаимодействуя с белками формирует трехмерные структуры, изменяет характеристики белковых соединений [14].
В связи с выявленным различием в про-теомном составе, предполагается что биоматериал, предварительно децеллюляризированный физическими методами и обработанный глицерином, скорее всего отличается по биологическим свойствам от децеллюляризированной лиофилизированной амниотической мембраны, предварительно не обработанной глицерином. Для уточнения данного предположения нами выполнено экспериментальное исследование на двух группах животных. Выполненная имплантация биоматериала в подкожный карман в области холки переносилась животными хорошо. Животные выводились из эксперимента на 12 сутки послеоперационного периода и иссеченные фрагменты ткани с имплантированной де-целлюляризованной амниотической мембраной подвергались морфологическому исследованию. Полученные данные свидетелствуют о различной реакции тканей, окружающих имплантиро- ванные фрагменты лиофилизированной амниотической мембраны I и II групп.
Лиофилизированная амниотическая мембрана на микропрепаратах тканей животных I группы хорошо визуализируется, сохраняется волокнистое строение, отмечается незначительный отек (рис. 7). Окружающие ткани инфиль- трированы единичными макрофагами и фибробластами. Единичные кровенаполненные сосуды. Единичные тучные клетки (среднее значение – 2,38, из них дегранулированных – 1,65 при подсчете в 10 полях зрения каждого из 5 гистологических препаратов).
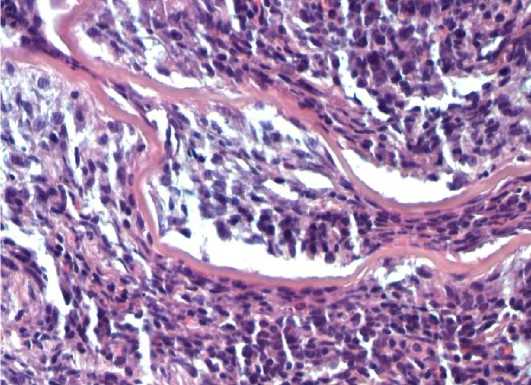
Рисунок 7. Кожная зона имплантации фрагмента лиофилизированной амниотической мембраны, обработанной глицерином. Окраска гематоксилин-эозином. Ув. 400
Figure 7. Histological section of the implantation site of a glycerol-treated lyophilized amniotic membrane fragment. Hematoxylin and eosin stain. Mag. 400
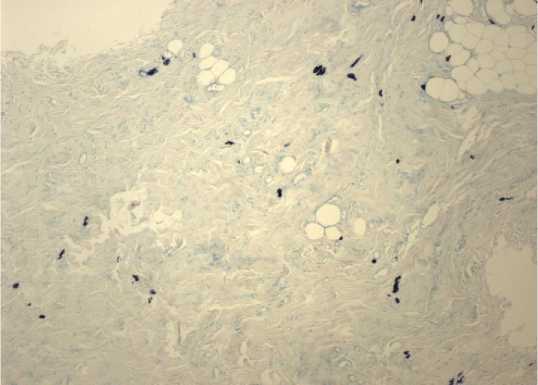
Рисунок 8. Кожная зона имплантации фрагмента лиофилизированной амниотической мембраны, обработанной глицерином. Окраска толуидиновым синим. Ув. 100
Figure 8. Histological section of the implantation site of a glycerol-treated lyophilized amniotic membrane fragment. Toluidine blue stain. Mag. 100
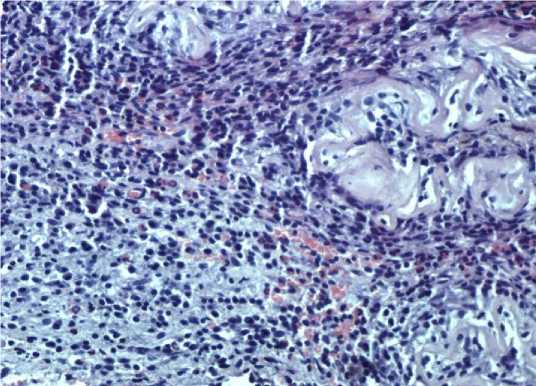
Рисунок 9. Гистологический препарат зоны имплантации фрагмента лиофилизированной амниотической мембраны без обработки глицерином. Окраска гематоксилин-эозином. Ув. 400
Figure 9. Histological section of the implantation site of a lyophilized amniotic membrane fragment without glycerol treatment. Hematoxylin and eosin stain. Mag. 400
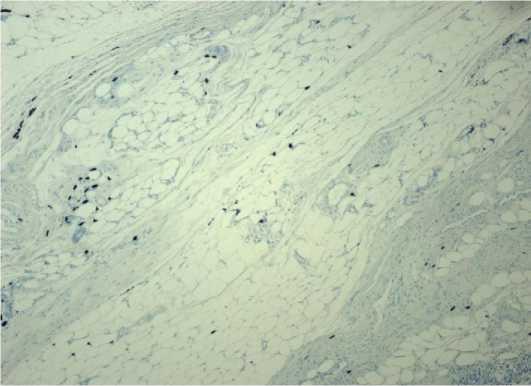
Рисунок 10. Гистологический препарат зоны имплантации фрагмента лиофилизированной амниотической мембраны без обработки глицерином. Окраска толуидиновым синим. Ув. 100
Figure 10. Histological section of the implantation site of a lyophilized amniotic membrane fragment without glycerol treatment. Toluidine blue stain. Mag. 100
На препаратах II группы (биоматериал без обработки глицерином перед лиофилизацией) отмечается более выраженный лизис и замещение лиофилизированной амниотической мембраны, выраженная макрофагальная инфильтрация. Окружающие ткани менее отечные, значительно инфильтрированы тучными клетками, отмечается множество вновь образованных сосудов. Тучных клеток на данных препаратах было обнаружено значительно больше (среднее значение – 7,5, из них дегранулированных – 6,85 при подсчете в 10 полях зрения каждого из 5 гистологических препаратов).
Визуализация тучных клеток путем окраски срезов толуидиновым синим позволила выявить как количество, так и качество – состояние дегрануляции клеток. Необходимо отметить расположение тучных клеток в некотором отдалении от имплантированного биоматериала, вокруг сосудов.
Особенностью технологии предварительной обработки биоматериала, подвергаемого лиофилизации в тканевом банке БиоТех СамГМУ является применение физических методов. Главным различием обработки двух групп фрагментов амниотической мембраны, полученной от одного донора, являлась обработка I группы фрагментов глицерином. Глицерин часто применяется при консервации амниотической мембраны [10, 14, 15]. Следовательно, выявленные нами различия в составе протеома изученных фрагментов определяются применением глицерина на этапе предварительной обработки амниотической мембраны. Меньшее количество идентифицированных белков в структуре образцов лиофилизированной амниотической мембраны, обработанной глицерином, объясняется стабилизирующей функцией глицерина вовремя лиофилизации, который взаимодействуя с белками формирует трехмерные структуры, изменяет характеристики белковых соединений и меняет механизм влияния на окружающие ткани [3, 15, 16]. Наиболее показательно в нашем случае это проявляется в отношении ангиогенеза. В структуре фрагментов де- целлюляризованной лиофилизированной амниотической мембраны предварительно пропитанного глицерином имеется 13 белков непосредственно регулирующих ангиогенез. Из них по данным из открытых ресурсов PANTHER и neXtProt шесть белков являются индукторами, семь белков ингибируют ангиогенез [17, 18].
Результаты морфологического исследования показали более выраженную реакцию на биоматериал без использования глицерина при его подготовке. В частности, на микропрепаратах I группы исследования значительно меньше инфильтрация тучными клетками и не наблюдается вновь образованных сосудов. Тогда как на микропрепаратах, где имплантировался биополимер, не пропитанный глицерином, имелась значительная инфильтрация тучными клетками и множество вновь образованных сосудов.
ЗАКЛЮЧЕНИЕ
Физические методы децеллюляризации и консервации позволяют сохранить анатомическую структуру и белковые соединения, определяющие биологическую активность амниотической мембраны.
Обработка биоматериала глицерином децеллю-ляризованной лиофилизированной амниотической мембраны способствует сохранению в структуре ткани разных по составу белковых соединений, определяющих биологическую активность.
Биоматериал, не пропитанный глицерином, имеет в составе большее количество протеинов, способствует большей клеточной инфильтрации и активизирует неоангиогенез. Напротив, амниотическая мембрана, предварительно обработанная глицерином, не вызывает выраженной воспалительной реакции и не приводит к развитию вновь образованных сосудов.
Следовательно, для различных реконструктивных операций возможен подбор децеллюля-ризованной амниотической мембраны, обработанной различными методами и обладающей различными биологически активными свойствами.


