Жирнокислотный состав подкожного жира байкальской нерпы разного возраста
Автор: Аверина Е.С., Пинтаева Е.Ц., Раднаева Л.Д.
Журнал: Вестник Бурятского государственного университета. Философия @vestnik-bsu
Рубрика: Органическая химия
Статья в выпуске: 3, 2009 года.
Бесплатный доступ
Исследован жирнокислотный состав подкожной жировой ткани особей байкальской нерпы различного возраста. Сравнительный анализ выявил систематические различия между образцами жира взрослых особей, щенками и эмбрионами байкальской нерпы и объектом их питания. Выявлено, что особи байкальской нерпы имеют различный жирнокислотный состав во внутреннем и внешнем слое подкожного жира: жирнокислотный состав внутреннего слоя более близок к составу жира объектов питания, чем состав жирных кислот внешнего слоя.
Байкальская нерпа, жировая ткань, липиды, жирные кислоты
Короткий адрес: https://sciup.org/148178795
IDR: 148178795
Blubber fatty acids of Baikal seal
The fatty acid (FA) composition was determined in the blubber of Baikal seals Phoca sibirica of different age, and was compared with FAs of the main prey of the Baikal seal, the endemic golomyanka Comephorus baikalensis. This study has shown that both endogenous factors and the general lipid composition of the ecosystem have influence on the layering and composition of FA in the blubber of top predator Phoca sibirica.
Текст научной статьи Жирнокислотный состав подкожного жира байкальской нерпы разного возраста
Байкальский тюлень (нерпа) Phoca (Pusa) Sibirica Gmel – единственное эндемичное млекопитающее Байкала, является вершиной пищевой пирамиды озера. Статус байкальской нерпы как основного объекта биомониторинга закреплен в ФЗ "Об охране озера Байкал". Популяция насчитывает около 100 тыс. особей [1].
Липиды играют важную роль в метаболических процессах водных организмов и являются основным источником энергии для роста и воспроизводства гидробионтов. Липиды подкожного жира морских млекопитающих (а это до 50% массы тела у некоторых видов) являлись объектом многих исследований [2-8]. Основное внимание в этих работах уделяется жирным кислотам – «строительным блокам» липидов, изучение которых позволяет осветить экологические, таксономические и медицинские аспекты.
Несмотря на уникальные экологические и биологические характеристики озера Байкал, исследования, связанные с изучением состава липидов этого единственного вида млекопитающих Байкала, в литературе весьма немногочисленны [9, 10]. Тогда как жирнокислотный состав подкожного жира арктического кольчатого тюленя P. Hispida hispida и трех других подвидов: P. Hispida botnica (Балтийское море), P. Hispida ladogensis (Ладожское озеро) и P. Hispida saimensis (оз. Сайма, Финляндия) достаточно хорошо изучен [11-13].
В связи с этим большой интерес представляет анализ состава жиров пресноводных тюленей, вопрос зависимости жирнокислотного состава жира тюленей от состава кислот в жирах пищевых объектов, а также анализ жирнокислотного состава особей в возрастном аспекте.
Материалы и методы
Особи байкальской нерпы различного возраста были выловлены во время промыслового лова в районе Ушканьих островов оз. Байкал, заливах Провал и Чивыркуйский, в различные сезоны 20012008 гг., общее число животных – 52. Образцы жира весом около 20 мг были отобраны из подкожного жира тюленей послойно: возле шкуры (верхний слой) и непосредственно возле мышечной ткани животного (внутренний слой) и перенесены в толстостенные стеклянные пробирки с тефлоновыми закручивающимися пробками. Байкальские голомянки (основной объект пищевой базы нерпы) были пойманы сетями в районе Ушканьих островов. Рыбы были тщательно гомогенизированы, около 40 мг каждой пробы были перенесены в стеклянные пробирки.
Все образцы были метилированы одноступенчатым методом [14] обработкой 2 н раствором хлороводорода в метиловом спирте в течение 2 ч при 90°С. Анализ жирнокислотного состава проводился методом ГЖХ на хроматографе НР-6890 с масс-селективным детектором 5973N, колонка CP-WAX 52CB Chrompack (25 м х 0.25 мм), температура инжектора - 250°С, температура колонки программировалась следующим образом: 90°С в течение 4 мин, далее температура повышалась до 165°С со ско- ростью 30°С/мин., с последующим увеличением до 225°С (3°С/мин.). Температура масс-селективного детектора - 250°С. Для анализа образцов была использована стандартная смесь, содержащая 20 жирнокислотных эфиров (GLC-68D Nu-Chek-Prep; Elysian, Minnesota, USA).
Полученные данные жирнокислотного состава исследованных образцов были обработаны методом главных компонент, представленным в программном пакете «Sirius 7.0» [15]. Этот проекционный метод статистического анализа позволяет интегрировать информацию обо всех объектах и показателях одновременно в n-мерном пространстве и получить график, который является проектированием всех образцов на двухмерную систему, где оси системы – первая и вторая принципиальные компоненты [16].
Результаты и обсуждение
Анализ состава жировой ткани пресноводных тюленей и объектов их питания
В изученных образцах жира байкальской нерпы и основного объекта их питания – байкальской голомянки – идентифицировано 50 жирных кислот (табл. 1). Состав ЖК подкожного жира млекопитающих – это результат сложных процессов запаса, мобилизации, биосинтеза и транспорта липидов. Доминирующим источником ЖК для морских млекопитающих является пищевая база, так, все ЖК липидов изученных рыб обнаружены в подкожном жире изученных тюленей, хотя и в различных концентрациях.
В подкожном жире байкальской нерпы отмечается высокое содержание С18- и n6 ПНЖК, источниками которых является планктон. Общее увеличение концентраций n6 ПНЖК в жирах пресноводных тюленей наблюдается на фоне более низких концентраций n3 ПНЖК, в основном 20:5n3. Высокие уровни n6 и С18 ПНЖК и низкие уровни С20 и С22 МНЖК характерны также для пресноводных подвидов Phoca vitulina mellonae из северного Квебека (Канада) в отличие от его морских сородичей P. vitulina concolor и P. vitulina richardsi [17]. Несмотря на то, что в литературных источниках описан общий ЖК состав пресноводных гидробионтов [18], сравнительные данные по составу ЖК основных объектов питания и водных млекопитающих до сих пор не были освещены.
Применение мультивариационного анализа главных компонент позволило ясно продемонстрировать выявленные различия жирнокислотного состава между образцами байкальского тюленя и голомянки, с одной стороны, и морскими кольчатыми тюленями и полярной треской – с другой (рис. 1). Полученный график показывает наличие различий между образцами жира байкальской нерпы и объектами их питания – голомянками. Необходимо также отметить, что тюлени имеют различный жирнокислотный состав во внутреннем и внешнем слое подкожного жира (рис.1).
Обнаружено, что концентрации МНЖК с 14 и 18 углеродными атомами и более высоки в верхнем слое, а МНЖК с 20 и 24 углеродными атомами – во внутреннем слое подкожного жира тюленей; уровень 16:1n9 и 20:1n11 кислот (которые, в соответствии с положением двойной связи, являются результатом пероксисомального укорачивания цепи) повышается в верхнем слое. Содержание насыщенных жирных кислот выше в липидах внутреннего слоя. Что касается ПНЖК, изомеры 18:2 кислот в наибольшей степени аккумулируются в липидах верхнего слоя, ПНЖК с 16 углеродными атомами – во внутреннем слое жира.
В настоящее время для объяснения стратификации ЖК в подкожных жирах морских млекопитающих рассматриваются эндогенные ЖК, т.е. НЖК и ПНЖК с 14, 16 и 18 углеродными атомами [19, 20]. Полагают, что эндогенно синтезируемые ЖК мобилизуются в меньшей степени и потому доминируют в более стабильном верхнем слое, тогда как диетарные ЖК запасаются или мобилизуются по мере необходимости [21].
При сравнении ЖК состава внутреннего и верхнего слоев подкожного жира байкальской нерпы с жирнокислотным составом объектов питания (голомянки) было показано, что состав внутреннего слоя наиболее близок к составу пищевой базы (рис. 1), что не противоречит литературным данным [22, 23]. Послойные различия ЖК состава проявляются в наибольшей степени у взрослых байкальских тюленей по сравнению с составом жира щенков нерпы. Выявлено, что на ЖК состав внутреннего слоя оказывает влияние не только диетарный эффект, но и происходит эндогенный синтез и селективные процессы послойного распределения ЖК. Такие же различия наблюдались также у дельфинов Phocoena phocoena [21]. При этом, хотя состав внутреннего слоя подкожного жира тюленей отличен от состава жирных кислот объектов пищевой базы (табл. 1, рис. 1), тем не менее наблюдается общий характер изменения состава в направлении «рыба – внутренний слой подкожного жира тюленя» как для морских, так и для пресноводных гидробионтов.
Жирнокислотный состав байкальской нерпы различного возраста
Наряду с распределением ЖК в подкожной жировой ткани представляет интерес сравнительный анализ ЖК состава подкожного жира особей разного возраста. Обнаружено, что жирнокислотный состав подкожного жира щенков байкальской нерпы (25-30 дней) отличен от состава жира взрослых животных (рис.2). График главных компонент демонстрирует явные различия состава как в ряду «щенки нерпы – взрослые животные» (по первой принципиальной компоненте), так и различия между внутренним и верхним слоями, по второй принципиальной компоненте. В составе жиров щенков наблюдаются более высокие относительные концентрации 18:1n9 и 18:1n7 и низкие концентрации всех n6 и n3 ПНЖК (табл. 1).
Рис. 1. График метода главных компонент образцов жира байкальской нерпы и их основной пищевой базы – голомянки
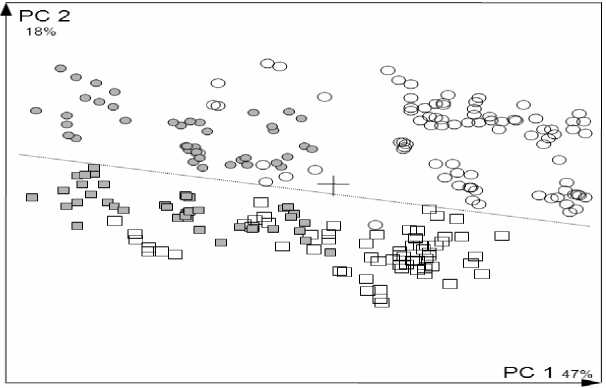
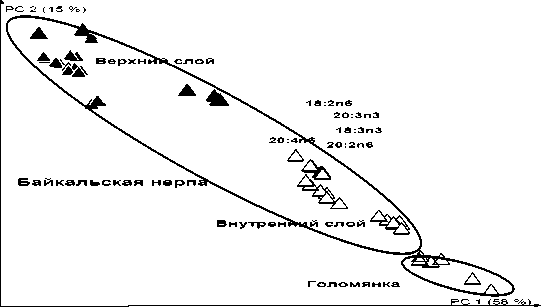
Рис. 2. График метода главных компонент образцов жира байкальской нерпы разного возраста: круг – образцы внутреннего слоя, квадрат – образцы верхнего слоя, темные фигуры – образцы щенков нерпы, светлые – взрослые животные
Жирнокислотный состав подкожного жира эмбрионов и щенков байкальской нерпы отличается от состава подкожного жира взрослых особей более низким содержанием ПНЖК, короткоцепочечных НЖК и МНЖК. При этом указанные различия проявлялись в наибольшей степени у эмбрионов, нежели у щенков нерпы. Подобные закономерности были обнаружены в подкожной жировой ткани новорожденных и взрослых тюленей Cystophora cristata [24] и новорожденных и взрослых особей белых китов Delphinapterus leucas [25]. Предполагается, что ПНЖК из жировой ткани самок тюленей, например Phoca vitulina , трансформируются в организм эмбрионов без изменений [24], и эти ПНЖК в основном используются для построения внутренних органов и тканей растущих эмбрионов и потому запасаются в подкожной жировой ткани в меньшей степени. Эндогенная продукция НЖК и МНЖК (которая происходит в раннем возрасте, ввиду необходимости быстрого накопления запаса жира и таким образом формирования необходимой защиты) также может вносить вклад в различие состава подкожного жира эмбрионов, щенков и взрослых особей. Высокие уровни НЖК в жире эмбрионов могут являться следствием стабильных высоких температур, в которых они находятся.
Таблица 1
Жирнокислотный состав (% ± станд. отклон.) жиров байкальской нерпы Phoca sibirica , кольчатого тюленя Phoca hispida , байкальской голомянки Comephorus baikalensis и полярной трески Boreogadus saida
|
Жирные кислоты * |
Эмбрионы нерпы |
Щенки нерпы |
Взрослые особи нерпы |
Голомянка |
||
|
Верхний слой |
Внутренний слой |
Верхний слой |
Внутренний слой |
|||
|
14:0 |
5,0 ± 0,1 |
4,0 ± 0,4 |
4,2 ± 0,4 |
3,8 ± 0,7 |
5,9 ± 0,9 |
6 ± 1 |
|
14:1n5 |
1,3 ± 0,3 |
1,5 ± 0,2 |
0,8 ± 0,2 |
2,0 ± 0,4 |
0,9 ± 0,3 |
0,25 ± 0,09 |
|
15:0 |
0,32 ± 0,01 |
0,34 ± 0,02 |
0,37 ± 0,03 |
0,31 ± 0,04 |
0,45 ± 0,08 |
0,46 ± 0,04 |
|
i-15:0 |
0,09 ± 0,01 |
0,68 ± 0,06 |
0,62 ± 0,04 |
0,59 ± 0,07 |
0,71 ± 0,09 |
0,7 ± 0,2 |
|
ai-15:0 |
0,11 ± 0,01 |
0,28 ± 0,02 |
0,27 ± 0,02 |
0,29 ± 0,04 |
0,31 ± 0,05 |
0,31 ± 0,07 |
|
16:0 |
24,0 ± 3,0 |
6,4 ± 0,4 |
10,0 ± 1 |
5,0 ± 1,0 |
11,0 ± 2 |
15,6 ± 0,3 |
|
16:1n9 |
4,0 ± 0,5 |
0,75 ± 0,07 |
0,69 ± 0,06 |
0,7 ± 0,1 |
0,7 ± 0,2 |
0,41 ± 0,07 |
|
16:1n7 |
19,0 ± 4,0 |
21,5 ± 0,7 |
17 ± 2 |
20 ± 2,0 |
15 ± 2 |
11 ± 3 |
|
16:1n5 |
0,23 ± 0,02 |
0,36 ± 0,03 |
0,35 ± 0,04 |
0,35 ± 0,03 |
0,35 ± 0,05 |
0,32 ± 0,02 |
|
16:2n6 |
0,10 ± 0,09 |
0,7 ± 0,1 |
0,7 ± 0,1 |
0,9 ± 0,1 |
1,1 ± 0,4 |
1,0 ± 0,3 |
|
16:3n4 |
<0,01 ± 0,00 |
0,26 ± 0,07 |
0,24 ± 0,06 |
0,3 ± 0,1 |
0,4 ± 0,1 |
0,5 ± 0,2 |
|
16:4n1 |
0,07 ± 0,06 |
0,14 ± 0,04 |
0,12 ± 0,03 |
0,20 ± 0,06 |
0,3 ± 0,1 |
0,2 ± 0,1 |
|
17:0 |
0,5 ± 0,2 |
0,32 ± 0,06 |
0,43 ± 0,07 |
0,24 ± 0,05 |
0,40 ± 0,09 |
0,29 ± 0,07 |
|
i-17:0 |
0,32 ± 0,08 |
0,51 ± 0,02 |
0,52 ± 0,03 |
0,46 ± 0,08 |
0,48 ± 0,07 |
0,54 ± 0,02 |
|
ai-17:0 |
0,25 ± 0,03 |
0,5 ± 0,1 |
0,55 ± 0,05 |
0,55 ± 0,06 |
0,6 ± 0,1 |
0,69 ± 0,08 |
|
b-17:1 |
0,1 ± 0,1 |
0,22 ± 0,05 |
0,21 ± 0,04 |
0,25 ± 0,03 |
0,27 ± 0,04 |
0,27 ± 0,04 |
|
17:1n8 |
0,3 ± 0,1 |
0,76 ± 0,04 |
0,69 ± 0,05 |
0,8 ± 0,1 |
0,56 ± 0,08 |
0,45 ± 0,08 |
|
18:0 |
3,2 ± 0,8 |
0,59 ± 0,07 |
1,3 ± 0,3 |
0,6 ± 0,1 |
1,5 ± 0,3 |
3,0 ± 0,3 |
|
i-18:0 |
0,02 ± 0,02 |
0,24 ± 0,02 |
0,26 ± 0,01 |
0,26 ± 0,06 |
0,24 ± 0,08 |
0,5 ± 0,1 |
|
18:1n9 |
21,0 ± 1,0 |
30,0 ± 5 |
32,0 ± 5 |
24,0 ± 6,0 |
18,0 ± 6,0 |
16,0 ± 2,0 |
|
18:1n7 |
6,5 ± 0,2 |
7,1 ± 0,8 |
7,6 ± 0,7 |
5,9 ± 0,9 |
5,0 ± 1 |
4,9 ± 0,8 |
|
18:1n5 |
0,7 ± 0,2 |
0,33 ± 0,03 |
0,31 ± 0,02 |
0,32 ± 0,09 |
0,30 ± 0,07 |
0,34 ± 0,05 |
|
18:2n7 |
1,2 ± 0,1 |
0,25 ± 0,05 |
0,20 ± 0,04 |
0,22 ± 0,09 |
0,15 ± 0,08 |
0,05 ± 0,03 |
|
18:2n6 |
0,6 ± 0,1 |
3,5 ± 0,4 |
3,9 ± 0,4 |
4,2 ± 0,7 |
4,1 ± 0,5 |
4,4 ± 0,8 |
|
18:2n4 |
0,3 ± 0,1 |
0,31 ± 0,03 |
0,31 ± 0,03 |
0,33 ± 0,03 |
0,33 ± 0,04 |
0,27 ± 0,05 |
|
18:3n6 |
0,15 ± 0,03 |
0,59 ± 0,05 |
0,47 ± 0,06 |
0,40 ± 0,07 |
0,28 ± 0,07 |
0,19 ± 0,04 |
|
18:3n3 |
0,13 ± 0,06 |
1,6 ± 0,3 |
1,7 ± 0,3 |
2,3 ± 0,6 |
3,0 ± 0,7 |
3,0 ± 0,6 |
|
18:4n3 |
0,1 ± 0,1 |
2,1 ± 0,5 |
1,9 ± 0,4 |
2,1 ± 0,5 |
2,7 ± 0,8 |
2,1 ± 0,3 |
|
19:0 |
0,18 ± 0,09 |
0,2 ± 0,1 |
0,16 ± 0,06 |
0,23 ± 0,07 |
0,2 ± 0,1 |
0,14 ± 0,02 |
|
20:0 |
0,13 ± 0,02 |
0,3 ± 0,3 |
0,1 ± 0,1 |
0,05 ± 0,07 |
0,1 ± 0,1 |
0,16 ± 0,03 |
|
20:1n11 |
1,8 ± 0,9 |
0,1 ± 0,1 |
0,1 ± 0,1 |
0,3 ± 0,1 |
0,3 ± 0,2 |
0,12 ± 0,04 |
|
20:1n9 |
0,35 ± 0,04 |
0,2 ± 0,1 |
0,3 ± 0,1 |
0,35 ± 0,06 |
0,5 ± 0,2 |
0,8 ± 0,1 |
|
20:1n7 |
0,36 ± 0,08 |
0,4 ± 0,2 |
0,2 ± 0,2 |
0,3 ± 0,1 |
0,3 ± 0,2 |
0,20 ± 0,02 |
|
20:2n6 |
1,2 ± 0,1 |
0,2 ± 0,1 |
0,2 ± 0,1 |
0,4 ± 0,1 |
0,6 ± 0,3 |
0,71 ± 0,08 |
|
20:3n3 |
<0,01 ± 0,00 |
0,17 ± 0,03 |
0,18 ± 0,04 |
0,20 ± 0,04 |
0,23 ± 0,04 |
0,28 ± 0,02 |
|
20:4n6 |
2,1 ± 0,2 |
1,7 ± 0,3 |
1,3 ± 0,3 |
2,0 ± 0,3 |
2,0 ± 0,3 |
4,0 ± 2,0 |
|
20:4n3 |
0,03 ± 0,03 |
0,4 ± 0,1 |
0,3 ± 0,1 |
0,6 ± 0,2 |
0,6 ± 0,2 |
0,38 ± 0,04 |
|
20:5n3 |
1,0 ± 0,2 |
3,0 ± 0,8 |
2,4 ± 0,6 |
4,0 ± 1,0 |
4,0 ± 1,0 |
7,0 ± 2,0 |
|
21:5n3 |
<0,01 ± 0,00 |
0,18 ± 0,06 |
0,17 ± 0,05 |
0,25 ± 0,07 |
0,28 ± 0,09 |
0,20 ± 0,04 |
|
22:0 |
<0,01 ± 0,00 |
0,01 ± 0,01 |
0,00 ± 0,01 |
0,01 ± 0,02 |
0,02 ± 0,02 |
0,08 ± 0,01 |
|
22:1n11 |
0,04 ± 0,02 |
0,03 ± 0,02 |
0,04 ± 0,01 |
0,01 ± 0,00 |
0,01 ± 0,00 |
<0,01 ± 0,00 |
|
22:1n9 |
<0,01 ± 0,00 |
0,01 ± 0,01 |
0,00 ± 0,01 |
0,05 ± 0,03 |
0,07 ± 0,02 |
0,16 ± 0,04 |
|
22:1n7 |
0,22 ± 0,09 |
0,10 ± 0,03 |
0,09 ± 0,03 |
0,05 ± 0,02 |
0,05 ± 0,02 |
0,08 ± 0,01 |
|
22:4n6 |
0,2 ± 0,2 |
0,23 ± 0,05 |
0,23 ± 0,05 |
0,3 ± 0,1 |
0,5 ± 0,1 |
0,16 ± 0,05 |
|
22:5n6 |
0,4 ± 0,1 |
0,5 ± 0,1 |
0,5 ± 0,2 |
1,0 ± 0,4 |
1,3 ± 0,5 |
1,2 ± 0,4 |
|
22:5n3 |
0,5 ± 0,2 |
2,2 ± 0,6 |
2,2 ± 0,6 |
3,4 ± 0,9 |
4,0 ± 1,0 |
0,9 ± 0,2 |
|
22:6n3 |
1,8 ± 0,5 |
4,0 ± 1 |
4,0 ± 1 |
7,0 ± 2,0 |
10,0 ± 3,0 |
10,0 ± 4,0 |
|
24:0 |
0,02 ± 0,02 |
<0,01 ± 0,00 |
<0,01 ± 0,00 |
0,01 ± 0,01 |
0,01 ± 0,01 |
0,05 ± 0,02 |
|
24:1n9 |
0,24 ± 0,04 |
0,01 ± 0,01 |
0,02 ± 0,02 |
0,05 ± 0,05 |
0,15 ± 0,06 |
1,1 ± 0,6 |
|
неид |
0,2 0,1 |
0,10 0,03 |
0,09 0,03 |
0,05 0,03 |
0,04 0,07 |
<0,00 0,00 |
* – первая цифра указывает на число углеродных атомов, вторая – на количество ненасыщенных связей, третья – на первый углеродный атом при двойной связи от метильной группы.
ЖК состав подкожного жира эмбрионов имеет 2 специфические особенности: 1) содержание 16:1n9 кислоты (положение двойной связи, которое указывает на то, что она является результатом пероксисомального укорачивания цепи) выше по сравнению с жирами щенков и взрослых нерп. Таким образом, в эмбрионах происходит пероксисомальное укорачивание цепи кислот для регуляции физико-химических свойств липидов; 2) в подкожной жировой ткани эмбрионов наблюдаются более высокие концентрации 20:1n11 кислоты. В случае байкальской нерпы этот факт не может быть объяснен укорачиванием цепи 22:1n11 кислоты, так как содержание данной кислоты очень мало и в подкожном жире и в основных пищевых объектах. Таким образом, появление 20:1n11 кислоты может объясняться удлинением цепи кислоты 20:0 с последующим Δ9-десатурированием. Это предположение обосновано также с учетом того, что процессы удлинения цепи могут протекать более активно в условиях высоких температур, в которых находятся эмбрионы, чем при холодных температурах окружающей среды, воздействующих на подкожную жировую ткань взрослых животных.
С возрастом состав подкожного жира щенков постепенно достигает ЖК состава жировой ткани взрослых животных. Было показано, что эти изменения от новорожденных к взрослым соответствуют лактационному периоду. Так, для щенков хохлача изменения происходят в течение очень короткого лактационного периода – 4 дня [24], тогда как детеныши белого кита (лактационный период – более года) достигают состава подкожного жира, который близок к составу жира их матери через 1 г [25]. Различия, выявленные в жирнокислотном составе жиров взрослых особей и щенков байкальской нерпы, обусловлены тем, что продолжительность лактационного периода байкальского тюленя составляет 45-75 дней (в зависимости от ледовой ситуации), а возраст исследованных в настоящей работе щенков байкальской нерпы составлял 25-30 дней. Таким образом, представленный сравнительный анализ выявил систематические различия между образцами жира взрослых особей, щенками и эмбрионами байкальской нерпы, а также между объектом их питания. Необходимо также отметить, что особи байкальской нерпы имеют различный жирнокислотный состав во внутреннем и внешнем слое подкожного жира, при этом жирнокислотный состав внутреннего слоя более близок к жирнокислотному составу жира объектов питания, чем ЖК состав внешнего слоя.
Работа выполнена при поддержке гранта РФФИ р _ Сибирь № 08-05-98029.


