Злокачественная филлоидная опухоль молочной железы
Автор: Зугумова М.Ш., Степанянц Н.Г., Завьялов А.А., Павлов К.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические случаи
Статья в выпуске: 2 (84), 2023 года.
Бесплатный доступ
Введение. Филлоидная опухоль, также известная как листовидная или интраканаликулярная фиброаденома с клеточной стромой, - редкая патология, которая составляет 0,3-0,5 % всех новообразований молочной железы. Филлоидная опухоль отличается потенциальной возможностью трансформации в саркому молочной железы за счет злокачественных изменений в строме. Саркома молочной железы - это редкая неэпителиальная злокачественная опухоль, которая встречается в 1 % случаев от всего количества злокачественных опухолей молочной железы и 5 % всех сарком мягких тканей. Первичные саркомы молочной железы представляют собой редкие и гистологически разнородные злокачественные новообразования, публикации на данную тему ограничены. Описание клинического случая. В статье представлено клиническое наблюдение пациентки со злокачественной филлоидной опухолью молочной железы, которой выполнено хирургическое лечение в объеме радикальной мастэктомии по Мадден. Обсуждение. Клинический случай интересен редким видом фиброэпителиальной опухоли и трудностью окончательной верификации гистогенеза на предоперационном этапе в виду сложности дифференцировки злокачественной листовидной опухоли от метапластической карциномы. Выводы. Специалистам предстоит провести немалое количество гистохимических и генетических исследований большого количества случаев злокачественных филлоидных опухолей молочной железы для выработки эффективного алгоритма тактики лечения данной патологии..
Листовидная фиброаденома, филлоидная опухоль, саркома молочной железы, радикальная мастэктомия
Короткий адрес: https://sciup.org/142238972
IDR: 142238972 | УДК: 616-006 | DOI: 10.17238/2072-3180-2023-2-116-122
Malignant phylloid breast tumor
Introduction. A phylloid tumor, also known as a leaf-shaped or intracanalicular fibroadenoma with a cellular stroma is a rare pathology that accounts for 0.3-0.5 % of all breast neoplasms. A phylloid tumor is characterized by the potential for transformation into a breast sarcoma due to malignant changes in the stroma. Breast sarcoma is a rare non-epithelial malignant tumor that occurs in 1 % of cases of the total number of malignant breast tumors and 5% of all soft tissue sarcomas. Primary breast sarcomas are rare and histologically heterogeneous malignant neoplasms, publications on this topic are limited. Description of the clinical case. The article presents a clinical observation of a patient with a malignant phylloid breast tumor who underwent surgical treatment in the volume of a radical mastectomy according to Madden. Discussion. The clinical case is interesting for the rare type of fibroepithelial tumor and the difficulty of final verification of histogenesis at the preoperative stage due to the difficulty of differentiating malignant leaf-shaped tumor from metaplastic carcinoma. Conclusions. Specialists will have to conduct a considerable number of histochemical and genetic studies of a large number of cases of malignant phylloid breast tumors to develop an effective algorithm for the treatment of this pathology.
Текст научной статьи Злокачественная филлоидная опухоль молочной железы
Актуальность. Филлоидная опухоль (phyllodes tumor, phyllon – «лист» и eidos – «вид»), также известная как листовидная или интраканаликулярная фиброаденома с клеточной стромой – редкая патология, которая составляет 0,3–0,5 % всех новообразований молочной железы [1] и имеет частоту около 2,1 на миллион [2]. В связи с низкой распространенностью заболеваемости и небольшим количеством рандомизированных исследований по данной тематике, в настоящее время нет стандартизированного подхода к диагностике филлоидных опухолей, а их комплексное лечение малоизучено [3]. Эти гистологически разнородные фиброэпителиальные опухоли, которые встречаются достаточно редко, отличаются полиморфизмом морфологического строения и имеют бифазную структуру; своеобразное клиническое течение: быстрый рост, большие размеры, полициклические контуры, морфологическую многоклеточность, богатство ретикулярной соединительной ткани веретенообразными клетками. Листовидные опухоли встречаются практически в любом возрасте: и в период раннего полового созревания, и в зрелости, и в старости. В литературных источниках возрастной интервал встречаемости описывается от 10 до 90 лет, однако пик заболеваемости приходится на 45–49 лет и редко встречается у подростков и пожилых людей. Фил-лоидная опухоль молочной железы имеет высокий потенциал трансформации в саркому за счет злокачественных изменений в соединительной ткани [4].
Впервые филлоидный тип опухоли описан еще в 1774 году как «гигантская фиброаденома», а в 1827 году их в своих работах упоминает Chelius. Мюллер Иоганнес первым использовал понятие «cystosarcoma phyllodes» из-за макроскопического сходства с саркомой [5]. В 1943 году Ackerman и Cooper выявили злокачественный биологический потенциал этой опухоли. До этого она относилась к доброкачественной патологии. Всемирная организация здравоохранения в 1981 году приняло определение «филлоидная опухоль». С этого момента их гистологически классифицируют как доброкачественные, пограничные и злокачественные, относительно таких признаков как: разрастание стромы, края опухоли, индекс митотической активности, клеточная атипия и некроз опухоли [6].
Саркома молочной железы – это редкая неэпителиальная злокачественная опухоль, которая встречается приблизительно в 1 % случаев от всего количества злокачественных опухолей молочной железы и около 5 % всех сарком мягких тканей. Первичные саркомы молочной железы представляют собой редкие и гистологически разнородные злокачественные новообразования с ограниченными публикациями [7].
Хирургическое вмешательство в лечении первичных локальных форм опухолей молочной железы неэпителиального происхождения является основным методом. При выборе оптимального объема хирургического вмешательства в первую очередь следует ориентироваться на морфологический тип опухоли, так как он достоверно оказывает влияние на прогноз заболевания. Остальные иммуногистохимические и клинические особенности определяют о характере опухолевого процесса дополнительную информацию. К примеру, при неоднозначном патоморфологическом заключении на предоперационном этапе на основании размеров опухоли, скорости роста, экспрессии иммуногистохимических маркеров и активной клеточной пролиферации можно относительно точно судить о степени злокачественности новообразования молочной железы неэпителиального происхождения.
Цель исследования: продемонстрировать клинический случай, который интересен редким видом фиброэпителиальной опухоли и трудностью окончательной верификации гистогенеза на предоперационном этапе в виду сложности дифференцировки злокачественной листовидной опухоли от метапластической карциномы.
Описание клинического случая
Пациентка Ш., 48 лет обратилась с жалобами на уплотнение в правой молочной железе. Локально при осмотре (рис. 1): молочные железы асимметричные, справа отмечается деформация контура молочной железы за счет объемного образования, визуально определяющееся в проекции верхних квадрантов; выделения из сосков отсутствуют. В левой молочной железе пальпаторно на фоне явлений диффузной мастопатии очаговых образований не выявлено; в правой молочной железе в проекции верхних квадрантов определяется плотное опухолевое бугристое образование диаметром 6 см, с неровными нечеткими контурами; кожные покровы над образованием не изменены, симптом «площадки» отрицательный, регионарные лимфатические узлы пальпаторно не изменены.
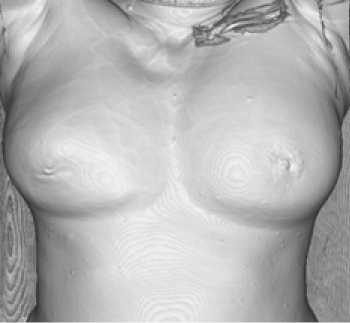
Рис. 1. Внешний вид пациентки на момент обращения: деформированный контур правой молочной железы
Fig. 1. Appearance of the patient at the time of treatment: deformed contour of the right breast
По данным ультразвукового исследования в верхневнутреннем квадранте правой молочной железы ближе к ареоле определяется объемное гетерогенное образование диаметром 60*84 мм. Описаны четкие неровные контуры пониженной эхогенности, неоднородная структура за счет линейных гиперэхогенных включений и анэхогенных включений размерами 44*23*32 мм. При цветовом допплеровском кодировании – смешанный кровоток: линейная скорость кровотока (ЛСК) в интранодулярных сосудах 4,2 см/сек, индекс резистентности (IR) 0,58; в перинодулярных сосудах ЛСК 5,6 см/сек, IR 0,54; BIRAD S–5 (рис. 2 (а, б, в). В подмышечной области справа визуализируются сравнительно измененные лимфатические узлы с четкими ровными контурами, с утолщенной гиперэхогенной сердцевиной, размерами 21*20 мм, 20*10 мм, без кровотока при ЦДК (рис. 3).

Рис. 2 (а, б, в). Ультразвуковая картина опухоли правой молочной железы
Fig. 2 (a, b, c). Ultrasound picture of the tumor of the right breast
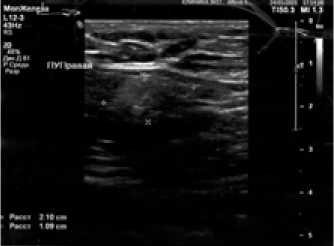
Рис. 3. Ультразвуковая картина увеличенного лимфатического узла правой подмышечной области Fig. 3. Ultrasound picture of the enlarged lymph node of the right axillary region
По маммографическому заключению: в правой молочной железы в проекции верхненаружного квадранта визуализируется гиперденсное бугристое объемное образование с неровными контурами диаметром 7*6 см (рис. 4).
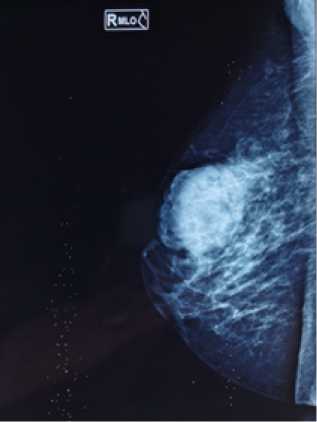
Рис. 4. Маммография справа
Fig. 4. Mammography on the right
С целью верификации диагноза и определения тактики лечения выполнена трепан-биопсия опухоли правой молочной железы. Гистологическое заключение № 339ИГХ/21 ФМБЦ от 21. 01. 2021: в биоптате среди клеточного детрита и эритроцитов определяются фрагменты опухоли, представленые диффузно расположенными среди рыхлой отечной соединительнотканной стромы, атипичными клетками со светлой эозинофильной цитоплазмой и выраженно полиморфными ядрами. Гистологическая картина соответствует злокачественной опухоли без явных признаков органоспецифичности. Для определения гистогенеза опухоли выполнено иммуногистохимическое исследование. В клетках опухоли определяется диффузная экспрессия vimentin
(структурный белок промежуточных филаментов соединительных тканей и других тканей мезодермального происхождения). В клетках опухоли отсутствует экспрессия CK pan (общий цитокератин; белок, из которого состоит внутриклеточный промежуточный филамент цитоскелета эпителиальных клеток), CD45 (белок (тирозиновая протеинфосфатаза), регулирующий Src-семейство киназ, который экспрессируется на поверхности всех гемопоэтических клеток), S-100 (функциональный тканеспецифический кальций-связывающий белок). Гистологическая картина и иммунофенотип соответствуют низкодифференцированному злокачественному новообразованию молочной железы. Преимущественно следует думать о злокачественной филлоидной опухоли молочной железы, а также о метапластической карциноме. Окончательная верификация гистогенеза опухоли возможна только после исследования операционного материала.
Пациентка по месту амбулаторного прикрепления обследована в соответствии со стандартом, утвержденным при очаговой патологии молочных желез. Учитывая злокачественный характер и размеры опухолевого образования, с целью исключения прорастания опухоли в окружающие ткани грудной клетки и вторичных очагов метастатического характера, выполнено дообследование в объеме: КТ органов грудной клетки, КТ органов брюшной полости с в/в контрастированием, МРТ головного мозга с в/в контрастированием и Остеосцинтиграфия. Данных за изменения метастатического характера не выявлено.
По данным КТ органов грудной клетки в проекции правой молочной железы определяется объемное кистозно-солидного строения образование с бугристыми контурами размерами 60*85 мм, накапливающее контрастное вещество по капсуле и солидному компоненту, без признаков инвазии в мышцы передней грудной стенки (рис. 5 (а, б).
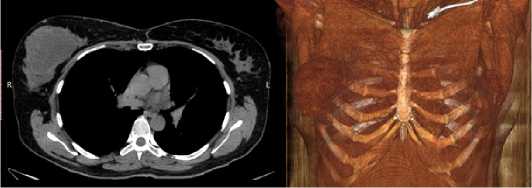
Рис. 5 (а, б). Визуализация опухоли правой молочной железы на компьютерной томографии
Fig. 5 (a, b). Visualization of the tumor of the right breast on computed tomography
С учетом имеющихся данных (большого размера образования, занимающего половину части молочной железы, предлежания к сосково-ареолярному комплексу, злокачественного характера роста опухоли, измененных подмышечных лимфатических узлов по данным ультразвукового исследования, а также отсутствия по данным иммуногистохимического исследования четкой дифференцировки между саркомой и карциномой молочной железы) пациентке решено выполнить радикальную мастэктомию по Мадден.
По результатам гистологического заключения № 2758– 87+ИГХ/21 ФМБЦ от 15. 02. 2021 картина соответствует низ-кодифференцированой (FFCCSG Grade 3) мягкотканной опухоли молочной железы (рисунок 6а, 6б) максимальным размером в отдельном микропрепарате 2 см, без лимфососудистой инвазии, без вовлечения края резекции и без метастазов в 16 исследованных лимфатических узлах. С учетом того, что первичные недифференцированные плеоморфные саркомы молочной железы наблюдаются исключительно редко, прежде всего, следует думать о злокачественной филлоидной опухоли молочной железы. По результатам иммуногистохимического исследования исключена метапластическая карцинома молочной железы (рис. 7, 8).
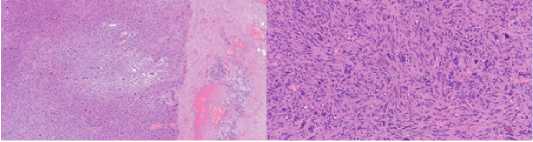
Рис. 6 (а, б). Гистологическая картина низкодифференцированой (FFCCSG Grade 3) мягкотканной опухоли молочной железы: а – опухоль с относительно четкими границами и участками некроза, х40; б – солидные скопления атипичных клеток с выраженно полиморфными ядрами и многочисленными (в том числе патологическими митозами), многочисленные многоядерные клетки, х200. Окраска гематоксилином и эозином
Fig. 6 (a, b). Histological picture of a low–grade (FFCCSG Grade 3) soft tissue breast tumor: a – tumor with relatively clear boundaries and necrosis sites, x40; b – solid clusters of atypical cells with pronounced polymorphic nuclei and numerous (including pathological mitoses), numerous multinucleated cells, x200. Stained with hematoxylin and eosin
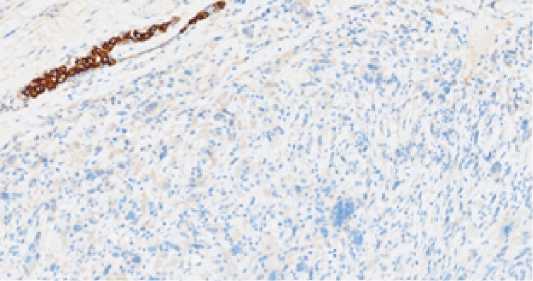
Рис. 7. Отсутствие экспрессии СK pan в клетках опухоли (положительный внутренний контроль – экспрессия в эпителии протоков молочной железы). Иммуногистохимический метод, х 200 Fig. 7. Absence of SC pan expression in tumor cells (positive internal control – expression in the epithelium of the ducts of the breast). Immunohistochemical method, x 200
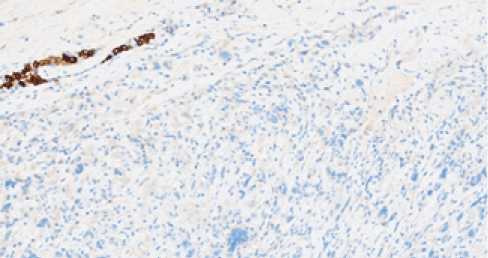
Рис. 8. Отсутствие экспрессии СK 8–18 в клетках опухоли (положительный внутренний контроль – экспрессия в эпителии протоков молочной железы). Иммуногистохимический метод, х 200.
Fig. 8. Lack of expression of SC 8–18 in tumor cells (positive internal control – expression in the epithelium of the ducts of the breast). Immunohistochemical method, x 200
После получения результатов гистологического исследования пациентка проконсультирована химиотерапевтом и радиотерапевтом: учитывая радикальный характер оперативного вмешательства, данные гистологического и иммуногистохимического исследований, рекомендовано динамическое наблюдение.
В раннем, позднем и отсроченном послеоперационном периоде осложнений не было.
За пациенткой в течение года проводится динамический контроль. По результатам контрольных обследований данных за прогрессирование опухолевого процесса нет. С пациенткой проведены разъяснительные беседы о необходимости дальнейшего наблюдения и выполнения плановых обследований.
Обсуждение
Филлоидные опухоли (ФО) по данным международной гистологической классификации, которая в 2012 году была пересмотрена и принята рабочей группой, входящей в состав Международного агентства по изучению рака (International Agency for Research on Cancer, IARC), относят к фиброэпителиальным опухолям. Их делят на:
– 9020/0, доброкачественные;
– 9020/1, промежуточные;
– 9020/3, злокачественные [6].
Доброкачественные ФО отличаются высокой стромальной клеточностью. Их характеризуют низкая митотическая активность (менее 4 митозов в 10 полях зрения) и умеренная клеточная атипия [8]. При проведении проточной цитофлоуметрии с целью определения плоидности в доброкачественных ФО определяется 100 % диплоидия опухолевых клеток. В данной группе отдаленные рецидивы в литературе не описаны.
Пограничные ФО характеризуются большей степенью стромальной клеточности. В них гораздо больше выражены атипия фибробластов и полиморфизм. Количество митозов составляет от 4 до 9 в 10 полях зрения (при ×400). При проведении проточной цитофлоуметрии с целью определения плоидности в доброкачественных ФО выявляются диплоидные и анеуплоидные клетки. Индекс пролиферативной активности у пограничных ФО высокий: 48 % (19,8 % – число делящихся клеток в G2 + M фазе, что близко к проценту клеток с наличием экспрессии белка Ki67 у сарком). Отдаленные рецидивы встречаются очень редко [8].
Злокачественные ФО (периканаликулярные стромальные опухоли низкой степени злокачественности, гистологическая классификация 2012 года) характеризуют крупные участки оксифильных масс, образующих тяжи в виде малиновых нитевидных субстанций, в составе которых определяются множественные опухолевые клетки [8].
Только в случае обнаружения эпителиальных клеток и злокачественных мезенхимальных клеток (клеток саркомы) возможно установить диагноз «злокачественная филлоидная опухоль». Основной особенностью филлоидных опухолей является их высокий потенциал к рецидивированию, малигнизации и преобразованию в саркомы [8].
Однако присутствие эпителиального компонента не является препятствием для развития карциномы. В литературных источниках встречаются случаи малигнизации сразу двух компонентов, в результате чего развивается карциносаркома. Для такой опухоли характерно как гематогенное, так и лимфогенное метастазирование [9].
Развитие саркомы может быть как первичное (de novo), так и вторичное. Последнее встречается гораздо чаще вследствие озлокачествления стромального компонента доброкачественной филлоидной опухоли. В литературе описаны клинические случаи саркомы молочной железы по прошествии времени после лучевой терапии злокачественных заболеваний (рака шейки матки, рака молочной железы, лимфомы Ходжкина) [10]. Саркомы молочной железы по своей морфологической составляющей гетерогенны, между тем наиболее часто встречаются липосаркомы, ангиосаркомы и недифференцированные плеоморфные саркомы.
На момент обнаружения ФО могут достигать довольно больших размеров (более 3 см), в связи с характерным для них экспансивным, быстрым ростом. Для сарком молочной железы характерно метастазирование гематогенным путем, чаще в печень, легкие и костный мозг. Метастазирование лимфогенным путем при данной патологии не встречается, а вовлечение грудных мышц и кожи наблюдается крайне редко. К наиболее важным факторам прогноза относят наличие чистого края резекции и размер опухоли. По большей части эти аспекты определяют долгосрочную выживаемость [7].
Хирургический метод на сегодняшний день остается основным в лечении сарком молочной железы. Он может быть выполнен в объеме мастэктомии или, если позволяет клиническая ситуация, органосохранной операции (при условии чистых краев резекции) [11]. Вопрос по поводу подмышечной лимфаденэктомии является спорным и обсуждаемым в каждом конкретном клиническом случае. Она рекомендована к выполнению только в случае подтипа карциносаркомы, при диссеменированном заболевании или же при наличии подозрительных на предоперационном этапе лимфатических узлов. В литературе вовлечение лимфатических узлов описывается крайне редко. По поводу назначения адъювантной терапии (химиотерапия и/или лучевая терапия) у пациентов с саркомой молочной железы в настоящее время имеются разногласия [7]. В литературных источниках описаны преимущества адъювантной лучевой терапии в снижении частоты локального рецидива у пациенток с опухолями больших размеров или с положительными хирургическими краями резекции [12]. Специалистам предстоит провести немалое количество гистохимических и генетических исследований большого количества случаев злокачественных филлоидных опухолей молочной железы для выработки эффективного алгоритма тактики лечения данной патологии.
Выводы
Злокачественная ФО молочной железы встречается крайне редко и является непростой для диагностики патологией с уникальными клиническими, гистологическими и цитогенетическими характеристиками.
Для гистологического исследования наиболее информативным является материал удаленной опухоли. Это дает возможность при дифференциальной диагностике убедиться в полном отсутствии эпителия. Но правильный диагноз позволяет установить только иммуногистохимическое исследование.
Хирургический метод лечения при злокачественных ФО молочной железы на сегодняшний день является ведущим. Адъювантная лучевая терапия нецелесообразна при радикальном хирургическом лечении с отрицательными краями резекции. Гормональная терапия при лечении злокачественной ФО не эффективна, а рациональность применения адъювантной химиотерапии остается спорной, поскольку в ее отношении на сегодняшний день не проведено рандомизированных исследований.
Список литературы Злокачественная филлоидная опухоль молочной железы
- Rowell M. D., Perry R. R., Hsiu J. G., and Barranco S. C., “Phyllodes tumors,” The American Journal of Surgery, 1993, № 3, pp. 376-379. https://doi.org/10.1016/s0002-9610(05)80849-9
- Bernstein L., Deapen D., and Ross R. K., “The descriptive epidemiology of malignant cystosarcoma phyllodes tumors of the breast,” Cancer, 1993, № 10, pp. 3020-3024. URL: https://europepmc.org/article/med/8387873.
- Жгулева А. А., Алтынпара А. И. Современный взгляд на диагностику и лечение филлоидных опухолей молочной железы. Материалы Всероссийского научного форума студентов с международным участием «Студенческая наука - 2020». Спецвыпуск, 2020. № 3. С. 901.
- Денчик Д. А., Воротников И. К., Быкова А. В., Любченко Л. Н. Листовидные опухоли молочных желез. Злокачественные опухоли, 2012. № 1. С. 40-43.
- Закиряходжаев А. Д., Широких И. М., Харченко Н. В., Запиров Г. М., Сарибекян Э. К., Н. В. Аблицова Н.В. и др. Филлоидные опухоли молочных желез. Современное состояние проблемы. Исследования и практика в медицине, 2017. № 2. С. 13-22.
- Шаши Пракаш Мишра, Сатьендра Кумар Тивари, Манджари Мишра, Аджай Кумар Кханна, «Филлодная опухоль груди: обзорная статья», Международные научные исследования, 2013. № 2. С. 1-10.
- Сопромадзе С. В., Соболевский В. А., Феденко А. А., Крохина О. В., Горбачева О. Ю., Соловьева А. С. Саркома молочной железы. Выбор тактики лечения. Факторы прогноза. Саркомы костей, мягких тканей и опухоли кожи, 2019. № 2. С. 25-33.
- Родионова Л. М., Мехеда Л. В., Фомина Л. Я. Сложности цитологической диагностики фиброэпителиальных опухолей: фиброаденома и филлоидная опухоль. Клин. эксп. Морфология, 2020. № 1. С. 20-29.
- Григорчук О. Г., Богатырев В. Н., Лазарев А. Ф., Соколова В. К., Фролова Т. С., Базулина Л. М. Цитологическая диагностика листовидных опухолей и сарком молочной железы. Опухоли женской репродуктивной системы, 2005. № 1. С. 23-28.
- Sheth G. R., Cranmer L. D., Smith B. D., Grasso-Lebeau L., Lang J. E. Radiationinduced sarcoma of the breast: a systematic review. The Oncologist, 2012, № 3, рр. 405-418. https://doi.org/10.1634/theoncologist.2011-0282
- Zelek L. et al. Prognostic factors in primary breast sarcomas: a series of patients with long-term follow-up. Journal of clinical oncology: official journal of the American Society of Clinical Oncolog, 2003, № 13, рр. 2583-2588. https://doi.org/10.1200/JCO.2003.06.080
- Harris J. R., Lippman M. E., Morrow M., Osborne C. K., ed. Diseases of the Breast. Ed. 4. Philadelphia: Lippincott Williams & Wilkins, 2010, № 1, рр. 800-802.
- Корженкова Г. П., Касымова А. А. Злокачественная листовидная опухоль на примере клинического случая. Вестник рентгенологии и радиологии, 2021. № 3. С. 178-182.


