Злокачественные трофобластические опухоли
Автор: Ульрих Е.А., Румянцев А.А., Телетаева Г.М., Хохлова С.В., Урманчеева А.Ф., Тюляндина А.С.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Практические рекомендации
Статья в выпуске: 3S2-2 т.14, 2024 года.
Бесплатный доступ
Хориокарцинома, трофобластическая болезнь, трофобластическая неоплазия, опухоль плацентарного ложа, эпителиоидная трофобластическая опухоль, инвазивный пузырный занос
Короткий адрес: https://sciup.org/140307410
IDR: 140307410 | DOI: 10.18027/2224-5057-2024-14-3s2-1.2-07
Текст статьи Злокачественные трофобластические опухоли
Трофобластическая болезнь (ТБ) представлена спектром расстройств, связанных с беременностью, которые включают доброкачественные/предраковые заболевания (полный и частичный пузырный занос, атипический узел плацентарного ложа), а также злокачественные процессы, такие как инвазивный пузырный занос, хориокарцинома, трофобластическая опухоль плацентарного ложа и эпителиоидная трофобластическая опухоль (табл. 1). Трофобластическая неоплазия — термин, используемый для злокачественных и резистентных опухолей.
1. КЛАССИФИКАЦИЯ И ОПРЕДЕЛЕНИЕ СТАДИИ
Морфологическая классификация и принципы стадирования трофобластической болезни представлены в табл. 1 и 2, рис. 1 и 2, классификация факторов риска резистентности — в табл. 3.
Таблица 1. Международная морфологическая классификация трофобластической болезни (IARC, 5-е издание, Лион, 2020 г.)
|
Источник |
Гистологический тип |
Морфологический код1 |
МКБ-10 |
|
Ворсины хориона |
Полный пузырный занос |
9100/0 |
О01 |
|
Частичный пузырный занос |
9103/0 |
О01 |
|
|
Инвазивный/метастатический пузырный занос |
9100/1 |
D39 |
|
|
Атипический ворсинчатый хорион |
– |
– |
|
Источник |
Гистологический тип |
Морфологический код1 |
МКБ-10 |
|
Промежуточный трофобласт |
Хориокарцинома |
9100/3 |
С58 |
|
Трофобластическая опухоль плацентарного ложа |
9104/1 |
D39 |
|
|
Гиперэргическая реакция плацентарного ложа |
– |
– |
|
|
Эпителиоидная трофобластическая опухоль |
9105/3 |
С58 |
|
|
Узел плацентарного ложа/атипический узел плацентарного ложа |
– |
– |
|
|
Смешанные трофобластические опухоли |
– |
– |
1 Морфологический код: цифра под дробью «0, 1, 3» означает: 0 — доброкачественная (опухоль), 1 — пограничная (опухоль), 3 — злокачественная (опухоль).
2. ДИАГНОСТИКА
2.1. Клинические проявления
Таблица 2. Стадии трофобластической болезни в соответствии с классификацией FIGO, 2020 г. (аналогичны классификации FIGO 2000 г. для трофобластической болезни)
|
Стадия |
Локализация опухоли |
|
I |
Локализуется в пределах матки |
|
II |
Распространяется за пределы матки, но ограничена половыми органами (придатки, широкая связка матки, влагалище) |
|
III |
Метастазы в легких в сочетании или без поражения половых органов |
|
IV |
Метастазы другой локализации |
Таблица 3. Группы риска развития резистентности к лекарственной терапии при трофобластической болезни (прогностические критерии FIGO, 2020 г., аналогичны классификации FIGO 2000 г. для трофобластической болезни)
|
Параметр/количество баллов |
0 |
1 |
2 |
4 |
|
Возраст |
< 40 лет |
≥ 40 лет |
– |
– |
|
Предшествовавшая беременность |
Пузырный занос |
Аборт |
Доношенная беременность |
– |
|
Интервал между окончанием последней беременности и началом ХТ |
< 4 мес. |
4–6 мес. |
7–12 мес. |
> 12мес. |
|
Уровень β-ХГЧ в крови до начала ХТ, мМЕ/мл |
< 1000 |
1 000 — < 10 000 |
10 000 — < 100 000 |
≥ 100 000 |
|
Размер наибольшей опухоли (включая опухоль в матке), см |
< 3 |
3–5 |
> 5 |
– |
|
Локализация метастазов |
Легкие |
Селезенка, почки |
ЖКТ |
Головной мозг, печень |
|
Параметр/количество баллов |
0 |
1 |
2 |
4 |
|
Количество метастазов |
– |
1–4 |
5–8 |
> 8 |
|
Предшествующая неэффективная ХТ (количество препаратов) |
– |
– |
1 |
≥ 2 |
Сумма баллов ≤ 6 соответствует низкому риску развития резистентности опухоли к лекарственной терапии, сумма баллов ≥ 7 соответствует высокому риску развития резистентности опухоли к лекарственной терапии.
Пузырный занос не является злокачественной опухолью, однако, в 1–15% случаев возможна его малигнизация (табл. 4), опухоль характеризуется кровянистыми выделениями из половых путей, болями внизу живота, токсикозом и несоответствием размеров матки предполагаемому сроку беременности.
Таблица 4. Критерии высокого риска развития трофобластической неоплазии после пузырного заноса
|
Критерии |
Пузырный занос высокого риска |
|
Возраст |
< 19 лет либо > 40 лет |
|
Уровень β-ХГЧ перед эвакуацией пузырного заноса |
> 100,000 мМЕ/мл |
|
Количество беременностей |
≥ 4 |
|
Размеры матки |
Больше, чем предполагаемый срок гестации (> 4–6 нед., размер > 6 см) |
|
Текалютеиновые кисты яичников |
Билатеральные, ≥ 6 см |
|
Другие |
Осложнения во время беременности (гипертиреоидизм, токсикоз, преэклампсия, дыхательная недостаточность и т. п.) Рецидивирующие пузырные заносы в анамнезе Плохая приверженность к последующему наблюдению |
Основной симптом хориокарциномы — маточные кровотечения во время беременности или после ее окончания.
Клиническая манифестация метастазов зависит от их локализации (легкие, головной мозг, печень): кровохарканье, острая неврологическая симптоматика и др.
-
• Любая женщина с продолжающимися маточными кровотечениями после беременности (роды/аборт) относится к группе риска наличия трофобластической болезни.
-
2.2. Обследование
При маточных кровотечениях, продолжающихся в течение более чем 8 нед. после беременности (роды/аборт), должен быть выполнен тест на наличие β-ХГЧ в моче.
Рекомендуемый алгоритмм обследования представлен на рис. 1 и 2. Диагностика включает следующие обследования:
-
• для установления диагноза гистологическая верификация не является обязательной, достаточными являются клиническая картина и уровень/динамика β-ХГЧ;
-
• гинекологический анамнез с подробным выяснением особенностей предшествовавшей беременности;
-
• гинекологический осмотр;
-
• УЗИ/МРТ органов малого таза с в/в контрастированием, УЗИ/КТ органов брюшной полости с в/в контрастированием;
-
• определение уровня β-ХГЧ в крови (в табл. 5 представлены показатели β-ХГЧ вне беременности и при нормально протекающей беременности);
-
• рентгенография/КТ легких;
-
• при наличии метастазов в легких — МРТ головного мозга с в / в контрастированием;
-
• при подозрении на пузырный занос — эвакуация пузырного заноса с гистологическим исследованием удаленных тканей и дальнейшим мониторингом уровня β-ХГЧ и инволюции матки;
-
• периодичность мониторинга β-ХГЧ после эвакуации пузырного заноса:
– при частичном пузырном заносе — 1 раз в нед. до нормализации, далее — контроль через 1 мес.;
– при полном пузырном заносе — 1 раз в нед. до нормализации (см. пункт 2.3), далее — ежемесячно в течение 6 мес.;
-
• общий анализ крови;
-
• биохимический анализ крови;
-
• коагулограмма;
-
• общий анализ мочи.
-
2.3. Критерии диагноза, необходимые для инициации лечения (достаточно одного из признаков)
Таблица 5. Значения β-ХГЧ в отсутствие беременности и в различные сроки беременности в норме
|
Сроки беременности, акушерские недели |
Показатель β-ХГЧ, мМЕ/мл |
|
Небеременные женщины |
0–5 |
|
Результат сомнительный |
5–25 |
|
• Беременность 3–4 неделя |
25–156 |
|
• Беременность 4–5 неделя |
101–4870 |
|
• Беременность 5–6 неделя |
1110–31500 |
|
• Беременность 6–7 неделя |
2560–82300 |
|
Сроки беременности, акушерские недели |
Показатель β-ХГЧ, мМЕ/мл |
|
• Беременность 7–8 неделя |
23100–151000 |
|
• Беременность 8–9 неделя |
27300–233000 |
|
• Беременность 9–13 неделя |
20900–291000 |
|
• Беременность 13–18 неделя |
6140–103000 |
|
• Беременность 18–23 неделя |
4720–80100 |
|
• Беременность 23–41 неделя |
2700–78100 |
• Плато уровня β-ХГЧ в 4 последовательных пробах в течение 3 нед. после эвакуации пузырного заноса (1-й, 7-й, 14-й, 21-й дни);
• увеличение на 10 % и более уровня β-ХГЧ в 3 пробах в течение 2 нед. (1-й, 7-й, 14-й дни) после эвакуации пузырного заноса;
• персистенция β-ХГЧ в течение более 6 мес. после эвакуации полного пузырного заноса;
• повышенный уровень β-ХГЧ и наличие отдаленных метастазов (в легких и/или печени и/или головном мозге) при выявленной связи с предшествующей беременностью;
• гистологически верифицированная хориокарцинома.
3. ЛЕЧЕНИЕ3.1. Пузырный занос
Основным методом лечения гестационной трофобластической неоплазии является противоопухолевая лекарственная терапия, позволяющая достичь выздоровления у большинства больных с сохранением репродуктивной функции. Лечение должно быть начато в кратчайшие сроки и проводиться в специализированных отделениях, имеющих опыт лечения таких больных. Кровотечение из опухоли не является противопоказанием к началу ХТ, которую необходимо проводить одновременно с интенсивной гемостатической терапией. Рекомендуемые алгоритмы лечения злокачественных трофобластических опухолей представлены на рис. 3–6.
-
• Вакуум-аспирация пузырного заноса, при необходимости — острый кюретаж полости матки и цервикального канала с обязательным исследованием биопсийного (операционного) материала матки. Пациенткам с резус-отрицательным фактором необходимо ввести антирезус-иммуноглобулин. ХТ после эвакуации пузырного заноса в рутинной практике не проводится.
-
• Хирургическое лечение (гистерэктомия с сальпингэктомией может рассматриваться как начальное лечение только у пациенток, не желающих сохранять фертильность).
-
• Мониторинг β-ХГЧ после эвакуации пузырного заноса:
– при частичном пузырном заносе — 1 раз в нед. до нормализации, далее — контроль через 1 мес.;
– при полном пузырном заносе — 1 раз в нед. до нормализации, далее — ежемесячно в течение 6 мес.
-
3.2. Инвазивный пузырный занос и хориокарцинома
-
• Данные опухоли высоко чувствительны к ХТ. Лекарственная терапия (в сочетании с хирургическим вмешательством или без него) эффективна в 90–100% случаев трофобластической неоплазии низкого риска и в 80–90% случаев высокого риска. Для определения прогноза и тактики лечения необходимо классифицировать опухоль по стадии и группе риска развития резистентности (табл. 2, 3). Лечение следует проводить в специализированной клинике, располагающей современными возможностями диагностики и опытом успешного лечения этой категории больных. Тактика лечения должна быть определена на мультидисциплинарном консилиуме; – при опухолях низкого риска развития резистентности (< 6 баллов) рекомендуется монохимиотерапия (табл. 6, рис. 3);
– при опухолях высокого риска развития резистентности (≥ 7 баллов) — ХТ по схеме EMA-CO (табл. 6, рис. 4);
– при опухолях ультравысокого риска развития резистетности (≥ 13 баллов) возможно использование схемы EMA-CO, однако предпочтительнее схема EP/EMA (рис. 5). Для профилактики неконтролируемого лизиса опухоли и кровотечения, особенно при метастазах в головном мозге, а также в случае неудовлетворительного общего состояния пациентки (ECOG ≥ 3 баллов), целесообразно начинать индукционную ХТ с использования редуцированного режима: этопозид 100 мг/м 2 в/в и цисплатин 20 мг/м 2 в/в в 1-й и 2-й дни, 1–3 курса еженедельно под контролем β-ХГЧ до начала стандартной ХТ;
– у пациентов с метастазами в головном мозге увеличение дозы метотрексата в режимах EP/EMA и EMA-CO до 1000 мг/м 2 улучшает проникновение через гематоэнцефалический барьер; необходимо увеличить длительность инфузии с 12 до 24 часов и дополнительно использовать кальция фолинат 15 мг внутрь каждые 6 часов, 12 доз, начиная через 32 часа после начала инфузии метотрексата;
-
• при метастазах в головном мозге возможно стереотаксическое облучение или облучение гамма-ножом, а также ЛТ всего головного мозга в СОД 30 Гр суточными фракциями по 2 Гр одновременно с ХТ;
-
• самостоятельное хирургическое лечение (гистерэктомия с сальпингэктомией) при неметастатической форме может рассматриваться только у пациенток, не желающих сохранять фертильность;
-
• лекарственное лечение рекомендуется проводить до нормализации β-ХГЧ с последующими 2–3 консолидирующими курсами ХТ;
-
• требуется строгое соблюдение сроков начала очередного курса ХТ;
-
• мониторинг после лечения включает анализ β-ХГЧ ежемесячно в течение 12 мес.;
-
• в течение 12 мес. после лечения рекомендуется контрацепция, предпочтительны гормональные оральные контрацептивы.
Таблица 6. Режимы химиотерапии 1-й линии трофобластических опухолей
|
Группа риска |
Режим химиотерапии |
|
Низкий риск |
повторение курсов каждые 2 недели, (с 15-го дня, считая от 1-го дня предыдущего курса) |
|
Высокий риск |
ЕМА-СО
с последующей 12-часовой инфузией в дозе 200 мг/м²) в 1-й день – кальция фолинат 15 мг в/м через 24 часа после введения метотрексата, затем — каждые 12 ч (всего 4 дозы)
– Г-КСФ (короткого действия) 5 мкг/кг п/к в течение 3–4 дней в неделю, т. е. на 4-й, 5-й, 6-й, (7-й) дни и на 10-й, 11-й, 12-й, (13-й) дни каждого курса EMA-CO Повторение курсов с 15-го дня, считая от 1-го дня предыдущего курса |
|
Ультравысокий риск 4,5 |
ЕМА-ЕP
с последующей 12-часовой инфузией в дозе 200 мг/м²) в 1-й день – кальция фолинат 15 мг в/м через 24 ч после введения метотрексата, затем — каждые 12 ч (всего 4 дозы)
– Г-КСФ (короткого действия) 5 мкг/кг п/к в 9–14-й дни Повторение курсов с 15-го дня, считая от 1-го дня предыдущего курса ЕР-ЕМА
с последующей 12-часовой инфузией в дозе 200 мг/м²) 8 день – кальция фолинат 15 мг в/м через 24 ч после введения метотрексата, затем — каждые 12 ч (всего 4 дозы)
Повторение курсов с 15-го дня, считая от 1-го дня предыдущего курса |
-
1 Предпочтительный режим ввиду равной эффективности при меньшей токсичности.
-
2 Высокая вероятность неэффективности у пациенток с хорионкарциномой.
-
3 Чаринг-Кросский протокол, используемый в ряде экспертных клиник: метотрексат 50 мг в /м в 1-й, 3-й, 5-й, 7-й дни, кальция фолинат 15 мг внутрь во 2-й, 4-й, 6-й, 8-й дни через 24 часов после введения метотрексата; повторение курсов — с 15-го дня, считая от 1-го дня предыдущего курса.
-
2 Длительность инфузии метотрексата не должна превышать 12 часов в силу меньшей эффективности более длительной инфузии.
-
3 При метастазах в головном мозге рекомендуется увеличить дозу метотрексата до 1000 мг /м2, увеличить продолжительность инфузии с 12 до 24 часов, дополнительно использовать кальция фолинат 15 мг внутрь каждые 6 часов, всего 12 доз, начиная через 32 часа после начала инфузии метотрексата.
-
4 Возможно использование режима EMA-CO, однако, предпочтительнее режимы ЕМА-ЕP либо EP-EMA.
-
5 Для профилактики неконтролируемого лизиса опухоли и кровотечения, особенно при метастазах в головном мозге, целесообразно начинать лечение с режима «щадящей» индукции (этопозид 100 мг /м 2 в /в кап. и цисплатин 20 мг /м 2 в /в кап. в 1-й и 2-й дни, повторение курсов еженедельно в течение 1–3 недель до начала стандартной ХТ); у пациентов с метастазами в головном мозге увеличение дозы метотрексата до 1000 мг /м 2 улучшает проникновение через гематоэнцефалический барьер.
-
3.3. Опухоль плацентарного ложа и эпителиоидная трофобластическая опухоль
При метастазах в головном мозге возможно стереотаксическое облучение или облучение гамма-ножом, либо ЛТ всего головного мозга в СОД 30 Гр суточными фракциями по 2 Гр одновременно с ХТ.
Решение вопроса о ЛТ должно приниматься на консилиуме с участием специалистов, имеющих опыт лечения таких больных.
-
• Эти опухоли менее чувствительны к ХТ, имеют более высокую вероятность развития резистентности. Первым этапом рекомендуется хирургическое лечение (гистерэктомия с биопсией тазовых л/у, удаление потенциально операбельных метастатических очагов).
-
• При I cтадии болезни после выполнения гистерэктомии возможно наблюдение при четком мониторинге с помощью определения β-ХГЧ или КТ/МРТ (при неинфор-мативности β-ХГЧ) при соблюдении всех следующих условий:
– интервал от последней беременности менее 2 лет;
– поверхностная инвазия;
– отсутствие некротической ткани в опухоли;
– количество митозов менее 5 / 10.
-
• Во всех остальных случаях показано проведение системной лекарственной терапии с назначением адъювантной ХТ или ХТ 1-й линии при метастатических формах заболевания [ХТ с включением препаратов платины (EMA/EP, EP/EMA) либо другие режимы (TP/TE, BEP, VIP, ICE)].
-
• В случае крайней заинтересованности в сохранении фертильности возможна попытка неоадъювантной ХТ с включением препаратов платины и этопозида [(EMA/EP, EP/EMA)
-
3.4. Лечение резистентных форм
либо другие режимы (TP/TE, BEP, VIP, ICE)] с последующей органосохраняющей операцией и адъювантной ХТ в центрах, обладающих опытом лечения таких пациенток. Рекомендуемый алгоритм лечения опухоли плацентарного ложа и эпителиоидной трофобластической опухоли представлен на рис. 6.
Резистентность опухоли к ХТ 1-й линии возможна в 5% случаев трофобластической болезни низкого риска и в 30–40% трофобластической неоплазии высокого риска. Признаками резистентности являются:
-
• отсутствие снижения β-ХГЧ (плато) или снижение уровня β-ХГЧ менее чем на 10% в трех последовательных анализах крови, сданных в течение 10 дней;
-
• увеличение уровня β-ХГЧ во время или после окончания ХТ (в ближайшие 6 мес.) в трех последовательных анализах крови, сданных в течение 10 дней. Необходимо повторное полное клинико-инструментальное обследование с перерасчетом группы риска по FIGO (в соответствии с новой суммой баллов, табл. 3), лекар-ственное/комбинированное лечение (табл. 7).
Таблица 7. Лечение резистентных форм трофобластических опухолей
|
Группа риска |
Режим химиотерапии |
|
Низкий риск 1 |
|
|
Высокий риск 1 |
– ТР:
– ТЕ:
Г-КСФ (пролонгированного действия) 6 мг п/к во 2-й и в 16-й дни
– блеомицин 30 мг в/в в 1-й, 3-й, 5-й дни или в 1-й, 8-й, 15-й дни – этопозид 100 мг/м 2 в/в в 1–5-й дни – цисплатин 20 мг/м 2 в/в в 1–5-й дни Г-КСФ 5 (пролонгированного действия) 6 мг в 8-й день или Г-КСФ 5 (короткого действия) 5 мкг/кг п/к в 6–14-й дни. Повторение курсов каждые 3 нед., считая от первого дня предыдущего курса |
|
Группа риска |
Режим химиотерапии |
|
Высокий риск 1 |
• VIP – этопозид 75 мг/м 2 в/в в 1–5-й дни – ифосфамид 1200 мг/м 2 в/в в 1–5-й дни – месна 100% от дозы ифосфамида в/в болюсно за 15 мин. до введения ифосфамида, затем — через 4 и 8 часов после введения ифосфамида в 1–5-й дни – цисплатин 20 мг/м 2 в/в в 1–5-й дни Г-КСФ (пролонгированного действия) 6 мг в 8-й день или Г-КСФ (короткого действия) 5 мкг/кг п/к в 6–14-й дни. Повторение курсов каждые 3 нед., считая от первого дня предыдущего курса
– ифосфамид 1200 мг/м 2 в/в в 1–3-й дни – месна 100% от дозы ифосфамида в/в болюсно за 15 мин. до введения ифосфамида, затем — через 4 и 8 часов после введения ифосфамида в 1–3-й дни – карбоплатин AUC4 в/в в 1-й день – этопозид 75 мг/м 2 в/в в 1–3-й дни Г-КСФ (пролонгированного действия) 6 мг п/к в 4-й день или Г-КСФ (короткого действия) 5 мкг/кг п/к в 6–14-й дни. Повторение курсов каждые 3 нед., считая от первого дня предыдущего курса
– паклитаксел 250 мг/м 2 в/в в 1-й день – ифосфамид 1500 мг/м 2 в/в во 2–5-й дни – месна 100% от дозы ифосфамида в/в болюсно за 15 мин. до введения ифосфамида, затем — через 4 и 8 часов после введения ифосфамида во 2–5-й дни – цисплатин 25 мг/м 2 в/в во 2–5-й дни. Повторение курсов каждые 3 нед., считая от первого дня предыдущего курса Дополнительные режимы для пациенток с резистентностью к полихимиотерапии6
Повторение курсов каждые 3 нед., считая от первого дня предыдущего курса
Повторение курсов каждые 4 нед., считая от первого дня предыдущего курса
– авелумаб 800 мг в/в каждые 2 нед.
|
-
6 Лекарственные препараты, которые продемонстрировали эффективность при лечении резистентных форм в выборочных исследованиях.
-
7 Возможно в комбинации с системной лекарственной терапией.
-
3.5. Трофобластическая болезнь на фоне развивающейся беременности
Трофобластическая болезнь на фоне успешно развивающейся беременности — крайне редкое состояние и встречается с частотой 1 случай на 22–100 тыс. беременностей; наблюдается при бихориальных беременностях (на фоне замещения пузырным заносом одного из плодов), крайне редко — при монохориальных беременностях (в случае интраплацентарной хориокарциномы). Существует возможность пролонгирования таких беременностей.
Диагностика
-
• Гистологической верификации не требуется;
-
• УЗИ малого таза, брюшной полости;
-
• МРТ малого таза, брюшной полости без контрастирования;
-
• оценка уровня β-ХГЧ в динамике;
-
• рентгенография легких с экранированием области матки или МРТ легких;
-
• пренатальное инвазивное тестирование кариотипа плода в случае сомнения, является ли беременность полным пузырным заносом с сосуществующим нормальным близнецом или возможной одноплодной беременностью с частичным пузырным заносом;
-
• пренатальное инвазивное тестирование кариотипа плода при монохориальной беременности в случаях подозрения на интраплацентарную хориокарциному;
-
• оценка функции щитовидной железы;
-
• оценка акушерских рисков.
-
3.6. Лечение пациенток с остаточной опухолью
-
3.7. Наблюдение
Необходимо совместное принятие решения о пролонгировании/прерывании беременности междисциплинарным консилиумом с участием онколога, акушера-гинеколога, неонатолога. В случае пролонгирования беременности существует риск преждевременных родов, замершей беременности, кровотечения, перинатальных осложнений.
Ведение пациентки осуществляется акушером-гинекологом, онкологом. Наблюдение и родоразрешение должны осуществляться в специализированном перинатальном центре, имеющем опыт ведения таких пациенток.
В случае пролонгирования беременности после родов обязательно гистологическое исследование опухоли, мониторинг уровня β-ХГЧ, мониторинг инволюции матки, КТ грудной, брюшной полости.
В составе комбинированного лечения резистентных опухолей рассматривается в том числе хирургический метод лечения (гистеротомия, гистерэктомия, метастазэктомия).
Остаточные «опухолевые узлы» после завершения лечения и нормализации уровня β-ХГЧ не всегда требуют хирургического удаления, возможно их динамическое наблюдение. Нормальный уровень β-ХГЧ даже при наличии визуализируемой «остаточной опухоли» в матке или других локализаций свидетельствует о ремиссии и дополнительного лечения не требует.
Повышение уровня β-ХГЧ (в 3 последовательных исследованиях в течение 14 дней) в период ремиссии у больных с «остаточной опухолью» свидетельствует о неизлечен-ности (резистентности) опухоли. Если после тщательного обследования «остаточная опухоль» является единственной локализацией, следует рассмотреть вопрос о хирургическом лечении.
Необходим тщательный мониторинг за больными трофобластическими новообразованиями:
-
• После удаления частичного пузырного заноса наблюдение завершается после двух отрицательных результатов β-ХГЧ, полученных с интервалом 4 нед. (получение отрицательного результата, далее — контроль через 4 нед., при отрицательном β-ХГЧ наблюдение завершается)
-
• После удаления полного пузырного заноса и нормализации уровня β-ХГЧ в течение 56 дней наблюдение следует продолжать еще 6 мес. от момента удаления пузырного заноса (с ежемесячным определением β-ХГЧ)
-
• После удаления полного пузырного заноса в отсутствие нормализации β-ХГЧ в течение 56 дней следует продолжать наблюдение до его нормализации и далее в течение еще 6 мес. от момента нормализации β-ХГЧ (с ежемесячным определением β-ХГЧ)
-
• После окончания лечения по поводу злокачественной трофобластической болезни рекомендуется ежемесячное определение β-ХГЧ в течение года
-
• Контрацепция после окончания лечения злокачественной трофобластической болезни рекомендуется в течение 1 года, предпочтение отдается гормональным контрацептивам.
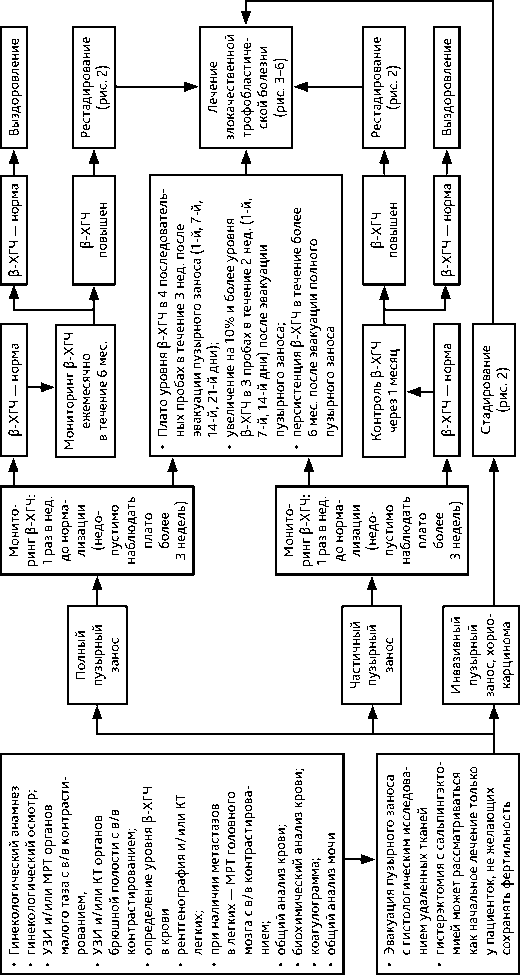
Рисунок 1. Рекомендуемый алгоритм лечения пузырного заноса
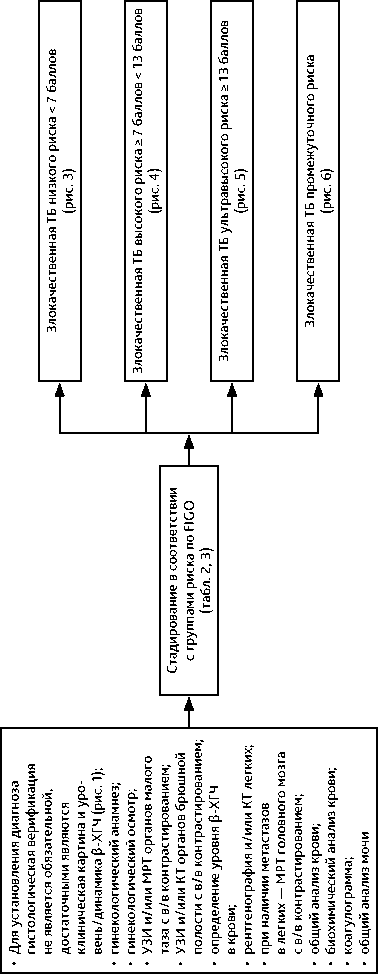
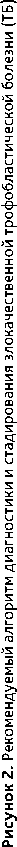
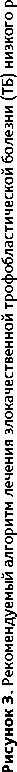
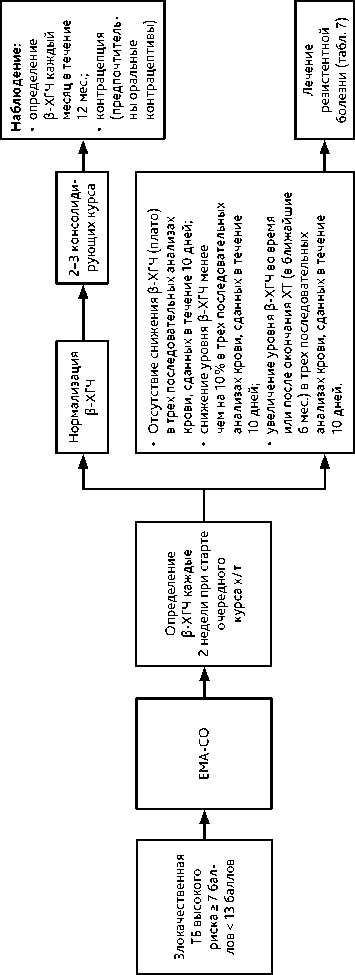
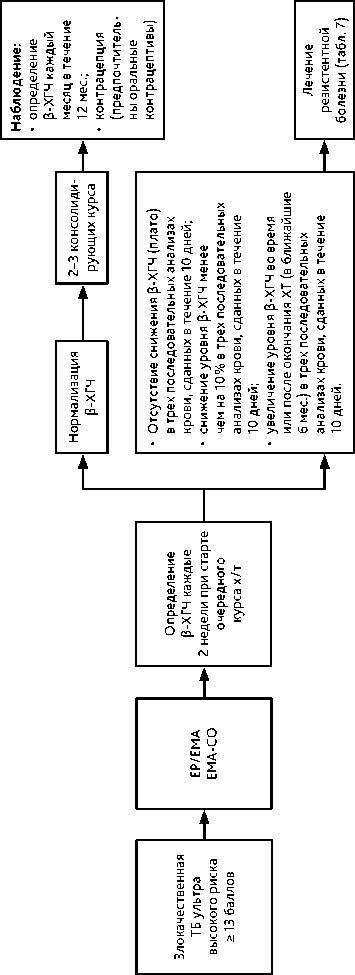
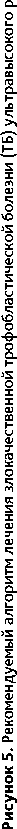
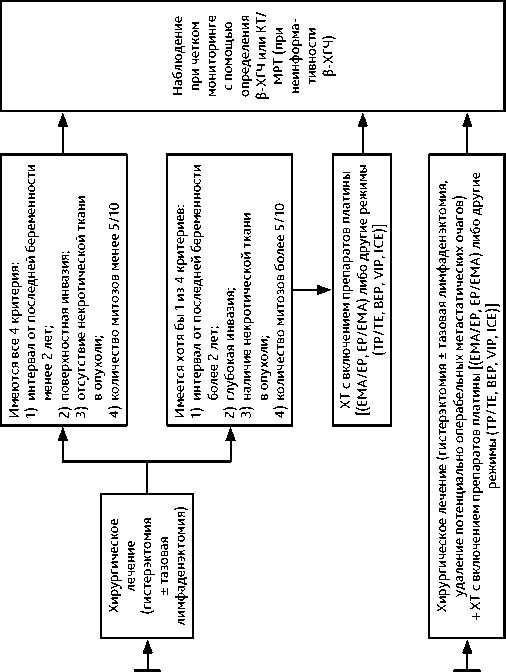

Рисунок 6. Рекомендуемый алгоритм лечения злокачественной трофобластической болезни (ТБ) промежуточного риска (опухоли плацентарного ложа и эпителиоидной трофобластической опухоли)
| том /vol. 14(3s2) 2024
ЗЛОКАЧЕСТВЕННЫЕ
Malignant
Tumors


