Значение удаления внутренней пограничной мембраны при лечении диабетического макулярного отека: серия клинических случаев
Автор: Телятов Б.А., Балкар С.Ш.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4S1 т.19, 2024 года.
Бесплатный доступ
Актуальность. Витреоретинальная хирургия (ВРХ) признана предпочтительным методом лечения диабетического макулярного отека (ДМО), сопутствующего дополнительной патологии витреомакулярного интерфейса (ВМИ). Эмпирические данные, полученные в результате многочисленных исследований, дают противоречивые результаты, поэтому необходимость пилинга внутренней ограничивающей мембраны (ВПМ) остается нерешенной.Цель. Выяснить результаты хирургического вмешательства у пациентов с ДМО в результате эпимакулярного фиброза (ЭМФ), сравнив случаи с пилингом ВПМ и без него.Материалы и методы. В этой рукописи представлена сравнительная оценка трех клинических случаев. У пациентов были аналогичные клинические проявления и исторические медицинские данные. Во всех случаях пациентам проводили ВРХ по поводу ДМО, сочетающегося с ЭМФ. В двух случаях был проведен пилинг ВПМ, а в третьем случае ВПМ был сохранен.Результаты. Анализ данных наблюдений и оценка анатомических и функциональных параметров выявили осложнения у первого и второго пациентов на позднем послеоперационном этапе, тогда как у третьего пациента состояние стабилизировалось.Заключение. Представленные клинические случаи показывают, что анатомические и функциональные результаты не всегда коррелируют. Повышенный риск осложнений, связанных с нарушением архитектуры и функциональности сетчатки во время пилинга, требует критической оценки клинического обоснования этого метода.
Сахарный диабет, диабетическая ретинопатия, диабетический макулярный отек, витрэктомия, пилинг впм, оптическая когерентная томография
Короткий адрес: https://sciup.org/140307899
IDR: 140307899 | DOI: 10.25881/20728255_2024_19_4_S1_49
The importance of removing the inner boundary membrane in the treatment of diabetic macular edema: a series of clinical cases
Vitreoretinal surgery (VRH) is recognized as the preferred method of treating diabetic macular edema (DMO), concomitant with additional pathology of the vitreomacular interface (VMI). Empirical data obtained as a result of numerous studies give contradictory results, therefore, the need for peeling of the internal limiting membrane (VPM) remains unresolved.Purpose. To find out the results of surgical intervention in patients with DMO as a result of epimacular fibrosis (EMF) by comparing cases with and without HPV peeling.Materials and methods. This manuscript presents a comparative assessment of three clinical cases. The patients had similar clinical manifestations and historical medical data. In all cases, patients underwent HRH for DMO combined with EMF. In two cases, the VPM was peeled, and in the third case, the VPM was preserved.Results. An analysis of the observational data and an assessment of anatomical and functional parameters revealed complications in the first and second patients at the late postoperative stage, while in the third patient the condition stabilized.
Текст научной статьи Значение удаления внутренней пограничной мембраны при лечении диабетического макулярного отека: серия клинических случаев
Актуальность
Международная диабетическая федерация (International Diabetes Federation, IDF) сообщила, что в 2021 году более 537 миллионов человек трудоспособного возраста страдали сахарным диабетом (СД). Согласно прогнозам, к 2030 году число диагностированных пациентов с диабетом возрастет до 700 миллионов [1].
Наиболее часто встречаемыми причинами возникновения отека в макулярной области являются: возрастная макулярная дегенерация (ВМД) [2], окклюзия центральной вены сетчатки [3] и диабетический макулярный отек (ДМО) [4; 5].
В настоящее время структура и функция макулярной области и их роль в возникновении диабетического макулярного отека и эпимакулярного фиброза (ЭМФ) полностью не изучены. ДМО, коррелирует с нейродеге-неративными биомаркерами [6], и зависит от накопления в витреальной полости воспалительных агентов, в основном фактора роста эндотелия сосудов (VEGF) [7–10]
механическими силами в стекловидном теле, которые приводят к образованию ЭМФ [10; 11]. Основным методом лечения является введение ингибиторов ангиогенеза в витреальную полость [5; 10; 12], но из-за тракционного фактора их эффективность в лечении ДМО значительно ограничена [5].
Витреоретинальная хирургия является эффективным методом лечения устойчивого диабетического макулярного отека, сочетающегося с ЭМФ. Эта процедура обычно включает микроинвазивную витрэктомию с последующем удалением эпимакулярной мембраны. При этом, необходимость одновременного пилинга внутренней пограничной мембраны (ВПМ) по-прежнему остается предметом постоянных дискуссий [12; 13], а интраоперационная панретинальная коагуляция сетчатки не оказывает значимого влияния на состояние макулярной зоны [14].
Когда эпимакулярный фиброз возникает в результате диабетического макулярного отека, многие исследователи

рекомендуют проводить витрэктомию с пилингом ВПМ. В соответствии с этими исследованиями происходит значительное уменьшение центральной толщины сетчатки (ЦТС), повышение максимально коррегируемой остроты зрения (МКОЗ) и устранение факторов, способствующих развитию дальнейшей пролиферации [15–18].
Исследователи указывают на недостатки методологии, включая повреждение клеток Мюллера при повышении уровня адгезии ВПМ, что приводит к нарушению структуры сетчатки, возникновению субфовеолярной атрофии [19; 20] и последующему снижению светочувствительности [21]. В связи с этим была предложена технология контролируемого пилинга, которая повышает точность и снижает травматичность, сохраняя зрительные функции [22].
Тем не менее многочисленные научные исследования не выявили существенных функциональных и анатомических преимуществ пилинга ВПМ при лечении тракционного диабетического макулярного отека [13; 17; 20; 23].
Цель: продемонстрировать результаты хирургического лечения пациентов с ДМО и ЭМФ, сравнив случаи с пилингом ВПМ и без него.
Материал и методы
В статье представлены 3 клинических случая, в которых проводилось хирургическое лечение пациентов с ДМО в сочетании с ЭМФ.
Лечение проводилось на базе ФГБНУ «НИИГБ им. М.М. Краснова».
Клинический случай №1. Пациент Г., 63 года. В результате анализа стандартных и специализированных офтальмологических обследований был установлен следующий клинический диагноз: OU — непролиферативная диабетическая ретинопатия, диабетический макулярный отек и эпимакулярный фиброз. Данные, относящиеся к анамнезу, систематически представлены в таблице 1.
Методология и последовательные этапы ВРХ. На начальном этапе проводилась трехпортовая центральная витрэктомия методом 25G. На следующем этапе был проведен ряд вмешательств на структурах ВИ: после индукции ЗОСТ и удаления ЗГМ проводили окраску ВПМ эндовитреальным красителем, который затем удаляли. С помощью эндовитреального пинцета выполнен мебрано-пилинг и пилинг ВПМ. Операция завершена заполнением витреальной полости физиологическим раствором.
Клинический случай №2. Больная Т., 30 лет. По результатам стандартного и специализированного офтальмологического обследования установлен диагноз: OU - Пролиферативная диабетическая ретинопатия. Состояние после лазеркоагуляции сетчатки. OS - Эпимакуляр-ный фиброз. Диабетический макулярный отек. Данные анамнеза представлены в таблице 1 и на рисунке 1.
Техника и этапы ВРХ: 2 этапа операции аналогично случаю 1. Операция завершена заполнением витреальной полости физиологическим раствором.
Табл. 1. Данные анамнеза и дооперационного обследования пациентов
|
Случай 1 |
Случай 2 |
Случай 3 |
|
|
Пол |
Мужской |
Женский |
Женский |
|
Возраст, лет |
63 |
30 |
60 |
|
Тип СД |
2 |
1 |
2 |
|
Диагноз |
НПДР, ДМО, ЭМФ |
ПДР, ДМО, ЭМФ |
ПДР, ТРОС, Частичный гемофтальм |
|
МКОЗ |
0,1 |
0,4 |
Движение руки у лица |
|
МКОЗ (ETDRS) |
36 |
65 |
2 |
|
ЦТС, МКМ |
599 |
408 |
629* |
|
ЭМФ |
ДА |
Да |
Да |
|
Катаракта |
Артифакия |
Артифакия |
Артифакия |
|
Состояние фовеа |
Интраре-тинальные кисты >70% толщины, ДМО |
Макулярный профиль деформирован, ОНЭ |
**Пролиферативная ткань с тракционным компонентом |
Примечание : * – по данным ИОКТ; **по данным ОКТ (визуализация при гемофтальме); СД – сахарный диабет; НПДР – непролиферативная диабетическая ретинопатия; ДМО – диабетический макулярный отек, ЭМФ – эпимакулярный фиброз; МКОЗ – максимально корригированная острота зрения, определенная с помощью визометрии по таблице Головина-Сивцева; МКОЗ (ETDRS) – МКОЗ, определенная по таблице ETDRS; ЦТС – центральная толщина сетчатки; ОНЭ – отслойка нейроэпителия сетчатки.
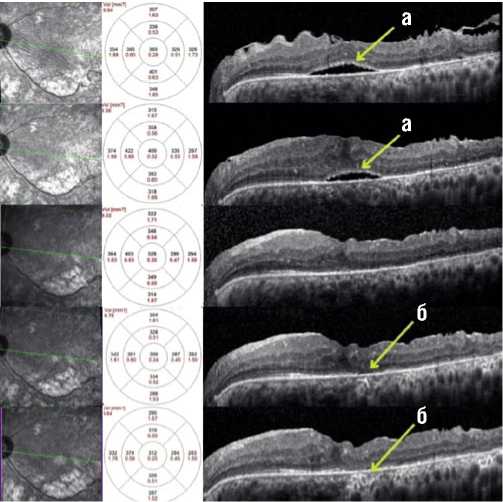
Рис. 1. ОКТ, клинический случай №2 в динамике на фоне лечения. Сверху вниз, соответственно – до лечения, 1, 3 и 6 месяцев и отдаленные результаты (1,5 года) после хирургии. Пилинг ВПМ выполнен (а – сохраняющаяся в послеоперационном периоде ОНЭ, б – зона атрофии ПЭС).
Клинический случай №3. Больная С., 60 лет. По результатам стандартного и специализированного офтальмологического обследования установлен диагноз: OU – Пролиферативная диабетическая ретинопатия. OS – Частичный гемофтальм. Тракционная отслойка

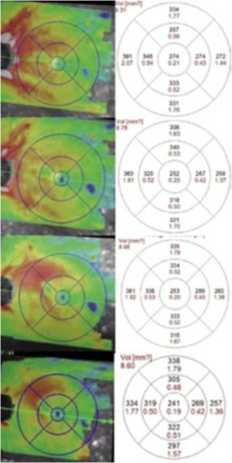
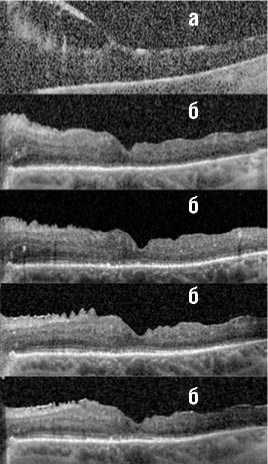
Рис. 2. ОКТ, клинический случай №3 в динамике на фоне лечения. Сверху вниз, соответственно – до лечения, 1, 3 и 6 месяцев и отдаленные результаты (1,5 года) после хирургии. ВПМ сохранена (а – ге-мофтальм, пролиферативный фиброзный тяж, б – зона фовеа стабильна, макулярный профиль сохранен).
сетчатки. Данные анамнеза представлены в таблице 1 и на рисунке 2.
Техника и этапы ВРХ: 1-м этапом выполнена трехпортовая субтотальная витрэктомия 25G. На 12 час установлен источник дополнительного освещения (шендельер) 29G. С применением склерокомпрессии выполнено удаление базиса стекловидного тела. На 2-м этапе отлично от случая 1,2: с помощью эндовитреального пинцета и вертикальных эндовитреальных ножниц выполнено частичное удаление пролиферативных тканей в области ДЗН и сосудистых аркад. Диатермокоагуляция источников кровотечения. С помощью эндовитреального пинцета выполнен мебранопилинг без пилинга ВПМ. Операция завершена заполнением витреальной полости воздухом (менее 1/5 объема) и физиологическим раствором.
Результаты и обсуждение
Таблица 2 иллюстрирует изменения анатомических и функциональных аспектов оперированных глаз через 1, 3 и 6 месяцев после операции, а также долгосрочные результаты. Во всех случаях через месяц после операции наблюдалось незначительное улучшение остроты зрения и снижение значений ЦТС и ЦМО по сравнению с исходным уровнем. Окончательный анатомический и функциональный результат лечения оценивался через 6 месяцев после операции и основывался на долгосрочных показателях (1,5– 2 года). Результаты исследования представлены на рисунках 1,2 и в таблице 2. В случае №1 мониторинг наблюдения отслеживает прогрессирование послеоперационной ДМО и долгосрочное прогрессирование фовеолярной атрофии. В случае №2 через 6 месяцев наблюдалась парафовеолярная атрофическая область. В случае №3 через 6 месяцев ДМО не
Табл. 2. Данные послеоперационного динамического наблюдения пациентов
|
Случай 1 |
Случай 2 |
Случай 3 |
|
|
Объем удаления впм |
пилинг ВПМ |
пилинг ВПМ |
ВПМ сохранена |
|
Терапия АНТИ-VEGF в послеоперационном периоде |
да |
нет |
нет |
|
1 месяц после операции |
|||
|
МКОЗ |
0,1 |
0,3 |
0,3 |
|
МКОЗ (ETDRS) |
35 |
61 |
62 |
|
ЦТС, МКМ |
373 |
409 |
274 |
|
Состояние фовеа |
деформация профиля, интраретиналь-ные кисты <70% толщины |
деформация профиля, онэ в области фовеа |
отек отсутствует, нормализация фовеального профиля и ЦТС |
|
3 месяца после операции |
|||
|
МКОЗ |
0,15 |
0,4 |
0,4 |
|
МКОЗ (ETDRS) |
40 |
67 |
65 |
|
ЦТС, МКМ |
238 |
329 |
252 |
|
Состояние фовеа |
деформация профиля, интраретиналь-ные кисты <50% толщины |
отек отсутствует, нормализация фовеального профиля и ЦТС |
отек отсутствует, нормализация фовеального профиля и ЦТС |
|
6 месяцев после операции |
|||
|
МКОЗ |
0,1 |
0,5 |
0,4 |
|
МКОЗ (ETDRS) |
38 |
69 |
66 |
|
ЦТС, МКМ |
203 |
309 |
253 |
|
Состояние фовеа |
деформация профиля, интраретиналь-ные кисты >70% толщины |
отек отсутствует, нормализация фовеального профиля, атрофический очаг субфовеолярно |
отек отсутствует, нормализация фовеального профиля и ЦТС |
|
Отдаленные результаты (1,5–2 года) |
|||
|
МКОЗ |
0,13 |
0,5 |
0,4 |
|
МКОЗ (ETDRS) |
39 |
73 |
68 |
|
ЦТС, МКМ |
190 |
312 |
241 |
|
Состояние фовеа |
деформация профиля, интраретиналь-ные кисты >70% толщины |
отек отсутствует, нормализация фовеального профиля, увеличение атрофического очага |
отек отсутствует, нормализация фовеального профиля и ЦТС |
было обнаружено. Большинство исследований, в которых необходим пилинг ВПМ, основаны на предположении, что пилинг не только удаляет тракционный компонент, но и способствует улучшению резорбции отека [24], однако изменения плотности капиллярной сосудистой сети не происходит [25]. В этих клинических случаях следует отметить, что в случае №1, когда ВПМ удаляется, ДМО снова появляется при использовании ингибиторов ангиогенеза, как в случае №3, когда ВПМ сохраняется, ДМО не возникает на поздней послеоперационной стадии. Также возможно, что пилинг ВПМ привел к послеоперационной атрофии фовеальной области в случае №1 и субфовеолярной атрофии пигментного эпителия в случае №2.
Заключение
Витреоретинальная хирургия является одним из методов лечения диабетического макулярного отека, однако анатомические и функциональные результаты не всегда совпадают. Исследование показало, что хотя через месяц после операции наблюдается небольшое улучшение остроты зрения и снижение центральной толщины сетчатки, на более поздних сроках возникают послеоперационные осложнения, такие как диабетический макулярный отек и фовеолярная атрофия при проведении пилинга ВПМ. Это подчеркивает сложность клинических исходов и необходимость дальнейших исследований для понимания механизмов, влияющих на результаты после операции.
Список литературы Значение удаления внутренней пограничной мембраны при лечении диабетического макулярного отека: серия клинических случаев
- IDF DIABETES ATLAS 10th edition 2021. [URL].
- Haydinger C. D. et al. Mechanisms of macular edema //Frontiers in Medicine. – 2023. – Т. 10. – С. 1128811.
- Петрачков Д. В., Кривошеина О. И., Запускалов И. В. Наш опыт лечения тромбоза центральной вены сетчатки и ее ветвей с помощью эпиретинального введения гемазы // Офтальмохирургия. – 2008. – №4. – С. 32-34.
- Казайкин В. Н. Диабетическая ретинопатия: клиника, диагностика и лечение/ВН Казайкин-М., ООО «НПЦ Мединформ», 2016.
- Prevalence and risk factors for epiretinal membrane: the Singapore Epidemiology of Eye Disease study / N. Cheung, S.P. Tan, S.Y. Lee [et al.] // Br.J. Ophthalmol. – 2017. – Vol. 101, №3. – P. 371-376
- Петрачков Д. В., Будзинская М. В., Павлов В. Г. [и др.]. Нейродегенеративные биомаркеры ответа на терапию диабетического макулярного отека // Вестник офтальмологии. – 2020. – Т. 136, №4-2. – С. 201-206. – DOI 10.17116/oftalma2020136042201.
- Semeraro F. et al. Diabetic retinopathy: vascular and inflammatory disease //Journal of diabetes research. – 2015. – Т. 2015. – №. 1. – С. 582060.
- Stehphen J. Ryan. Non proliferative diabetic retinopathy, Chap 67 // In: Retina – Vol II – 4th edn – pp 1275–1276
- dell′ Omo R. et al. Vitreous mediators in retinal hypoxic diseases //Mediators of Inflammation. – 2013. – Т. 2013. – №. 1. – С. 935301.
- Шишкин М.М., Юлдашева Н.М. Диабетический макулярный отек: современные взгляды на патогенез и выбор методов лечения // Вестник Национального медико-хирургического Центра им. Н. И. Пирогова. 2012. №1.
- Agarwal D. et al. The vitreomacular interface in diabetic retinopathy //Journal of Ophthalmology. – 2015. – Т. 2015. – №. 1. – С. 392983.
- Петрачков Д. В., Будзинская М. В., Аржуханов Д. Д. Роль пилинга внутренней пограничной мембраны сетчатки в лечении диабетического макулярного отека //Вестник офтальмологии. – 2020. – Т. 136. – №. 4-2. – С. 359-366.
- Khattab A. A. A., Ahmed M. M., Hammed A. H. Pars plana vitrectomy for tractional diabetic macular edema with or without internal limiting membrane peeling //Medical Hypothesis, Discovery and Innovation in Ophthalmology. – 2022. – Т. 11. – №. 3. – С. 110.
- Петрачков Д. В., Барышев К. В., Аржуханов Д. Д. Влияние интраоперационной панретинальной лазеркоагуляции сетчатки на морфометрические показатели макулярной области у пациентов с диабетической ретинопатией в ранние сроки наблюдения // Саратовский научно-медицинский журнал. – 2021. – Т. 17, №2. – С. 356-361.
- Петрачков Д. В., Будзинская М. В., Матющенко А. Г. [и др.]. Вискодиссекция с контрастированием эпиретинальных мембран в хирургии пролиферативной диабетической ретинопатии // Вестник офтальмологии. – 2021. – Т. 137, №4. – С. 18-23. DOI 10.17116/oftalma202113704118.
- Pendergast S. D. et al. Vitrectomy for diffuse diabetic macular edema associated with a taut premacular posterior hyaloid //American journal of ophthalmology. – 2000. – Т. 130. – №. 2. – С. 178-186.
- Yanyali A. et al. Modified grid laser photocoagulation versus pars plana vitrectomy with internal limiting membrane removal in diabetic macular edema //American journal of ophthalmology. – 2005. – Т. 139. – №. 5. – С. 795-801.
- Uemura A. et al. Visual field defects after uneventful vitrectomy for epiretinal membrane with indocyanine green–assisted internal limiting membrane peeling //American journal of ophthalmology. – 2003. – Т. 136. – №. 2. – С. 252-257.
- Tadayoni, R. Choroidal Neovascularization Induces Retinal Edema and its Treatment Addresses this Problem / R. Tadayoni // J. Ophthalmic Vis. Res. – 2014. – Vol. 9, №4. – P. 405-406.
- Romano M. R. et al. Macular hypotrophy after internal limiting membrane removal for diabetic macular edema //Retina. – 2014. – Т. 34. – №. 6. – С. 1182-1189.
- Аржуханов Д. Д., Петрачков Д. В., Матющенко А. Г. Влияние толщины и сосудистой плотности сетчатки на ее светочувствительность при диабетическом макулярном отеке // Точка зрения. Восток - Запад. – 2021. – №2. – С. 37-40. DOI 10.25276/2410-1257-2021-2-37-40.
- Патент №2751284 C1 Российская Федерация, МПК A61F 9/007. Способ пилинга внутренней пограничной мембраны (ВПМ) сетчатки: №2020139590: заявл. 02.12.2020: опубл. 12.07.2021 / Д. В. Петрачков, В. М. Филиппов, А. Г. Матющенко, В. Г. Павлов; заявитель Федеральное государственное бюджетное научное учреждение “Научно-исследовательский институт глазных болезней”.
- Yamamoto T. et al. Vitrectomy for diabetic macular edema with and without internal limiting membrane removal //Ophthalmologica. – 2005. – Т. 219. – №. 4. – С. 206-213.
- Bikbov M. M., Fayzrakhmanov R. R., Kalanov M. R. Effect of internal limiting membrane peeling on morpho-functional state of the retina in patients with proliferative diabetic retinopathy (preliminary report) //Vestnik oftalmologii. – 2018. – Т. 134. – №. 1. – С. 63-69.
- Филиппов В. М., Петрачков Д. В. Влияние пилинга внутренней пограничной мембраны на сосудистую плотность капиллярных сплетений сетчатки // Современные технологии в офтальмологии. – 2023. – №2(48). – С. 140-148. DOI 10.25276/2312-4911-2023-2-140-148.


