2-ундецилоксиэтанол-1 – агрегационный феромон черных сосновых усачей рода Monochamus: синтез и испытания
Автор: Фролова Л.Л., Кукольщикова Ю.А., Кучин А.В., Вендило Н.
Журнал: Известия Коми научного центра УрО РАН @izvestia-komisc
Рубрика: Химические науки
Статья в выпуске: 4 (16), 2013 года.
Бесплатный доступ
По реакции Вильямсона синтезирован 2-ундецилоксиэтанол-1 – агрегацион- ный феромон жуков усачей рода Monochamus. Первые полевые испытания для привлечения черных сосновых усачей в ловушки, проведенные в Орен- бургской области в национальном парке «Бузулукский бор» в 2012г., про- шли успешно.
Феромоны, сосновые усачи, 2-ундецилоксиэтанол-1, синтез, ловушки, мониторинг, испытания
Короткий адрес: https://sciup.org/14992636
IDR: 14992636 | УДК: 632.936.2+547.573
2-undecyloxyethanol-1 - aggregation pheromone of black pine beetles of genus Monochamus: synthesis and testing
2-Undecyloxyethanol-1 - the aggregation pheromone of longhorn beetle of genus Monochamus - was synthesized by Williamson's reaction. First field tests to at- tract black pine beetles in the traps carried out in the national park "Buzuluk- sky Forest" of Orenburg region in 2012 were successful.
Текст научной статьи 2-ундецилоксиэтанол-1 – агрегационный феромон черных сосновых усачей рода Monochamus: синтез и испытания
Массовое размножение вредных насекомых ежегодно приводит к повреждению лесов и ослаблению насаждений. В итоге – снижение их продуктивности, нарушение целевых функций, порча древесины и нежелательные экологические последствия [1]. Эффективная защита леса от вредителей, локализация и ликвидация очагов их размножения возможны лишь при своевременном выявлении повреждений. Это определяется результативностью лесопатологического мониторинга, которая существенно повышается при использовании синтетических феромонов, или аттрактантов как аналогов природных веществ, привлекающих насекомых. Помещенные в специальные ловушки феромоны позволяют своевременно определить начало роста численности вредителя, что особенно важно для применения лесозащитных мер. Феромоны, применяемые в микродозах, экологически безопасны, так как являются природными веществами, которые быстро испаряются и не загрязняют окружающую среду. Кроме того, они не фитотоксичны и безопасны для всех объектов флоры и фауны. Ограничений к их применению нет. Как правило, феромоны воздействуют из- бирательно на насекомых именно того вида, за которым осуществляется надзор.
Усачи, или дровосеки – разнообразное, широко распространенное и в практическом отношении важное семейство жесткокрылых, насчитывающее в мировой фауне более 20 тыс. видов. На территории бывшего Советского Союза известно около 890 видов, в фауне европейского Северо-Востока России – 69 [2]. В лесах России наиболее распространенными являются большой черный пихтовый (хвойный) усач (Monochamus urussovi Fisch.) и большой черный сосновый усач (Mono-chamus galloprovincialis Germ.) [3]. Первый наибольший вред приносит в лесах Сибири, Алтая и на Дальнем Востоке, размножаясь в огромных количествах в очагах сибирского шелкопряда и пихтовой пяденицы, на гарях, а также на лесных складах и в местах лесозаготовок. В европейской части России этот вид широко распространен в северной части лесной зоны и сравнительно малочислен в ее южной части. В очагах сибирского шелкопряда большой усач в первую очередь заселяет пихту, затем ель, лиственницу и кедр. Большой хвойный черный усач не только разрушает древесину, но и является очень опасным вредителем растущего леса. Первоначально жук-усач размножается в насаждениях, поврежденных сибирским шелкопрядом. После того, как популяция насекомых достигает высокой численности, усачи устремляются для дополнительного питания в соседние здоровые массивы леса и ослабляют их, подгрызая большую часть ветвей, которые усыхают. Поврежденные жуками насаждения теряют свою ценность для эксплуатации.
Черный сосновый усач (см. фото) является вредителем сосновых лесов в южной части лесной зоны, лесостепи и степной зоны европейской части России, ленточных боров Западной Сибири. Он размножается в очагах корневой губки, на гарях, на очагах хвоегрызущих насекомых, подкорного клопа, в ослабленных засухой сосняках, в местах лесозаготовок и на складах древесины, где заселяет лесоматериалы и крупные порубочные остатки. Жуки соснового усача светолюбивы и предпочитают из-реженные, хорошо прогреваемые насаждения. Их лет начинается в середине июня и продолжается до сентября. Жуки дополнительно питаются тонкой корой веточек и побегов, что часто приводит к их высыханию.

Фото. Черный сосновый усач рода Monochamus galloprovincialis Germ.
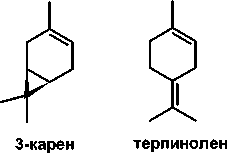
Ранее было показано, что для мониторинга усачей можно использовать летучие вещества дерева-хозяина (α- и β-пинены, 3-карен, терпинолен, мирцен) и компоненты феромонной композиции жуков рода Ips – ипсенол, ипсдиенол, 2-метил-3-бутен-2-ол, цис -вербенол (рисунок) [4, 5].
Совсем недавно было установлено, что 2-ун-децилоксиэтанол-1 является продуцируемым зрелыми самцами агрегационным феромоном нескольких видов усачей рода Monochamus [6, 7]. Авторы показали, что синтетический 2-ундецилокси-этанол-1 в сочетании с другими компонентами, представленными на рис. 1, можно использовать не только для контроля за численностью этих насекомых вредителей, но и в условиях вспышки их массового размножения для отлова и уничтожения.
Материал и методы
ГЖХ анализ (газо-жидкостная хроматография) проводили на хроматографе: SHUMADZU GC-2010AF, колонка HP1, детектор – пламенно-ионизационный, газ-носитель – гелий. ИК-спектры снимали в тонком слое на приборе “IR Prestige 21” фирмы Shimadzu. ЯМР-спектры регистрировали на приборе Bruker AVANCE-II-300, рабочая частота 300 МГц (1Н) и 75 МГц (13С) в CDCl 3 и DMSO-d6 с использованием стандартных импульсных программ фирмы Bruker для одно- и двумерных экспериментов.
Для колоночной хроматографии использовали силикагель 60 (70-230 меш) фирмы Alfa-Aesar. ТСХ (тонкослойная хроматография) выполняли на пластинах Сорбфил, элюенты: гексан, петролейный эфир-диэтиловый эфир, проявитель – 10%-ный раствор фосфорномолибденовой кислоты в этаноле.
Синтез 2-ундецидоксиэтанола-1. В трех-горлую колбу на 250 мл, снабженную холодильником, термометром, капельной воронкой, помещали раствор этиленгликоля (9.3 г или 8.4 мл, 0.15 моль) в 50 мл сухого диметилформамида (ДМФА). При перемешивании в токе инертного газа небольшими порциями в течение 30 мин добавляли 1.8 г (0.075 моль) гидрида натрия (NaH). Затем температуру повышали до 55-60 °С, при этом смесь превращалась в гелеобразную массу. После её охлаждения до комнатной температуры по каплям вводили ун-децилбромид (7.05 г, 0.03 моль), далее температуру реакции повышали до 63-65 °С и перемешивали
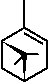
α -пинен
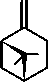
β -пинен

мирцен
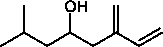
ипсенол

ипсдиенол
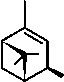
2-метил-3-бутен-2-ол цис -вербенол
Рис.
5 ч (табл. 1, строка 3). После охлаждения смесь экстрагировали этилацетатом, промывали насыщенным раствором NaCl и сушили над MgSO4. После удаления растворителя выход продукта составил 6.68 г. Содержание веществ в смеси определяли методом ГЖХ. Колоночной хроматографией на SiO2 сначала выделяли ундекан, непревращенный ундецилбромид (петролейный эфир), затем диэфир, производные диметилформамида, ундеканол и в последнюю очередь целевой продукт
–
2-ундецидоксиэтанол-1, препаративный выход которого составил 38 %.
Таблица 1
Результаты синтеза 2-ундецилоксиэтанола-1
2-Ундецилоксиэтанол-1 (1): ИК-спектр (ν, см-1): 3423 (OH), 2924, 2854, 1462, 1371, 1360, 1122 (C-O-C), 1066 (C-O-C), 891, 721. ЯМР 1H (300 МГц, δ): 0.87 (т, СH 3 ), 1.26 (16H, м), 1.49 (м, СH 2 ), 3.38 (4H, м, O-CH 2 -СH 2 -O), 3.49 (2H, к, СH 2 -O), 4.56 (т, OH). ЯМР 13C (75 МГц, δ): 72.5 (C1), 70.8 (C2), 60.7 (C1), 31.9 (C2), 29.8 (C3), 29.5, 29.5, 29.4, 29.2, 29.1 (C4-С8), 26.1 (C9), 22.6 (C10), 14.4 (C11).
Ундециловый спирт (6): ИК-спектр (ν, см-1): 3336 (OH), 2924, 2854, 1462, 1377, 1057, 721. ЯМР 1H (300 МГц, δ): 0.91 (т, СH 3 ), 1.29 (16H, м), 1.6 (2H, м), 3.66 (т, СH 2 -OH). ЯМР 13C (75 МГц, δ): 63.1 (C11), 32.8 (C10), 31.9 (C9), 29.6-29.3 (C8-C4), 25,75 (C3), 22.7 (C2), 14.1 (C1).
Ундекан (7): ИК-спектр (ν, см-1): 2954, 2924, 2854, 1460, 1375, 908.
N,N-Диундецилформамид (8): ИК-спектр (ν, см-1): 2926, 2854, 1730(C=O), 1462, 1176, 1120(C-O-C), 723. ЯМР 1H (300 МГц, δ): 0.85 (т, СH 3 , 6.5 Гц), 1.24 (32H, м), 1.58 (4H, м), 4.08 (т, СH 2 , 6.5 Гц), 8.2 (c). ЯМР 13C (75 МГц, δ): 162.7 (C14), 63.9 (C11), 31.7-28.5 (C4-C10), 25.7 (C3), 22.5 (C2), 14.4 (C1).
N,N-Бис-(2-ундецилоксиэтил)-формамид (9): ИК-спектр (ν, см-1): 2926, 2854, 1730(C=O), 1460, 1379, 1355, 1180, 1126(C-O-C), 837, 723. ЯМР 1H (300 МГц, δ): 0.85 (т, СH 3 , 6.5 Гц), 1.23 (32H, м), 1.45 (4H, м), 3.38 (т, СH 2 , 6.5 Гц), 3.56 (т, СH 2 , 5 Гц), 4.2 (т, СH 2 , 5 Гц), 8.2 (c). ЯМР 13C (75 МГц, δ): 162.7
(C14), 70.7 (C11), 68.2 (C12), 63.3 (C13), 31.7 (C9), 29.5-29.1 (C4-C8,C10), 26 (C3), 22.5 (C2), 14.4 (C1).
H 3 C (CH2)9 CH2 OH
+
CH 2 CH2
OH
Результаты исследований
Одним из методов синтеза простых эфиров является дегидратация спиртов в присутствии кислотных катализаторов, однако обычно таким образом получают симметричные эфиры [8]. Синтез простых эфиров можно осуществить раскрытием эпоксидов спиртами или алкоголят-ионами в присутствии кислотных или основных катализаторов или оксида алюминия [9]. Но наилучшим общим методом получения как симметричных, так и несимметричных эфиров до сих пор остается реакция
Вильямсона, открытая в 1850 г. [10]. Этот метод заключается в обработке алкилгалогенида ал- коголят-ионами, полученными из спирта. Для получения алкоксидов чаще всего используют металлический натрий или гидрид натрия. Синтез эфиров можно осуществить взаимодействием галогени-
KOH в диметилсульфок- сиде, а также при использовании межфазного катализа [11]. Так, в работе [12] предложено использование 50%-ного водного раствора гидроксида натрия и тетрабутиламмоний бисульфата (ТВАВ) в качестве катализатора межфазного переноса для получения простых эфиров с выходом выше 90%. Авторами работы показано [13], что несимметричные простые эфиры олигоэтиленгликолей с выходом 70-90% можно синтезировать взаимодействием алкилхлоридов или алкилбромидов с 5-10-кратным избытком соответствующего гликоля в 50%-ном водном растворе NaOH при температуре 100 °С в течение 24 ч.
Синтез гидроксиэфира (1) проводили двумя методами: a) взаимодействием ундеканола-1 (2) с этиленгликолем (3) при кипячении в толуоле в присутствии пара-толуолсульфокислоты (pTsOH) [14], но реакция не прошла ни за 3, ни за 10 ч. (схема 1); б) по реакции Вильямсона – взаимодействием 1-бромундекана (4) с алкоголятом, полученным из этиленгликоля (3) и NaH в среде ДМФА в различных условиях. Результаты экспериментов приведены в табл. 1. Основными продуктами реакции являются моно- (1) и диэфир этиленгликоля (5), ундеканол-1 (6), образующийся, вероятно, в результате гидролиза исходного бромида. В качестве побочных минорных продуктов обнаружены унде- pTsOH толуол, кипяччение 10 ч реакция не идет
Схема 1.
HO CH2 CH2 OH
H 3 C (CH 2 ) 9 CH 2 Br NaH, ДМФА H3C (CH 2 ) 9 CH 2 O CH 2 CH 2 OH +
4 a,Д
H 3 C (CH 2 ) 9 CH 2 O CH 2
I + H 3 C (CH 2 ) 9 CH 2 OH + H 3 C (CH 2 ) 9 CH 3 +
H3C ^^^^^^e (CH2)9 CH2 O CH 3 2 9 2 3 2 93
3 29 22
H 3 C (CH 2 ) 9 CH 2 O CH
3 29 2 2 4
H3C ^^^^^^^^^ (CH2)9 CH2 O CH 3 29 2 2 4
H 3 C (CH 2 ) 9 CH 2
N
H 3 C (CH 2 ) 9 CH 2
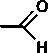
Схема 2.
кан ( 7 ) и производные диметилформамида – ( N , N -диундецилформамид 8, N , N -бис-(2-ундецилокси-этил)-формамид 9 ) (схема 2).
Использование только двукратного избытка этиленгликоля ( 3 ) по отношению к исходному бромиду ( 4 ) приводит к невысокой конверсии ~60%. При мольном соотношении C 11 H 23 Br:(СH 2 OH) 2 1:5, времени реакции 5-7 ч и температуре 60-70 °C конверсия исходного соединения составляет 88-90%, однако в продуктах реакции содержится значительное количество диэфира ( 5 ) (25-33%) и ундеканола-1 (10-14%). Селективность образования целевого продукта составляет 39-49%. При конверсии ундецил-бромида ( 4 ) 76-80% содержание диэфира снижается до 11-13%, а селективность образования 2-ундецилоксиэтанола-1 повышается до 51-59%. Наилучшие результаты по селективности и выходу гидроксиэфира ( 1 ) были получены при проведении реакции в течение 7 ч при комнатной температуре с обработкой реакционной смеси на следующий день. В этом случае образуется менее 5% ундеканола-1, который создает определенные трудности при хроматографическом разделении продуктов реакции, так как имеет значение R f очень близкое к R f , целевого гидроксиэфира. В 2012 г. было наработано и передано на полевые испытания в Институт химических средств защиты растений (г. Москва) 4 г 2-ундецилоксиэтанола-1 чистотой 100% по данным ГЖХ и ЯМР-спектроскопии. Для продолжения испытаний в других районах России, страдающих от нашествия усачей, в 2013 г. было синтезировано 12 г гидроксиэфира.
Результаты испытаний ловушек и диспенсеров с разным составом по привлечению черных усачей рода Monochamus
Поскольку испытаний по привлечению усачей в ловушки с помощью феромона в России не проводились, необходимо было изучить опыт зарубежных исследователей. Проанализировав результаты испытаний канадских ученых, наша задача при разработке ловушки для привлечения усачей заключалась в создании такой ее конструкции, которая бы учитывала недостатки всех ранее испытанных ловушек и отвечала бы следующим требованиям: темный вертикальный силуэт, устойчивая к ветру,

облегченная конструкция и небольшой сухой приемник, который не могут покинуть насекомые.
Для привлечения черного соснового усача в ловушку были составлены аттрактивные смеси из веществ дерева-хозяина с добавлением компонентов феромонов короедов рода Ips , так как в природе усачи заселяют деревья после того, как их «отработали» короеды. Для этих смесей были использованы диспенсеры с вкладышем внутри и тонкой или толстой пленкой внутреннего слоя, через который происходит испускание веществ. Для испарения 2-ундецилоксиэта-нола применен диспенсер, который способен равномерно испускать вещество в течение 4 месяцев.
Испытания проводили в Национальном парке «Бузулукский бор», который расположен на территории Оренбургской и Самарской областей, его общая площадь почти 107 тыс. га [15, 16]. Бузулукский бор ведёт свою историю с послеледникового периода, считается, что чистый сосновый лес сформировался около 3–4 тыс. л.н. Бор почти со всех сторон окружен полосой лиственного леса, граничащего с безлесной степью. Более 2/3 лесного массива занято сосновыми лесами. Бузулукский бор закрепляет своей корневой системой около 60 тыс. га песков. Если бы не бор, то вся эта масса песка оказалась бы на черноземах, примыкающих к нему полей. Неоспоримое значение бора заключается и в улучшении некоторых климатических факторов района. Только за последние два десятилетия известно несколько случаев, когда бор гасил разрушительную силу штормовых ветров, он ослабляет иссушающее действие суховеев, приходящих в степное Заволжье с юго-востока. Примыкающие к нему с севера поля меньше испытывают их пагубное влияние. Бузулукский бор – своеобразный местный источник дополнительных осадков. Поглощая почвенную и атмосферную влагу, он испаряет ее своей могучей кроной. Накапливающиеся над ним пары воды конденсируются и в виде дождя выпадают на прилегающие к нему поля, поэтому неудивительно, что их урожайность отличается относительной стабильностью и является повышенной.
По распоряжению Правительства Российской Федерации от 29 декабря 2007 г. № 1952-Р «Бузулукскому бору» присвоен статус Национального парка, который образован в целях сохранения и восстановления уникального природного комплекса – единственного в степном Заволжье лесного массива.
Участки, на которых проводились испытания, заложены в сосновых насаждениях, пострадавших от урагана в 2010 г. На данных участках зафиксирована повышенная численность черного соснового усача: имеется большое количество старого ветровала и бурелома, «отработанных» черным сосно- вым усачом, а также свежего сухостоя и усыхающих деревьев сосны, заселенных этим вредителем. Испытания проводились с 21.06.2012 по 22.08.2012 г. Лёт черного соснового усача на момент установки ловушек уже начался, пик лёта пришелся на конец июня. В 2012 г. в связи со вспышкой массового размножения лёт усача был очень интенсивный практически в течение всего лета. Учеты имаго черного соснового усача и прочих видов насекомых, попавших в ловушки в первое время, проводили два раза в неделю, с середины июля – один раз в неделю. На каждом участке вывешено по 20 пластиковых ловушек. В стаканы для сбора жуков помещена инсектицидная пластина. Черный сосновый усач привлекался в феромонные ловушки в больших количествах: всего 14 790 особей (табл. 2).
Заключение
Результаты исследований и изучения возможности применения веществ, привлекающих усачей рода Monochamus , указывают на перспективы использования смеси 2-ундецилоксиэтанола-1 с компонентами феромонов короедов рода Ips и с летучими веществами дерева-хозяина для мониторинга усачей и массового вылова их в ловушки. Испытания сезона 2013 г. будут проведены в других регионах России и направлены на уменьшение количества диспенсеров в ловушке с целью облегчения практического применения феромонных ловушек для мониторинга черного соснового усача.
Работа выполнена при частичной финансовой поддержке ОХНМ РАН №5, грант 12-Т-3-1004.
Таблица 2
Результаты отлова соснового усача в феромонные ловушки на двух участках испытаний по датам учета
|
№ УПН |
Количество черного соснового усача по датам учёта, шт. |
о 0) о CD |
||||||||||||
|
CD О CM CM |
CD О LD CM |
CD О 00 CM |
О CM О |
О LD О |
О ci О |
О CO |
О ci |
о LD CM |
00 о о |
00 о об о |
00 о LD |
00 о см см |
||
|
1 |
426 |
400 |
1405 |
479 |
415 |
650 |
366 |
836 |
563 |
544 |
496 |
399 |
480 |
7459 |
|
2 |
- |
555 |
1439 |
360 |
424 |
552 |
383 |
767 |
564 |
573 |
594 |
570 |
550 |
7331 |
|
1+2 |
426 |
955 |
2844 |
839 |
839 |
1202 |
749 |
1603 |
1127 |
1117 |
1090 |
969 |
1030 |
14790 |
Таблица 3
Результаты испытания разных вариантов привлекающих смесей в национальном парке «Бузулукский бор»
Варианты № 1. № 2. № 3. № 4.
|
Участки № 1 № 2 п Всего № 1 п № 2 п Всего № 1 п № 2 п Всего № 1 п № 2 |
Всего |
|
Кол-во жуков, шт. 1369 1206 2576 2348 2114 4462 1413 1568 2981 2329 2443 Самцы, шт. 350 317 667 704 605 1309 370 455 825 669 693 Самки, шт. 1019 890 1909 1644 1509 3153 1043 1113 2156 1660 1750 Среднее, шт./лов. 257 446 298 |
4772 1362 3410 477 |
Были испытаны в разных комбинациях четыре варианта смесей, состоящих из α-пинена, 2- 1
метил-3-бутен-2-ола, аналога ипсдиенола, цис -вер- .
бенола, ипсенола, этанола и 2-ундецилоксиэта-нола. Все варианты составов показали хорошие результаты (табл. 3). Наиболее эффективными были варианты №4 и №2, которые привлекали усачей приблизительно в 1,5-2 раза эффективнее, чем ва- 2. рианты №1 и №3. Количество самок соснового усача в ловушках практически всегда превышало количество самцов. Соотношение это не имеет какой-то постоянной величины. Вероятно, самки более чувствительны к испытанным аттрактивным сме- 3. сям.
Список литературы 2-ундецилоксиэтанол-1 – агрегационный феромон черных сосновых усачей рода Monochamus: синтез и испытания
- Методические рекомендации по применению новых феромонов вредителей леса для ведения лесопатологического мониторинга Утверждены приказом Федерального агентства лесного хозяйства от 04.05.2010 №177, г. Москва 2010.
- Татаринова А.Ф., Никитский Н.Б,. Долгин М.М. Усачи, или Дровосеки (Coleoptera, Ceramby-cidae). Фауна европейского Северо-Востока России. Усачи. Т. VIII, ч.2. СПб.: Наука, 2007. 301 с.
- Исаев А.С., Рожков А.С., Киселев В.В. Черный пихтовый усач Monochamus urussovi (Fish.). Новосибирск: Наука, 1988. 270 с.
- Fan J, Kang L., Sun J. Role of host volatiles in mate location by the Japanese pine sawyer, Monochamus alternatus Hope (Coleoptera: Cerambycidae)//Environ. Entomol. 2007. Vol. 36. P. 58-63.
- Allison J.D., Borden J.H., McIntosh R.L., еt al. Kairomonal response by four Monochamus species (Coleoptera: Cerambycidae) to bark beetle pheromones//J. Chem. Ecol., 2001. Vol. 27. P. 633-646.
- Pajares J., Бlvarez G., Ibeas F, еt al. Identification and Field Activity of a Male-Produced Aggregation Pheromone in the Pine Sawyer Beetle, Monochamus galloprovincialis//J. Chem. Ecol., 2010. Vol. 36. №6. P. 570-583.
- Macias-Samano J.E., Wakarchuk D., Millar J.G., Hanks L.M. 2-Undecyloxy-1-ethanol in combination with other semiochemicals attracts three Monochamus species (Coleoptera: Cerambycidae) in British Columbia, Canada//Canad. Entomol., 2012. Vol. 144, № 6. Р. 764-768.
- Дж. Марч Органическая химия. Т. 2. М.: Мир, 1987. C. 123.
- Posner G, Rogers D. Organic reactions at alumina surfaces. Mild and selective opening of epoxides by alcohols, thiols, benzeneselenol, amines, and acetic acid//J. Am. Chem. Soc., 1977. Vol. 99, №25. P. 8208-8214.
- Химическая энциклопедия. Т. 1. М.: Советская энциклопедия, 1988. С. 367-368.
- Johnstone R., Rose M. A rapid, simple, and mild procedure for alkylation of phenols, alcohols, amides and acids//Tetrahedron, 1979. Vol. 35. №18. P. 2169-2173.
- Freedman H.H., Dubois R.A. An improved Williamson ether synthesis using phase transfer catalysis//Tetrahedron Letters, 1975. Vol. 16. №38. P. 3251-3254.
- Gibson T. Phase-transfer synthesis of monoalkyl ethers of oligoethylene glycols//J. Org. Chem., 1980. Vol. 45, 6. P. 1095-1098.
- Gonnissen P., Voorspoels M. Fosfluconazole derivatives, synthesis, and use in long acting formulations//W02010105910 A1, 23/09/2010.


