Ab-initio моделирование влияния ближнего окружения примесей углерода на энергию их растворения в ГЦК-железе
Автор: Ридный Ярослав Максимович, Мирзоев Александр Аминулаевич, Мирзаев Джалал Аминулович
Рубрика: Физика
Статья в выпуске: 2 т.5, 2013 года.
Бесплатный доступ
В программном пакете WIEN2k проведено первопринципное моделирование равновесной структуры и свойств ГЦК-железа. Получены оптимальные параметры, позволяющие построить наиболее точную модель. Произведено вычисление энергий растворения атомов углерода, их взаимного расположения и вклада упругих эффектов в энергию системы для немагнитного (НМ) и антиферромагнитного двухслойного (АФМД) состояний ГЦК железа.
Первопринципное моделирование, гцк-железо, примеси углерода
Короткий адрес: https://sciup.org/147158764
IDR: 147158764 | УДК: 669.112.227.1:538.915
Ab-initio simulation of influence of shortrange ordering carbon impurities on the energy of their dissolution in the FCC-iron
The first principle simulation of equilibrium structure and FCC-iron characteristics was carried out by the software package WIEN2k. The optimal parameters which allow building the most accurate model were generated. Energies of dissolution of carbon atoms, their relative positions and the contribution of the elastic effects to the energy of system were calculated for non-magnetic (NM) and doublelayer antiferromagnetic states (AFMD) of FCC-iron.
Текст научной статьи Ab-initio моделирование влияния ближнего окружения примесей углерода на энергию их растворения в ГЦК-железе
Сплавы на основе железа, несмотря на развитие производства пластмасс, керамики, композитов, остаются основными конструкционными материалами. Исключительным достоинством чёрных металлов является, прежде всего, их дешевизна, а также универсальность — при помощи небольших добавок можно резко изменить свойства их сплавов. Например, внедрение всего лишь 1 ат. % углерода радикально повышает прочность железа. Железо является полиморфным металлом [1, 2]: при нагревании выше 911 °С низкотемпературное α-железо с ОЦК решеткой превращается в γ-железо с ГЦК решеткой. Углерод растворяется в обеих фазах железа, так что при температурах выше 723–911 °С существует аустенит – раствор углерода в γ-Fe, ниже этого интервала возникает феррит –раствор углерода в α-Fe [2]. Растворимость углерода в γ-Fe довольно высока – до 2 масс. %. Напротив, α-железо растворяет очень мало углерода. Наибольшая растворимость (0,025 масс. % ) наблюдается при 723 °С. В ходе медленного охлаждения аустенита он превращается в феррит, а избыток углерода сверх равновесной концентрации выделяется в виде карбида Fe 3 C. Поэтому превращение аустенита при охлаждении стали, помимо перестройки решетки, требует прохождения процесса диффузии углерода в аустените и феррите.
Углерод образует твердый раствор внедрения как с γ-, так и с α-железом, что было установлено довольно давно [1]. По результатам совместного измерения плотности р и параметра кристаллической решетки а для серии сплавов удается рассчитать число атомов n, приходящихся на одну элементарную ячейку:
n = P a 3 Na IA , (1)
где A - средняя атомная масса, а Na - число Авогадро. Наблюдавшееся возрастание n при увеличении содержания углерода в аустените и феррите однозначно свидетельствовало об образовании углеродом растворов внедрения в решетках железа. В структуре γ- и α-железа существуют пустоты (поры), ограниченные атомами железа, расположенными в вершинах октаэдра или тетраэдра, в связи с чем их называют октаэдрическими и тетраэдрическими порами. Вопрос о том, в порах какого типа расположены атомы углерода в решетках γ-Fe и α-Fe, вызвавший многолетнюю дискуссию, был решен на основе данных экспериментов по ядерному гамма-резонансу и нейтронографии [2]. Было показано, что атомы углерода в обеих решетках располагаются в октаэдрических порах (ОП).
Ридный Я.М., Мирзоев A.A., Ab-initio моделирование влияния ближнего окружения Мирзаев Д.А. примесей углерода на энергию их растворения в ГЦК-железе
В условиях быстрого охлаждения аустенита, когда диффузия углерода подавлена, происходит бездиффузионное мартенситное превращение, при котором все атомы углерода принудительно переходят в решетку мартенсита, а последняя, хотя и похожа на решетку α-железа, имеет слабую тетрагональность [1–3]. Возникновение тетрагональности и бездиффузионный характер мартенситного ГЦК-ОЦК превращения был объяснен Бейном, который обратил внимание, что ГЦК-решетку можно превратить в объемно-центрированный куб при небольшом сжатии вдоль оси ОZ и растяжении в направлениях осей OX и OY (бейновская деформация). Октапоры ГЦК-решетки вместе с располагающимися в них атомами углерода переходят только в октапоры типа «Z» решетки ОЦК-железа. При этом все атомы углерода растягивают решетку в одном Z-направлении, и она из кубической превращается в тетрагональную. Хотя теория Бейна общепри-знана, вопрос теоретического обоснования ее справедливости остается открытым.
В связи с этим, вопрос о распределении атомов углерода в ГЦК-решетке железа и их упорядочении остаётся очень важным. Очевидно, что мартенсит наследует расположение атомов углерода в аустените, которое, в свою очередь, зависит от характера взаимодействия соседних атомов углерода. Среди многочисленных характеристик аустенита наиболее чувствительной к особенностям распределения атомов углерода по октапорам оказалась активность углерода в γ-фазе αγ c [4]. Еще Вагнер с сотрудниками [5] показали, что при отсутствии взаимодействия между атомами углерода величина активности дается выражением:
αγ = xc ,
c 1 - βxc где xc - доля атомов углерода в сплаве, а коэффициент р = 2. Однако результаты экспериментального изучения активности углерода в γ-железе показали, что величина αγc с увеличением содержания углерода возрастает сильнее, чем это предписывает формула (2). Было высказано предположение, что это обстоятельство связано с наличием отталкивания между ближайшими атомами углерода, что и приводит к уменьшению числа возможных мест их расположения. Даркен и Смит [6] математически оформили данную идею, введя величину е - энергию взаимодействия рассматриваемого атома углерода с другими атомами С, расположенными в любой из 12 октапор ближайшего окружения. Окончательный результат для активности оказался таким:
xc
αγ = , c 1-(14-12θ)xc
где θ = exp( - ε kT ) . Сопоставление с экспериментальными данными для активности углерода позволило определить величину е = 0,065 эВ/атом, что для 1200 К дает р = 7,6. Видно, что учет отталкивания действительно увеличивает активность углерода в растворе.
Темкиным и Шварцманом [7], а затем Кауфманом [8] была развита модель блокировки, вко-торой выдвинуто предположение, что каждый атом С блокирует, т.е. делает недоступным для заполнения другими атомами углерода, некоторое число m октапор, ближайших к нему. В этом варианте:
ln αγ c = ln
xc 1 - ( m + 1) xc
.
Параметру m придавали значение 5 в [9], и 4 в [7]. Последнее значение можно интерпретировать в модели, что атомы углерода занимают только октапоры, расположенные в центре кубов. Квазихимическая модель (модель мягкого отталкивания) была разработана В.А. Кожеуровым [10], и позднее Мак-Лелланом [9]. В ней принимается, что атом углерода отталкивает с энергией е 1 любой атом углерода, расположенный в первой координационной сфере исходного атома. Совпадение теории и экспериментальных данных достигается при е 1 = 0,085 эВ/атом [11]. Позднее Большовым Л.А. [12] была развита более общая теория, учитывающая энергии взаимодействия пар атомов углерода не только в первой, но и последующих координационных сферах.
Поскольку все рассмотренные и сильно различающиеся модели позволяют довольно точно описать активность углерода в аустените, можно заключить, что данные об активности не позволяют провести детальную реконструкцию распределения углерода в ГЦК-железе.
Важные данные о распределении углерода получены в экспериментах по ядерному гамма-резонансу (^ГР). ^ГР-спектр аустенита имеет особенности, заключающиеся в существовании
Физика
центрального максимума от атомов железа, не имеющих в своем окружении атомов углерода, и дублета от атомов железа, соседствующих с углеродом в ближайших междоузлиях. Обзор мессбауэровских исследований распределения углерода в аустените был сделанГаврилюкомВ.Г. [13] и Надутовым В.М. [14]. Было показано, что, хотя в выводах исследователей имеются противоречия, в основном большинство авторов склоняются в пользу модели жесткого отталкивания, т.е. блокировки октапор не только в первой, но и во второй координационной сфере. Этот вывод согласуется с результатами расчета энергии взаимодействия пары атомов углерода при их расположении в первом и втором соседствах – +0,15 эВ и 0,4 эВ, полученными Гаврилюком В.Г. методом функций Грина [13]. В диссертации Надутова В.М. [14] методом Монте-Карло были получены области возможных значений энергий взаимодействия атомов углерода в первой и второй координационных сферах на основании мессбауровских экспериментов. Было показано, что энергия отталкивания атомов углерода во второй координационной сфере в разы превышает отталкивание в первой сфере и превосходит величину 0,08 эВ.
Таким образом, экспериментальными методами довольно легко определить концентрацию углерода, но достоверно установить позиции атомов углерода в решетке железа, а также структуру их ближнего порядка на данный момент времени представляет очень сложную и дорогостоящую задачу. Поэтому в последние годы все большее внимание уделяется методам перво-принципного компьютерного моделирования, главным достоинством которых является отсутствие каких-либо входных данных, влияющих на достоверность результатов при использовании минимального количества подгоночных параметров.
Джианг и др. исследовали энергию растворения углерода в ферромагнитном(ФМ) состоянии ГЦК железа в программном пакете VASP [15]. Энергия растворения вычислялась относительно графита и составила –0,17 эВ. Этот результат оказался существенно ниже экспериментального значения 0,36 эВ, полученного в работе [16] методом рассеяния электронов. В работе [17] в программном пакете SIESTA проводилось моделирование растворения углерода в АФМД состоянии ГЦК-железа, энергия составила 0,55 эВ. В ряде работ [18–20] рассматривали растворение второго атома углерода в ГЦК-решетке железа и показали, что атомы углерода предпочитают располагаться на максимально возможном расстоянии. Наиболее полный анализ растворения углерода проведён в работе Медведевой [18], но она ограничилась только немагнитным (НМ) состоянием железа.
Видно, что несмотря на значительное количество работ, посвященных изучению растворения углерода в железе, вопросы о расположении атомов углерода, энергиях их растворения, а также энергиях взаимодействия между атомами углерода остаются открытыми. В связи со всем вышесказанным, целью данной работы являлось ab-initio моделирование влияния расположения соседних примесей на энергию растворения атома углерода в различных магнитных фазах ГЦК-железа с помощью программного пакета WIEN2k [21].
Реальное ГЦК-железо существует в парамагнитном состоянии, при температурах порядка 1000 °С. Его магнитный момент равняется 0,6 μb [22]. Моделирование парамагнитного состояния методами зонной теории в пакете WIEN2k довольно затруднительно, поскольку они позволяют проводить моделирование лишь коллинеарных магнитных состояний. Поэтому мы будем описывать парамагнитное состояние с помощью двух приближений – немагнитного (НМ), в котором магнитные моменты равны нулю, и в антиферромагнитном двухслойном состоянии (АФМД). Согласно работе [23] оно является наиболее стабильным из коллинеарных магнитных состояний в ГЦК-железе.
Методы
В данной работе расчёты проводись первопринципным полнопотенциальным методом LAPW, с учетом обобщенного градиентного приближения PBE-GGA в программном пакете WIEN2k, обеспечивающим высокую точность расчета полной энергии при минимальном количестве подгоночных параметров.
В методе LAPW [24] волновые функции, зарядовая плотность и потенциал разлагаются по сферическим гармоникам в неперекрывающихся атомных сферах радиуса Rmt и по плоским волнам в остальной области элементарной ячейки. Предполагается, что внутри маффин-тин сферы зарядовая плотность сферически-симметрична. Волновые функции в междоузлии раскладываются по плоским волнам с максимальным волновым вектором Kmax. Эта величина является одним
Ридный Я.М., Мирзоев A.A., Ab-initio моделирование влияния ближнего окружения Мирзаев Д.А. примесей углерода на энергию их растворения в ГЦК-железе из основных параметров, влияющих на точность, так как она определяет число базисных функций (размер матриц). Для интегрирования в обратном пространстве и вычисления электронной плотности использовалась схема Монхорста–Пака с сеткой из N k точек в зоне Бриллюэна. ^ем больше используется точек, тем выше точность интегрирования, однако при этом возрастает расчетное время, поэтому оптимальное значение определяется из условия достижения требуемой точности энергии системы.
В нашей работе использована ГЦК-суперячейка, состоящая из 32 атомов. Была проведена оптимизация параметров моделирования, которая показала, что для достижения требуемой точности расчета полной энергии в 1 мРб/систему, необходимо использование следующих параметров: R mt (Fe) = 2,0 а.е., Kmax = 5 а.е.–1. Эти значения совпадают с параметрами, определёнными в работах [25, 26] для ОЦК железа. Для определения геометрических параметров необходимо использование N k = 64 точки, а чтобы гарантировать точность вычисления полной энергии в 1 мРб, необходимо его увеличить до Nk =343.
Для определения энергии растворения углерода относительно фазы графита использовалась формула:
N H = E (Fe 32 C) - E (Fe 32 ) - E (C), (5) где E (Fe32C1) – энергия отрелаксированной суперячейки, состоящей из 32 атомов железа и одного атома углерода, находящегося в октапоре, E (Fe 32 ) – энергия суперячейки состоящей из 32 атомов железа, а E (C) – энергия одного атома углерода в решётке графита. Для нахождения энергии растворения второго атома углерода формула (1) преобразуется:
A H 2 = E (Fe 32 C2) - E (Fe 32 C) - E (C). (6)
В формуле (6) E (Fe 32 C 2 ) – энергия релаксированной суперячейки, состоящей из 32 атомов железа и двух атомов углерода находящихся в октапорах.
Для нахождения энергии взаимодействия между атомами углерода из энергии системы с двумя атомами углерода вычитается энергия двух суперячеек, содержащих одиночные атомы углерода, и суммируется с энергией беспримесной суперячейки ГЦК железа:
A V = E (Fe 32 C 2 ) - 2 E (Fe32C) + E (Fe32). (7)
Для нахождения энергии углерода в графите мы использовали значения параметров решётки, полученные из рентгеноструктурных данных ( а = 2,462 Å, c = 6,656 Å [15]). В расчете использовались оптимизированные параметры Kmax = 5 а.е.–1, Rmt(С) = 1,2 а.е. Количество k -точек было увеличено по сравнению с работой [15] для обеспечения точности в 1мРб/систему от N k = 256 до N k = 300.
Растворение углерода и деформация решётки
Для получения равновесных параметров суперячейки ГЦК-железа с растворенными атомами углерода была проведена атомно-силовая релаксация системы и объемная минимизация энергии. Была получена зависимость параметра решётки от концентрации углерода, приведенная на рис. 1.
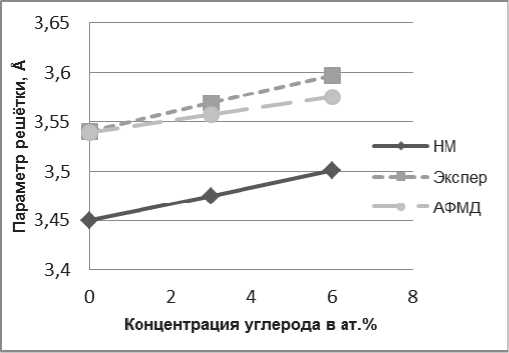
Рис. 1. График зависимости параметра решётки от концентрации углеро^а. Штрихова^ лини^ – АФМ^ состо^ние, короткий пунктир – экспериментальные значени^, сплошна^ лини^ – НМ состо^ние
При ее построении мы использовали результаты моделирования с растворенными одним и двумя атомами углерода. Было получено, что растворение одиночного атома С в НМ ГЦК-железе увеличивает параметр решётки с 3,45 Å до 3,475 Å и расталкивает ближайшие атомы железа на 7,5 %. При растворении углерода в АФМД состоянии происходит увеличение параметра решётки с 3,54 Å до
3,555 Å, и образование в первом окружении слегка несимметричного октаэдра, у которого апи-
кальный атом с противоположным направлением спина относительно других атомов железа
Физика
смещается лишь на 4 %, другой апикальный атом - на 6,5 %, тогда как планарные атомы - на 7,1 %. Полученные результаты находятся в согласии с аналогичными результатами, полученными Н. Медведевой в работах [18, 23], где при растворении углерода в НМ состоянии было получено, что атом С увеличивает параметр решётки с 3,456 А до 3,472 А и расталкивает ближайшие атомы железа на 7,7 %, а при растворении углерода в АФМД состоянии с 3,53 А до 3,55 А.
Реальное ГЦК-железо существует при температурах выше 911 °С. При такой температуре атомы углерода имеют практически одинаковую вероятность нахождения во всех конфигурационных сферах. Поэтому для вычисления параметра решётки было взято среднее значение параметра решётки, которое составило для НМ < a > = 3,5 А и для АФМД < a > = 3,575 А. Экспериментальная зависимость параметра решётки от концентрации и температуры была получена в работе [27] нейтронной дифракцией.
Проведя сравнение наших результатов с экстраполяцией экспериментальных результатов (рис. 1), мы пришли к выводу, что АФМД-состояние намного лучше описывает железо, чем НМ, и для него наблюдается довольно хорошее согласие углового коэффициента зависимости параметра решётки от концентрации углерода.
Энергии растворения атомов углерода в ГЦК железе
При использовании формулы (1), нами была вычислена энергия растворения атома углерода. В табл. 1 приведено сравнение нашей энергии с данными других работ, среди которых и экспериментальные данные для парамагнитного железа [28, 29].
Таблица 1
Значени^ энергии растворени^ о^ного атома углеро^а в октапоре ^л^ немагнитного состо^ни^ (Результаты пре^ставлены ^л^ концентрации 3 ат. % углеро^а)
|
Статья |
Состояние |
Энергия, мэВ |
|
[28] |
эксп. (парамагнитное) |
360 |
|
[29] |
эксп. (парамагнитное) |
420 |
|
[28] |
НМ |
145 |
|
Данная работа |
НМ |
180 |
|
[17] |
АФМД |
550 |
|
Данная работа |
АФМД |
340 |
Видно, что энергия, полученная при растворении углерода в решётке ГЦК-железа, находя- щегося в АФМД-состоянии, практически совпадает с экспериментальным значением.
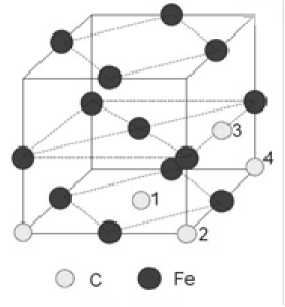
Рис. 2. Возмо^ные располо^ени^ атомов углеро^а в ^чейке Fe32
Наиболее полный анализ растворения второго атома углерода проведён в работе [18], однако он был проведен только для НМ-состояния матрицы. В суперячейке из 32 атомов железа существует 4 координационных сферы (рис. 2). Конфигурация с двумя ближайшими атомами углерода, образующими 180° C-Fe-C позицию, является наименее энергетически выгодной. Наши данные для НМ-состояния хорошо согласуются с данными Медведевой [18].
В табл. 2 приведено сравнение значений энергии растворения 2 атомов углерода, полученных в нашем расчете как для НМ, так и для АФМД-фазы ГЦК-железа. Для их получения использовалась формула (6).
Таблица 2
Значени^ энергии растворени^ второго атома углеро^а
|
Номер конфигурации |
НМ, мэВ |
АФМД, мэВ |
|
1 |
260 |
510 |
|
2 |
1400 |
840 |
|
3 |
150 |
470 |
|
4 |
310 |
250 |
Проведя анализ полученных результатов, был сделан вывод, что энергия растворения второго атома углерода близка к энергии растворения первого для всех конфигураций, кроме второй.
Ридный Я.М., Мирзоев A.A., Мирзаев Д.А.
Для оценки упругих взаимодействий в рассматриваемой системе мы нашли разность полной энергии релаксированной системы и энергии системы, в которой не производилось релаксации. Назовем эту величину энергией упругой релаксации. Данные представлены в табл. 3.
Для атомов углерода, находящихся во второй координационной сфере, релаксация оказалась наиболее слабой, потому что атомы углерода находятся на одной линии и разделены одним атомом Fe, который по этой причине не двигается. Скорее всего, это обстоятельство и объясняет энергетическую невыгодность данной конфигурации.
Таблица 3
Значения энергий упругой релаксации ( E relax - E nerelax )
|
Номер конфигурации |
НМ, мэВ |
АФМД, мэВ |
|
1 |
–4220 |
–2600 |
|
2 |
–3180 |
–2140 |
|
3 |
–4000 |
–2460 |
|
4 |
–3860 |
–2600 |
Для вычисления энергии взаимодействия между атомами была использована формула (7). В табл. 4 мы привели значения энергий растворения второго атома углерода для различных конфигураций в суперячейки состоящей из 32 атомов железа.
Таблица 4
Значения энергий взаимодействия между атомами углерода
|
Номер конфигурации |
Гаврилюк В.Г. [13], мэВ |
Данная работа, НМ, мэВ |
Данная работа, АФМД, мэВ |
|
1 |
150 |
80 |
170 |
|
2 |
400 |
1220 |
500 |
|
3 |
– |
–30 |
130 |
|
4 |
– |
130 |
–90 |
Видно, что учет магнитных эффектов (АФМД-состояние матрицы) несколько уменьшает отталкивание атомов углерода во второй координационной сфере, но увеличивает его в первой и третьей сферах. Атомы углерода в ГЦК-железе отталкиваются и предпочитают занимать наиболее удалённые позиции. Полученные нами значения энергии взаимодействия между атомами углерода в АФМД-состоянии матрицы хорошо согласуются с работой Гаврилюка В.Г. [13], в которой он получил указанные энергии, используя метод функции Грина. Это говорит о том, что АФМД-приближение для описания магнитного состояния может быть использовано для расчета как структуры реального ГЦК-железа, так и энергии взаимодействия атомов углерода в нем.
Заключение
Таким образом, в результате проведенных исследований:
-
1. Были найдены: энергия растворения приходящаяся на один атом углерода (при концентрации 3 ат.%) и энергии растворения второго атома углерода (при концентрации 6 ат.%, в зависимости от их взаимного расположения) в суперячейке из 32 атомов ГЦК решётки железа.
-
2. Растворение одиночного атома С в НМ ГЦК-железе увеличивает параметр решётки с 3,45 Å до 3,475 Å и расталкивает ближайшие атомы железа на 7,5 %. При растворении углерода в АФМД-состоянии происходит увеличение параметра решётки с 3,54 Å до 3,555 Å и образование в первом окружении слегка несимметричного октаэдра.
-
3. Показано, что между соседними атомами углерода в ГЦК-железе наблюдается отталкивание при их расположении в первой, второй и третьей координационных сферах. При этом наиболее сильно отталкивание между вторыми ближайшими соседями.
-
4. Показано, что для моделирования свойств ГЦК-железа с примесями углерода лучше использовать АФМД-состояние матрицы, чем НМ-состояние.
Список литературы Ab-initio моделирование влияния ближнего окружения примесей углерода на энергию их растворения в ГЦК-железе
- Кристаллография, рентгенография и электронная микроскопия/Я.С. Уманский, Ю.А. Скаков, А.Н. Иванов, Л.Н. Расторгуев. -М.: Металлургия. -1982. -632 с.
- Курдюмов, Г.В. Превращения в железе и стали/Г.В. Курдюмов, Л.М. Утевский, Р.И. Энтин. -М.: Наука. -1977. -C. 236.
- Хачатурян, А.Г. Углерод в мартенсите стали. Несовершенства кристаллического строения и мартенситные превращения/А.Г. Хачатурян. -М.: Наука, 1971. -C. 34-45.
- Могутнов, Б.М. Термодинамика железо-углеродистых сплавов/Б.М. Могутнов, Н.А. Томилин, Л.А. Шварцман. -М.: Металлургия, 1972. -C. 328.
- Dunwald, H. Thermodynamische Untersuchungen zum System Eisen-Kohlenstoff-Sauerstoff/H. Dunwald, C. Wagner//Z. Anorg. Allgem Chem. -1931. -Vol. 199. -P. 321-346.
- Darken, L.S. Appendix to the paper by Smith R.P. Equilibrium of iron-carbon alloys/L.S. Darken, R.P. Smith//J.Amer.Chem. Soc. -1946. -№ 7. -P. 1163-1175.
- Темкин, М.И. Активность углерода в аустените/М.И. Темкин, Л.А. Шварцман//Журнал физической химии. -1949. -№ 6. -С. 755-760.
- Kaufman, L. Thermodynamics of bainite reaction/L. Kaufman, S.V. Radcliffe, M. Cohen/Decomposition of Austenite by Diffusional Processes: сб. науч. тр. -AIME, New York: Interscience Publishers, 1962. -P. 313-352.
- McLellan, R.B. A quassi-chemical treatment of interstitial solid solutions: it application to carbon austenite/R.B. McLellan, W.W. Dunn//J.Phys.Chem.Solids. -1969. -V. 30, № 11. -P. 2631-2637.
- Кожеуров, В.А. К термодинамике растворов внедрения/В.А. Кожеуров//Известия ВУЗов. Черная металлургия. -1965. -№ 2. -С. 10-16.
- Dunn, W.W. The Application of Quassi-chemical Solid Solution Model to Carbon Austenite/W.W. Dunn, R.B. McLellan//Metall Trans. -1970. -Vol. 1, № 5. -P. 1263-1265.
- Большов, Л.А. Изучение ближнего порядка в аустентите системы Fe-C методами статистической теории и Монте-Карло/Л.А. Большов, В.Н. Суслов.//Физика металлов и металловедение. -2004. -Т. 98, № 6. -P. 3-7.
- Гаврилюк, В.Г. Распределение углерода в стали/В.Г. Гаврилюк. -Киев: Наукова Думка, 1987.-C. 208.
- Надутов, В.М. Межатомное взаимодействие и распределение атомов внедрения в железоазотистых и железо-углеродистых сплавах: автореферат дис. д-ра физ.-мат. наук/В.М. Надутов. -Киев: ИМФ НАН Украины им. Г.В.Курдюмова, 1997. -55 с.
- Jiang, D.E. Carbon dissolution and diffusion in ferrite and austenite from first principles/D.E. Jiang, E.A. Carter//Physical Review B. -2003. -Vol. 67. -P. 214103.
- Slane, J.A. Experimental and Theoretical Evidence for Carbon-Vacancy Binding in Austenite/J.A. Slane, C. Wolverton, R. Gibala//Metallurgical and Materials Transactions A. -2004. -Vol. 35, № 8. -P. 2239-2245.
- Magnetism and Local Distortions near Carbon Impurity in g-Iron/D.W. Boukhvalov, Y.N. Gornostyrev, M.I. Katsnelson, A.I. Lichtenstein.//Physical Review Letters. -2007. -Vol. 99. -P.247205.
- Ивановский Л.И. Распределение примесей Mn, Al, Si, С в аустените и их влияние на энергии дефектов упаковки/Л.И. Ивановский, Н.И. Медведева.//Фазовые переходы, упорядоченные состояния и новые материалы. -2012. -№ 10. -P. 24-28.
- Timoshevskii, A.N. Ab-initio modeling of the short range order in Fe-N and Fe-C austenitic alloys/A.N. Timoshevskii, S.O. Yablonovskii//Functional Materials. -2011. -Vol. 18, № 4. -P. 517522.
- Gavriljuk, V.G. Change in the electron structure caused by C, N and H atoms in iron and its effect on their interaction with dislocations/V.G. Gavriljuk, V.N. Shivanyuk, B.D. Shanina//Acta Materialia. -2005. -Vol. 53. -P. 5017-5024.
- Schwarz, K. Electronic structure calculations of solids using the WIEN2k package for material science/K. Schwarz, P. Blaha, G.K.H. Madsen//Computer Physics Communications. -2002. -Vol. 147. -P. 71-76.
- The Role of the Nature of Magnetic Coupling on the Martensitic Transformation in Fe-Ni/M. Acet, E.F. Wassermann, K. Andersen et al.//Journal de Physique IV France. -1997. -Vol. 7, № C5. -P. 401-404.
- Medvedeva, N.I. Magnetism in bcc and fcc Fe with carbon and manganese/N.I. Medvedeva, D.V. Aken, J.E. Medvedeva//Journal of Physics: Condensed Matter. -2010. -Vol. 22. -P. 316002.
- Cottenier, S. Density Functional Theory and the family of (L)APW-methods: a step-by-step introduction/S. Cottenier, 2004. [http://www.wien2k.at/reg_user/textbooks/DFT_and_LAPW-2_cottenier.pdf]
- Урсаева, А.В. Выбор оптимальных параметров для построения максимально точной модели ОЦК-железа/А.В. Урсаева, Г.Е. Рузанова, А.А. Мирзоев.//Вестник ЮУрГУ. Серия «Математика. Механика. Физика». -2010. -Вып. 2. -№ 9(185). -С. 97-101.
- Ракитин, M.C. Изменение электронной структуры a-железа, содержащего внедренные атомы водорода/M.C. Ракитин, А.А. Мирзоев, Д.А. Мирзаев//Вестник ЮУрГУ. Серия «Металургия». -2010. -Вып. 14. -№ 13(189). -P. 67-71.
- The lattice parameters of austenite and ferrite in Fe-C as functions of carbon concentration and temperature/M. Onink, C.M. Brakman, F.D. Tichelaar et al.//Scripta Metallurgica Et Materialia.-1993. -Vol. 29, № 8. -P. 1011-1016.
- Slane, J.A. Experimental and Theoretical Evidence for Carbon-Vacancy Binding in Austenite/J.A. Slane, C. Wolverton, R. Gibala//Metallurgical and Materials Transactions A. -2004. -Vol. 35, № 8. -P.2239-2245.
- Lobo, J.A. Thermodynamics of carbon in austenite and Fe-Mo austenite/J.A. Lobo, G.H. Geiger//Metallurgical Transactions A. -1976. -Vol. 7, № 8. -P. 1359-1364.


