Ab initio моделирование влияния кремния на образование карбида Fe3C в ОЦК-железе
Автор: Верховых А.В., Мирзоев А.А., Мирзаев Д.А.
Рубрика: Физика
Статья в выпуске: 4 т.10, 2018 года.
Бесплатный доступ
Представлены результаты первопринципного моделирования влияния кремния на энергию формирования цементита и парциальную энтальпию. Моделирование проводилось в рамках теории функционала плотности (DFT) полнопотенциальным методом линеаризованных присоединенных плоских волн (FP LAPW) с учетом обобщенного градиентного приближения (GGA’96) в программном пакете WIEN2k. Были изучены различные концентрации примеси кремния в цементите, а именно, 1,6, 3,2 и 6 ат. % как в позиции замещения атома железа (S и G-позиции), так и атома углерода (С-позиция). Была выполнена объемная оптимизация структур. Найдены равновесные параметры решетки как цементита без примеси, так и в присутствии кремния, которые отлично согласуются с экспериментальными и теоретическими данными. Энергия формирования для концентрации 3,2 ат. % в С-позиции оказалась -0,03 эВ, что может говорить о стабилизации цементита. Но при этом парциальная энтальпия для всех положений кремния положительна, и значит, кремний остается в твердом растворе ОЦК-Fe, что находится в хорошем согласии с результатами других теоретических и экспериментальных работ. Было получено, что чем больше концентрация кремния, тем ниже средний магнитный момент на атомах железа.
Первопринципное моделирование, цементит, кремний, энергия формирования, парциальная энтальпия
Короткий адрес: https://sciup.org/147232798
IDR: 147232798 | УДК: 669.111.31 | DOI: 10.14529/mmph180409
Ab initio simulation of silicon influence on Fe3C carbide formation in BCC-iron
Results of first-principles simulation of silicon influence of the energy of cementite formation and on partial enthalpy are presented in the article. Simulation was carried out in the frameworks of the Density Functional Theory (DFT) using the full-potential- linearized-augumented-plane-wave method (FP LAPW) taking into account the generalized gradient approximation (GGA’96) in WIEN2k software package. Various concentrations of silicon admixtures in cementite were studied, namely 1,6, 3,2 and 6 at. % for both the position of displacement of iron atom (positions S and G) and of carbon atom (position C). Volumetric optimization of all structures was carried out. Equilibrium parameters of the grid were determined both for cementite without admixtures (a = 4,510; b = 5,063; c = 6,747 Å), and for cementite with silicon, which excellently comply with experimental and theoretical data. Formation energy for concentration of 3,2 at. % in position C turned out to be -0,03 electron-volt, which can signify cementite’s stabilization. Though at that, partial enthalpy for all positions of silicon is positive which means that silicon remains in solid solution BCC-Fe, which is in a good compliance with results of other theoretical and experimental works. It was determined that the more is concentration of silicon, the lower is average magnetic moment on iron atoms. Moreover, it became possible to show that energy characteristics of the system significantly depend on the size of a super cell. This effect is connected with the use of periodic boundary conditions during calculations, and shows the presence of interactions between silicon atoms in neighboring super cells.
Текст научной статьи Ab initio моделирование влияния кремния на образование карбида Fe3C в ОЦК-железе
Промышленные материалы, такие как стали и сплавы на основе железа, всегда содержат примеси внедрения (углерод, азот, кислород, водород) и замещения (кремний, фосфор, сера), которые либо преднамеренно добавляют в сплав, либо данные примеси попадают в материал при изготовлении. Даже небольшая концентрация этих примесей может существенно повлиять на свойства материала [1–4]. Углерод является одной из наиболее важных примесей, так как увеличивает долговечность сталей и повышает порог хладноломкости. Примесь кремния всегда присутствует в сплаве, поскольку его добавляют специально во время плавления для удаления оксида железа и увеличения срока службы и предела текучести стали.
Свойства железоуглеродистых сплавов во многом определяются образованием карбида железа, цементита Fe3C, который обладает высокой прочностью и служит основной упрочняющей фазой в сталях, но в то же время делает сталь более хрупкой. Хорошо известно, что стабильность данного карбида является очень чувствительной к примесям, например, экспериментально показано, что V, Cr, Mn и Mo стабилизируют цементит [5]. Что же касается примеси кремния, то его влияние до сих пор не установлено. Поскольку растворимость Si в цементите низкая, а влияние кремния на растворимость углерода в феррите (ОЦК-железе), и, следовательно, на стабильность цементита, имеет противоречивые экспериментальные данные [6–9].
Согласно данным фазовой диаграммы [10], для того чтобы структура цементита оставалась стабильной, необходимо, чтобы примесь кремния не превышала 4 ат. %. Ранее уже были проведены исследования влияния примеси кремния на образование цементита, но в работах была использована система, в которой концентрация примеси кремния составляла либо 6 ат. % [11– 13], либо 0,8 ат. % [14, 15]. Поэтому представляет интерес исследование влияния различных
Верховых А.В., Мирзоев А.А., Ab initio моделирование влияния кремния Мирзаев Д.А. на образование карбида Fe 3 C в ОЦК-железе концентраций примесей кремния на образования Fe 3 C (1,6; 3,2 и 6 ат. %) как в позиции замещения атома железа, так и атома углерода.
Методы
Все расчеты проводились в программном пакете WIEN2k [16] полнопотенциальным методом линеаризованных присоединенных плоских волн с учетом обобщенного градиентного приближения, что обеспечивает высокую точность результатов моделирования в рамках теории функционала плотности. Для расчетов использовался мощный вычислительный комплекс Торнадо.
Цементит Fe3C имеет орторомбическую решетку, принадлежащую к пространственной группе Pnma . Элементарная ячейка с параметрами a = 4,524; b = 5,089; c = 6,744 Å [17] содержит 12 атомов железа и 4 атома углерода. Атомы железа в решетке цементита занимают две кристаллографически неэквивалентные позиции – G (general) и S (special). Суперячейки состояли из 16, 32 и 64 узлов орторомбической решетки (1×1×1), (1×1×2) и (2×1×2), заполненных 12, 24 и 48 атомами железа и 4, 8 и 16 атомами углерода соответственно. Один из атомов Fe (в позиции G или S) или из атомов С (в позиции С) был заменен 1 атомом примеси замещения – Si. При интегрировании в обратном пространстве и вычислении электронной плотности использовалась схема Монхорста–Пака с сеткой 8×8×8, 6×6×6 и 4×4×4 k -точек зоны Бриллюэна, соответственно. Расчеты проводились при значениях параметров моделирования: параметр сходимости K max = 5 a.е.–1, радиусы MT-сфер R mt (Fe) = 2,00 a.е., R mt (Si) = 2,00 a.е. (в позиции замещения G и S ) и 1,70 a.е. (в позиции замещения С), R mt (C) = 1,45 a.е., E cut = –7,0 Рб (340 эВ). Для кремния в позиции замещения углерода, ввиду малости поры, радиус МТ-сферы был уменьшен до 1,70 а.е. Для ферромагнитного α-железа был определен равновесный параметр решетки 2,842 Å, что хорошо согласуется с экспериментальным значением 2,867 Å [18]. Критерием сходимости для всех расчетов было воспроизведение полной энергии и заряда с точностью не менее 10–4 Рб и 10–3 е – соответственно, а силы на каждом из атомов не превышали значения 1 мРб/а.е (0,025 эВ/Å). Все это обеспечивает погрешность результатов расчетов не более 0,01 эВ.
Энергия формирования, E f , для цементита была оценена с помощью формулы:
Ef = E(Fek Cn) - kE(Fe) - nE(C), где Fek Cn – полная энергия кристалла цементита (k – количество атомов Fe, n – количество атомов C); E(Fe) – энергия 1 атома Fe в ОЦК структуре; E(C) – энергия 1 атома углерода в структуре графита.
Энергия формирования цементита в присутствии примеси кремния была вычислена как ESS = E(Fek—m Sim Cn) - (k - m)E(Fe) - mE(Si) - nE(C), где E(Fek-m Sim Cn) - полная энергия кристалла цементита с примесью кремния (k - количество атомов Fe, m – количество атомов Si , n – количество атомов C; E(Si) – энергия 1 атома кремния в структуре алмаза. Аналогичное уравнение применяется для случая замены атома углерода кремнием.
При этом изменение энергии формирования цементита при добавлении примеси кремния определялось как
A Ef = E f - E f .
Положительная энергия образования свидетельствует о невозможности существования стабильной фазы при нормальных условиях, то есть соединение нестабильно по отношению к разделению на отдельные фазы, и возможны принципиальные трудности его синтеза. Близкое к нулю положительное значение может означать, что данная фаза является метастабильной, но выбором условий синтеза (температура, быстрая закалка, напыление и т. д.) можно реализовать такое состояние.
В стали легирующие элементы при достаточно низких концентрациях обычно не находятся в своих исходных состояниях, а растворяются либо в ОЦК-Fe, либо в цементите. Следовательно, целесообразно будет определить такую величину, как парциальная энтальпия [14]
E Fe = E (Fe q ) + E (Fe k - 1 SiC n ) - E (Fe q - 1 Si) - E (Fe k C n ),
Физика где E(Feq) и E(Feq-1Si) - энергии ОЦК структуры железа из 54 атомов и в присутствии примеси кремния, соответственно.
EC = q-fE(Feq) + E(Fe,- SiC„) - E(Feq- Si) - p-lE(Fek Cn), pq q n q p n где коэффициенты q = 54, f = 4 (количество атомов в формульной единице), p = N/f (N – количество атомов в системе).
Стабилизация влечет за собой перенос Si из твердого раствора Si в ОЦК-Fe в цементитную фазу, в то время как дестабилизация подразумевает, что легирующий элемент остается в твердом растворе ОЦК-Fe. Отсюда следует, что (положительное) отрицательное значение Ep указывает на то, что легирующий элемент (де)стабилизирует структуру и переходит в (ОЦК-Fe) цементитную фазу.
Результаты и обсуждение
Объемная оптимизация систем
Начальные параметры решетки чистого цементита совпадали с экспериментальными данными (объем элементарной ячейки 155,32 Å3) [17]. В первую очередь были зафиксированы отношения a/b , a/c , b/c . При сохранении данных величин изменялся полный объем системы от
–2 % до 2 % (рис. 1, а). Оптимизация по объему проводилась путем проведения серии расчетов, позволяющих выявить зависимость энергии системы от ее объема. Аппроксимация полученных данных проводилась с помощью уравнения состояния Мурнагана. Для того чтобы не писать громоздкие значения энергии введена относительная энергия, равная разнице между энергией системы и 419588,492 эВ.
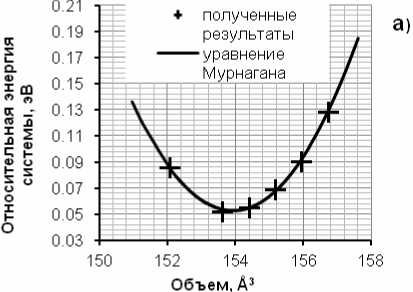
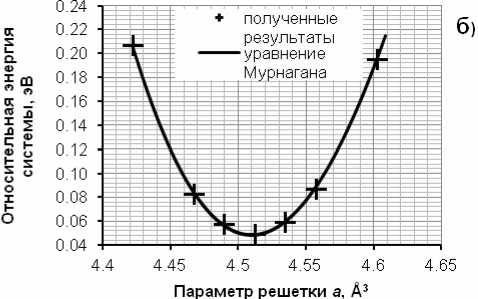
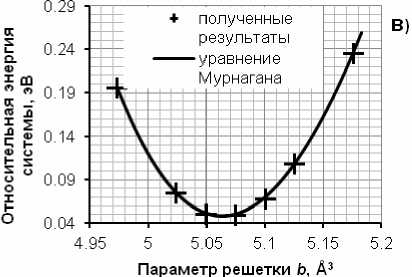
Рис.1. Объемная оптимизация параметров решетки Fe 3 C. Зависимость относительной энергии системы от объема (а); от значения а (б); от значения параметра b (в); от значения параметра c (г)
Согласно уравнению Мурнагана наименьшей энергии отвечает объем системы, соответствующий 153,925 Å3: a 1 = 4,512; b 1 = 5,074; c 1 = 6,723 Å. После этого фиксируются параметры b и c , а варьируется параметр a от –2 % до 2 % (рис. 1, б ). Наименьшей энергии отвечает объем системы имеющий значение 153,85 Å3: a 2 = 4,510 (–0,05 % от a 1 ); b 1 = 5,074; c 1 = 6,723 Å. Далее фиксируются параметры a и c , а меняется параметр b от –2 % до 2 % (рис. 1, в ). В соответствии с уравнением Мурнагана, наименьшей энергии отвечает объем системы,
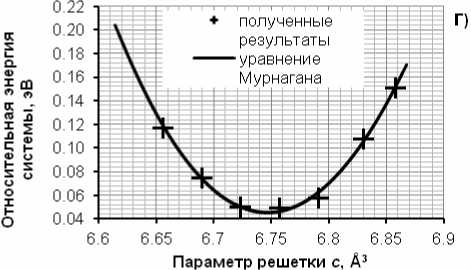
Верховых А.В., Мирзоев А.А., Ab initio моделирование влияния кремния Мирзаев Д.А. на образование карбида Fe 3 C в ОЦК-железе равный 153,508 A3: a 2 = 4,510; b 2 = 5,063 (-0,22 % от b i ); c 1 = 6,723 А. На завершающем этапе параметры а и b принимают фиксированное значение, а параметр c варьируется в диапазоне значений от -2 % до 2 % (рис. 1, г ). Таким образом, было получено, что минимальной энергии системы соответствуют следующие параметры решетки (154,045 А3): а 2 = 4,510; b 2 = 5,063; c 2 = 6,747 А (+0,36 % от c 1 ). В табл. 1 представлено сравнение наших результатов с другими данными как теоретическими, так и экспериментальными.
Таблица 1
Параметры решетки цементита. Сравнение полученных результатов с данными других авторов
|
Параметр |
Данная работа |
Вычисления [11] |
Вычисления [14] |
Эксперимент [17] |
|
a |
4,510 А |
4,462 А |
4,477 А |
4,525 А |
|
b |
5,063 А |
5,128 А |
5,032 А |
5,089 А |
|
c |
6,747 А |
6,651 А |
6,708 А |
6,744 А |
|
Объем эл. ячейки |
154,04 А3 |
152,20 А3 |
151,12 А3 |
155,32 А3 |
На одну элементарную ячейку цементита приходится объем, равный 154,04 А3, что на 0,8 % меньше экспериментального значения. Исходя из зависящих от температуры экспериментальных констант решетки [19], экстраполяция до нулевой температуры дает объем решетки 154,4 А3, что примерно на 0,23 % больше расчетного. Что указывает на хорошее согласие наших результатов с экспериментальными данными. Аналогичным образом была выполнена объемная оптимизация систем цементит-кремний, результаты представлены в табл. 2.
Таблица 2
Результаты объемной оптимизации структур цементита с примесью кремния в G и S позициях замещения (в системе, состоящей из N = 16, 32 и 64 атомов). Объем элементарной ячейки (V) и изменение объема относительно чистого цементита (ΔV)
|
Тип |
Параметры |
16 |
32 |
64 |
|
G |
a, b, c (А) |
4,529; 5,032 ; 6,757 |
4,528; 5,044; 6,753 |
4,510; 5,055; 6,756 |
|
V, (А3) |
154,01 (151,97 [11]) |
154,24 |
154,02 |
|
|
А V, (А3) |
-0,03 (-0,23 [11]) |
0,19 |
-0,02 |
|
|
S |
a, b, c (А) |
4,531; 5,027; 6,707 |
4,515; 5,040; 6,737 |
4,513; 5,052; 6,736 |
|
V, (А3) |
152,77 (151,44 [11]) |
153,29 |
153,58 |
|
|
А V, (А3) |
-1,28 (-0,76 [11]) |
-0,76 |
-0,46 А3 |
Таблица 3
Расстояния между Si и ближайшими атомами (l), и соответствующий объем многогранника Вороного для атома кремния (VВ) (в системе, состоящей из N = 16, 32 и 64 атомов) (в скобках значения объема многогранника Вороного для атома (C,G,S) чистого цементита)
|
Тип |
Параметры |
16 |
32 |
64 |
|
G |
l (А) |
2,44 2,495 2,284 2,637 2,7 2,597 2,525 2,552 2,475 2,481 2,541 2,566 2,181 2,718 |
2,418 2,184 2,610 2,474 2,891 2,460 2,461 2,536 2,529 2,381 2,571 2,580 2,701 2,441 |
2,612 2,513 2,382 2,368 2,594 2,190 2,863 2,481 2,705 2,454 2,473 2,573 2,559 2,466 |
|
V b , (А3) |
10,67 (10,24) |
10,66 (10,24) |
10,68 (10,24) |
|
|
S |
l (А) |
2,692 2,575 2,692 2,034 2,691 2,575 2,667 2,667 2,474 2,033 2,595 2,596 2,474 2,586 |
2,571 2,474 2,599 2,673 2,036 2,673 2,699 2,473 2,571 2,048 2,675 2,583 2,583 2,676 |
2,453 2,563 2,677 2,080 2,686 2,678 2,065 2,562 2,453 2,700 2,611 2,611 2,700 2,608 |
|
V b , (А3) |
10,51 (10,61) |
10,66 (10,24) |
10,65 (10,61) |
|
|
С |
l (А) |
2,224 2,3 80 2,210 2,222 2,202 2,202 2,213 2,379 2,554 |
2,219 2,551 2,243 2,219 2,227 2,397 2,242 2,397 2,225 |
2,203 2,203 2,206 2,206 2,766 2,408 2,223 2,222 2,408 |
|
V b , (А3) |
9,22 (7,45) |
9,41 (7,45) |
9,40 (7,45) |
Из данных, представленных в табл. 2, можно увидеть, что для случая положения атома кремния в G и S-позициях при увеличении количества атомов в системе объем, приходящийся на
Физика элементарную ячейку изменяется незначительно для всех случаев. Необходимо отметить, что для случая расположения кремния в C-позиции (16 атомов) при выполнении объемной оптимизации происходит существенное изменение объема (ΔV = 9,54 Å3), что согласуется с данными другой работы (~10 Å3 [14]). Поэтому для правильной оценки энергетических характеристик взаимодействия кремния с цементитом в С-позиции объемная оптимизация не выполнялась.
В табл. 3 представлены расстояния между атомом кремния и ближайшим окружением, а также соответствующий объем многогранника Вороного для атома Si.
Из данных, представленных в табл. 3, можно увидеть, что для случая расположения атома кремния в С -позиции (рис. 2, в ) с увеличением количества атомов в системе объем многогранника Вороного, приходящийся на атом Si, уменьшается. Максимальное изменение V наблюдается при расположении Si в S -позиции (рис. 2, б ) (с 10,51 Å3 при 16 атомах до 10,65 Å3 при 64 атомах). Для случая расположения кремния в G-позиции (рис. 2, а ) наблюдаются незначительные изменения, порядка 0,05 Å3.
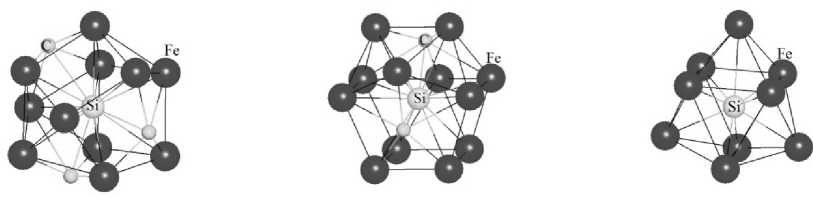
Рис. 2. Первое окружение для атома кремния в Fe 3 C: а) G -позиция; б) S -позиция; в) C -позиция
Результаты расчетов энергии формирования (энтальпии), ее изменение и парциальной энтальпии, которые являются характеристикой стабильности системы приведены в табл. 4.
Таблица 4
Энергетические характеристики систем цементит-кремний. Ef – энергия формирования цементита, ESfi – энергия формирования цементита в присутствии кремния, ЛЕf - изменение энергии формирования цементита, EX -p парциальная энтальпия ( X = Fe, C)
|
N |
Тип |
Ef ,эВ |
ESi , эВ f , |
Л Е у ,эВ |
Л Еу , эВ/ф.е. |
EX , эВ p |
|
16 |
С |
0,91 |
1,02 |
0,11 |
0,03 |
1,62 |
|
S |
1,32 |
0,41 (0,34[11,13]) |
0,10 |
1,69 (1,65[13]) |
||
|
G |
1,15 |
0,24 (0,24[11], 0,18[13]) |
0,06 |
1,52 (1,55[15], 1,40[13] ) |
||
|
32 |
С |
1,82 |
1,78 |
-0,03 |
0,00 |
1,47 |
|
S |
2,23 |
0,41 |
0,05 |
1,69 |
||
|
G |
1,94 |
0,13 |
0,02 |
1,41 |
||
|
64 |
С |
3,64 |
3,81 |
0,17 |
0,01 |
1,57 |
|
S |
4,02 |
0,38 |
0,02 |
1,66 |
||
|
G |
3,76 |
0,12 |
0,01 |
1,40 |
Полученное значение энергии образования для Fe 3 C (0,227 эВ или 0,06 эВ/атом) находится в хорошем согласии с экспериментальными данными (0,05 ^ 0,08 эВ/атом) [20, 21] и результатами предшествующих теоретических оценок (0,22, 0,22, 0,26) [11, 12, 13]. Энергия образования Fe 3 C является положительной величиной, что согласуется с метастабильным характером цементита, в частности с его достаточно легким распадом, сопровождающимся образованием свободного углерода в виде графита.
При рассмотрении результатов изменения энергии формирования мы видим, что для состояния атома кремния в С -позиции (32 атома) эта величина отрицательна, и, следовательно, можно говорить о стабилизации цементита. Однако, если мы обратим внимание на парциальную энтальпию, то для всех положений кремния она положительна, и значит, кремний остается в твердом растворе ОЦК-Fe, что находится в хорошем согласии с другими данными [14, 15]. Кроме
Верховых А.В., Мирзоев А.А., Ab initio моделирование влияния кремния Мирзаев Д.А. на образование карбида Fe 3 C в ОЦК-железе того, это согласуется с экспериментальными данными, поскольку Si используются для подавления образования цементита в TRIP-сталях [22]. Из результатов изменения энергии формирования цементита в присутствии кремния на формульную единицу и парциальной энтальпии наблюдается существенная зависимость данных от размера суперячейки. Данный эффект связан с периодическими граничными условиями и показывает наличие взаимодействия между атомами кремния в соседних суперячейках.
Рассчитанные средние локальные магнитные моменты на атомах железа, углерода и кремния, а также полная намагниченность приведены в табл. 5 для различной концентрации последнего. Также для сравнения представлены значения средних магнитных моментов атомов железа и углерода в чистом цементите. Полученные результаты для магнитных моментов на атомах железа для Fe 3 C (2,00 и 1,91 µ В на атомах Fe s и Fe g , соответственно) хорошо согласуются как с данными предыдущих расчетов [11–13, 15], так и с экспериментальным средним значением 1,78 µВ [23]. На атомах углерода наблюдается небольшой индуцированный магнитный момент – 0,11 µ В .
Таблица 5
Средние локальные магнитные моменты на атомах Fe, C и Si ( m , µ В ) и полная намагниченность ( M , µ В на элементарную ячейку) в системе с одним атомом кремния
|
N |
Тип |
Fes m |
m Feg |
с m |
m Si |
M |
|
16 |
С |
1,94 |
1,79 |
–0,11 |
–0,05 |
21,43 |
|
S |
1,95 |
1,76 |
–0,09 |
–0,05 |
19,21 |
|
|
G |
1,81 |
1,75 |
–0,09 |
–0,07 |
18,77 |
|
|
32 |
С |
1,97 |
1,87 |
–0,11 |
–0,05 |
22,08 |
|
S |
1,97 |
1,84 |
–0,10 |
–0,05 |
20,83 |
|
|
G |
1,94 |
1,87 |
–0,10 |
–0,07 |
20,99 |
|
|
64 |
С |
2,01 |
1,90 |
–0,11 |
–0,06 |
22,45 |
|
S |
1,99 |
1,89 |
–0,11 |
–0,06 |
21,79 |
|
|
G |
1,98 |
1,90 |
–0,11 |
–0,08 |
21,83 |
|
|
Fe 3 C |
2,00 |
1,91 |
–0,11 |
– |
22,50 |
|
При замещении Fe или С на Si наблюдается существенное изменение магнитных моментов атомов железа, которое практически исчезает для системы, состоящей из 64 атомов. Рассчитанный магнитный момент на атоме кремния имеет небольшое отрицательное значение –0,05÷–0,08µВ, что незначительно отличается от теоретического значения, полученного для Si в ОЦК-железе (–0,09 µ В ), а также согласуется с данными других теоретических работ [11–13]. Намагниченность систем и магнитные моменты на атомах снижаются с увеличением концентрации Si, связано это, прежде всего, с деформацией решетки. Наблюдается явный упругий эффект, который является дальнодействующим и при увлечении размера системы его влияние уменьшается (см. табл. 3).
На рис. 3 изображена полная плотность электронных состояний (DoS) для 16 и 64-атомных систем (как примеры объемной и вытянутой структур). В структуре DoS легко выделяются парциальные полосы подрешетки железа (от –7,5 до 5 эВ), локальные пики углерода (от –13,6 до –11,5 эВ) и кремния (от –10 до –8 эВ).
Примесь кремния дает вклад в DoS выше –5 эВ, что указывает на образование прямых связей между Si3 p -Fe3 d , что является причиной понижения магнитного момента на атомах железа. В случае G -позиции кремния происходит непосредственное связывание Si-Fe, в то время как для S -позиции – через соседний атом углерода. Также для С и G -позиции кремния наблюдается щель в p - d -полосе. Для системы из 64 атомов пики для атома кремния более узкие по сравнению с 16атомной системой, то есть повышается высота Fe3 d -полосы, что и приводит к увеличению магнитного момента на атомах железа. В силу операции трансляции при малом размере ячейки атомы кремния и углерода находятся близко, и происходит существенное перераспределение электронной плотности между железом, углеродом и кремнием с понижением среднего магнитного момента у атомов железа. С увеличением размера ячейки данный эффект ослабевает.
Физика
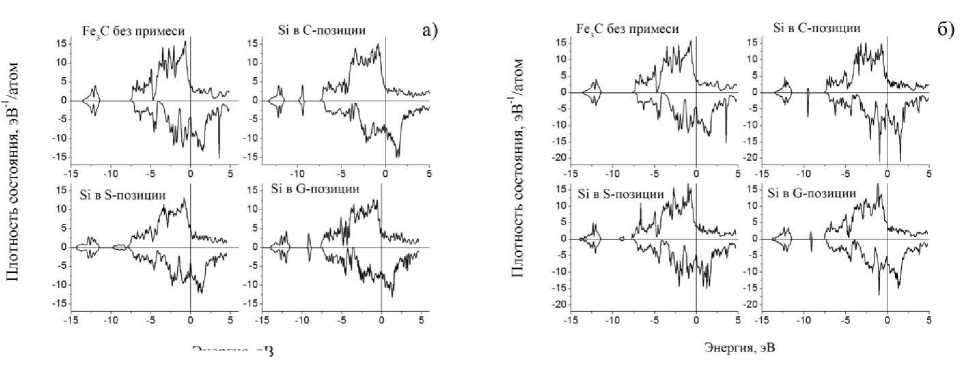
расположении атома Si в системы из 16 атомов; б) При расположении атома Si в системы из 64 атомов. Вертикальная сплошная линия обозначает уровень Ферми
Энергия, эВ
Рис. 3. Полная плотность состояний системы: а ) При
Заключение
Проведенные расчеты кремния в цементите показали, что для всех исследуемых случаев наиболее энергетически выгодны замещения позиций атома углерода, что указывает на отталкивающий эффект между данными примесями. С ростом концентрации Si при его расположении в позиции углерода намагниченность системы возрастает. В случае же расположения кремния в G - и S -позициях наблюдается резкое уменьшение намагниченности. Связано это, прежде всего, с деформацией решетки. Было получено, что для атома кремния в С-позиции (32 атома) энергия формирования отрицательна, и, следовательно, можно говорить о стабилизации цементита. Однако парциальная энтальпия для всех положений кремния положительна и значит, кремний остается в твердом растворе ОЦК-Fe, что в целом согласуются с экспериментальными наблюдениями. Было получено, что чем больше концентрация кремния, тем ниже средний магнитный момент на атомах железа. Данный эффект является следствием использования при расчетах периодических граничных условий и указывает на наличие взаимодействий между атомами кремния в соседних суперячейках.
Исследование поддержано грантом Российского научного фонда № 16-19-10252.
Список литературы Ab initio моделирование влияния кремния на образование карбида Fe3C в ОЦК-железе
- Bain, E.C. Alloying elements in steel / E.C. Bain, H.W. Paxton. - Metals Park, Ohio: Amer. Soc. for Metals, 1966. - 254 p.
- Deeley, P.D. Ferroalloys & alloying additives handbook / P.D. Deeley, K.J.A. Kundig, H.R. Spendelow. - Newfield, N.J.: Shieldalloy Corp., 1981. - 127 p.
- Гуляев, А.П. Металловедение / А.П. Гуляев. - М.: Металлургия, 1986. - 541 с.
- Гудремон, Э. Специальные стали / Э. Гудремон. - Москва: Металлургиздат, 1959. - Т. 1. - 1959. - 952 с.
- Umemoto, M. Influence of alloy additions on production and properties of bulk cementite / M. Umemoto, Z.G. Liu, K. Masuyama, K. Tsuchiya // Scripta Materialia. - 2001. - Vol. 45, no. 4. - P. 391-397.
- Influence of substitutional atoms on the solubility limit of carbon in BCC iron / H. Saitoh, K. Ushioda, N. Yoshinaga, W. Yamada // Scripta Materialia. - 2011. - Vol. 65, no. 10. - P. 887-890.
- Imai, Y. Influence of alloying elements on solubility of carbon and nitrogen in ferrite iron / Y. Imai, K. Masumoto, M. Sakamoto // Bulletin of the Japan Institute of Metals. - 1968. - Vol. 7. - Issue 3. - P. 137-152.
- Borchers, H. Zementitbildung in Stählen mit niedrigem Kohlenstoffgehalt / H. Borchers, W. König // Archiv für das Eisenhüttenwesen. - 1963. - Vol. 34, no. 6. - P. 453-463.
- Leak, D.A. Solubility and Diffusion of Carbon in a Silicon-Iron Alloy / D.A. Leak, G.M. Leak // J. Iron Steel Inst. - 1958. - Vol. 189, № 3. - P. 256-262.
- Лякишев, Н.П. Диаграммы состояния двойных металлических систем / Н.П. Лякишев. - Т.1. - М.: Машиностроение, 1996. - 991 c.
- Jang, J.H. Substitutional solution of silicon in cementite: A first-principles study / J.H. Jang, I.G. Kim, H.K.D.H. Bhadeshia // Computational Materials Science. - 2009. - Vol. 44, no. 4. - P. 1319-1326.
- Electronic structure and magnetic properties of Fe3C with 2p and 3p impurities / O.Y. Gutina, N.I. Medvedeva, I.R. Shein et al. // Physica status solidi (b). - 2009. - Vol. 246, no. 9. - P. 2167-2171.
- Ande, C.K. First-principles prediction of partitioning of alloying elements between cementite and ferrite / C.K. Ande, M.H.F. Sluiter // Acta Materialia. - 2010. - Vol. 58, no. 19. - P. 6276-6281.
- Ande, C.K. First-principles calculations on stabilization of iron carbides (Fe3C, Fe5C2 and η-Fe2C) in steels by common alloying elements / C.K. Ande, M.H.F. Sluiter // Metallurgical and Materials Transactions A. - 2012. - Vol. 43. - Issue 11. - P. 4436-4444.
- Partitioning of Cr and Si between cementite and ferrite derived from first-principles thermodynamics / H. Sawada, K. Kawakami, F. Körmann et al. // Acta Materialia. - 2016. - Vol. 102. - P. 241-250.
- Schwarz, K. Solid state calculations using WIEN2k / K. Schwarz, P. Blaha // Computational Materials Science. - 2003. - Vol. 28, no. 2. - P. 259-273.
- Fasiska, E.J. On the cementite structure / E.J. Fasiska, G.A. Jeffrey // Acta Crystallographica. - 1965. - Vol. 19, no. 3. - P. 463-471.
- Эмсли, Д. Элементы / Д. Эмсли. - М.: Мир, 1993. - 255 с.
- Thermal expansion and crystal structure of cementite, Fe3C, between 4 and 600 K determined by time-of-flight neutron powder diffraction / I.G. Wood, L.Vočadlo, K.S. Knight, D.P. Dobson et al. // Journal of Applied Crystallography. - 2004. - Vol. 37, no. 1. - P. 82-90.
- Meschel, S.V. Standard enthalpies of formation of some 3d transition metal carbides by high temperature reaction calorimetry / S.V. Meschel, O.J. Kleppa // Journal of alloys and compounds. - 1997. - Vol. 257, no. 1-2. - P. 227-233.
- Guillermet, A.F. Cohesive properties and vibrational entropy of 3d-transition metal carbides / A.F. Guillermet, G. Grimvall // Journal of Physics and Chemistry of Solids. - 1992. - Vol. 53, no. 1. - P. 105-125.
- DOI: 10.1016/0022-3697(92)90019-A
- Influence of alloying elements on the kinetics of strain-induced martensitic nucleation in low-alloy, multiphase high-strength steels / L. Samek, E. De Moor, J. Penning, B.C. De Cooman // Metallurgical and Materials Transactions A. - 2006. - Vol. 37, no. 1. - P. 109-124.
- Shull, C.G. Neutron diffraction studies of the magnetic structure of alloys of transition elements / C.G. Shull, M.K. Wilkinson // Physical Review. - 1955. - Vol. 97, no. 2. - P. 304-310.
- DOI: 10.1103/PhysRev.97.304


