Адаптация растений-регенерантов пшеницы к условиям ex vitro: работа устьиц
Автор: Мартыненко Елена Викторовна, Круглова Наталья Николаевна, Дубровная Оксана Васильевна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Биотехнология
Статья в выпуске: 5-3 т.13, 2011 года.
Бесплатный доступ
Исследован устьичный аппарат листьев регенерантов пшеницы, полученных в условиях высокой влажности и низкой освещенности in vitro, в процессе их постепенной адаптации к условиям пониженной влажности воздуха и высокой освещенности ex vitro. Установлено, что к концу эксперимента регенеранты ex vitro и интактные растения имели сходные значения устьичной проводимости. Сравнительный цитологический анализ устьиц адаптированных ex vitro регенерантов и интактных растений in vivo продемонстрировал их морфологическое сходство при меньших размерах устьиц регенерантов. Предложенный способ постепенной адаптации к условиям ex vitro позволяет добиваться высокой выживаемости регенерантов.
Выживаемость регенерантов, устьичная проводимость, яровая мягкая пшеница triticum aestivum l, адаптация
Короткий адрес: https://sciup.org/148200434
IDR: 148200434 | УДК: 576.5/.7.085.23:581.1
Adaptation of wheat plant-regenerants to ex vitro conditions: stomata functioning
The investigation of leaves stomatal apparatus of wheat regenerants, obtained under conditions of high humidity and low illumination in vitro was carried out during their gradual (15 days period) adaptations to conditions of the lowered air humidity and high illumination ex vitro. It was established, that at the end of experiment regenerants ex vitro and intact plants had similar values of stomatal conductivity. The comparative cytological analysis of stomata of adapted ex vitro regenerants and intact plants in vivo showed their morphological similarity, although the regenerants had smaller sizes of stomata. The offered method of gradual adaptation to ex vitro conditions allows achieving high survival rate of regenerants.
Текст научной статьи Адаптация растений-регенерантов пшеницы к условиям ex vitro: работа устьиц
Большинство биотехнологических методов культуры in vitro направлено на получение в конечном этапе полноценных фертильных растений-регенерантов. Основная проблема в этой области исследований – низкая выживаемость растений-регенерантов при переносе их из условий культуры in vitro, характеризующихся высокой влажностью воздуха и низкой освещенностью, в посткультуральные условия ex vitro , характеризующиеся пониженной влажностью воздуха и высокой освещенностью.
Разработка эффективной системы получения полноценных, с качественными семенами, растений-регенерантов остается актуальной и до настоящего времени. Несмотря на то, что накоплен значительный фактический материал, касающийся различных аспектов исследования выживаемости растений-регенерантов, многие вопросы остаются открытыми. Так, слабо изучена работа устьичного аппарата в процессе развития регенерантов in vitro и ex vitro и особенно в критический момент переноса регенерантов из условий in vitro в условия ex vitro . Согласно литературным данным, регенеранты, полученные in vitro , имеют низкую выживаемость при переносе в условия ex vitro из-за формирования у них аномального устьичного аппарата [15]. Однако в литературе отсутствуют данные детальных физиологических и цитологических исследований устьиц растений-регенерантов, адаптируемых к условиям ex vitro .
В связи с этим цель данной работы заключалась в физиологической и цитологической оценке устьиц растений-регенерантов пшеницы в процессе развития in vitro , в критический момент переноса из условий in vitro в условия ex vitro и в процессе адаптации к условиям ex vitro.
МАТЕРИАЛ И МЕТОДЫ
Объектом исследования послужила яровая мягкая пшеница сорта Башкирская 26, перспективная для климатической зоны Южного Урала,[6] семена которой были любезно предоставлены к.с.-х.н. В.И. Никоновым, заведующим лабораторией селекции и семеноводства Башкирского НИИ СХ РАСХН (г. Уфа).
Предварительно было выявлено, что незрелые зародыши этого сорта пшеницы c высокой отзывчивостью формируют морфогенные каллусы в условиях культуры in vitro. Для данного эксперимента использовали растения-регенеранты в фенофазе кущения, полученные in vitro из морфогенных каллусов зародышевого происхождения, и интактные растения в той же фенофазе. Растения-регенеранты до 7-х сут фенофазы кущения выращивали in vitro в пробирках в климатической камере MLR-351H (Sanyo, Japan) при 16-часовом фотопериоде, освещенности 25000 лк. Затем их переносили в почвенную смесь и в течение 5-ти сут содержали в той же климатической камере при относительной влажности воздуха (ОВВ) 90 % и щадящем световом режиме (освещенность 16000 лк). На следующем этапе эксперимента ОВВ в климатической камере снижали до 60 %. На 8-е сут эксперимента растения-регенеранты переносили на воздух на светоплощадку при освещенности 16000 лк и 16часовом фотопериоде. С 13-х сут и до конца эксперимента освещенность составляла 25000 лк.
Интактные растения до 7-х сут фенофазы кущения и далее выращивали на светоплощадке при 16часовом фотопериоде и освещенности 25000 лк.
Для физиологической оценки реакции устьиц растений обеих групп использовали показатель устьичной проводимости, характеризующий степень открытости устьиц, что позволяет оценить интенсивность транспирации и сдвиги в водном обмене.интенсивность транспирации и сдвиги в водном обмене. Показатель устьичной проводимо- сти измеряли с помощью автоматического поро-метра (MK Delta-T, UK). Временные цитологические препараты, полученные согласно общепринятой методике [7] просматривали на микроскопе проходящего света Axio Imager A1 (Carl Zeiss, Jena). Статистическую обработку полученных результатов проводили, используя программы Excel с учетом основных статистических параметров.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В качестве точки отсчета использовали показатель устьичной проводимости «пробирочных» растений-регенерантов на 7-е сут фенофазы кущения, находящихся в климатической камере (освещенность 25000 лк), перед их высадкой в почвенную смесь. Устьичная проводимость таких растений-регенерантов составила 151 мМоль/м2с, что в 1,7 раза превышало устьичную проводимость интактных растений того же возраста (90 мМоль/м2с), растущих в почвенной смеси на светоплощадке при той же освещенности (рис. 1А). Возможно, это обусловлено более высокой относительной влажностью воздуха в пробирках.
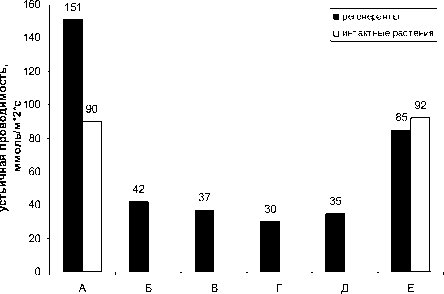
Рис. 1 . Устьичная проводимость растений-регенерантов в процессе адаптации к условиям ex vitro в сравнении с аналогичными показателями интактных растений : А – растения-регенеранты в пробирках перед высадкой в почвенную смесь и интактные растения в почвенной смеси (освещенность 25000 лк); Б – 1-е сут эксперимента, растения-регенеранты в почвенной смеси (ОВВ 90 %, освещенность 16000 лк); В - 5-е сут эксперимента, растения-регенеранты в почвенной смеси (ОВВ 90 %, освещенность 16000 лк); Г – 7-е сут эксперимента, растения-регенеранты в почвенной смеси (ОВВ 60 %, освещенность 16000 лк); Д – 10-е сут эксперимента, растения-регенеранты в почвенной смеси (воздух, освещенность 16000 лк); Е – 15-е сут эксперимента, адаптированные растения-регенеранты и интактные растения в почвенной смеси (воздух, освещенность 25000 лк)
В критический момент переноса регенерантов в условия ex vitro показатель устьичной проводимости резко снижался (до 42 мМоль/м2с) по сравнению с «пробирочными» растениями (рис. 1Б). На 5-е сут эксперимента его значение составило 37 мМоль/м2с (рис. 1В). Уменьшение устьичной проводимости в данном случае можно расценивать как следствие фотоактивной реакции устьиц на понижение освещенности.
На следующем этапе эксперимента ОВВ в климатической камере уменьшали до 60 %. Показатель устьичной проводимости продолжал падать и на 7-е сут эксперимента достиг 30 мМоль/м2с (рис. 1Г).
На 8-е сут опыта устьичная проводимость перенесенных на светоплощадку растений-регенерантов (освещенность 16000 лк и 16-часовой фотопериод) начинала повышаться и на 10-е сут эксперимента достигла 35 мМоль/м2с (рис. 1Д), что свидетельствует о начале адаптации растений-регенерантов к изменившимся условиям.
Повышение освещенности светоплощадки до 25000 лк на 13-е сут эксперимента привело к резкому повышению показателя устьичной проводимости адаптируемых растений-регенерантов, и на 15-е сут эксперимента этот показатель (85 мМоль/м2с) был сопоставим с аналогичным показателям интактных растений (92 мМоль/м2с) (рис. 1Е). Возможно, такое резкое повышение обусловлено увеличением степени открытости устьиц под действием света. С другой стороны, оно свидетельствует о нормализации функционирования устьиц у растений-регенерантов. Степень выживаемости растений-регенерантов, по имеющимся в литературе сведениям [8,9], в среднем, составляет 50-60 %. При предложенном нами варианте постепенной адаптации растений-регенерантов к условиям ex vitro отмечена высокая выживаемость растений-регенерантов – 83 %.
Проведенный морфометрический анализ выявил, что устьица растений-регенерантов, адаптированных к условиям ex vitro (на 15-е сут эксперимента), морфологически не отличаются от устьиц интактных растений в той же фазе развития (рис. 2). В то же время устьица регенерантов имеют меньшие размеры. Так, длина устьиц растений-регенерантов составляла, в среднем, 55.04±1.45 мкм, тогда как у интактных растений она была равна 67.71±1.49 мкм.
Согласно литературным данным, уменьшение размеров устьиц характерно для растений-регенерантов и других представителей цветковых растений, причем авторы также отмечают нормальное функционирование устьиц растений-регенеранов [10-15].
Таким образом, данные по устьичной проводимости растений-регенерантов яровой мягкой пшеницы, полученных in vitro и адаптированных к условиям ex vitro, свидетельствуют о нормальном функционировании устьиц при их меньших размерах. Предложенный нами вариант постепенной адаптации к условиям ex vitro позволит добиваться высокой выживаемости растений-регенерантов.
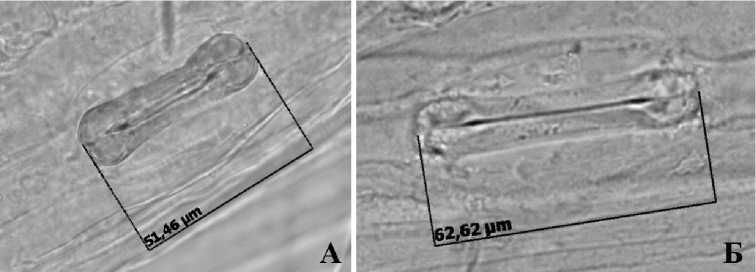
Рис. 2 . Морфология устьиц адаптированных растений-регенерантов (А) и интактных растений (Б) в фенофазе кущения на 15-е сут эксперимента.
Авторы благодарны к.б.н. Веселовой С.В. и к.б.н. Зайцеву Д.Ю. за помощь в проведении части экспериментальной работы.
Работа выполнена при поддержке РФФИ-Поволжье (грант № 08-04-97045), а также по программе «Ведущие научные школы РФ» (грант № НШ 7637.2010.4).
Список литературы Адаптация растений-регенерантов пшеницы к условиям ex vitro: работа устьиц
- Sallanon H., Tort M., Coudret A. The ultrastructure of micropropagated and greenhouse rose plant stomata//Plant Cell, Tissue and Organ Culture. 1993. V. 32 P. 227-233.
- Pospisilova J. Effect of air humidity on the development of functional stomatal apparatus//Biologia Plantarum. 1996. V. 38. № 2. P. 197-204.
- Noe N., Bonini L. Leaf anatomy of highbush blueberry grown in vitro and during acclimatization to ex vitro conditions//Biologia Plantarum. 1996. V. 38. № 1. P. 19-25.
- Fordham M.C., Harrison-Murray R., Knight L. Effects of leaf wetting and high humidity on stomatal function in leafy cutting and intact plants of Corylus maxima//Physiologia Plantarum. 2001. V. 113. P. 233-240.
- Joshi P., Joshi N., Purohit S.D. Stomatal characteristics during micropropagation of Wrightia tomentosa//Biologia Plantarum. 2006. V. 50. № 2. P. 275-278.
- Характеристика сортов сельскохозяйственных культур, включенных в Госреестр по Республике Башкортостан. Пособие для агрономов/[под ред. Д.Б. Гареева]. Уфа, 1997. 96 с.
- Паушева З.П. Практикум по цитологии растений. М.: Колос, 1988. 170 с.
- Plant biotechnology and molecular markers/[Eds Srivastava S., Narula A., Srivastava S.]. New Delhi: Anamaya Publishers, 2004. P. 325.
- Plant cell and tissue culture -a tool in biotechnology. Basics and application/[Eds Neumann K.-H., Kumar A., Imani J.]. Berlin, Heidelberg: Springer-Verlag, 2009. P. 333.
- Gribble K., Sarafis K., Nailon J., Holford P., Uwins P. Environmental scanning electron microscopy of the surface of normal and leaves of Gypsophila paniculata (Babies, Breath) cultured in vitro//Plant Cell Reports. 1996. V. 15 P. 771-776.
- Ali-Ahmad M., Hughes G.H., Safadi F. Studies on stomatal function, epicuticular wax and stem-root transition region of polyethylene glycol-treated and nontreated in vitro grape plantlets//In vitro Cellular and Developmental Biology Plant. 1998. V. 34. P. 1-7.
- Estrada-Luna A.A., Davies Jr F.T., Egilla J.N. Physiological changes and growth of micropropagated chille ancho pepper plantlets during acclimatization and post-acclimatization//Plant Cell, Tissue and Organ Culture. 2001. V. 66. P. 17-24.
- Brutti C.B., Rubio E.J., Llorente B.E., Apostolo N.M. Artichoke leaf morphology and surface features in different micropropagation stages//Biologia Plantarum. 2002. V. 45. № 2. P. 197-204.
- Jo E.-A., Tewari R.K., Hahn E.-J., Paek K.-Y. In vitro sucrose concentration affects growth and acclimatization of Alocasia amazonica plantlets//Plant Cell, Tissue and Organ Culture. 2009. V. 96. P. 307-315.


