Алгоритм диагностики аденомиоза с использованием неинвазивных методов исследования
Автор: Сорокина А.В., Радзинский В.Е., Зиганшин Р.Х., Арапиди Г.П.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.6, 2011 года.
Бесплатный доступ
Предлагается использовать неинвазивный двухступенчатый подход к ранней диагностике аденомиоза. Обследовано 120 пациенток с диагнозом «аденномиоз» различной степени тяжести и 30 практически здоровых пациенток составили контрольную группу. На первом этапе проводилось протеомное профилирование сыворотки крови с использованием МАЛДИ масс-спектрометрии, что позволило дифференцировать пациенток с аденомиозом и контрольную группу. На втором этапе проводилось исследование цитокинов (ИЛ-6, ИЛ-10) и факторов роста (EGF, VEGF) в сыворотке крови c использованием иммуноферментного анализа, что позволило выявлять активные формы аденомиоза и тем самым определять прогноз течения.
Аденомиоз, малди масс-спектрометрия, ил-6, ил-10, факторы роста
Короткий адрес: https://sciup.org/140187887
IDR: 140187887 | УДК: 618.14-006.55:616-08-039.75
Algorithm of diagnosis of adenomyosis by non-invasive methods
The using of non-invasive methods are offered to early diagnosis of adenomyosis. Comparative MALDI mass spectrometry profiling of blood serum samples from patients with verified adenomyosis (n=120) as well as from a control group of healthy women (n=30) has been carried out. Mass spectrometry profiles demonstrated sensitivity and specificity close to 100% for the detection of adenomyosis. On the second stage we discovered the production of cytokines (IL-6, IL-10) and growth factors (EGF, VEGF) by an enzyme-linked immunosorbent assay from women with adenomiosis. We observed that levels of IL-6, IL-10, EGF, VEGF are correlated with the severity of the disease and prognosis.
Текст научной статьи Алгоритм диагностики аденомиоза с использованием неинвазивных методов исследования
Эндометриоз является одной из наиболее актуальных проблем современной гинекологии и встречается у более чем 50% женщин репродуктивного возраста, причем в последние годы отмечается неуклонный рост данной патологии, и его ранняя диагностика чрезвычайно актуальна.
Среди всех поражений генитальным эндометриозом частота аденомиоза достигает 70–90%; помимо этого заболевание имеет склонность к рецидивированию после медикаментозной терапии [1].
По данным ряда авторов эффективность лечения аденомиоза зависит от степени его активности, определение которой на дооперационном этапе, представляет большие трудности. Существующие на сегодняшний день методы определения функциональной активности аденомиоза, в основном, базируются на степени выраженности той или иной клинической симптоматики, либо на эффективности лечения, что во многом является субъективным и не позволяет выявлять ранние стадии заболевания [5].
И.И. Куценко (1994) предложены морфо-функциональные критерии активных форм эндометриоза по результатам исследования удаленных маток, а также в соскобах эндометрия, где производится визуально-количественная оценка митотического режима и гистохимический анализ содержания РНК и ДНК. Недостатком данных подходов является их ретроспективный характер, необходимость инвазивного вмешательства (раздельное диагностическое выскабливание стенок полости матки под контролем гистероскопа). Применение данных ме- тодов ограничено у пациенток, получавших гормонотерапию, а также у находящихся в менопаузе [6].
В диагностике аденомиоза в настоящее время широко используется ультразвуковая диагностика (УЗИ). Точность выявления рассматриваемой патологии по данным разных авторов колеблется от 74,4% до 96,8%, и в ряде случаев имеют место расхождения в диагнозе, установленном при трансвагинальном УЗИ и патомор-фологическом исследовании удаленной матки [5].
В последнее время как за рубежом, так и в нашей стране предпринимаются усилия для создания малоинвазивных скрининговых методов диагностики аденомиоза и определения степени его активности.
Для поиска в сыворотке крови новых маркеров различных заболеваний все чаще используются постгеномные методы анализа, среди которых протеомные технологии занимают ведущие позиции.
Для анализа такой структуры, как сыворотка крови используются различные методы фракционирования, позволяющие выделять из такой сложной смеси белков и пептидов относительно узкие и воспроизводимые по составу фракции, которые в дальнейшем анализируют масс-спектрометрией.
Масс-спектрометрия – метод анализа вещества путем определения массы (чаще, отношения массы к заряду) и относительного количества ионов, получаемых при ионизации и фрагментации исследуемого вещества. За разработку этого метода Джон Фенн и Коичи Танаке были удостоены Нобелевской премии по химии в 2002 году [4].

В литературе описаны примеры успешного применения этого метода для выявления различий между сывороткой крови больных раком желудка, прямой кишки, простаты, гепатоклеточной карциномы, эндометрия, яичников и сывороткой крови здоровых людей [3].
Рядом преимуществ по сравнению с другими вариантами масс-спектрометрии обладает времяпролетная МАЛДИ масс-спектрометрия, а именно большей производительностью и чувствительностью.
Однако данный метод диагностики позволяет лишь дифференцировать одно заболевание от другого; определить степень активности с помощью масс-спектрометрии не представляется возможным. В связи с этим, на втором этапе диагностики можно использовать определение иммунологических маркеров, а именно цитокинов и факторов роста в сыворотке крови.
Установлено, что цитокины и факторы роста являются важными регуляторами клеточной пролиферации и дифференцировки, наряду с гормонами.
К настоящему времени можно считать доказанной роль многих цитокинов и факторов роста в патогенезе эндометриоза [8]. В то же время, лишь очень небольшое число исследований касалось аденомиоза.
Цитокины вовлечены фактически в каждое звено иммунитета, включая дифференцировку предшественников клеток иммунной системы, представление антигена, клеточную активацию и пролиферацию, экспрессию молекул адгезии и острофазового ответа [2].
В настоящий момент диагностическая значимость оценки уровня концентрации цитокинов заключается в констатации самого факта ее повышения или понижения у данного больного с конкретным заболеванием, причем для оценки тяжести и прогноза течения заболевания целесообразно определять концентрацию как про- (интерлейкин-6 – ИЛ-6), так и противовоспалительных (интерлейкин-10 – ИЛ-10) цитокинов в динамике [9].
Повышение содержания таких факторов роста, как сосудисто-эндотелиальный (VEGF) и эпидермальный (EFG) создает благоприятные условия для инвазии и последующего роста жизнеспособных фрагментов эндометрия [7].
Таким образом, целью данного исследования явилось выявление в сыворотке крови пациенток потенциальных маркеров, которые можно будет использовать для диагностики, определения степени тяжести и прогноза аденомиоза.
Материалы и методы
Для достижения поставленной цели в период с 2006 по 2010 гг. было проведено обследование 150 пациенток, из которых 120 – больные аденомиозом разной степени активности и распространенности (основная группа) и 30 – практически здоровых женщин репродуктивного возраста (контрольная группа). Исследование проводилось на материалах гинекологических отделений ГКБ № 64, ГКБ № 29, НМХЦ им. Н.И. Пирогова Росздрава г. Москвы.
Аденомиоз был диагностирован клинически с использованием дополнительных методов обследования: УЗИ, гистероскопия, морфологическое исследование.
Протеомное профилирование сывороток крови проводили в лаборатории Института Биоорганической химии им. М.М. Шемякина и Ю.А. Овчинникова РАН.
Для фракционирования образцов сывороток крови использовали набор для профилирования, содержащий магнитные микрочастицы со слабой катионообменной поверхностью MB -WCX производства компании Bruker Daltonics (Германия). Описание этого набора для профилирования, а также рекомендованного для него протокола фракционирования можно найти на Интернет странице компании – www.bdal.de .
Фракционирование сывороток крови проводили на специализированном роботе ClinProt robot (Bruker Daltonics, Германия), по протоколу, рекомендованному производителем магнитных микрочастиц.
Масс-спектры получали с использованием время-пролетного масс-спектрометра Ultraflex (Bruker Daltonics, Германия).
Масс-спектрометрические данные анализировали с использованием компьютерной программы ClinProTools 2.1 (Bruker Daltonics, Германия). Математические модели для классификации масс-спектров смеси пептидов и белков, полученных после фракционирования сывороток крови, строили на основе Генетического Алгоритма (ГА) и Управляемой Нейронной Сети (Supervised Neural Network, УНС).
Для построения классификационных моделей масс-спектры каждой из групп «контроль» и «аденомиоз» разделяли пополам, одну пару использовали для построения классификационной модели, а вторую – для ее валидации.
Содержание ИЛ-6 и ИЛ-10 в сыворотке крови определяли твердофазным иммуноферментным методом с использованием диагностических тест-систем ЗАО «Вектор-Бест» (Россия); для изучения факторов роста VEGF и EGF использовали тест-системы BioSource International. Исследование проводили в лаборатории клинической иммунологии ГКБ № 29.
Результаты и их обсуждение
Анализ клинического течения аденомиоза не обнаружил у больных достаточных различий в возрасте, времени наступления менархе и количества родов в зависимости от степени инвазии эндометриоза в миометрий.
В связи с выявленными различиями и особенностями в клиническом течении и молекулярно-биологических процессах, в работе мы использовали термины «активный» и «неактивный» аденомиоз, отражающие степень клинической и морфологической активности эндометриоидного процесса [6].
В зависимости от степени выраженности основных клинических проявлений, характерных для аденомиоза, все исследованные пациенты (n=120) условно были раз-

делены на 2 клинические группы: I группу составили 76 пациенток с клинически активным аденомиозом; II группу – 44 пациентки с клинически неактивным аденомиозом.
Для определения форм клинической активности произвели оценку наиболее распространенных клинических проявлений аденомиоза – болевого синдрома и гиперполименореи.
Определение степени болевого синдрома осуществляли с помощью системы для оценки выраженности болей и дисменореи, согласно которой интенсивность боли определялась в баллах: 1–3 балла – слабая боль; 4–6 – умеренная боль; 7–9 – сильная [1].
Общеизвестно, что наличие аденомиоза часто сопровождается маточными кровотечениями, зачастую вызывающими анемизацию больных. В связи с чем, ги-пер- и полименорею различали без анемии и с анемией. По степени тяжести различали легкую (Hb 90–110 г/л), среднюю (Hb 70–90г/л) и тяжелую (Hb – ниже 70 г/л) анемию.
Пациенток с умеренной и сильной болью и пациенток с гиперполименореей в сочетании с анемией средней и тяжелой степени относили к I группе больных с клинически активным проявлением заболевания. Больных со слабой болью, отсутствием анемии или гиперполименореей в сочетании с анемией легкой степени относили ко II группе пациенток, с клинически неактивным аденомиозом.
Анализ длительности заболевания аденомиозом в зависимости от момента начальных клинических проявлений до первой госпитализации позволил выявить, что при активном аденомиозе продолжительность данного периода в более, чем 50% случаев составила 1–5 лет, а при неактивном аденомиозе – 6–10 лет, то есть для активного аденомиоза характерна меньшая длительность заболевания с момента первых симптомов до госпитализации и соответственно быстрое прогрессирование процесса.
В I группе гиперпластические процессы эндометрия (81,5%) и миома матки (75,6%) выявлены чаще, чем во II группе (60,2% и 31,5%). Эндометриоидные кисты яичников наблюдались у 25,2% больных с активным аденомиозом и всего лишь у 3,5% пациенток из II группы.
На первом этапе исследования проводилось масс-спектрометрическое профилирование сывороток крови больных аденомиозом и контрольной группы.
На основании масс-спектрометрического профилирования сывороток крови после их фракционирования на магнитных микрочастицах со слабой катионообменной поверхностью (MB-WCX) были построены классификационные модели с использованием обоих математических алгоритмов. При использовавшихся параметрах обработки масс-спектров в них воспроизводимо детектировали 96 пиков. После изучения вклада площадей отдельных пиков в классификационные модели, 3 пика были выделены как наиболее значимые для их специфичности и чувствительности (рис. 1). Чувствительность и специфичность метода приближалась к 100%.
На втором этапе исследования проводился твердофазный иммуноферментный анализ ИЛ-6, ИЛ-10, VEGF и EGF, что позволило выявить взаимосвязь между степенью активности аденомиоза и концентрацией данных белков в сыворотке крови.
При анализе значений концентраций ИЛ-6, ИЛ-10 полученных методом ИФА, были получены следующие данные – рис. 2.
Присутствие в сыворотке крови ИЛ-6 обнаружено у 49 (81,6%) больных аденомиозом; из них 34 (69,4%) пациенток I группы – средняя концентрация 435,5 пг/мл и 15 (30,6%) пациенток II группы – средняя концентрация 223,6 пг/мл (р<0,05). В контрольной группе ИЛ-6 в сыворотке крови обнаружено не было.
Присутствие в сыворотке крови ИЛ-10 обнаружено у 32 (53,3%) больных аденомиозом; из них 22 (68,7%) пациенток I группы – средняя концентрация 324,5 пг/мл и 10 (31,3%) пациенток II группы – средняя концентрация 164,1 пг/мл (р<0,05). В контрольной группе ИЛ-10 обнаружен у 3(10%) пациенток – средняя концентрация 145,2 пг/мл.
Степень участия цитокинов в патогенезе аденомиоза находится в прямой зависимости от стадии иммунного ответа, степени вовлеченности в него различных субпопуляций иммунокомпетентных клеток, тяжести и распространенности патологического процесса. Изменение иммунореактивности обследованных пациенток аденомиозом сопровождалось активацией продукции провос-палительных цитокинов (ИЛ-6) и в меньшей степени противовоспалительных цитокинов (ИЛ-10).
При анализе значений концентраций EFG и VEGF, полученных методом ИФА, были получены следующие данные – рис. 3.
Средняя концентрация в сыворотке крови EFG в I группе составила 647,4 пг/мл, во II группе – 334,5 пг/мл, в контрольной группе – 45,9 пг/мл.
Средняя концентрация в сыворотке крови VEFG в I группе составила 725,3 пг/мл, во II группе – 250,6 пг/мл, в контрольной группе – 38,3 пг/мл.
По нашим данным содержание в сыворотке крови таких цитокинов, как ИЛ-6 и ИЛ-10, а также факторов роста – VEGF и EGF повышено в сравнении с контрольной группой, что согласуется с данными литературы, касающимися наружного эндометриоза [8].
Заключение
Привлекательность использования сыворотки крови для диагностики различных заболеваний обусловлена, главным образом, тем обстоятельством, что она наиболее полно представляет фенотип человека, его состояние в конкретный момент времени [3]. Еще одно немаловажное достоинство сыворотки крови – ее доступность, поскольку она является наиболее распространенным в медицинской практике первичным клиническим образцом.
На сегодняшний день нет однозначного ответа на вопрос, в какой связи находятся регистрируемые

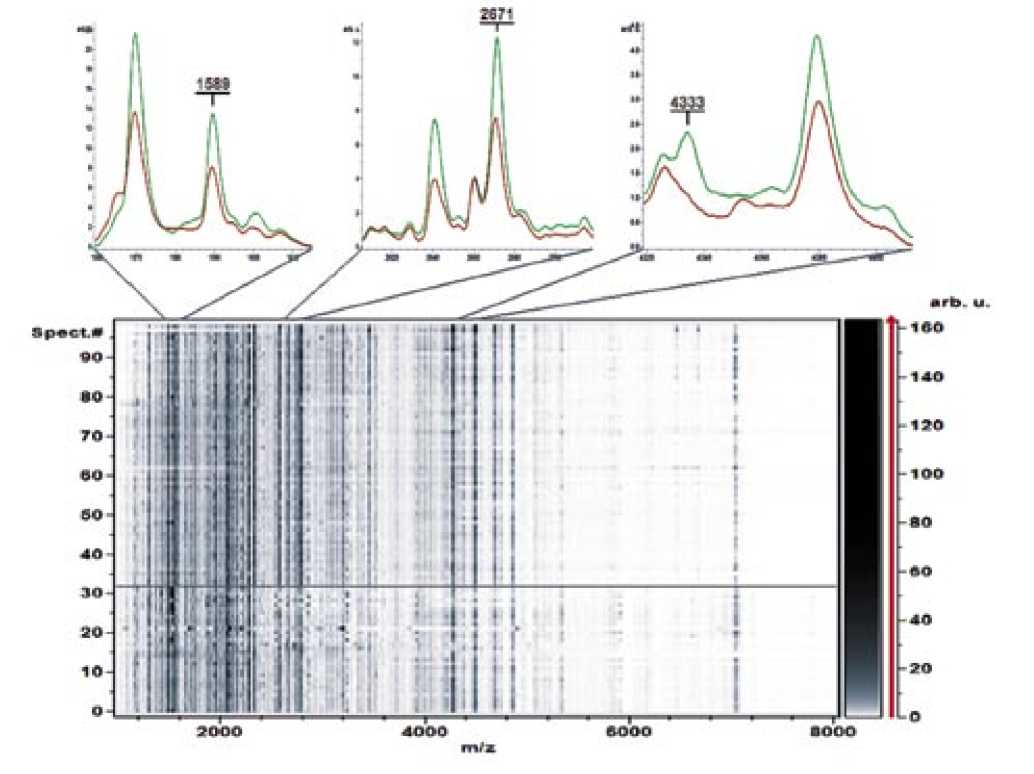
Рис. 1. Итоговый анализ масс-спектрометрических профилей образцов сывороток крови групп «аденомиоз» и «контроль», фракционированных с использованием магнитных микрочастиц MB-WCX
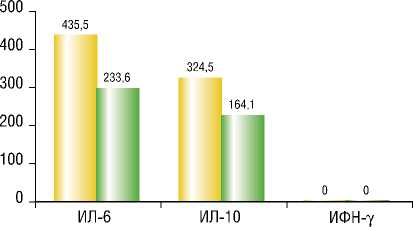
Активный аденомиоз I ■ Неактивный аденомиоз
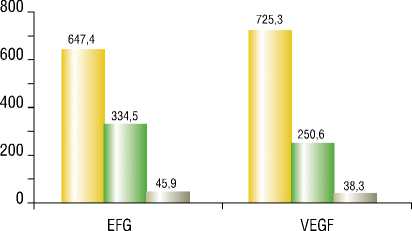
Активный аденомиоз Контроль
I ■ Неактивный аденомиоз
Рис. 2. Уровень цитокинов в сыворотке крови у больных аденомиозом
Рис. 3. Уровень факторов роста в сыворотке крови у больных аденомиозом
масс-спектрометрией в сыворотке крови изменения пептидно-белковых паттернов с исследуемым патологическим процессом в организме. Предполагается, что эти изменения могут отражать реальные колебания концентраций белков и пептидов, напрямую ассоциированных с заболеванием.
Результаты исследования свидетельствуют о том, что клиническая активность аденомиоза обусловлена нарушениями молекулярно-биологических процессов. Для клинически активного аденомиоза характерно более выраженное повышение уровня ИЛ-6, ИЛ-10, VEGF и EGF, т.е. пролиферации, неоангиогенеза и иммуносупрессии.
Таким образом, применение масс-спектрометрического анализа сыворотки крови на первом этапе и определение концентрации цитокинов ИЛ-6, ИЛ-10, а также факторов роста VEGF и EGF на втором этапе диагностики позволяет не только достоверно поставить диагноз, но и определить степень активности заболевания, а значит и необходимость терапии в настоящий момент.
Список литературы Алгоритм диагностики аденомиоза с использованием неинвазивных методов исследования
- Адамян Л.В. Эндометриозы./Л.В. Адамян, В.И. Кулаков, Е.Н. Андреева -М.: Медицина. Издание 2-е, 2006. -416 с.
- Адамян Л.В. Цитокины в перитонеальной жидкости и периферической крови больных с сочетанными доброкачественными заболеваниями матки./Л.В. Адамян, Х.З. Гусаева, И.А. Василенко и др.//Проблемы репродукции. -2008. № 6. -С. 16-19.
- Зиганшин Р.Х. Поиск потенциальных биомаркеров рака яичников в сыворотке крови./Р.Х. Зиганшин, Д.Г. Алексеев, Г.П. Арапиди и др.//Биомедицинская химия.-2008. -№ 54. -С. 408-419.
- Ильина Е.Н. Масс-спектрометрия нуклеиновых кислот в молекулярной медицине./Е.Н.Ильина, В.М.Говорун//Биоорганическая химия. -2009. -№ 2(35). С. 1-16.
- Ищенко А.И. Эндометриоз: современные аспекты./А.И. Ищенко, Е.А. Кудрина. -М: ООО «Медицинское информационное агенство». 2008. -176 с.
- Куценко И.И. Генитальный эндометриоз./И.И. Куценко.-Краснодар: Адыгея. -1994. -192 с.
- Сидорова И.С. Неоангиогенез и экспрессия факторов роста в различных по клинической активности формах аденомиоза./И.С. Сидорова, А.Л. Унанян, Е.А. Коган и др.//Тезисы Первого Международного конгресса по репродуктивной медицине. -2006. -С. 86-7.
- Berkkanoglu M. Immunology and endometriosis/M.Berkkanoglu, A.Arici//AGRI. 2003. -50. -P. 48-59.
- Koumantakis E. Soluble serum interleukin-2 receptor, interleukin-6 and interleukin-1a in patients with endometriosis and in controls./E. Koumantakis, I. Matalliotakis, M. Neonaki//Arch Gynecol Obstet -1994. -255 -P. 107-12.


