Алгоритм и программное обеспечение для расчета термических циклов разделения газовых смесей с применением термодинамических критериев
Автор: Мазиков А.А.
Журнал: Программные системы: теория и приложения @programmnye-sistemy
Рубрика: Математическое моделирование
Статья в выпуске: 1 (70) т.17, 2026 года.
Бесплатный доступ
Методология оптимизационной термодинамики использована для решеня задачи о предельных возможностях термических циклов разделения и разработки алгоритма расчета и программного обеспечения. Существующие программы и алгоритмы для расчета термических циклов не применяли термодинамические критерии. Получены выражения для предельного КПД цикла и его максимальной производительности в зависимости от состава разделяемой смеси, величины и температуры греющего потока. Построена и параметризована граница области реализуемых режимов цикла в плоскости производительность – расход теплоты. Полученные алгоритмы использованы при разработке программного обеспечения для расчета термических циклов.
Термодиффузия, предельная емкость, уравнение термодинамического баланса, максимальный КПД, фактор необратимости
Короткий адрес: https://sciup.org/143185571
IDR: 143185571 | УДК: 621.1 | DOI: 10.25209/2079-3316-2026-17-1-85-103
Algorithm and software for calculating thermal cycles for the separation of gas mixtures using thermodynamic criteria
The methodology of optimization thermodynamics has been employed to address the problem of the ultimate capabilities of thermodiffusion separation cycles and to develop a corresponding calculation algorithm and software. Existing programs and algorithms for simulating thermodiffusion cycles did not incorporate thermodynamic criteria. Expressions have been derived for the cycle’s limiting efficiency and its maximum productivity as functions of the composition of the feed mixture, the magnitude, and the temperature of the heating stream. The boundary of the feasible operating region in the productivity–heat consumption plane has been constructed and parameterized. The developed algorithms have been implemented in dedicated software for calculating thermodiffusion cycles.
Текст научной статьи Алгоритм и программное обеспечение для расчета термических циклов разделения газовых смесей с применением термодинамических критериев
Термическое разделение газовых смесей
Оптимизационная термодинамика (термодинамика при конечном времени) рассматривает предельные возможности термодинамических процессов при таких ограничениях ( [1] – [4] и др.) как заданная продолжительность процесса или заданная интенсивность одного из потоков, ограниченная величина коэффициентов тепло- и массообмена, косвенно характеризующих размеры аппарата [5] . Подобного рода ограничения приводят к необходимости решения экстремальной задачи в классе необратимых процессов. Показателем необратимости является прирост или производство энтропии. Оптимальному решению соответствует как правило процесс с минимальной необратимостью.
Методология оптимизационной термодинамики такова:
-
(1 ) Для рассматриваемого процесса записывают уравнения термодинамических балансов (по веществу, энергии и энтропии). В последнее из этих уравнений входит производство энтропии.
-
(2) Решают задачу о минимальном производстве энтропии при тех или иных ограничениях. Решение этой задачи позволяет получить минимальное производство энтропии σ ∗ как функцию потоков и коэффициентов кинетики.
-
(3 ) Подстановка ст * в уравнения термодинамических балансов определяет область реализуемых режимов процесса. Эта область может быть неограниченной (производительность растет монотонно с ростом затрат энергии) или ограничена сверху (начиная с некоторой интенсивности затрат энергии полезный поток уменьшается из за роста необратимости). В последнем случае представляет интерес предельная величина полезного потока.
-
(4 ) Область реализуемости позволяет оценить возможность построения процесса с теми или иными показателями, оценить степень совершенства действующего процесса, наконец, решать задачи, сама постановка которых в рамках обратимой термодинамики не имела смысла.
Производство энтропии в термодинамической системе можно найти двумя способами. В действующей системе производство энтропии можно определить из уравнения энтропийного баланса, зная расходы и удельную энтропию входных и выходных потоков системы. В проектируемой системе производство энтропии может быть рассчитано как произведение внутренних потоков на движущие силы. При этом между потоком и движущей силой существует зависимость, определяющаяся видом кинетики. В простейшем случае поток пропорционален движущей силе с некоторым коэффициентом (тепло- или массообмена) [3]. Оценка производства энтропии, будучи использована в уравнениях термодинамических балансов, позволяет построить зависимость производительности процесса от затрат энергии в классе необратимых процессов.
В первой части работы рассмотрен термический цикл разделения, в котором процессы тепло- и массопереноса от источников к рабочему телу происходят раздельно, во второй — цикл абсорбционно-десорбционный, в котором тепло- и массоперенос происходят одновременно от каждого из источников к рабочему телу.
1. Термодинамический анализ термического цикла
В целом ряде технологических процессов происходит затрата высокопотенциального тепла с температурой T + с целью получения работы разделения [6] . При этом тепловой поток покидает систему с меньшей температурой [7] . Энтропия смеси снижается за счет ее разделения, но повышается при увеличении температуры. Суммарное производство энтропии положительно [8] .
В термическом цикле разделения рисунок 1 жидкое рабочее тело (абсорбент) контактирует с газовой смесью и поглощает один из компонентов, после чего смесь абсорбента с извлекаемым компонентом подается в систему, состоящую из кипятильника и конденсатора, в которых она последовательно испаряется, а затем конденсируется, причем при конденсации извлекаемый компонент остается в газовой фазе и выводится из системы, а конденсат возвращается в абсорбер при температуре близкой к температуре T b кипения абсорбента [9] .
-
1.1. Оценка КПД термического цикла разделения
Сделаем следующие допущения:
-
(1 ) Температура кипения Т ь и мольная теплота парообразования r смеси абсорбента с извлекаемым компонентом не зависят от концентрации x абсорбируемого компонента газовой смеси;
-
(2) Гидродинамика в абсорбере близка к идеальному смешению, а в кипятильнике и конденсаторе температуры горячего и холодного источников T + , T - постоянны;
g a
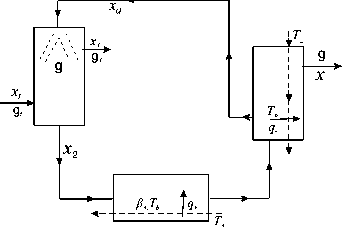
Рисунок 1. Общая структура термического абсорбционного цикла разделения
-
(3) Потери тепла в окружающую среду и затраты энергии на перекачку абсорбента пренебрежимо малы;
-
(4 ) Газовая смесь бинарная, и её состав определяется концентрацией абсорбируемого компонента. Состав газовой смеси x f на входе в систему задан, а температуры потоков на входе и на выходе из системы близки друг к другу;
-
(5 ) Циркулирующий поток на входе в абсорбер не содержит поглощаемого им компонента, а концентрация этого компонента x 0 в целевом потоке равна единице;
-
(6 ) Коэффициент массопереноса K в абсорбере не зависит от расхода абсорбента g a ;
-
(7 ) Температура абсорбента близка к температуре кипения T b , а температуры газа на входе и на выходе системы одинаковы;
-
(8 ) Поток теплообмена пропорционален разности температур, а поток массообмена пропорционален разности термодинамических потенциалов, так что
- (1) qi2 = в(Т1 - T2), gi2 = k(T1 - |2).
При этих допущениях запишем уравнения термодинамических балансов и найдем зависимость производительности цикла от затрат теплоты с учетом необратимости протекающих процессов [10] .
Если считать смесь идеальным раствором, то химический потенциал абсорбируемого компонента имеет форму
-
(2) д = д о (Т,Р ) + RT In x,
где M o (T, P ) — стандартный химический потенциал чистого компонента, R — унивеpсальная газовая постоянная; P — давление насыщенного паpа чистого компонента, R — универсальная газовая постоянная.
Движущая сила процесса изотермического массопереноса между М+ - М-подсистемами с концентрациями компонента х+ и х- равна ---—---. Так как стандартные потенциалы одинаковы, то движущая сила
u = R ln —.
x -
Поток направлен от подсистемы с большей к подсистеме с меньшей концентрацией.
При сделанных допущениях запишем уравнения теpмодинамических балансов для отдельных аппаратов и системы в целом.
Материальный баланс абсорбера при сделанных допущениях приводит к соотношениям для расходов и концентраций потоков на выходе из абсорбера:
xfgf - g g gi = gf - g, g2 = ga + g, x1 = '----S x2 = Ц .
g f - g g a + g
Движущая сила массопереноса в соответствии с (3) , (4)
xi (x f g f - g)q „
U a = R ln = R In —7— ---г— , g = KU a .
x 2 r(g f - g)g
Из неравенства xi > X2 с учетом (4) следует ограничение для расхода циркулирующего потока
g a > g
g f (1 - x f ) g f x f - g
Так как температура рабочего тела (абсорбента) не изменяется за цикл, то из энергетического баланса следует, что
-
(7) q + = q - = q = (g a + g)r = в + (т + - T b ) = в - (Т ь - T - ).
Из последнего равенства вытекает, что коэффициенты теплопроводности, а значит поверхности контактов в испарителе и в конденсаторе нельзя выбирать независимо
в + _ T b — T- e- = T + - T b ■
Согласно условию энтропийного баланса производство энтропии в системе равно разности между энтропией выходящих из системы и входящих в нее потоков [11]. Так что
-
(9) Tq- + (g f - g)s(x i ) - T - g f s(x f ) = ^
Здесь
s(x) = —R^x In x + (1 — x) ln(1 — x)j это молярная энтропия потока.
Производство энтропии равно произведению потоков g, q на движущие силы, причем знаки потоков и движущих сил совпадают. Движущие силы можно исключить через потоки, в этом случае с учетом (8) получим:
g 2 + ■. + = g 2 + q 2 (T + — t- )
K + в + T + T b + в-TbT - K + в + T + T - (T + — T b ) .
-
1.2. Приближенная оценка КПД термического абсорбционного цикла в обратимом процессе
Для получения приближенной оценки обратимого КПД цикла учтем, что производство энтропии и поток g массопереноса в десорбере стремятся к нулю [12] . Нетрудно показать, что при этом отношение g/g f стремится к x f , значение x 1 стремится к нулю, а отношение g/q стремится к значению:
п 0
9 = Ут - — Ут ^
q Xf s(x f )
где s — молярная энтропия потока.
-
1.3. Связь производительности и расхода теплоты в необратимом процессе
К условию (9) следует добавить уравнение кинетики массообмена (5) и уравнение теплового баланса испарителя
g = KR In x 1 = KR ln ( x f g f — g )q , g a + g = q .
x 2 r(g f — g)g r
После замены из последнего условия g a через q, g в неравенстве (6) получим неравенство для потока затрачиваемой теплоты
q > rg
g f - g g f x f - g .
Из условия (12) получим связь между потоком сырья g f , потоком массопереноса (продукта) g и расходом теплоты q
(x f g f — g^q r(g f — д)з
=exp (RK)-
Условие (14) можно разрешить относительно gf . Получим gf (q,g) = glq-^P^. qxf - rg exp g//RK)
Перепишем условие энтропийного баланса (9) с учетом (10) в форме:
g f s(x f ) - (gf - gbsM + K = q( T - - T + ) - T b ( e - T - + e + T + ) .
Так как x 1 зависит от потоков в соответствии с равенством (4) , второе слагаемое в левой части равенства (16) примет вид:
(g f - g) s(x i ) = -R [ (g f x f - д')ln(g f x f - g)
-
(17) + g f (1 - x f )ln(g f (1 - x f ))
- (g f - g) ln(g f - g) .
Уравнение (16) с учетом (17) после исключения g f из (15) связывает переменные g и q и позволяет найти зависимость g(q), а также проследить влияние на нее коэффициентов переноса, состава разделяемой смеси, подсчитать для каждой производительности расход сырья и расход абсорбента.
Правая часть B(q) равенства (16) зависит только от q, причем достигает максимума при
T b (1 / - — - 1 T -+) 2 (1/ в - - - - 1 / 3 + - + )
-
(18) q = q 0
Дальнейшее увеличение теплового потока только ухудшает возможности процесса.
Построить зависимость g(q) можно с помощью следующего алгоритма:
-
(1) Находим q 0 и задаем 0 < q i < q°.
-
(2) Подставляем q i в равенство (15) и получаем g fi (g} = g f (q i ,g).
-
(3) Решаем относительно g уравнение энтропийного баланса (16) , в котором правая часть равна B(q i ) = B i , а левая часть g f = g fi (g). Найденное значение g i представляет собой производительность цикла, соответствующую затратам теплоты q i .
На рисунке 2 (а) показана программная реализаци я1 расчета термического цикла разделения, а далее приводится пример расчёта со скриншотом результата.
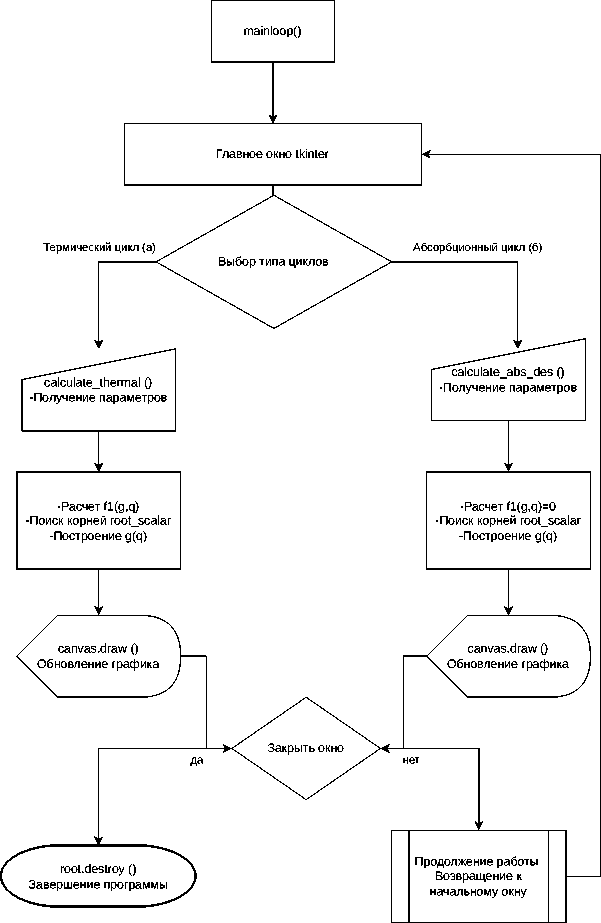
Рисунок 2. Блок-схема программы расчета термического (а) и абсорбционного (б) циклов разделения
Пример 1. Построение зависимости производительности от затраченного тепла в термическом цикле разделения
Зададим следующие значения параметров потоков
R = 8,31 Дж / моль ^ к ; T + = 353 К; T - = 293 К;
T b = 320 К; в + = 33 Вт / к ; в - = 37 Вт / к ;
r = 70 000 Д ж / м О ль ; K =1,7 К • моль 2 / сек • дж ; x f = 0,3 моль / моль ;
и построим зависимость производительности от затрат теплоты (рисунок 3) .
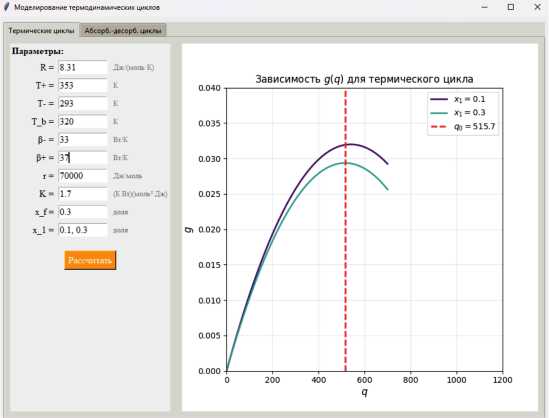
Рисунок 3. Граница реализуемости в плоскости производительность по сырью — затраты теплоты
Построение существенно облегчается, если считать x i константой, большей X f . Эта константа слабо влияет на зависимость g(q ).
С использованием полученных соотношений составлена программа расчета множества реализуемых режимов термического цикла разделения.
2. Абсорбционно - десорбционный цикл (АДЦ)
Расчетная схема процесса однокомпонентной абсорбции-десорбции приведена на рисунке 4.
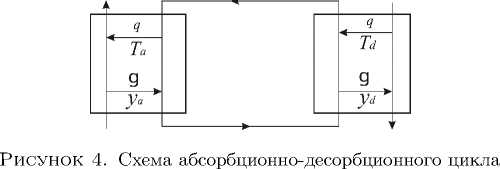
Раствор абсорбента циркулирует по замкнутому контуpу, контактируя в абсорбере с очищаемым газом и насыщаясь при этом абсорбтивом. Затем он pегенерирует в десорбеpе (отдавая поглощенный газ в парогазовую смесь (ПГС)) [13] . Далее ПГС подается в конденсатоp, где пары воды конденсируются, а в газовой фазе остается почти чистый отделяемый компонент. Тепло для процесса подводится в десорбеpе с паpогазовой смесью и пеpедается pаствоpу [14] . Очищаемый газ в абсорбеpе и ПГС в десорбеpе являются источниками , с которыми рабочее тело обменивается теплотой и веществом.
Примем следующие допущения:
-
(1 ) В абсорбере и десорбере поля температур и концентраций однородны (идеальное смешение);
-
(2) Концентрация отделяемого компонента в потоке, выходящем из конденсатора, равна единице, а в потоке абсорбента на входе в абсорбер близка к нулю;
-
(3 ) Температуры газа, поступающего в абсорбер и выходящего из конденсатора, близки друг к другу.
-
(4 ) Разделение в абсорбере и десорбере четкое, так что концентрация абсорбтива в потоке массообмена g и в целевом потоке g 0 равна единице. Следовательно,
-
(19) g f = g/x f , g i = g f (1 - x f ), g o = g,
-
а молярная энтропия выходящих потоков
s i = - R(x i In x i + (1 — x i ) ln(1 — x i )), i = 1, 2
равна нулю.
В силу цикличности изменения состояния рабочего тела потоки тепла q и вещества g в абсорбере и в десорбере одинаковы.
Уравнения кинетики тепло-массообмена имеют форму уравнений
Онсагера:
|
(20) |
1 1 P- P a q = J a IT : - Ta) - “ a It- - t.) = Xd ( ) - ad ( Pd - P + ) d T d T + d T d T + |
|
(21) |
g=-a a ( T - - T a ) + k a ( t- - T a ) = -a d ( T d - T + ) + k d ( T d - T ) ) |
Здесь индекс a соответствует абсорберу, а индекс d — десорберу, потоки, направленные к рабочему телу (циркулирующему раствору), положительны.
Введем обозначения для движущих сил процессов тепло - и массопере-носа в абсорбере и десорбере:
|
11- 1 1 _ T T u aq , T T~ u dq , P - - P a = P d - P + = rri ГГ1 uag , ГТ1 ГГ1 udg . T - T a T d T + |
Потоки связаны с движущими силами и коэффициентами Онсагера как
|
(22) |
q X a u aq a a u ag X d u dq a d u dg , g a a u aq + k a u ag a d u dq + k d u dg . |
Из этой системы уравнений можно выразить движущие силы через
|
потоки: |
X . g + a . q k . q + a . g |
|
(23) |
u a g = X к -a2 , u aq = к X -a2 , λ a k a - α a k a λ a - α a X d P + a d q k d q + a d g u dg = X d k d a d ’ u dq = k d X d - a d . |
Производство энтропии
|
(24) |
a = g(u .g + U dg ) + q(u .q + U dq ). |
Условие энтропийного баланса (разность между потоком энтропии, покидающим систему вместе с потоками теплоты и вещества, и потоком энтропии, поступающим в систему, равна производству энтропии в ней) определяет границу реализуемых режимов в необратимом процессе.
С учетом допущения о четком разделении уравнение энтропийного баланса можно записать через молярную энтропию потока сырья
S f = - R(x f In X f + (1 — X f ) ln(1 — X f ) как
-
(25) q ^1/T - — 1/T +) + -gS f (X f ) = a = g(u ag + U dg ) + q(u aq + U dq ).
Здесь зависимость движущих сил от потоков и коэффициентов тепломассообмена соответствует выражениям (23) .
В обратимом процессе производство энтропии равно нулю, и обратимый КПД цикла равен:
-
(26) П 0 = g/q = ^/T- - 1/ T + ) x f .
s f (x f )
После ввода обозначений _ 1 1
Za X a k a — a a , dd \ d k d — a d ,
A z a k a + z d k d , B z a ^ a + z d A d , C 2( z a a a + z d a d )
связь между производительностью цикла и расходом теплоты примет форму:
-
(27) Dg2 + —Sf (X f ) + Cgq = (1/T - — 1/T + )q — Aq 2 ,
xf где коэффициенты определяются только кинетикой тепло и массопереноса.
Из этого условия следует, что вследствие роста необратимости с ростом теплового потока производительность равна нулю не только при q = 0 но и при q max = 1 /T - — 1 /t + / a . Между этими значениями производительность цикла достигает максимума.
Пример 2. Построение зависимости производительности от затраченного тепла в АДЦ
Зададим начальные значения для потоков:
R =8,31 Дж / моль ^ к ;
Т ь = 320 К;
r = 70 000 Дж / моль ;
a = 40 000 моль • К / сек ;
Т + = 353 К;
в + = 33 Вт / к ;
K =1,7 К • моль 2 / сек ^ Дж ;
k =2 X 10 5 моль 2 • K / сек ^ Дж ;
Т - = 293 К;
в - = 37 Вт / к ;
X f = 0,3 моль / моль ;
А =2 X 10 7 Вт • К.
построим зависимость производительности от затрат теплоты в АДЦ по уравнению (27)
-
(28) Dg 2 + g-Sf (x f ) + Cgq = (1/T - - 1/T + )q - Aq 2 ,
С использованием полученных соотношений составлена программа расчета множества реализуемых режимов абсорбционно днсорбционного цикла разделения, интерфейс которой показан на рисунке 2 (б). Результаты расчетов по ней приведены на рисунке 5.
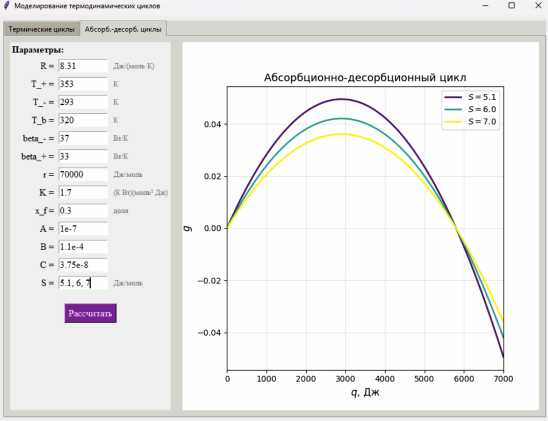
Рисунок 5. Зависимость производительности от затрат теплоты в АДЦ
Заключение
Проведен термодинамический анализ необратимых процессов в термических системах разделения, в которых поток тепла используют для разделения потока газа, с абсорбцией одного из веществ, содержащихся в нем. На основе условий энергетического, материального и энтропийного балансов, построены зависимости производительности циклов от расхода теплоты. Показано, что эти зависимости ограничены сверху и имеют максимум. Получены обратимые оценки КПД подобных процессов. На основании полученных алгоритмов разработано программное обеспечение для проведения расчетов и построения множества достижимых режимов.
Обозначения
T + — температура горячего источника тепла, К;
T - — температура холодного источника тепла, К;
T b — температура кипения абсорбента, К;
x f — концентрация абсорбируемого компонента в смеси, поступающей на разделение, моль/моль;
x a , x 2 — концентрация абсорбируемого компонента в абсорбенте на входе и на выходе из абсорбера, моль/моль;
g — поток массопереноса в абсорбере, моль/с;
g f , g 1 — потоки газовой смеси на входе и на выходе абсорбера, моль/с;
g 0 — поток газа на выходе десорбера, моль/с;
g a — поток абсорбента на входе в абсорбер, моль/с;
µ — химический потенциал, Дж/моль;
R — универсальная газовая постоянная, 8,31 Дж/(моль·К);
β + — коэффициент теплопроводности, Вт/К;
β - — коэффициент теплопроводности, Вт/К;
r — теплота парообразования, Дж/моль;
K — коэффициент теплопередачи, К моль 2 /сек Дж;
α — коэффициент, (моль·К)/сек;
λ — коэффициент, (Вт К);
k — коэффициент теплопередачи, К моль 2 /сек Дж;


