Алгоритм иммунизации против бруцеллеза
Автор: Савицкий Сергей Владимирович, Бронников Василий Сергеевич
Журнал: Вестник Омского государственного аграрного университета @vestnik-omgau
Рубрика: Ветеринарные науки
Статья в выпуске: 3 (19), 2015 года.
Бесплатный доступ
Существующая система профилактики бруцеллеза несовершенна: длителен период дифференциально-диагностических исследований; вакцины имеют остаточную вирулентность. Они могут увеличивать число клинических проявлений бруцеллеза. Вакцинация проводится без учета иммунологического состояния и биохимических характеристик. Целью наших исследований была оптимизация и усовершенствование системы противобруцеллезных мероприятий. Мы предлагаем достигать ее за счет применения разнотипных химических вакцин, контроля эффективности профилактики и с учетом иммунологических и биохимических показателей иммунизируемых животных, а также путем выбора сроков специфической профилактики и возможных предпосылок по переносу этих сроков. Предполагается использование не живых вакцин, как это практикуется сейчас, а химических, созданных на основе нативных антигенов бруцелл и иммуномодулирующей составляющей. Из нескольких десятков существующих запатентованных подобных препаратов отобрали три, наиболее подходящие для усовершенствования системы. У молодняка необходимо использовать вакцину на основе белково-полисахаридного комплекса. Она гипоаллергенна, но высокоагглютиногенна, позволяя контролировать эффективность иммунизации, создавать необходимый в дальнейшем специфический иммунный фон и выявлять гипореактивных и толерантных животных. Не имеет побочных реакций, а высокие серологические угасают полностью, по нашим данным, в течение месяца. У взрослых животных в зависимости от эпизоотологического состояния применяем две вакцины. В стадах с наличием инфекции используют вакцину на основе гликопротеида бруцелл. У здоровых животных она создает иммунитет, не осложненный серологическими реакциями, а у больных и латентно инфицированных провоцирует такие реакции, позволяя выбраковывать заболевших. В стадах без наличия бруцеллезной инфекции предлагаем применять вакцину на основе водонерастворимого комплекса бруцелл и поликатиона. Такая вакцина позволяет контролировать состояние специфического иммунитета, не мешает проведению дифференциальной диагностики, стимулирует неспецифический иммунитет и гораздо дешевле первых двух вариантов.
Бруцеллез, иммунизация, химическая вакцина, белково-полисахаридный комплекс, гликопротеид, агглютиногенность
Короткий адрес: https://sciup.org/142199076
IDR: 142199076 | УДК: 619:616.981.42+636.22/28
The algorithm for immunization against brucellosis
The existing system of brucellosis’ prevention is imperfect. The period of differential diagnostic examinations is long. The vaccines have residual virulence. Its can increase the number of clinical manifestations of brucellosis. The vaccination is carried out without taking into account the state of immunological and biochemical characteristics. The aim of our study was to optimize and improve the system of anti-brucellosis measures. We offer to achieve it by the use of different types of chemical vaccines, monitor the effectiveness of prevention and considering immunological and biochemical parameters of immunized animals and by selecting terms the specific prevention and possible prerequisites for the transfer of these terms. It involves the use of nonliving vaccines as it is practiced now, and chemical based on the native antigens of Brucella and immunomodulatory component. We seized three preparations, which are the most suitable for improvement of the system from existing several dozen patented similar. It is necessary to use a vaccine based on the protein-polysaccharide complex in young animals. It is hypoallergenic, but high agglutinogens that allows to control the effectiveness of immunization, create a necessary specific immune background in the further and identification hyporeactivity and tolerant animals. It hasn’t side reactions, and high serum reactions completely extinguished, according to our data, during the month. We apply two vaccines in adult animals depending on the epidemiological status. We use vaccine based on glycoprotein of Brucella in herds with infection. It creates immunity uncomplicated serological reactions in healthy animals and provoke such reactions in patients latently infected, allowing cast out diseased animals. We suggest using a vaccine based on a water-insoluble complex of brucella and polycation in herds without brucellosis infection. Such vaccine allows to control the status of specific immunity and it doesn’t interfere of the differential diagnosis, stimulates nonspecific immunity, and much cheaper than the first two variants.
Текст научной статьи Алгоритм иммунизации против бруцеллеза
Проблема бруцеллеза актуальна во многих странах мира [1]. Стандартное решение борьбы с инфекционными заболеваниями – установление точного диагноза, выбраковка или лечение заболевших, профилактика здоровых в данном случае не подходит. Сложность диагностических исследований состоит в том, что положительно реагировать при бруцеллезе могут как больные, так и здоровые или иммунизированные. Отрицательный результат бывает как у неконтаминированных, так и у животных с латентной инфекцией. Вносит определенную лепту и способность бруцелл к диссоциации, когда полностью меняется антигенная характеристика микроба или исчезает клеточная стенка. Антигенная мимикрия с наличием общих детерминант у бруцелл и макроорганизма приводит к иммунной анергии, специфической толерантности и аутоиммунитету. Лечение затруднено внутриклеточным паразитированием бруцелл. Антимикробные средства зачастую высокотоксичны или экологически небезопасны. Специфическая профилактика не обеспечивает абсолютного и длительного иммунитета. Вакцины имеют определенную степень вирулентности, провоцируют клинические нарушения, экологически опасны и способны видоизменяться в патогенный вариант [2]. Инактивированные иммуногены зачастую малоэффективны в производственных условиях.
Иммунология находится на достаточно высокой стадии развития: детально изучены механизмы иммунного ответа; выяснена роль отдельных тканей, органов и клеток в защите гомеостаза макроорганизма; определена структура и динамика реактивности иммунитета, необходимая для эффективного ответа на вторжение чужеродного материала. Вакцинология, выделившись в отдельную науку, применив эти достижения, пополнилась несколькими сотнями иммуногенов от значимых инфекционных заболеваний. Уже испытано несколько тысяч
иммуномодулирующих средств и приемов, позволяющих усиливать или ослаблять воздействие специфических вакцин.
Таким образом, предпосылки для создания высокоэффективной защиты от заболевания бруцеллезом созданы.
Многие исследователи, работающие в области борьбы с бруцеллезом, сталкиваются с неравнозначностью применения средств и методов. Так, вакцина, защищающая всех животных в одном эксперименте, оказывается малоэффективной в другом. Определенный комплекс специфических мероприятий, позволяющий в короткие сроки ликвидировать вспышку заболевания в одном случае, малоэффективен в другом и приводит к хронизации процесса.
Целью наших исследований была оптимизация и усовершенствование системы проти-вобруцеллезных мероприятий. В задачи входило выяснение факторов, влияющих на специфический противобруцеллезный иммунитет, и подбор оптимального метода иммунизации. Изучали состав иммуногена и его активность, влияние лекарственных, противопаразитарных и иммунозначимых манипуляций (вакцинация от других инфекций, диагностическая аллергия), возраста и физиологического состояния.
Объекты и методы
Для иммунизации использовали белково-полисахаридный антиген (БПА) [3], глико-протеидный антиген (ГП) [4] и протективный антигенный комплекс [5]. Эксперименты проводили на морских свинках и крупном рогатом скоте. Эффективность иммунизации определяли по устойчивости к заражению 10-кратной заражающей дозой B. abortus 544. Сывороточные антитела выявляли в реакции агглютинации и связывания комплемента.
Результаты исследований
При бруцеллезе эффективность применения специфической вакцины может отличаться в 5 и более раз, от 100%-ной защиты поголовья от заражения вирулентным штаммом до 20%. Даже в строго контролируемых условиях одна и та же вакцина, аналогичная по дозе, способу применения, защищает в одном эксперименте 80% животных, а в другом – 60%.
В наших исследованиях противопаразитарные средства как стимулировали противо-бруцеллезный иммунитет, например, левомизол, так и угнетали, например, ивермек. Влияло на иммуногенность и рН вакцины. А предварительное введение анальгезирующих средств или антибиотиков мешало развитию специфического иммунитета, изменяло его характер, активируя или угнетая антителообразование.
У разных видов животных различается структура иммунной системы, соответственно и реактивность на бруцеллез и противобруцеллезную иммунизацию. Так, морские свинки менее устойчивы к заражению, но вырабатывают большее количество антител, чем крысы и крупный рогатый скот. Внутрикожное введение одного и того же иммуногена по сравнению с подкожным приводит к повышению специфической активности препарата у крыс и неэффективно у крупного рогатого скота и морских свинок.
Нюансы иммунного реагирования существуют и у одного вида. Так, в наших исследованиях крупный рогатый скот разных стад продуцировал в ответ на вакцинацию разный уровень антител как по количеству, так и по длительности выявления (несмотря на то, что вакцина одной и той же серии вводилась в один день в аналогичных условиях у животных одинаковой породы, то есть с одним и тем же генотипом).
В связи с этим считаем необходимым создание алгоритма иммунизации, в котором учитывались бы основные параметры влияния на специфический противобруцеллезный иммунитет.
По нашему мнению, профилактика должна базироваться на использовании инактивированных иммуногенов. Введение химической вакцины, которая состоит из нативного им-мунозначимого антигена и иммуномодулирующей составляющей, активирует в короткие сроки (несколько часов) центральные органы иммунной системы (селезенку, печень). В наших исследованиях это приводило к защите значительной доли одномоментно зараженных экспериментальных животных и всего поголовья через 2–3 недели после иммунизации.
Механизм действия живых вакцин несколько иной. Вводимая сотня миллиардов микробных клеток дессиминирует по всему организму, контактирует с большинством периферических иммунокомпетентных клеток. Если химическую вакцину можно добавлять у гипо-реактивных животных или снижать у гиперреактивных, подбирать иммуноген по оптимальной структуре, использовать при надобности иммуностимуляторы или иммунодепрессанты, то с живой вакциной это невозможно.
Из запатентованных и предложенных к применению инактивированных противобру-целлезных вакцин мы выбрали три.
Одна из них [4] содержит в качестве антигена гликопротеид бруцелл – биополимер, предотвращающий внутриклеточное переваривание микроорганизма. Вакцина на его основе инагглютиногенна и может в первую очередь применяться на взрослом поголовье, так как не осложняет дифференциально диагностических исследований. В нашей работе подобная вакцина на 20% превосходила по эффективности живую, применяемую в производстве. Она способна провоцировать латентно больных и поэтому главная область ее применения – оздоровление инфицированных бруцеллезом стад.
Другая вакцина [3] создана на основе белково-полисахаридного антигена и, в отличие от первой, высокоагглютиногенна, вследствие этого не подходит для взрослых животных, но незаменима у молодняка с низкореактивной, незрелой иммунной системой. Этот иммуноген позволяет контролировать эффективность иммунизации через 15 дней после введения, выявляя гипореактивных, ареактивных и толерантных животных. Она же в большей дозе и в сочетании с иммуностимулятором может служить для исправления иммунных нарушений.
При необходимости иммунизации здоровых животных рекомендуем применять химическую вакцину на основе протективного антигена бруцелл и поликатиона [5]. Ее преимущества в доскональной изученности как в экспериментальных условиях (лабораторные животные, телята, коровы), так и в многолетних производственных условиях. Использовалась при оздоровлении острых и хронических очагов бруцеллеза. С ее применением от рождения до продуктивного животного выращены коровы ОАО «Октябрьское» Черлакского района Омской области. Использовалась для создания иммунного фона у коров Одесского района Омской области. Доказана ее эффективность и безвредность при многолетнем изучении на крупном рогатом скоте Калачинского района Омской области. Одно из ее преимуществ – низкая агглютиногенность. С одной стороны, при исследовании в короткие после введения сроки можно проконтролировать по наличию реакций эффективность проведенной иммунизации, а с другой, реакции невысокие и быстро угасающие не препятствуют специфическим дифференциально-диагностическим исследованиям. Немаловажна и низкая себестоимость препарата.
Во время вспышки бруцеллеза выделили сопутствующую инфекцию, вызванную Y.enterocolitica, провели эксперимент. Установлено: переболев иерсиниозом, снижается возможность выработки противобруцеллезного иммунитета в течение месяца (срок наблюдения), хотя элиминация патогена произошла через 9 дней.
В производственных условиях столкнулись с фактом неэффективной иммунизации против бруцеллеза химической вакциной. Вакцина применялась в арьергарде комплекса иммунологических мероприятий. Проводилась туберкулинизация, затем вакцинации против сибирской язвы и эмкара, потом противопаразитарная обработка. Подобная иммунологическая схема, примененная в экспериментальных условиях, привела к полному отсутствию защиты от бруцеллеза. Длительность такой специфической иммунодепрессии, установленная в другом эксперименте, составила три месяца. Причем нарушения касались как химической, так и живой вакцины, применяющейся в современном производстве.
На другом сельскохозяйственном предприятии длительно выявлялись единичные больные животные. Традиционно иммунизация была приурочена к холодному времени года. Анализ показал низкое содержание белка и витаминов в сыворотке крови, случаи кетоза и на- рушение кислотно-щелочного равновесия. Перенос сроков иммунизации на благоприятный период позволил в комплексе с другими мерами оздоровить хронический очаг бруцеллеза.
Основываясь на вышеперечисленных фактах, мы попытались составить алгоритм специфических иммунных мероприятий, обеспечивающих оптимальную защиту от бруцеллеза.
Алгоритм иммунизации против бруцеллеза: применение инактивированного иммуногена, высокоагглютиногенного у молодняка крупного рогатого скота и низкоагглютиноген-ного у взрослых животных; проведение специфической противобруцеллезной иммунизации не ранее чем через три месяца после иммунозначимых событий:
– диагностики, связанной с аллергическими исследованиями, пункцией, провокацией,
-
– противопаразитарных обработок,
-
– иных инфекционных заболеваний,
-
– иммунизаций от других инфекций,
-
– наркоза и лечения обезболивающими, антимикробными препаратами,
-
– патофизиологического состояния.
Вакцина вводится в период биохимического оптимума, когда содержание в сыворотке белка, витаминов, микроэлементов, кислотно-щелочное равновесие соответствуют норме.
Сроки вакцинации должны переносится из-за экстремальных физических (температура окружающей среды, влажность) и химических факторов.
Контроль эффективности иммунизации проводят через 15 дней после введения вакцины по специфическим серологическим реакциям. Их отсутствие свидетельствует о гипоэргии иммунной системы и требует дополнительного специфического стимула высокоактивными препаратами с коррекцией Т- и В-дефектов иммуномодуляторами.
Оптимальный срок иммунизации против бруцеллеза устанавливают по наибольшему сочетанию благоприятных факторов (рисунок). Так, два иммунных оптимума с марта по середину мая соответствуют трехмесячной удаленности от иммунологических манипуляций, проводимых в начале ноября и середине мая. Биохимический оптимум с июня по ноябрь соответствует нормализации обменных процессов, а физиологический – наилучшему общему состоянию у взрослых животных или возрасту молодняка, достигшего сроков допустимой иммунизации. Неблагоприятные факторы отмечены точками: с середины июня по середину октября отсутствуют. Совпадение благоприятных факторов с середины августа до середины октября указывает на потенциальную эффективность иммунизации против бруцеллеза в этот период.
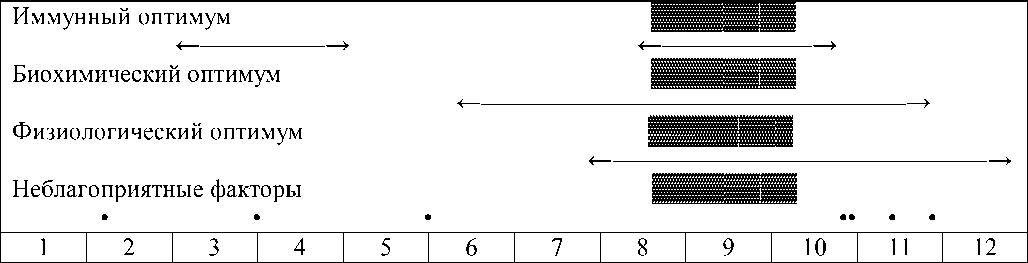
▓ – оптимальное сочетание факторов, благоприятные сроки для иммунизации против бруцеллеза.
←―→ – показатели в норме.
(1–12) – месяцы (январь – декабрь).
Пример расчетной таблицы оптимальных сроков иммунизации против бруцеллеза
Выводы
Таким образом, бруцеллез крупного рогатого скота – актуальная и нерешенная проблема. Иммунизация против этого заболевания без учета состояния иммунной системы и биохимических критериев малоэффективна. Для усовершенствования специфической профилактики бруцеллеза необходимо использовать разнотипные химические вакцины в оптимальные для иммунизации сроки. Контроль эффективности необходимо проводить через 15 дней после введения препарата.
Список литературы Алгоритм иммунизации против бруцеллеза
- Brucellosis 2011. International Research Conference (Including the 64th Annual Brucellosis Research Conference) Buenos Aires -Argentina September 21-23, 2011. -140 р.
- Предпат. № 17648 Республика Казахстан. Способ повышения вирулентности бруцелл/Воробьёв А.Л.; опубл. 15.08.2006, Бюл. № 8. -2 с.
- Драновская, Е.А. Изучение иммуногенных свойств бруцеллезного протективного антигена при ревакцинации/Е.А. Драновская, П.А. Вершилова//ЖМЭИ. -1976. -№ 12. -С. 94-97.
- Григорьева, Г.И. Факторы патогенности как протективные антигены при конструировании вакцин/Г.И. Григорьева, П.Е. Игнатов//Сельскохозяйственная биология. -1987. -№ 12. -С. 100-104.
- Пат. № 2398597 Российская Федерация, МПК А61К39/10 (2006.01). Способ получения протективного антигенного комплекса бруцелл/Бронников В.С. . -№ 2008150696/10; заявл. 22.12.2008; опубл. 10.09.2010.


