Алгоритм персонализированной терапии больных алкоголизмом с коморбидными нарушениями детоксицирующей функции печени и когнитивными расстройствами
Автор: Кисель Наталья Игоревна, Бедарев Роман Игоревич, Мандель Анна Исаевна, Шушпанова Тамара Владимировна, Мазурова Лариса Васильевна, Новожеева Татьяна Петровна, Солонский Анатолий Владимирович, Гарганеева Наталья Петровна, Бурдовицина Татьяна Григорьевна, Гончикова Ирина Александровна, Попова Тамара Александровна
Журнал: Сибирский вестник психиатрии и наркологии @svpin
Рубрика: Клиническая наркология
Статья в выпуске: 4 (117), 2022 года.
Бесплатный доступ
Актуальность. Нарушение метаболических процессов печени в результате воздействия алкогольной интоксикации снижает когнитивное функционирование и индуцирует когнитивные расстройства. С выраженностью метаболических расстройств связана тяжесть осложнений алкоголизма. У больных алкоголизмом с коморбидным поражением печени признаки когнитивных нарушений наблюдаются уже на ранних стадиях заболевания и сопровождаются расстройствами внимания, памяти, восприятия, что в дальнейшем зачастую приводит к социальной дезадаптации и инвалидизации. Цель. Выявление взаимосвязи показателей нарушения детоксицирующей функции печени и когнитивных расстройств у больных с алкогольной зависимостью для разработки алгоритма персонализированной терапии. Материалы и методы. На базе отделения аддиктивных состояний НИИ психического здоровья сформирована исследовательская выборка (n=40) из лиц мужского пола, средний возраст которых составил 42,4±11,9 года, с диагностированными по МКБ-10 психическими расстройствами и расстройствами поведения, связанными с употреблением алкоголя (F10), нарушениями детоксицирующей функции печени и когнитивными расстройствами. Для оценки динамики психического состояния у пациентов с алкогольной зависимостью дважды (припоступлении и после комплексной терапии) проведено психологическое тестирование с использованием шкалы тревоги Гамильтона. Скрининг когнитивных нарушений осуществляли по Монреальской когнитивной шкале(MoCA), оценку кратковременной и долговременной памяти - по психодиагностическим тестам (Пиктограммы, Заучивание 10 слов). Обсессивно-компульсивная шкала (ОКШ) влечения к алкоголю использовалась для самооценки идеаторных проявлений отношения к алкоголю. Исследовались в динамике биохимические показатели крови (АЛТ, АСТ, общий билирубин, прямой и непрямой билирубин, холестерин, щелочная фосфатаза). Результаты. На фоне проводимой медикаментозной терапии произошел регресс обсессивно-компульсивного влечения к алкоголю, что подтверждается снижением среднего балла по ОКШ с 36,5±4,2 до 3,47±2,03 балла. Нормализовались биохимические показатели крови (АЛТ, АСТ, общий билирубин, холестерин). Улучшились когнитивные способности, что обосновывается повышением суммарного количества баллов по MoCA (22,7±4,3 балла - на момент поступления,26,5±1,6 балла - после терапии). Выводы. У пациентов с тяжелым течением алкогольной зависимости на фоне поражения печени, о чем свидетельствовало 3-кратное и более увеличение показателей АЛТ и АСТ в сыворотке крови по сравнению с нормой, выявлены низкие показатели кратковременной и долговременной памяти, выраженные нарушения зрительно-конструктивного праксиса и возможностей, концентрации внимания, что подтверждается суммарными (15,9±1,3 балла) значениями по Монреальской Шкале оценки когнитивных функций. Восстановление или компенсация детоксицирующей функции печени и улучшение когнитивного потенциала за счет примененияв комбинированной схеме терапии препаратов, сочетающих гепатопротекторный и нейропротекторный эффекты,становится благоприятным фактором для последующих этапов реабилитации пациентов и профилактики рецидивов алкогольной зависимости.
Алкогольная зависимость, когнитивные расстройства, метаболические процессы, детоксицирующая функция печени, персонализированная терапия
Короткий адрес: https://sciup.org/142237368
IDR: 142237368 | УДК: 616.89-008.441.13:616.36-008:616.89-008.46:616-085 | DOI: 10.26617/1810-3111-2022-4(117)-33-43
Algorithm for personalized therapy of patients with alcoholism with comorbid disorders of the detoxifying function of the liver and cognitive disorders
Background. Disfunctions of the metabolic processes of the liver as a result of exposure to alcohol intoxication reduce cognitive functioning and induce cognitive disorders. The severity of complications of alcoholism is associated with the severity of metabolic disorders. In patients with alcoholism with comorbid liver damage, signs of cognitive impairment are observed already in the early stages of the disease and are accompanied by disorders of attention, memory, perception, which in the future often lead to social maladaptation and disability. Objective. Identification of the relationship between indicators of disturbance of the detoxifying function of the liver and cognitive disorders in patients with alcohol dependence in order to develop an algorithm for personalized therapy. Materials and Methods. Based on the Addictive State Department of Mental Health Research Institute, the study sample (n=40) was formed of males, whose mean age was 42.4±11.9 years, with mental and behavioral disorders diagnosed according to ICD-10, associated with alcohol use (F10), impaired detoxifying liver function and cognitive impairment. To assess the dynamics of the mental state in patients with alcohol dependence, psychological testing was carried out twice (at admission and after complex therapy) using the Hamilton anxiety scale. Cognitive impairment was screened using the Montreal Cognitive Scale (MoCA), short-term and long-term memory was assessed using psychodiagnostic tests (Pictograms, Learning 10 words). The obsessive-compulsive scale (OCS) of craving for alcohol was used for self-assessment of ideational manifestations of attitudes towards alcohol. The dynamics of blood biochemical parameters (ALT, AST, total bilirubin, direct and indirect bilirubin, cholesterol, alkaline phosphatase) were studied in dynamics. Results. Against the background of ongoing drug therapy, there was a regression of obsessive-compulsive craving for alcohol, which was confirmed by a decrease in the mean score for OCS from 36.5±4.2 to 3.47±2.03 points. Blood biochemical parameters (ALT, AST, total bilirubin, cholesterol) normalized. Cognitive abilities improved, which was justified by an increase in the total number of MoCA scores (22.7±4.3 points at the time of admission, 26.5±1.6 points after therapy). Findings. In patients with severe alcohol dependence on the background of liver damage, as evidenced by a 3-fold or more increase in serum ALT and mood disorders AST compared with the norm, low indicators of short-term and long-term memory, severe impairment of visual-constructive praxis and abilities, concentration of attention, which was confirmed by the total (15.9±1.3 points) values according to the Montreal Cognitive Assessment Scale. Restoration or compensation of the detoxifying function of the liver and improvement of cognitive potential due to the use of drugs combining hepatoprotective and neuroprotective effects in a combined therapy regimen becomes a favorable factor for subsequent stages of patient rehabilitation and prevention of relapses of alcohol dependence.
Текст научной статьи Алгоритм персонализированной терапии больных алкоголизмом с коморбидными нарушениями детоксицирующей функции печени и когнитивными расстройствами
Проблема употребления алкоголя с вредными последствиями для здоровья актуальна для России в целом и регионов Сибири и Дальнего Восток в частности [1, 2, 3]. В странах Европы, кроме Ирландии и Великобритании, в первые месяцы пандемии COVID-19 потребление алкоголя хотя и снизилось, но это не коснулось населения с низким и средним доходами, что авторы объясняют усилением дистресса и более низкой доступностью алкоголя [4]. В серии опубликованных в Lancet отчетов приводятся доказательства масштабных усилий общественного здравоохранения для снижения вредного воздействия алкоголя и резюмируется эффективность и рентабельность вмешательств [5]. Когнитивные расстройства при алкогольной зависимости (АЗ) связаны с нарушением метаболических звеньев фармакометаболизирующей функции печени [6]. Авторы 62 зарубежных работах оценивали когнитивную дисфункцию при алкоголизме: коэффициент интеллекта, беглость речи/язык, скорость обработки информации, рабочая память, внимание, решение проблем и исполнительные функции, торможение и импульсивность, вербальное обучение, вербальная память, зрительное обучение, зрительная память, зрительно-пространственные способности. С позиций гипотезы диффузного мозга показано, что когнитивная дисфункция может сохраняться в среднем 1 год после детоксикации от алкоголя [7]. Специфические мнестико-интеллектуальные нарушения (абстрактного мышления, концептуальных возможностей, памяти) имеют место у 45-70% больных АЗ. Мнестические расстройства в виде нарушений оперативной и кратковременной памяти, снижения активного внимания проявляются на ранних стадиях алкоголизма. В этом ракурсе представляют интерес исследования обратимости когнитивных нарушений при АЗ [8, 9].
Нарушения детоксицирующей функции печени, прямое токсическое влияние алкоголя и его метаболитов, рост проницаемости гематоэнцефалического барьера относят к факторам металкогольного поражения мозга. Серьезным осложнением алкогольной болезни печени является когнитивная дисфункция у пациентов с хронической алкоголизацией. У больных алкоголизмом поврежденная печень не может эффективно удалять из крови нейротоксичные метаболиты, такие как аммиак, марганец и др.
[10, 11, 12, 13, 14]. В результате эти молекулы могут проникать в мозг, оказывая множество токсических повреждающих эффектов, влияющих на нормальную активность нейротрансмиттеров, нарушают когнитивные и моторные функции и вызывают структурные изменения в ЦНС. C целью предотвращения или лечения больных алкоголизмом с метаболическими нарушениями печеночной функции в настоящее время создаются новые подходы к изучению алгоритма персонализированной терапии больных алкоголизмом с коморбидными нарушениями детоксицирующей функции печени и когнитивными расстройствами.
При алкоголизме с сопутствующими патологиями более выраженная потеря нейронов затрагивает широкий спектр анатомических областей, особенно подкорковые ядра. Существуют доказательства связи дефицита тиамина и последствий заболевания печени с патогенезом связанного с алкоголем повреждения головного мозга. Частая встречаемость других факторов (расстройства настроения) может влиять на исследования патологии головного мозга и должна учитываться при изучении нейропатологии алкоголизма [15].
Посредством нарушения метаболической и детоксикационной функций печени осуществляется негативное воздействие алкогольной интоксикации на когнитивные функции, в связи с чем у больных АЗ с коморбидным поражением печени наблюдаются признаки печеночной энцефалопатии (ПЭ). В клинической практике трудной задачей во многих случаях оказывается дифференциальная диагностика ПЭ и когнитивных нарушений, развивающихся при злоупотреблении алкоголем. При минимальной ПЭ пациенты могут иметь нормальные способности в области памяти, языка, моторных навыков, однако из-за нарушений постоянного внимания у них отмечается задержка времени в выборе реакции. Такие пациенты демонстрируют изменения по результатам психометрических и нейрофизиологических испытаний. У пациентов с легкой и среднетяжелой ПЭ по итогам исследований психического статуса снижены показатели краткосрочной памяти, концентрации внимания [16, 17]. Создание эффективного комплекса терапии у больных с нарушениями детоксицирующей функции печени и когнитивными расстройствами при АЗ является актуальной задачей [18, 19].
ЦЕЛЬ ИССЛЕДОВАНИЯ
Выявление взаимосвязи показателей нарушения детоксицирующей функции печени и когнитивных расстройств у больных с алкогольной зависимостью для разработки алгоритма персонализированной терапии.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование выполнено на базе отделения аддиктивных состояний НИИ психического здоровья Томского НИМЦ. Из числа обратившихся была сформирована исследовательская выборка (n=40) пациентов мужского пола в возрасте от 21 до 62 лет, средний возраст которых составил 42,4±11,9 года, с диагностированными по МКБ-10 психическими расстройствами и расстройствами поведения, связанными с употреблением алкоголя (F10), нарушениями детоксицирующей функции печени и когнитивными расстройствами. У всех пациентов имелись проявления алкогольного абстинентного синдрома (ААС) разной выраженности в виде вегетативных, аффективных, диссомнических, астенических, когнитивных нарушений. Возраст появления ААС составлял 37,8±10,4 года, толерантность к алкоголю на момент обследования ‒ 976,6±413,9 мл крепких (40°) напитков. У большинства (n=34, 85%) пациентов в клинической картине АЗ выявлены амнестические формы опьянения по типу алкогольных палимпсестов, их манифестация произошла в среднем в 39,7±9,4 года. Обнаружено преобладание (n=26, 65%) пациентов с повторными госпитализациями (2 и более раз).
Для оценки динамики психического состояния и когнитивных нарушений использовали психодиагностическое тестирование по шкале тревоги Гамильтона, Монреальской шкале оценки когнитивных функций (MoCA), обсессивнокомпульсивной шкале (ОКШ) оценки влечения к алкоголю. Исследование когнитивных функций включало оценку: 1) кратковременной памяти при динамическом предъявлении 10 слов, 2) возможности памяти при воспроизведении 10 слов через 1 час, 3) долговременной памяти по зрительным опорам с помощью теста Пиктограмма при воспроизведении слов по рисункам пиктограммы через 1 час. Когнитивные функции исследовали дважды: при поступлении (начало лечения) и после комплекса медикаментозной, физио- и психотерапии (окончание лечения).
По методике Заучивание 10 слов оценивают состояние памяти, степень утомляемости и активности внимания (Лурия А.Р., 1962; Рубинштейн С.Я., 1970). Методика использует параметры: 1) число слов, воспроизведенных в третьем предъявлении (показатель запоминания и активного внимания); 2) количество слов при воспроизведении спустя 1 час (показатель собственно памяти). Дополнительную информацию дают сведения о наличии лишних слов, вводимых пациентами при воспроизведении слов и «застревании» на них во время последующих повторов, что может свидетельствовать о наличии органических поражений головного мозга или отражать индивидуально значимую личностную нагрузку, а искажения и ошибки при воспроизведении слов могут задавать новый смысл стандартным понятиям.
Метод пиктограмм использовали при исследовании особенностей опосредованного запоминания и его продуктивности, характера мыслительной деятельности, уровня сформирования понятийного мышления, долговременной памяти по зрительным опорам через 1 час. Когнитивные функции исследовались дважды: при поступлении и после проведения комплекса медикаментозной, физио- и психотерапии.
По Обсессивно-компульсивной шкале влечения к алкоголю оценку проводили в трех точках (3-й, 10-й и 21-й дни нахождения в стационаре). Шкала предназначена для самооценки идеатор-ных проявлений за последнюю неделю. Пункты 1-6 оценивают выраженность проявления первичного влечения к алкоголю, пункты 7-14 – выраженность вторичного ПВА, возникающего впроцессе употребления алкоголя, с оценкой того, насколько они затрудняли повседневную деятельность, вызывали стресс и беспокойство, сколько усилий приходилось прилагать для того, чтобы противостоять им. Суммарный балл имеет значение в интервале от 0 до 56.
Для определения степени поражения печени, тяжести нарушения детоксицирующей функции печени использовали данные УЗИ органов брюшной полости, биохимические показатели крови, общий анализ крови.
Статистическую обработку данных проводили с применением пакета стандартных прикладных программ Statistica for Windows (V. 10.0). Количественные данные представлены в виде M±SD (M – среднее арифметическое, SD – стандартное отклонение). Соответствие нормальности распределения проводили по критерию Шапиро-Уилка. В случае отличного от нормального распределения количественные данные представлены в виде медианы, 25 и 75 квартилей. Сравнение показателей до и после терапии проводили по критерию Вилкоксона t (сравнение связанных групп данных). Статистически значимыми считали различия при р<0,05.
Персонализированный алгоритм комплекс- печени, улучшение когнитивных способностей, ного лечения, проводимого в рамках исследо- снижение влечения к алкоголю, коррекцию кования, направлен на восстановление функций морбидных психических расстройств (табл. 1).
Т а б л и ц а 1. Схема медикаментозной терапии больных с алкогольной зависимостью, нарушениями детоксицирующей функции печени и когнитивными расстройствами
|
Вид терапии |
Класс препаратов |
Лекарственные препараты, дозы, схемы применения |
|
Дезинтоксикационная терапия (4-6 дней) |
Плазмозамещающие растворы |
Изотонический раствор натрия хлорида 0,9% до 400 мл/сутки в/в капельно |
|
Витаминтерапия (20 дней) |
Витамины |
Раствор тиамина бромида 5% по 50-150 мг/сутки в/м. Раствор пиридоксина гидрохлорида 5% по 50-150 мг/сут в/м |
|
Гепатопротекторы (5 дней в/в применения или 20 дней внутрь) |
Аминокислоты и их производные. Гипоазотеми-ческие препараты. Метаболические препараты. Гепатопротекторы |
Гептрал, гептор 400 мг в/в капельно в 200 мл NaCl 0,9%. Самеликс 400 мг в/в. Орнилатекс 10,0 в/в капельно в 200 мл NaCl 0,9%. Ремаксол 400 мл в/в капельно. Карсил по 1 драже 3 раза в день |
|
Психофармакотерапия (курс 21 день) |
Транквилизаторы (от 3 до 15 дней) |
Сибазон по 10-40 мг/сут в/в капельно в 200 мл NaCl 0,9%. Сомнол по 7,5 мг на ночь. Элзепам до 4 мг/сут. Фензитат до 4 мг/сут |
|
Нейролептики (от 3 до 15 дней) |
Тералиджен до 10 мг/сут. Хлопротиксен до 30 мг/сут. Тиаприд до 200 мг/сут |
|
|
Вегетостабилизаторы (от 10 до 20 дней) |
Грандаксин до 150 мг/сут |
|
|
Антиконвульсанты, нормотимики (21 день) |
Карбамазепин до 600 мг/сут. Финлепсин до 400 мг/сут |
|
|
Ноотропные средства (от 5 до 21 дней) |
Пирацетам 5,0 в/в струйно до 1200 мг/сут. Глицин до 600 мг/сут. Пантогам до 1000 мг/сут. Пикамилон до 150 мг/сут |
|
|
Антидепрессанты (от 3 до 21 дней) |
Эсциталопрам 10 мг/сут. Бринтелликс 10мг/сут. Вальдоксан 25 мг/сут. Флувоксамин 100 мг/сут. Флуоксетин 20 мг/сут. Рексетин 30 мг/сут |
|
|
Метаболическая терапия (от 5 до 10 дней) |
Препараты с нейропро-текивным действие |
Мексидол 5%-2,0 в/м. Кортексин 10 мг/сут. Актовегин 5,0 в/в капельно в 100 мл NaCl 0,9% |
|
Сенсибилизирующая к алкоголю терапия (15-20 дней) |
Препараты для патогенетической терапии алкоголизма |
Мидзо до 30 капель/сутки. Эспераль 500 мг/сут. Тетурам 150 мг/сут |
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
По результатам лабораторного исследования на рисунке 1 представлены показатели функции печени у больных алкогольной зависимостью с коморбидными нарушениями детоксицирующей функции печени и когнитивными расстройствами в двух точках: до и после терапии.
Практически у всех (n=39, 97,5%) пациентов в сыворотке крови повышен показатель аланинаминотрансферазы (АЛТ) ‒ 72,5±6,4 ед/л (норма до 35 ед/л). У большинства (n=25, 65%) обследованных повышен уровень аспартатаминотрансферазы (АСТ) ‒ 80,5±7,6 ед/л (при норме до 42 ед/л). Более чем у половины (n=22, 55%) пациентов уровень общего билирубина составил 27,8±2,6 мкмоль/л (при норме от 8,5 до 20,5 мкмоль/л). Средние показатели прямого и непрямого билирубина в крови обследованных так же превышали нормативные значения: 6,5±0,8 и 22,2±2,6 мкмоль/л соответственно (при норме от 0 до 5,1 и от 6,4 до 14,4).
У большинства (n=36, 90,0%) пациентов после курса медикаментозной терапии биохимические показатели нормализовались: АЛТ ‒ 28,5±2,5, АСТ ‒ 33,1±3,3, общий билирубин ‒ 11,3±0,8, прямой билирубин ‒ 2,4±0,3, непрямой билирубин ‒ 8,9±0,7, ЩФ ‒ 61,3±4,9, общий холестерин ‒ 4,6±0,2, что подтверждается их статистически значимым (p=0,021) снижением в сравнении с таковыми при поступлении. Повторное исследование АЛТ у незначительной части (n=4, 10,0%) пациентов показало по-прежнему высокие значения: 63,4 ед/л, 48,9 ед/л, 52,3 ед/л, 68,3 ед/л соответственно.
Таким образом, исследования маркёров функции печени у обследованных пациентов до проведения курса терапии и после его завершения с использованием гепатотропных препаратов, стимулирующих функцию печени, обнаружили, что трансаминазы АЛТ и АСТ, а также показатели билирубина снижались, приближаясь к нормативному уровню. Т.е. прием гепато- протекторов восстанавливал функцию печени, что способствовало повышению её детоксикационной активности. Однако уровни щелочной фосфатазы, отражающей нарушение / воспаление поджелудочной железы, не изменились, общий уровень холестерина не превышал таковой в норме, что может объясняться алиментарным снижением поступления калорийной пищи в связи с периодом алкоголизации пациентов до поступления в стационар.
Биохимические исследования показателей функции печени в сыворотке крови у больных алкоголизмом
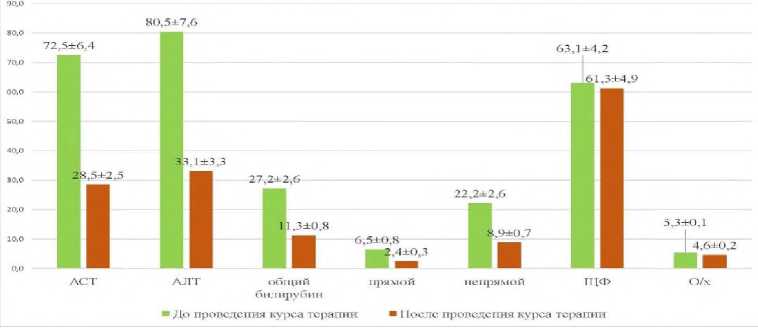
Рисунок 1. Распределение показателей функции печени в сыворотке крови у больных алкоголизмом до и после проведения курса терапии (p=0,021)
Результаты УЗИ-диагностики печени и поджелудочной железы обследуемых пациентов с алкогольной зависимостью приведены в таблице 2. По совокупности биохимических показателей, клинической картины, дополнительных методов обследования у большинства (n=26, 65,0%) пациентов диагностировали реактивный гепатит в результате употребления алкоголя.
Таблица 2. Распределение результатов ультразвуковой диагностики печени и поджелудочной железы у пациентов с алкогольной зависимостью
|
Диагноз |
Абс. |
% |
|
Гепатомегалия |
32 |
80,0 |
|
Признаки жирового гепатоза |
24 |
60,0 |
|
Диффузные изменения паренхимы печени |
26 |
65,0 |
|
Диффузные изменения поджелудочной железы |
26 |
65,0 |
|
Признаки липоматоза поджелудочной железы |
18 |
45,0 |
|
Признаки хронического холецистита |
40 |
100,0 |
По ОКШ средний общий (36,5±4,2) балл на момент поступления в стационар соответствовал выраженному влечению к алкоголю. После курса медикаментозной терапии данный показатель снизился до 3,47±2,03. При поступлении преобладали (n=37, 92,5%) пациенты с зафиксированным очень сильно выраженным влечением к алкоголю (общий балл >29), у остальных (n=3, 7,5%) установлено сильное влечение к алкоголю (21-28 баллов). К 21-му дню пребы- вания в стационаре у 3 (7,5%) пациентов сохранялось незначительное (7-13 баллов) влечение, а у большей (n=37, 92,5%) части пациентов признаки влечения к приему алкоголя (<6 баллов) практически нивелировались.
После медикаментозного лечения у большинства пациентов редуцировались или снизились тревожные переживания и эмоциональный дискомфорт из-за переживания неудовлетворенности разными сферами деятельности, что подтверждалось результатами повторного исследования по шкале тревоги Гамильтона (9,1±3 балла). В то же время у некоторых пациентов при выписке сохранялись остаточные проявления неудовольствия и озабоченности, беспокойства и напряженности из-за возможного срыва и возобновления алкоголизации, переживания по поводу будущего.
По результатам психодиагностического обследования с помощью метода 10 слов у большинства (n=28, 70,0%) пациентов при поступлении выявлено снижение кратковременной памяти (непосредственное воспроизведение). По итогам серии предъявлений 10 слов при последнем предъявлении (отсроченное воспроизведение) объем восстановленных в памяти слов возрос до 7 (4, 5, 6, 6, 7 слов), через 1 час ‒ 4 слова. По окончании лечения у трети (n=13, 32,5%) пациентов выявлено улучшение памяти: в результате предъявления 10 слов в динамике респонденты воспроизводили 10 слов, через 1 час ‒ 8. С меньшей (n=7, 17,5% и n=4, 10%) частотой зафиксировано воспроизведение 9 и 7, 8 и 7 слов соответственно.
По данным исследования опосредованной памяти методом Пиктограмма у большинства (n=30, 75,0%) пациентов при поступлении была снижена способность запоминания (воспроизведение от 8 до 10 понятий из 15 предложенных). По окончании терапии преобладали (n=20, 66,6%) пациенты, продемонстрировавшие улучшение памяти, в виде способности запоминать больший объем информации (повторение от 13 до 15 понятий из 15 заданных).
Оценка выраженности когнитивных нарушений по Монреальской шкале включала зрительное и речеслуховое восприятие, внимание, беглость (в том числе темп и ритм) речи, правильность употребления понятий, ориентации. У большинства (n=34, 80%) пациентов при поступлении были снижены конструктивные навыки: дискоординация двигательной (моторной) сферы, неточность движений при воспроизведении букв, цифр, геометрических фигур, стрелок. По окончании лечения пациенты с полным восстановлением (n=30, 75,0%) моторно-двигательного функционирования преобладали по сравнению с пациентами с частичным восстановлением (n=4, 10,0%).
На момент поступления в стационар при воспроизведении фраз, арифметическом счете и реакции на звук у подавляющей части (n=33, 82,5%) пациентов выявлено снижение концентрации внимания. В ходе лечения продуктивность внимания была восстановлена полностью (n=27, 67,5%) или частично (n=6, 15%). Сниженное владение беглостью речи (n=24, 60%) было скорректировано полностью (n=22, 55%) либо частично (n=2, 5%). Полностью устранены нарушения ориентации во времени, выявленные у каждого пятого пациента (n=8, 20%).
Таким образом, у большинства пациентов после комплексной терапии обнаружено статистически значимое (p=0,00033) улучшение когнитивных функций, что подтверждается суммарным количеством баллов по тесту MoCA: 22,7±4,3 ‒ до лечения, 26,5±1,6 ‒ после лечения (сравнение связанных групп данных по критерию Вилкоксона t).
Исследование связи между нарушением детоксицирующей функции печени и снижением когнитивного функционирования у больных алкоголизмом показало, что у каждого четвертого пациента (n=9, 22,5%) с 3-кратным и более повышением показателей АСТ и АЛТ по сравнению с нормой (42 и 35 ед/л) выявлены низкие показатели кратковременной и долговременной памяти, выраженные нарушения зрительноконструктивной деятельности, ограничение возможностей активной деятельности, снижение способностей к концентрации внимания. Такой вывод подтверждается статистически значимым (p=0,00021) различием суммарных значений по данным сравнительной оценки когнитивных функций по Шкале MoCA между пациентами с 3-кратным и более повышением и пациентами с менее чем 3-кратным увеличением показателей АСТ и АЛТ: 15,9±1,3 балла и 22,7±4,3 балла (по критерию Вилкоксона t).
В результате терапии обнаружено улучшение когнитивных функции у пациентов с алкогольной зависимостью и коморбидным нарушением детоксицирующей функции печени. Прием медикаментозной терапии не усугублял течение сопутствующей патологии и не вызывал нежелательных реакций в ответ на прием лекарственных средств (табл. 3). Эффективность терапии оценивалась с учетом количества пациентов, у которых на фоне персонализированных медикаментозных назначений нормализовались показатели когнитивных функций (в % от общего числа больных с когнитивными нарушениями).
Т а б л и ц а 3. Эффективность комплексной терапии больных алкоголизмом с нарушением детоксицирующей функции печени и когнитивными расстройствами
|
Когнитивные нарушение |
Наличие нарушений |
Улучшение значительное |
Эффективность терапии (%) |
|
|
3-й день |
21-й день |
21-й день |
||
|
КП |
28 |
2 |
26 |
92,8% |
|
ДП |
30 |
4 |
26 |
86,6% |
|
ЗКН |
34 |
4 |
30 |
88,2% |
|
В |
33 |
6 |
27 |
81,8% |
|
Р |
24 |
2 |
22 |
91,6% |
|
О |
4 |
0 |
4 |
100,0% |
П р и м е ч а н и е. В 1-м столбце приведены обозначения: КП – кратковременная память, ДП – долговременная память, ЗКН – зрительно-конструктивные навыки, В – внимание, Р – речь, О – ориентация.
ЗАКЛЮЧЕНИЕ
У больных АЗ с коморбидным нарушением детоксицирующей функции печени (наличие 3-кратного и более повышения показателей АЛТ и АСТ в сравнении с нормой) зарегистрированы низкие показатели кратковременной и долговременной памяти, нарушения зрительноконструктивного праксиса и пространственноориентированных возможностей, нарушения концентрации внимания, что подтверждается суммарными значениями по данным Монреальской шкалы оценки когнитивных функций. Достигнутый в процессе реабилитации регресс когнитивных нарушений, подтверждённый субъективными и объективными психометрическими шкалами, демонстрирует эффективность алгоритма персонализированной терапии с использованием гепатопротекторных, метаболических и ноотропных лекарственных средств, в совокупности способствующих восстановлению или стимуляции детоксицирующей функции печени у пациентов с АЗ. Восстановление детоксицирующей функции печени и когнитивного потенциала становится благоприятным фактором для дальнейшей реабилитации пациентов и профилактики рецидивов алкогольной зависимости. Предложенный нами алгоритм персонализированной терапии больных АЗ с коморбидными нарушениями детоксицирующей функции печени и когнитивными расстройствами повышает эффективность лечения за счет включения в комбинированную схему терапии препаратов с сочетанными нейропротекторным и гепато-протекторным эффектами, стимулирующих основные метаболические звенья функционирования гепатобилиарного тракта.
Список литературы Алгоритм персонализированной терапии больных алкоголизмом с коморбидными нарушениями детоксицирующей функции печени и когнитивными расстройствами
- Социально значимые заболевания населения России в 2021 году. Статистические материалы. М., 2021. 73 с. Socially significant diseases of the population of Russia in 2021. Statistical materials. Moscow, 2021:73 (in Russian).
- Kilian C, Rehm J, Allebeck P, Braddick F, Gual A, Barták M, Bloomfield K, Gil A, Neufeld M, O'Donnell A, Petruželka B, Rogalewicz V, Schulte B, Manthey J; European Study Group on Alcohol Use and COVID-19. Alcohol consumption during the COVID-19 pandemic in Europe: a large-scale cross-sectional study in 21 countries. Addiction. 2021 Dec;116(12):3369-3380. doi: 10.1111/add.15530. Epub 2021 Jun 9. PMID: 34109685.
- Семке В.Я., Куприянова И.Е., Шушпанова Т.В. Психическое здоровье населения Сибири и Дальнего Востока. Журнал неврологии и психи-атрии им. С.С. Корсакова. 2007. Т. 107, № 3. С. 78. Semke VYa, Kupriyanova IE, Shushpanova TV. Mental health of the population of Siberia and the Far East. S.S. Korsakov Journal of Neurology and Psychiatry. 2007;107(3):78 (in Russian).
- Бохан Н.А., Мандель А.И., Артемьев И.А., Неви-димова Т.И., Батухтина Е.И., Воеводин И.В., Аболонин А.Ф., Солонский А.В., Прокопьева В.Д., Тощакова В.А., Епимахова Е.В., Шушпано-ва Т.В. Клинико-патобиологические закономерности формирования и патоморфоза алкоголизма в социально-организованных популяциях. Сибирский вестник психиатрии и наркологии. 2015. № 3 (88). С. 53-63. Bokhan NA, Mandel AI, Arte-myev IA, Nevidimova TI, Batukhtina EI, Voevodin IV, Abolonin AF, Solonsky AV, Prokopieva VD, Toshchakova VA, Epimakhova EV, Shushpanova TV. Clinical and pathobiological patterns of for-mation and pathomorphosis of alcoholism in socially organized populations. Siberian Herald of Psychiatry and Addiction Psychiatry. 2015;3(88):53-63 (in Rus-sian).
- Beaglehole R, Bonita R. Alcohol: a global health priority. Lancet. 2009 Jun 27;373(9682):2173-4. doi: 10.1016/S0140-6736(09)61168-5. PMID: 19560583.
- Бохан Н.А., Мандель А.И., Артемьев И.А., Ветлу-гина Т.П., Иванова С.А., Солонский А.В., Неви-димова Т.И., Новожеева Т.П., Шушпанова Т.В., Стоянова И.Я. Нейробиологические и психосоци-альные закономерности формирования клиниче-ской гетерогенности аддиктивных расстройств (региональный, профилактический аспекты). Си-бирский вестник психиатрии и наркологии. 2009. № 5 (56). С. 20-26. Bokhan NA, Mandel AI, Arte-myev IA, Vetlugina TP, Ivanova SA, Solonsky AV, Nevidimova TI, Novozheeva TP, Shushpanova TV, Stoyanova IYa. Neurobiological and psychosocial regularities in the formation of the clinical heteroge-neity of addictive disorders (regional, preventive as-pects). Siberian Herald of Psychiatry and Addiction Psychiatry. 2009;5(56):20-26 (in Russian).
- Stavro K, Pelletier J, Potvin S. Widespread and sustained cognitive deficits in alcoholism: a meta-analysis. Addict Biol. 2013 Mar;18(2):203-13. doi: 10.1111/j.1369-1600.2011.00418.x. Epub 2012 Jan 20. PMID: 22264351.
- Пешковская А.Г., Мандель А.И., Иванова С.А., Прокопьева В.Д. Влияние алкоголизма на когни-тивные функции у представителей коренного населения Сибири. Сибирский вестник психиат-рии и наркологии. 2016. № 4 (93). С. 105-110. Peshkovskaya AG, Mandel AI, Ivanova SA, Prokop-ieva VD. Influence of alcoholism on cognitive func-tions among representatives of the indigenous popula-tion of Siberia. Siberian Herald of Psychiatry and Ad-diction Psychiatry. 2016;4(93):105-110 (in Russian).
- Бохан Н.А., Мандель А.И., Иванова С.А., Прокопьева В.Д., Артемьев И.А., Невидимова Т.И., Мастерова Е.И., Воеводин И.В., Аболонин А.Ф., Шушпанова Т.В. Старые и новые проблемы в наркологии в контексте междисциплинарных исследований. Вопросы наркологии. 2017. № 1. С. 26-62. Bokhan NA, Mandel AI, Ivanova SA, Prokopieva VD, Artemyev IA, Nevidimova TI, Masterova EI, Voevodin IV, Abolonin AF, Shush-panova TV. Old and new problems in narcology in the context of interdisciplinary research. Journal of Addiction Issues. 2017;1:26-62 (in Russian).
- Квартыч Е.И., Тихонова И.Н., Помазанова Е.В. Метаболизм этанола в печени и предрасполо-женность к алкоголю. Социология. Философия. Прикладные исследования. 2020. № 6. С. 21-24. Kvartych EI, Tikhonova IN, Pomazanova EV. Me-tabolism of ethanol in the liver and predisposition to alcohol. Sociology. Philosophy. Applied Re-search. 2020;6:21-24 (in Russian).
- Сутько И.П., Семененя И.Н., Шляхтун А.Г. Роль изоформ цитохрома Р450 эндоплазматического ретикулума гепатоцитов в метаболизме этанола. Гепатология и гастроэнтерология. 2021. Т. 5, № 2. С.132-137. Sutko IP, Semenenya IN, Shlyakhtun AG. The role of isoforms of cytochrome P450 of the endoplasmic reticulum of hepatocytes in the metabolism of ethanol. Hepatology and Gastroen-terology. 2021;5(2):132-137 (in Russian).
- Маев И.В., Абдурахманов Д.Т., Андреев Д.Н. Алкогольная болезнь печени: современное со-стояние проблемы. Терапевтический архив. 2014. № 86, № 4. С. 108-116. Maev IV, Abdurakhmanov DT, Andreev DN. Alcoholic liver disease: state-of-the-art. Therapeutic Archive. 2014;86(4):108-116 (in Russian).
- Жмуров Д.В., Парфентева М.А., Семенова Ю.В., Рубцов Д.А. Цирроз печени. Colloquium-journal. 2020. № 11 (63). С. 57-62. Zhmurov DV, Parfenteva MA, Semenova YuV, Rubtsov DA. Cir-rhosis of the liver. Colloquium-journal. 2020;11(63):57-62. doi:10.24411/2520-6990-2020-11732 (in Russian).
- Киселева Я.В., Жариков Ю.О., Р.В. Масленников Р.В., Павлов Ч.С., Николенко В.Н. Молекуляр-ные аспекты прогрессирования фиброза печени алкогольной этиологии. Медицинский вестник Северного Кавказа. 2020. Т. 15, № 2. С. 288-293. Kiseleva YaV, Zharikov YuO, RV Maslennikov RV, Pavlov ChS, Nikolenko VN. Molecular aspects of the progression of liver fibrosis of alcoholic etiology. Medical Bulletin of the North Caucasus. 2020;15 (2):288-293 (in Russian).
- Sutherland GT, Sheedy D, Kril JJ. Neuropathology of alcoholism. Handb Clin Neurol. 2014;125:603-15. doi: 10.1016/B978-0-444-62619-6.00035-5. PMID: 25307599.
- Шевченко О.И., Лахман О.Л., Катаманова Е.В. Характеристика когнитивных нарушений при ал-когольной и дисциркуляторной энцефалопатии. Журнал неврологии и психиатрии им. С.С. Кор-сакова. 2020. Т. 120, № 5. С. 16-23. Shevchenko OI, Lakhman OL, Katamanova EV. Comparative characteristic of cognitive impairment in alcoholic and discirculatory encephalopathy. S.S. Korsakov Journal of Neurology and Psychiatry. 2020; 120(5): 16-23. https://doi.org/10.17116/jnevro202012005116 (in Russian).
- Очилов У.У., Тураев Б.Т., Хушвактова Д.Х. Распространенность когнитивных нарушений у пациентов с алкоголизмом. Вестник науки и об-разования. 2020. № 17-2 (95). С. 104-106. Ochi-lov UU, Turaev BT, Khushvaktova DKh. The prev-alence of cognitive impairment in patients with al-coholism. Bulletin of Science and Education. 2020; 17-2(95):104-106 (in Russian).
- Новожеева Т.П., Шушпанова Т.В., Удут В.В., Бохан Н.А. Создание фармакологических средств активации систем детоксикации: опыт и перспективы. Экспериментальная и клиническая фармакология. 2017. Т. 80, № 56. С. 23-24. Novozheeva TP, Shushpanova TV, Udut VV, Bo-khan NA. Creation of pharmacological agents for activating detoxification systems: experience and prospects. Experimental and Clinical Pharmacolo-gy. 2017. V. 80, No. 56. S. 23-24 (in Russian).
- Шушпанова Т.В., Бохан Н.А., Станкевич К.С., Новожеева Т.П., Мандель А.И., Счастный Е.Д., Кисель Н.И., Шушпанова О.В., Удут В.В., Боев Р.С., Князева Е.М. Инновационный модулятор ГАМК рецепторов – активатор микросомальной цитохром-Р450 оксидазной системы у больных алкоголизмом. Химико-фармацевтический журнал. 2020. Т. 54, № 11. С. 9-16. Shushpanova TV, Bokhan NA, Stankevich KS, Novozheeva TP, Man-del AI, Schastnyy ED, Kisel NI, Shushpanova OV, Udut VV, Boev RS, Knyazeva EM. An innovative modulator of GABA receptors ‒ an activator of the microsomal cytochrome P450 oxidase system in pa-tients with alcoholism. Chemical Pharmaceutical Journal. 2020. V. 54, No. 11. S. 9-16 (in Russian).


