Альвеококкоз. Неопреабельные поражения печени. Тактика ведения - трансплантация или медикаментозное лечение
Автор: Адырбек Б.Б., Ашимова А.С., Илямова Р.Б., Мэлс А.А., Махметов А.А., Розакулова Н.Ш., Якупова Д.Р.
Журнал: Теория и практика современной науки @modern-j
Рубрика: Медицина и здоровье
Статья в выпуске: 5 (107), 2024 года.
Бесплатный доступ
В данной статье отражены результаты исследования по оценке эффективности медикаментозного лечения (альбендозолом) неоперабельного альвеококкоза печени. Также отражено сравнение эффективности на основе данных о выживаемости пациентов после медикаментозного лечения и трансплантации печени при неоперабельном альвеококкозе печени. Исследование показало, что медикаментозное лечение эффективнее трансплантации печени.
Альвеококкоз печени, трансплантация печени, альбендазол, выживаемость
Короткий адрес: https://sciup.org/140306044
IDR: 140306044 | УДК: 617-089
Alveococcosis. Uncondible liver lesions. Management tactics - transplantation or drug treatment
This article reflects the results of a study assessing the effectiveness of drug treatment (albendazole) for inoperable alveococcosis of the liver. A comparison of effectiveness based on data on patient survival after drug treatment and liver transplantation for inoperable liver alveococcosis is also reflected. The study showed that drug treatment is more effective than liver transplantation.
Текст научной статьи Альвеококкоз. Неопреабельные поражения печени. Тактика ведения - трансплантация или медикаментозное лечение
Альвеолярный эхинококкоз (АЭ, альвеококкоз) – паразитарное заболевание, вызванное Echinococcus multilocularis. АЭ ведет себя как злокачественные опухоли: проникает в окружающую паренхиму печени, метастазирует в регионарные лимфатические узлы, а также гематогенным путем диссеминирует в легкие и головной мозг [10]. Прогноз нелеченого АЭ очень плохой: 10-летняя выживаемость 10-20%, 15-летняя выживаемость составляет практически 0% [11]. При отсутствии должного лечения высок риск развития угрожающих жизни гепатобилиарных осложнений АЭ, которые включают в себя: стриктуры желчных путей и рецидивирующий холангит вследствие внутригрудной инвазии, вторичный билиарный цирроз печени, желудочно-кишечные кровотечения из-за портальной гипертензии, абсцессы печени, острый тромбоз нижней полой вены и синдром Бадда-Киари [12].
Единственными стандартными методами лечения являются: хирургическое вмешательство с последующей двухлетней химиотерапией производными бензимидазола, но такое лечение подходит примерно 25–70% пациентов (с незапущенными процессами, диагностированными на ранних стадиях, то есть резектабельные поражения печени) [10,13,14]. У пациентов с запущенным альвеококкозом (нерезектабельные поражения печени, тотальное поражение печени) встает вопрос об альтернативных методах, так как стандартные операции здесь окажутся неэффективными и технически невыполнимыми. К альтернативным методам лечения нерезектабельных пациентов с альвеококкозом, можно отнести: трансплантацию печени и антипаразитарную терапию [15].
Определение распространенности процесса при АЭ позволяет сделать PNM-классификация предложенная ВОЗ в 1996 году [16]. PNM-классификация напоминает TNM-классификацию, использующуюся при оценке злокачественных опухолей. Если в TNM-классификации мы оцениваем: T (tumo ) – размер опухоли, N (nodus) – поражение лимфатических узлов, M (metastasis) – наличие метастазов в других органах, то в PNM-классификации мы оцениваем: P parasitic mass in the live ) – паразитарное образование в печени, N (involvement of neighbouring organs) – поражение соседних органов, M metastasis) – наличие метастазов в других органах. Исходя из имеющихся данных (образование печени, поражение соседних органов, метастазы в других органах) выставляется стадия заболевания, выделяют 4 стадии (Ⅰ,Ⅱ,Ⅲа,Ⅲб,Ⅳ стадии). Резектабельными (операбельными) принято считать Ⅰ и Ⅱ стадии альвеококкоза, нерезектабельными (неоперабельными) принято считать Ⅲб и Ⅳ стадии, а Ⅲа стадия является пограничной, где вопрос об оперативном лечении принимается лечащим врачом [16].
Так как Ⅲб, Ⅳ, и иногда Ⅲа стадии являются нерезектабельными, то таким пациентам предлагается либо трансплантация печени, либо антипаразитарная терапия, но четких критериев назначения того или иного метода лечения на сегодняшний день не имеется, но тем не менее каждый из методов имеет свои плюсы и минусы. Трансплантация печени является крайней мерой и должна применяться только в случаях нерезектабельного поражения печени альвеолярным эхинококком. Эффективность трансплантации наблюдается только у половины реципиентов трансплантата [17,18]. Кроме того, иммуносупрессивная терапия после трансплантации может увеличить размножение паразита и привести к метастатическому распространению альвеолярного эхинококка у пациентов, у которых метастазы отсутствовали [19,20]. К тому же имеются противопоказания к трансплантации печени – наличие отдаленных метастазов. Высокий уровень послеоперационной заболеваемости и смертности (30% в течение первых 6 месяцев после трансплантации), а также частота рецидивов (10% локально и 20% при отдаленных метастазах) в недавнем отчете из Турции даже поднимает этический вопрос применения трансплантации печени, особенно когда печень получена от живых доноров [21].
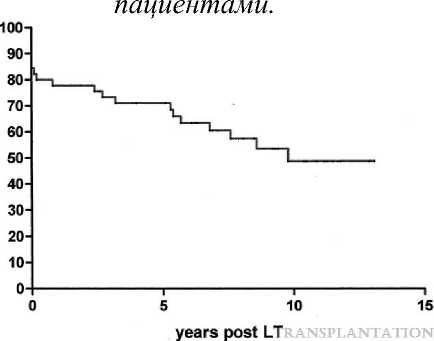
Анализ данных 45-ти пациентов, различных европейских клиник, с диагнозом альвеолярный эхинококкоз печени, которые имели неоперабельные поражения печени, но которым была проведена трансплантация печени. По имеющимся данным медиана наблюдения за этой серией (после трансплантации печени) из 45 пациентов составила 6,1 года (диапазон 0–11 лет). Выживаемость составила 77% через 1 год, 71% через 3 года, 71% через 5 лет и 49% через 10 лет, рисунок №2 [22].
Рисунок №2 Актуарная выживаемости после трансплантации печени при неизлечимом альвеолярном эхинококкозе печени: европейский опыт с 45
Что касается антипаразитарной терапии (АПТ), она используется в лечении всех стадий АЭ, как дополнительная терапия на начальных стадиях (при резектабельных поражениях печени), и как основная на запущенных стадиях (при нерезектабельных поражениях печени). АПТ основана на непрерывном введении препаратов бензимидазола: альбендозола (ABZ) или мебендазола (MBZ), которые являются единственными противоинфекционными препаратами, клинически эффективными для прекращения роста личинок Echinococcus [23,24]. MBZ был первым бензимидазолом, эффективность которого была доказана при лечении эхинококкоза [25]. В настоящее время MBZ является альтернативным препаратом только для тех пациентов, у которых при применении ABZ наблюдались серьезные побочные эффекты со стороны печени. Большинство этих пациентов испытывают схожие побочные эффекты при приеме обоих препаратов; однако некоторые люди могут переносить MBZ, что имеет решающее значение, когда пациентов нельзя оперировать, и их выживаемость полностью зависит от противоинфекционного лечения [26]. Говоря о побочных реакциях препаратов бензимидазола, наиболее часто встречаемые: острая печеночная недостаточность, острая почечная недостаточность, рабдомиолиз, апластическая анемия, многоформная эритема, синдром Стивенса-Джонсона и др.
Материалы и методы
Ретроспективный анализ историй болезни пациентов отделения «Гепатопанкреатобилиарной хирургии и трансплантации печени» Национального научного центра хирургии имени А.Н.Сызганова (ННЦХ) г.Алматы с диагнозом альвеолярный эхинококкоз печени. Критериями включения пациентов в исследование являются неоперабельные поражения печени альвеолярным эхинококком, то есть Ⅲ и Ⅳ стадии заболевания, критерии исключения – операбельные поражения печени альвеолярным эхинококком, т.е. Ⅰ и Ⅱ стадии заболевания, поставленные исходя из PNM-классификации. Таким образом в исследование были включены данные 41-го пациента. Из них: 11 пациентов с Ⅲа стадией альвеококкоза (27%), 11 пациентов с Ⅲб альвеококкоза (27%) и 19 пациентов с Ⅳ стадией альвеококкоза (46%). Кол-во исследуемых мужчин составило 23 пациента (56%), женщин – 18 пациентов (44%). Анализ данных по выживаемости 45 пациентов с неоперабельным АЭ после трансплантации печени в клиниках Европы, из которых мужчин – 21 (47%), женщин – 24 (53%) [26]. То есть всех пациентов можно поделить на две группы:
-
- пациенты на антипаразитарной терапии; - пациенты после трансплантации печени.
Статистический анализ
Данные были выражены как средние значения и медианы. Кривые выживаемости были построены с использованием метода Каплана-Мейера.
Результаты
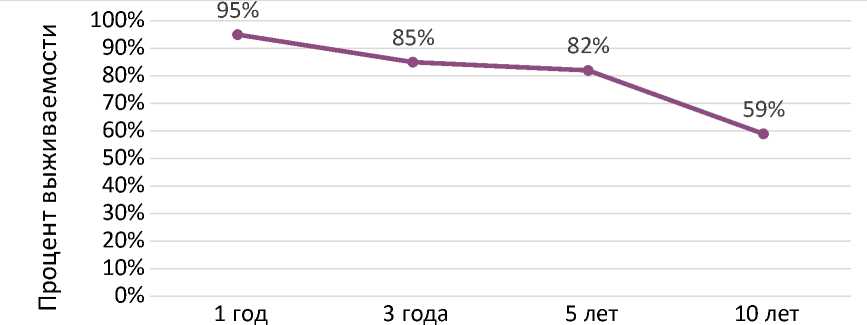
Нами были проанализированы истории болезни 41-го пациента отделения «Гепатопанкреатобилиарной хирургии и трансплантации печени» Национального научного центра хирургии имени А.Н.Сызганова (ННЦХ) г.Алматы с диагнозом альвеолярный эхинококкоз печени, которые имели неоперабельные поражения печени. Всем вышеуказанным пациентам в связи с неоперабельностью поражений печени и невозможностью проведения трансплантации печени была назначена антипаразитарная терапия с применением препарата группы бензимидазола – альбендазола. Выживаемость через 1 год составила – 95%, через 3 года - 85%, через 5 лет - 82%, через 10 лет – 59%, рисунок №3.
Рисунок №3 Актуарная выживаемости после антипаразитарной терапии альбендазолом, при неизлечимом альвеолярном эхинококкозе печени: отечественный опыт с 41 пациентом.
Прошедшее время после начала АПТ
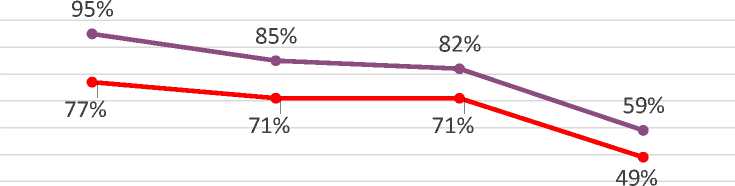
Сравнительный анализ выживаемости после трансплантации печени и антипаразитарной терапии альбендазолом отражен на рисунке №4
Рисунок №4 Сравнительный анализ выживаемости после трансплантации печени и антипаразитарной терапии альбендазолом, при неизлечимом альвеолярном эхинококкозе печени
100% о 90%
-
§ 80%
го 70% со 60%
I 50%
-
-О 40%
СО ,
-
I- 30%
-
о 20%
-
Q 10%
0%
1 год 3 года 5 лет 10 лет
Прошедшее время
После трансплантации печени После антипаразитарной терапии
Выводы
-
1. Был проведен анализ современной литературы на тему тактики ведения пациентов с запущенными стадиями альвеококкоза, который показал, что на сегодняшний день во всем мире нет единой принятой тактики ведения пациентов с вышеуказанным диагнозом;
-
2. После анализа литературы были использованы данные 45-ти пациентов из Европы с диагнозом неоперабельные поражения печени, которым в качестве выбора метода лечения была проведена трансплантация печени. Далее пациенты подверглись 10-летнему наблюдению, для оценки 1,3,5,10-летней выживаемости.
-
3. Проведен ретроспективный анализ историй болезни 41-го пациента отделения «Гепатопанкреатобилиарной хирургии и трансплантации печени» Национального научного центра хирургии имени А.Н.Сызганова (ННЦХ) г.Алматы с диагнозом альвеолярный эхинококкоз печени, которые имели неоперабельные поражения печени и которым была назначена антипаразитарная терапия. Выживаемость составила 95% через 1 год, 85% через 3 года, 82% через 5 лет и 59% через 10 лет.
-
4. Проведя сравнительный анализ на основании вышеуказанных данных, можно сделать вывод о том, что в нашем случае антипаразитарная терапия показала куда большую эффективность чем трансплантация печени, поэтому она будет рекомендоваться пациентам с запущенными стадиями альвеококкоза в первую очередь.
Выживаемость составила 77% через 1 год, 71% через 3 года, 71% через 5 лет и 49% через 10 лет.
Список литературы Альвеококкоз. Неопреабельные поражения печени. Тактика ведения - трансплантация или медикаментозное лечение
- Brunetti E, Kern P, Vuitton DA; Writing Panel for the WHO-IWGE. Expert consensus for the diagnosis and treatment of cystic and alveolar echinococcosis in humans. Acta Trop. 2010 Apr;114(1):1-16. doi: 10.1016/j.actatropica.2009.11.001. Epub 2009 Nov 30. PMID: 19931502.
- Wen H, Vuitton L, Tuxun T, Li J, Vuitton DA, Zhang W, McManus DP. Echinococcosis: Advances in the 21st Century. Clin Microbiol Rev. 2019 Feb 13;32(2):e00075-18. doi: 10.1128/CMR.00075-18. PMID: 30760475; PMCID: PMC6431127.
- Abdybekova A, Sultanov A, Karatayev B, Zhumabayeva A, Shapiyeva Z, Yeshmuratov T, Toksanbayev D, Shalkeev R, Torgerson PR. Epidemiology of echinococcosis in Kazakhstan: an update. J Helminthol. 2015 Nov;89(6):647-50. doi: 10.1017/S0022149X15000425. Epub 2015 Jul 10. PMID: 26160276.
- Torgerson PR, Shaikenov BS, Baitursinov KK, Abdybekova AM. The emerging epidemic of echinococcosis in Kazakhstan. Trans R Soc Trop Med Hyg. 2002 Mar-Apr;96(2):124-8. doi: 10.1016/s0035-9203(02)90276-2. PMID: 12055797.
- Ilana A, Upievich BE, Kenesovich KA, Bekbosynovna MS, Bakitzhanovna ZF, Esmagambetovich MK, Maratovich SY, Garipullievich SB, Gabdullinovich AR. Epizootiology and biological characteristics of echinococcosis in agricultural animals, dogs, wild carnivores, and rodents in the Western region of the Republic of Kazakhstan. Vet World. 2023 Nov;16(11):2277-2286. doi: 10.14202/vetworld.2023.2277-2286. Epub 2023 Nov 12. PMID: 38152272; PMCID: PMC10750758.
- McManus DP, Zhang W, Li J, et al. Echinococcosis. Lancet. 2003;362:1295–1304. http://dx.doi.org/10.1016/S0140-6736(03)14573-4.
- Eckert J, Deplazes P. Biological, epidemiological, and clinical aspects of echinococcosis, a zoonosis of increasing concern. Clin Microbiol Rev. 2004;17:107–135. http://dx.doi.org/10.1128/CMR.17.1.107-135.2004.
- Kantarci M, Bayraktutan U, Karabulut N, et al. Alveolar echinococcosis: spectrum of findings at cross-sectional imaging. Radiographics. 2012;32:2053– 2070. http://dx.doi.org/10.1148/rg.327125708.
- Aydin Y, Ogul H, Eren S. Diffuse alveolar echinococcosis. Med Clin (Barc). 2023 Jun 9;160(11):e7. English, Spanish. doi: 10.1016/j.medcli.2022.12.004. Epub 2023 Jan 14. PMID: 36646551.
- Kern P. Clinical features and treatment of alveolar echinococcosis. Curr Opin Infect Dis. 2010 Oct;23(5):505-12. doi: 10.1097/QCO.0b013e32833d7516. PMID: 20683265.
- Ammann RW, Eckert J. Cestodes. Echinococcus. Gastroenterol Clin North Am. 1996 Sep;25(3):655-89. doi: 10.1016/s0889-8553(05)70268-5. Erratum in: Gastroenterol Clin North Am 1996 Dec;25(4):vii. PMID: 8863045.
- Koch S, Bresson-Hadni S, Miguet JP, Crumbach JP, Gillet M, Mantion GA, Heyd B, Vuitton DA, Minello A, Kurtz S; European Collaborating Clinicians. Experience of liver transplantation for incurable alveolar echinococcosis: a 45-case European collaborative report. Transplantation. 2003 Mar 27;75(6):856-63. doi: 10.1097/01.TP.0000054230.63568.79. PMID: 12660515.
- Brunetti E, Kern P, Vuitton DA; Writing Panel for the WHO-IWGE. Expert consensus for the diagnosis and treatment of cystic and alveolar echinococcosis in humans. Acta Trop. 2010 Apr;114(1):1-16. doi: 10.1016/j.actatropica.2009.11.001. Epub 2009 Nov 30. PMID: 19931502.
- Chen KF, Tang YY, Wang R, Fang D, Chen JH, Zeng Y, Li B, Wen TF, Wang WT, Wu H, Xu MQ, Yang JY, Wei YG, Huang JW, Li JX, Zhang HZ, Feng X, Yan LN, Chen ZY. The choose of different surgical therapies of hepatic alveolar echinococcosis: A single-center retrospective case-control study. Medicine (Baltimore). 2018 Feb;97(8):e0033. doi: 10.1097/MD.0000000000010033. PMID: 29465544; PMCID: PMC5841995.
- Sato N, Namieno T, Furuya K, Takahashi H, Yamashita K, Uchino J, Suzuki K. Contribution of mass screening system to resectability of hepatic lesions involving Echinococcus multilocularis. J Gastroenterol. 1997 Jun;32(3):351-4. doi: 10.1007/BF02934492. PMID: 9213249.
- WHO Informal Working Group on Echinococcosis. Guidelines for treatment of cystic and alveolar echinococcosis in humans. Bull. World Health Organ. 1996; 74 (3): 231–242.
- Bresson-Hadni S, Koch S, Beurton I, et al. Primary disease recurrence after liver transplantation for alveolar echinococcosis: long-term evaluation in 15 patients. Hepatology. 1999;30:857–864.
- Koch S, Bresson-Hadni S, Miguet JP, et al. Experience of liver transplantation for incurable alveolar echinococcosis: a 45 case European collaborative report. Transplantation. 2003;75:856–863.
- Brunetti E, Kern P, Vuitton DA Writing Panel for the WHO-IWGE. Expert consensus for the diagnosis and treatment of cystic and alveolar echinococcosis in humans. Acta Trop. 2010;114:1–16.
- Bresson-Hadni S, Vuitton DA, Bartholomot B, et al. A twenty-year history of alveolar echinococcosis: analysis of a series of 117 patients from eastern France. Eur J Gastroenterol Hepatol. 2000;12:327–336.
- Ozdemir F, Ince V, Barut B, Onur A, Kayaalp C, Yilmaz S. 2015. Living donor liver transplantation for Echinococcus Alveolaris: single-center experience. Liver Transpl 21:1091–1095. doi: 10.1002/lt.24170.
- Koch S, Bresson-Hadni S, Miguet JP, Crumbach JP, Gillet M, Mantion GA, Heyd B, Vuitton DA, Minello A, Kurtz S; European Collaborating Clinicians. Experience of liver transplantation for incurable alveolar echinococcosis: a 45-case European collaborative report. Transplantation. 2003 Mar 27;75(6):856-63. doi:10.1097/01.TP.0000054230.63568.79. PMID: 12660515.
- Siles-Lucas M, Casulli A, Cirilli R, Carmena D. 2018. Progress in the pharmacological treatment of human cystic and alveolar echinococcosis: compounds and therapeutic targets. PLoS Negl Trop Dis 12:e0006422. doi: 10.1371/journal.pntd.0006422.
- Vuitton DA, Azizi A, Richou C, Vuitton L, Blagosklonov O, Delabrousse E, Mantion GA, Bresson-Hadni S. 2016. Current interventional strategy for the treatment of hepatic alveolar echinococcosis. Expert Rev anti Infect Ther 14:1179–1194. doi: 10.1080/14787210.2016.1240030.
- Davis A, Dixon H, Pawlowski ZS. 1989. Multicentre clinical trials of benzimidazole-carbamates in human cystic echinococcosis (phase 2). Bull World Health Organ 67:503–508.
- Vuitton D, Bresson-Hadni S. 2014. Alveolar echinococcosis: evaluation of therapeutic strategies. Expert Opin Orphan Drugs 2:67–86. doi: 10.1517/21678707.2014.870033.


