Анализ эффективности электромембранной очистки промышленных растворов от ионов никеля
Автор: Семилетова В.А., Шестаков К.В., Лазарев С.И., Полянский К.К.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Химическая технология
Статья в выпуске: 2 (104) т.87, 2025 года.
Бесплатный доступ
Электродиализная очистка технологических растворов от ионов Ni²⁺ является эффективным методом очищения сточных вод гальванических производств. В данном исследовании рассматривается кинетика процесса электродиализа, направленного на удаление никеля из растворов с различными начальными концентрациями. Эксперименты проводились на специально разработанных лабораторных установках с использованием анионо- и катионообменных мембран МА-41П и МК-40Л. Полученные результаты демонстрируют высокую степень очистки более 99%, что подтверждает перспективность применения электродиализа для промышленной очистки сточных вод от тяжелых металлов. Скорость и эффективность очистки сильно зависят от начальной концентрации никеля в растворе: при увеличении этой концентрации процесс очистки замедляется. Поэтому оптимальное значение плотности тока 20 А/м², которое обеспечивает баланс между высокой эффективностью удаления целевых веществ и приемлемыми затратами на электроэнергию и делает процесс разделения наиболее целесообразным для использования на практике. В работе технологическая схема очистки растворов от никеля с применением электродиализа, где обессоленный раствор можно повторно использовать в процессе производства, а концентрат использовать для восстановление ценных компонентов или утилизации.
Электродиализ, электродиффузия, никель, технологическая схема, ионообменная мембрана, кинетические характеристики
Короткий адрес: https://sciup.org/140312134
IDR: 140312134 | УДК: 66.081.6 | DOI: 10.20914/2310-1202-2025-2-112-120
Analysis of the efficiency of electromembrane purification of industrial solutions from nickel ions
Electrodialysis (ED) is a promising method for purifying wastewater from galvanic industries from heavy metal ions, in particular nickel (Ni²⁺). In this paper, we study the kinetics of the electrodialysis process using anion- and cation-exchange membranes (MA-41P and MK-40L) to remove Ni²⁺ from solutions with initial concentrations from 40 to 160 mg/l. It was found that the purification efficiency reaches 99.3%, which confirms the high selectivity of the method. The key factor affecting the speed and efficiency of the process is the current density. The optimal value of 20 A/m² ensures a balance between a high degree of purification and energy consumption. Increasing the current density above this value does not lead to a significant increase in efficiency, but significantly increases energy consumption. In addition, it is shown that at a high initial concentration of nickel (160 mg/l), the process slows down due to membrane saturation and possible sedimentation. An important aspect of the study was the analysis of the electrodiffusion permeability of membranes. It was found that with increasing current density, the permeability coefficient decreases by 55%, which is due to an increase in the concentration gradient and a change in the membrane properties under the influence of an electric field. Based on the experimental data, a process flow chart for cleaning industrial wastewater was proposed, including the stages of neutralization, electrodialysis, and concentrate utilization. Purified water can be returned to the production cycle, and nickel-containing concentrate can be recycled. The results of the work demonstrate the high efficiency of electrodialysis for cleaning wastewater from nickel and can be used to optimize industrial processes taking into account economic and environmental requirements.
Текст научной статьи Анализ эффективности электромембранной очистки промышленных растворов от ионов никеля
В современном мире проблема загрязнения окружающей среды становится все более актуальной. Одной из ключевых угроз для экосистем являются тяжелые металлы, которые попадают в воду и почву через промышленные выбросы,
сельскохозяйственные сточные воды и другие источники антропогенного воздействия. В связи с этим важно постоянно проводить разработку и внедрение эффективных технологий для очистки сточных вод от ионов тяжелых металлов.
Semiletova V.A., Shestakov K.V., Lazarev S.I., Polyansky K.K. Analysis of the efficiency of electromembrane purification of industrial solutions from nickel ions. Vestnik VGUIT [Proceedings of VSUET].
This is an open access article distributed under the terms of the Creative Commons Attribution 4.0 International License
Среди таких технологий особое место занимают мембранные методы разделения, которые благодаря своей высокой эффективности, простоте эксплуатации и компактным размерам становятся все более востребованными [1, 2]. К ним относят ультрафильтрацию, нанофильтрацию, обратный осмос, электродиализ (ЭД) и другие менее распространенные методы [3, 4]. ЭД использует электрическое поле для перемещения ионов через ионообменные мембраны, что позволяет избирательно удалять необходимые компоненты из жидкостей. Данный метод обладает существенными преимуществами и превосходит альтернативные технологии мембранной фильтрации:
Высокая селективность, позволяющая избирательно удалять ионы тяжелых металлов и других загрязнителей. Данное качество делает ЭД особенно эффективным для очистки сточных вод, содержащих специфические загрязнители.
Минимизация образования шлама. В ЭД-про-цессе электродиализа не происходит накопления твердых частиц на мембранах, что снижает риск засорения и упрощает обслуживание системы.
Эффективность при низких концентрациях делает ЭД подходящим для обработки сточных вод с малым содержанием загрязнителей.
Данная технология находит широкое применение в таких областях, как очистка сточных вод, опреснение воды, пищевая и химическая промышленность, очистка сточных вод гальванопроизводств. В очистке сточных вод ЭД эффективно удаляет тяжелые металлы, соли и органические загрязнители, что делает его привлекательным для использования на промышленных предприятиях. В пищевой отрасли ЭД применяется для устранения излишков солей и повышения качества продукции. В химической индустрии этот метод используют для выделения чистых химических веществ. [5–7].
В гальванической промышленности ЭД часто используют для извлечения ценных веществ из сильно концентрированных стоков, которые образуются при химической и электрохимической обработке стали и цветных металлов [8, 9]. Одним из наиболее часто применяющихся металлов является никель. Он находит широкое применение в гальваническом производстве благодаря своей исключительной коррозионной стойкости. Процесс никелирования обычно приводит к образованию значительных объемов сточных вод, часто содержащих концентрации катионов Ni2+ от 20 до 200 мг/л [10, 11]. Эти сточные воды чаще всего очищают с помощью химического осаждения, что приводит к образованию значительного количества шлама с массовой долей никеля в нем около 31,6% [12].
В исследованиях [13, 14] авторы с помощью ЭД-разделения смогли достичь удаления до 95% никеля из сточных вод, образованных после процесса никелирования. В работе [15] с помощью двухкамерного аппарата для электроосаждения и электродиализа одновременно восстанавливали никель, содержащийся в отработанных ваннах химического никелирования, и без вторичного загрязнения удаляли соединения фосфора. Результаты показали, что количество восстановленного никеля составило 82,34%. Авторы в работе [16] добились снижения концентрации Ni2+ в анолите и католите до 0,015 и 0,085 мг/л соответственно при изначально низкой начальной концентрации, равной 1 мг/л, за счет сочетания электродиализа и электроосаждения. В работе [17] исследовался процесс извлечения никеля из твердых шламов с использованием 0,1 М серной кислоты. Процесс включал в себя обработку шлама кислотой, электродиализное концентрирование и электровосстановление для извлечения никеля из полученного раствора на электроде. Выход никеля по току на катоде достигал 96%. Результаты ряда экспериментов [18] показывают, что максимальная степень извлечения ионов никеля достигается при напряжении 12 В, а оптимальная скорость подачи раствора для лабораторного аппарата составляет 0,13 м/с. Также было проведено концентрирование раствора, полученного обессоливанием промывной воды, с целью его повторного использования в технологическом цикле. В результате был получен раствор с концентрацией 34,1 г/л.
На основе проведенного литературного анализа работ [1–18], оценена важность проблемы очистки образующихся в процессе никелирования сточных вод и сформулирована цель работы.
Цель работы – исследование эффективности электромембранной очистки промышленных растворов гальванических производств от ионов никеля и технологическое оформление процесса. Для достижения поставленной цели был решен ряд задач, включая исследование кинетики ЭД-разделения и коэффициента электродиффу-зионной проницаемости.
Материалы и методы
Для проведения экспериментов и исследования кинетики ЭД-разделения использовалась специальная установка (рисунок 1), включающая ЭД-ячейку, а также три независимые линии циркуляции растворов, подключенные к ней. Каждая из этих линий предназначена для циркуляции обессоленного, концентрированного и приэлектродного (смешанных анолита и католита) растворов.
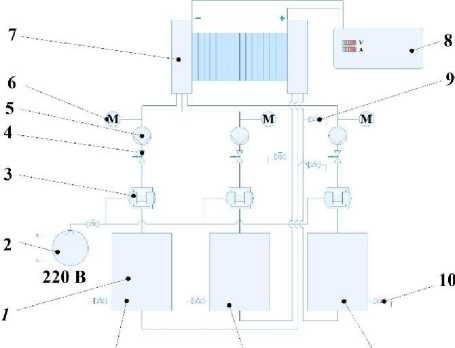
Обессоленный Концентрат Приэлектродный раствор раствор
Desalinated Concentrate Pre-electrode solution solution
Рисунок 1. Экспериментальная электродиализная установка: 1 – емкости для обессоленного, концентрированного и приэлектродного растворов; 2 – пневматический насос; 3 – масляный компрессор; 4 – контрольный клапан; 5 – расходомер; 6 – манометр; 7 – электродиализная ячейка; 8 – лабораторный источник питания; 9 – выпускной кран для сбора; 10 – выпускной кран для слива
-
Figure 1. Experimental electrodialysis setup: 1 – tanks for demineralized, concentrated and near-electrode solutions; 2 – pneumatic pump; 3 – oil compressor; 4 – control valve; 5 – flow meter; 6 – pressure gauge; 7 – electrodialysis cell; 8 – laboratory power source; 9 – collection outlet valve; 10 – drainage outlet valve
В электродиализной ячейке, общая схема которой показана на рисунке 2, под воздействием электрического поля ионы перемещаются через ионообменные мембраны, установленные в чередующемся порядке и образующие камеры разделения. Ширина межмебранного канала составляла 0,001 м, а активная площадь мембран – 0,0306 м2.
Catholite Desalinated Concentrate Analyte solution
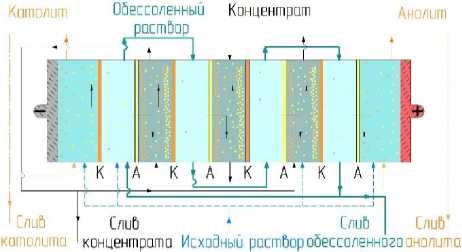
рпстбора
Catholyte drain Concentrate Initial solution Desalting Analyte drain solution drain drain
Рисунок 2. Схема электродиализного аппарата
-
Figure 2. Scheme of electrodialysis apparatus
Исследование коэффициента электро-диффузионной проницаемости было проведено на установке, представленной на рисунке 3. Установка состояла из разделительной ячейки, лабораторного источника питания и двух магнитных мешалок. Конструкция разделительной ячейки включала две квадратные камеры из оргстекла, прижатых друг к другу. Между камерами размещалась исследуемая мембрана, зафиксированная пластиковыми решетками. Внутри каждой камеры находился монополярный электрод, к которому подводился постоянный ток от источника питания. Рабочий раствор помещали в обе камеры, где для перемешивания использовались магнитные мешалки с якорями. Герметичность конструкции обеспечивалась силиконовым герметиком
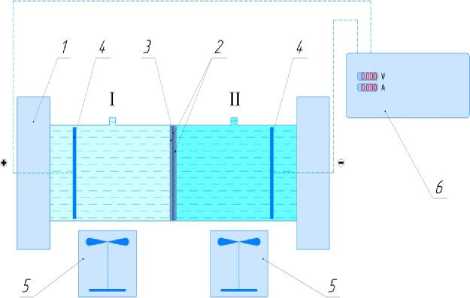
Рисунок 3. Экспериментальная электродиффузионная установка: 1 – прижимная плита; 2 – зажимная решетка; 3 – мембрана; 4 – электрод; 5 – магнитная мешалка; 6 – лабораторный источник питания
-
Figure 3. Experimental electrodiffusion setup: 1 – pressure plate; 2 – clamping grid; 3 – membrane; 4 – electrode; 5 – magnetic stirrer; 6 – laboratory power source
Для исследований использовались анионо-и катионообменные мембраны МА-41П и МК-40Л. Характеристики мембран представлены в таблице 1. Модельные водные растворы содержали нитрат никеля (Ni(NO₃)₂·6Н₂O) с различными начальными концентрациями, имитирующими реальные промышленные стоки. Более подробно компонентный состав растворов представлен в таблице 2.
Таблица 1.
Характеристики анионо- и катионообменных мембран
Table 1.
Characteristics of anion and cation exchange membranes
|
Характеристика Characteristics |
Марка | Mark |
|
|
МК-40Л |
МА-41П |
|
|
Толщина, мм | Thickness, mm |
0,3–0,5 |
0,3–0,5 |
|
Ионная группа | Ion group |
(SО 3 H) |
N(СН 3 ) |
|
Ионная форма – противоион Ionic form - counter ion |
Na+ |
Cl- |
|
Инертное связующее Inert binder |
полиэтилен polyethylene |
полиэтилен polyethylene |
|
Армирующая ткань Reinforcing fabric |
полиэфирная polyester |
полиамидная polyamide |
Таблица 2.
Характеристики исходных модельных растворов
Table 2.
Characteristics of the initial model solutions
|
Раствор Solution |
Исходная концентрация C 0 , мг/л Initial C 0 concentration, mg/L |
|
|
Ni2+ |
NО 3 - |
|
|
Н1 |
40,0 |
84,5 |
|
Н2 |
80,0 |
169,0 |
|
Н3 |
120,0 |
253,5 |
|
Н4 |
160,0 |
338,0 |
Перед началом серии экспериментальных исследований был проведен тщательный анализ литературных данных, в результате которого были выбраны оптимальные значения рабочих параметров экспериментов. Плотность тока варьировалась в диапазоне от 10 А/м² до 40 А/м². Средний расход разделяемого раствора в каждой секции был равен 300 л/ч, а исходный объем растворов – 5 л. Каждый отдельный эксперимент
Результаты и обсуждение
Одним из важных этапов исследования было наблюдение за влиянием исходной концентрации никеля и плотности электрического тока на процесс очистки. Эта часть исследования позволила нам глубже понять, как повышение концентрации никеля в растворе и изменение плотности тока воздействуют на эффективность данного процесса.
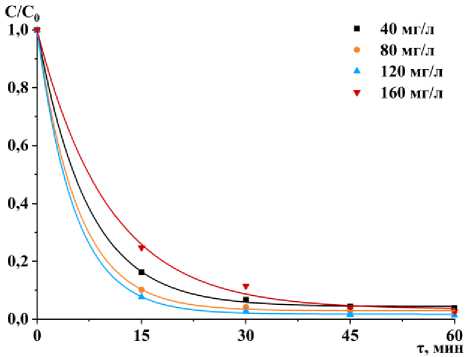
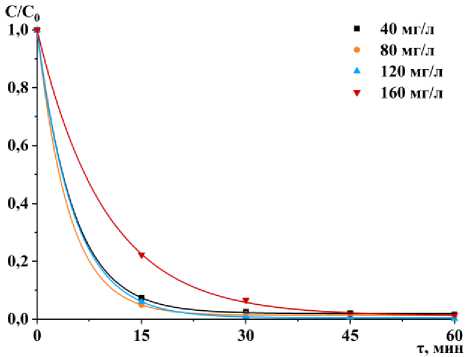
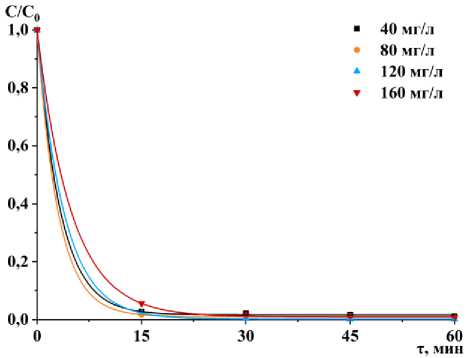
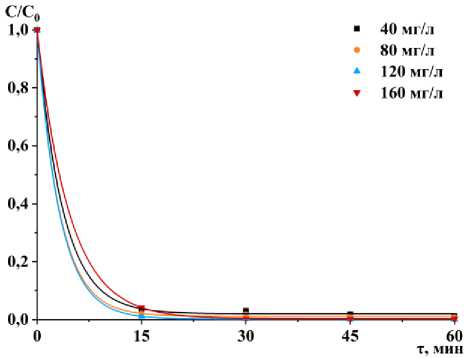
На рисунке 4 представлены результаты серии экспериментальных исследований, полученных при электродиализном разделении модельных растворов Н1, Н2, Н3 и Н4. Получены кинетические зависимости концентрации С ионов Ni2+, нормированной к исходной величине C 0 , в процессе ЭД-разделения при плотности тока 10, 20, 30 и 40 А/м2.
(a)
(b)
(c) (d)
Рисунок 4. Кинетические зависимости концентрации С ионов Ni2+, нормированной к исходной величине C 0 , от времени: (a) – 10 А/м2; (b) – 20; (c) – 30 А/м2; (d) – 40 А/м2
-
Figure 4. Kinetic dependences of the concentration C of Ni2+ ions, normalized to the initial value С 0 , on time: (a) – 10 А/m2; (b) – 20; (c) – 30 А/m2; (d) – 40 А/m2
Эксперименты по электродиализному разделению модельных водных растворов, содержащих Ni(NO₃)₂·6Н₂O, показали высокую эффективность метода. Степень очистки растворов в ряде случаев от катионов Ni²⁺ составила 98,5–99,3%, что демонстрирует потенциал электродиализа для применения в промышленных условиях. Было установлено, что при увеличении начальной концентрации никеля в растворе процесс очистки замедлялся. Так, в процессе разделения растворов Н1, Н2 и Н3 в большинстве экспериментов при всех плотностях тока кинетические зависимости от времени имели схожую форму и демонстрировали быстрое снижение концентрации ионов никеля. Однако при разделении растворов Н4 с увеличенной исходной концентрацией ионов Ni2+ процесс очистки проходил значительно медленнее [19–22]. Это может быть связано определенными факторами, которые влияют на эффективность технологии. Например, высокая концентрация ионов никеля в растворе может привести к перенасыщению и замедлению диффузии ионов к мембранам. Также на мембранах могут образовываться осадки, что приводит к их загрязнению, затрудняет движение ионов и в конечном итоге может потребовать более частой замены или очистки мембран. Эти данные подчеркивают важность оптимизации параметров процесса для обеспечения максимальной эффективности очистки при высоких концентрациях никеля.
Исследована эффективность разделения методом ЭД в течение одного часа при различных плотностях тока – от 10 А/м² до 40 А/м. На рисунке 4 представлены зависимости концентрации С ионов Ni2+, нормированной к исходной величине С0, от плотности тока.
С увеличением плотности тока нормированные концентрации уменьшаются, что указывает на эффективное удаление ионов из раствора. Чем выше плотность тока, тем быстрее происходит этот процесс. Это связано с тем, что более высокая плотность тока приводит к усилению электролитических процессов, что, в свою очередь, позволяет более эффективно извлекать загрязняющие вещества. Более высокие начальные концентрации в большинстве экспериментов приводят к меньшему относительному снижению концентрации при той же плотности тока. Это может объясняться насыщением ионоб-менных мембран либо ограниченностью возможностей переноса ионов при повышенных концентрациях. Как видно на рисунке 4, после достижения плотности тока в 20 А/м² дальнейший прирост эффективности очистки оказывается несущественным по сравнению с увеличением энергозатрат на процесс при большей плотности тока. С последующим увеличением плотности тока затраты на электроэнергию растут пропорционально, однако при этом прирост очистки остаётся минимальным и становится экономически невыгодным. На основании упомянутых наблюдений можно сделать вывод, что оптимальным значением плотности тока для рассматриваемой системы является именно 20 А/м². Такая плотность тока обеспечивает баланс между высокой эффективностью удаления целевых веществ и приемлемыми затратами на электроэнергию, что делает его наиболее целесообразным для использования на практике.
На рисунке 6 рассмотрено влияние плотности тока и исходной концентрации раствора на электродиффузионную проницаемость мембраны МК-40Л для катионов Ni2+.
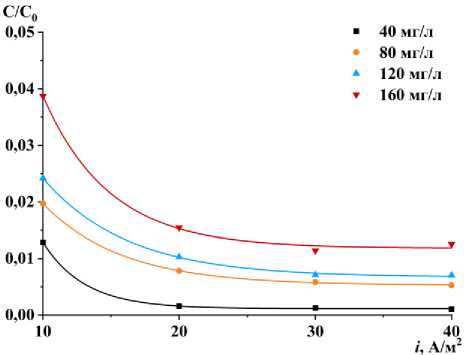
Рисунок 5. Зависимости концентрации С ионов Ni2+, нормированной к исходной величине C 0 , от плотности тока после часового ЭД-процесса
Figure 5. Dependences of the concentration of Ni2+ ions
C, normalized to the initial value C 0 , on the current density after an hour-long ED process
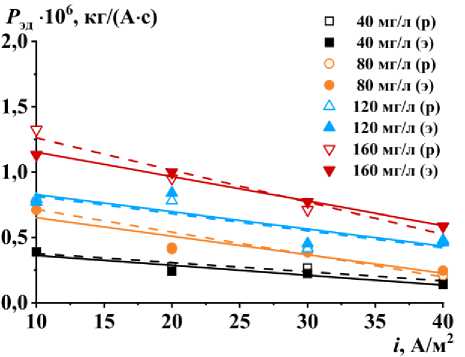
Рисунок 6. Зависимости электродиффузионной проницаемости мембраны МК-40Л для катионов Ni2+ от плотности тока при разной исходной концентрации С 0
Figure 6. Dependences of the electrodiffusion permeability of the MK-40L membrane for Ni2+ cations on the current density at different initial concentrations of С 0
Из данных видно, что электродиффузи-онная проницаемость мембраны МК-40Л для катионов Ni2+ уменьшается с увеличением плотности тока для всех концентраций раствора, что свидетельствует о снижении эффективности электродиффузионного переноса. Значения коэффициента электродиффузионной проницаемости Рэд колеблются в диапазоне от 0,140×10–6 до 1,324×10–6 кг/(А×с). Снижение его значений при увеличении плотности тока наблюдается для всех начальных концентраций растворов и составляет в среднем 55%. Это явление можно объяснить несколькими причинами. Во-первых, увеличение плотности тока ведет к усилению градиента концентрации по обеим сторонам мембраны, что усложняет процесс массопереноса. Из-за возрастающего сопротивления переносу вещества электродиффузия постепенно замедляется. Во-вторых, высокая плотность тока может вызывать увеличение температуры раствора в области мембраны, что, в свою очередь, может приводить к изменению физико-химических свойств самой мембраны. Кроме того, снижение электродиффузионной проницаемости может быть связано с более интенсивным взаимодействием катионов с матрицей мембраны, что ограничивает свободное движение ионов.
Для подтверждения полученных экспериментальных данных был проведен теоретический расчет значений коэффициента электродиффу-зионной проницаемости P эд . Его проводили на основе уравнения [23]:
Рэд = kCnnim exp(C0g)exp(A/ T), где k – эмпирический коэффициент, м5/(А2∙с); C0 – концентрация вещества в исходном растворе, кг/м3; i – плотность тока, А/м2; n, m – безразмерные эмпирические коэффициенты; g – эмпирический коэффициент, м3/кг; A – эмпирический коэффициент, К; T – абсолютная температура раствора, К.
Экспериментальные и расчетные значения производительности близки друг к другу, что свидетельствует о хорошей корреляции между теоретическими предположениями и реальными результатами измерений. Тем не менее наблюдаются незначительные отклонения, особенно выраженные при высоких концентрациях и низких напряжениях, которые могут быть вызваны ошибками измерений и расчетов. В целом разница между экспериментальными и теоретически рассчитанными значениями не превышала 10%.
Практическое применение
Разработка и внедрение эффективных технологических схем – залог успешной работы мембранных систем очистки, способствующий как экономии ресурсов, так и охране окружающей среды. Эффективные схемы позволяют достигать более высокого уровня удаления
Технологическая схема процесса электродиализной очистки сточных вод, предлагаемая для гальванического производства, изображена на рисунке 7. Схема предназначена для электродиализной очистки кислых промышленных растворов, содержащих ионы никеля. Кислые промышленные растворы сначала собираются в накопительной емкости 1 , после чего насосом 2 они подаются в аппарат для нейтрализации растворов 3 . Затем, нейтрализованный раствор поступает в электродиализатор 4 для очистки от ионов никеля. Очищенный раствор (дилюат) направляется в резервуар 5 для хранения очищенной воды, который предполагается повторно использовать в процессе гальванического производства. Концентрат, содержащий большое количество никеля, отправляется в емкость 6 для последующего концентрирования или использования в строительном производстве.
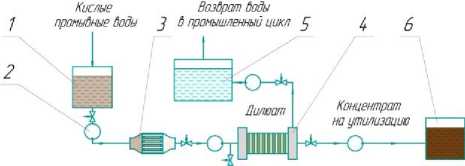
Рисунок 7. Технологическая схема разделения промышленных растворов с применением электродиализной очистки: 1 – емкость сбора кислых промывных вод;
2 – насос; 3 – аппарат нейтрализации растворов; 4 – электродиализатор; 5 – емкость сбора очищенной воды, 6 – емкость сбора растворов, подлежащих утилизации Figure 7. Technological scheme of separation of industrial solutions using electrodialysis purification: 1 – tank for collecting acidic wash water; 2 – pump; 3 – solution neutralization apparatus; 4 – electrodialyzer; 5 – tank for collecting purified water; 6 – tank for collecting solutions subject to disposal
Технологическая схема обладает высокой степенью адаптивности, позволяя оперативно реагировать на изменяющиеся производственные условия или прогнозируемый рост объемов обработки. Это достигается за счет модульной структуры, гибкой конфигурации параметров и возможности интеграции новых компонентов. Такая гибкость позволяет существенно увеличивать производительность системы, избегая при этом значительных капитальных вложений в новое оборудование или кардинальную перестройку всего процесса. Оптимизация отдельных узлов, перенастройка алгоритмов и масштабирование вычислительных ресурсов позволяют эффективно справляться с растущими потребностями и поддерживать конкурентоспособность предприятия.
Заключение
Проведенное исследование позволяет сделать следующие выводы:
-
1. Метод электродиализа является высокоэффективным для очистки водных растворов от ионов никеля, достигая степени очистки более 99%, при этом скорость удаления напрямую зависит от плотности тока. Это подтверждает возможность использования электродиализного метода для промышленной очистки растворов от тяжелых металлов. Было установлено, что скорость и эффективность очистки зависят от начальной концентрации никеля в растворе. При увеличении начальной концентрации процесс электродиализной очистки замедляется.
-
2. Для достижения максимальной производительности рассматриваемой системы рекомендуется использовать оптимальное значение плотности тока 20 А/м², которое обеспечивает баланс между высокой эффективностью удаления
-
3. Предлагается технологическая схема очистки растворов от никеля с применением ЭД, где обессоленный раствор можно повторно использовать в процессе производства, а концентрат использовать для восстановление ценных компонентов или утилизации.
Работа выполнена при финансовой поддержке Министерства науки и высшего образования РФ в рамках проекта «Теоретические и экспериментальные исследования электрокинетических и структурных характеристик полимерных мембран посредством применения искусственных нейронных сетей в процессах элек-тромембранной очистки промышленных растворов, содержащих ионы металлов» (FEMU-2024–0011).


