Анализ методов обнаружения пульсовой волны сигнала артериальной пульсации крови
Автор: Федотов Александр Александрович, Акулов Сергей Анатольевич
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Физика и электроника
Статья в выпуске: 6-1 т.15, 2013 года.
Бесплатный доступ
При регистрации сигнала артериальной пульсации крови наблюдаются искажения, обусловленные дыханием человека и воздействием электромагнитных полей на усилительные каскады регистрирующего блока. Наибольшее искажение вносят случайные помехи, обусловленные движением человека. Подавление двигательных артефактов, частотные компоненты которых перекрываются с основной полосой частот сигнала артериальной пульсации крови, представляет собой нетривиальную задачу. В данной статье рассматривается использование методов цифровой обработки биосигналов артериальной пульсации крови человека в условиях присутствия двигательных артефактов на основе применения кратномасштабных вейвлет-преобразований. Предложена структурная блок-схема обработки сигнала артериальной пульсации крови, включающая в себя этапы декомпозиции и реконструкции биосигнала. Показана высокая эффективность использования предлагаемого метода цифровой обработки сигнала артериальной пульсации крови на основе применения кратномасштабных вейвлет-преобразований по сравнению с использованием классического метода на основе фильтрации скользящего среднего.
Сигнал артериальной пульсации крови, цифровая фильтрация биосигналов, кратномасштабное вейвлет-преобразование
Короткий адрес: https://sciup.org/148202523
IDR: 148202523 | УДК: 57.087
Analysis of methods for detecting pulse waves of arterial pulsation signal
During the acquisition of distal arterial pulse signal distortions caused by the breath of human and the effects of electromagnetic fields on the amplification units could be observed. The strongest distortion could be caused by the movement of the patient. Suppression of motion artifacts which frequency components overlap with the main spectral band of the distal arterial pulse signal is not a trivial task. This article is devoted to the distal arterial pulse signal processing method in the presence of motion artifact based on the multiresolution wavelet transform. The block diagram of the distal arterial pulse signal processing method composed of two stages of signal decomposition and signal reconstruction was proposed. The high efficiency of the proposed distal arterial pulse signal processing method based on multiresolution wavelet transform over using classical method based on the moving average filter was shown.
Текст научной статьи Анализ методов обнаружения пульсовой волны сигнала артериальной пульсации крови
Регистрация и обработка сигнала артериальной пульсации крови находит широкое применение в инструментальных системах кардиологической диагностики для мониторинга частоты сердечных сокращений, определения степени насыщения гемоглобина артериальной крови кислородом, исследования гемодинамических процессов в артериальном русле [1, 2].
Регистрация сигнала артериальной пульсации крови с помощью плетизмографических или сфигмографических датчиков сопровождается наличием помех физической и физиологической природы. Помехи электрической природы возникают в усилительном тракте систем регистрации сигнала артериальной пульсации крови в результате влияния внешних электромагнитных полей, создаваемых главным образом, электрической сетью питания [2, 3]. Помехи физиологического происхождения можно разделить на две группы: артефакты, обусловленные движениями пациента и помехи, создаваемые дыханием пациента.
Дыхательные тренды, присутствующие в сигнале артериальной пульсации крови, искажают изолинию и форму биосигнала. Двигательные артефакты носят случайный характер и приводят к наибольшим искажениям биосигнала. Об-
работка сигнала артериальной пульсации крови на фоне присутствия двигательных артефактов сталкивается с рядом трудностей, заключающихся в том, что природа появления двигательных артефактов имеет случайный характер, а их частотные компоненты перекрываются с основной полосой частот сигнала артериальной пульсации крови, что затрудняет использование классических методов линейной частотной фильтрации.
Основной задачей цифровой обработки сигнала артериальной пульсации крови является обнаружение пульсовой волны, основной характеристической точкой которой является систолический максимум. Эффективность обнаружения и точность измерения амплитудно-временных параметров пульсовой волны во многом определяет погрешность определения диагностических показателей, таких как частота сердечных сокращений и сатурация гемоглобина крови кислородом. Таким образом, актуальной задачей является разработка эффективных методик цифровой обработки сигнала артериальной пульсации крови в условиях воздействия широкополосных помех различной интенсивности с целью повышения эффективности детектирования пульсовой волны и определения ее амплитудно-временных характеристик с наименьшей погрешностью.
В настоящее время перспективным направлением в области обработки биосигналов, искаженных широкополосными шумами и помехами, является фильтрация на основе использования кратномасштабных вейвлет-преобразований [4].
Очистка сигналов от шума может быть реализована непосредственно удалением детализирующих коэффициентов высокочастотных уровней вейвлет-разложений [5].
Шумовые компоненты биосигналов, и особенно большие случайные выбросы значений сигналов, можно рассматривать в виде множеств локальных особенностей сигналов. Процедура вей-влет-преобразования сигнала является, по сути, результатом фильтрации исходного сигнала фильтром с конечной импульсной характеристикой, представляющей собой дискретизированные отсчеты базисного вейвлета.
Процедура обработки сигналов на основе применения кртаномасштабных вейвлет-преоб-разований включает в себя стадию декомпозиции и стадию реконструкции сигнала. Декомпозиция сигнала представляет собой разложение исходного сигнала на последовательность аппроксимирующих и детализирующих коэффициентов. Фильтрация сигналов от шума может быть реализована непосредственно полным или частичным удалением детализирующих коэффициентов высокочастотных уровней вейвлет разложений [5]. После стадии декомпозиции сигнала происходит удаление “шумовых компонент сигнала”, с последующей реконструкцией исходного сигнала, очищенного от шумов и помех.
Основу предлагаемой методики составляет использование пороговых функций на основе которых происходит ограничение уровня детализирующих коэффициентов вейвлет-преобразования. Задав определенный порог и «отсекая» коэффициенты ниже этого порога, можно значительно снизить уровень шума. Согласно теории вейвлет-пре- образований, низкочастотные (аппроксимирующие) коэффициенты вейвлет-разложения обладают большей энергией сигнала, что делает их более важными для использования на стадии реконструкции. Высокочастотные (детализирующие) коэффициенты вейвлет-разложения обладают меньшей энергией сигнала, и зачастую представляют собой шумовые компоненты исходного сигнала [4]. Таким образом, в задачах фильтрации сигнала представляется целесообразным отбросить детализирующие коэффициенты вейвлет-разложения, получаемые на ранних стадиях декомпозиции сигнала.
Основными этапами предлагаемого метода обработки сигнала артериальной пульсации крови являются:
-
1. Вычисление прямого вейвлет-преобразо-вания сигнала (выбор типа базисной вейвлет-функции и числа уровней вейвлет-разложения);
-
2. Изменение полученных коэффициентов преобразования по определенному правилу (выбор алгоритма нахождения порогового значения, выбор пороговой функции, выбор стратегии обработки детализирующих коэффициентов вейвлет-разложения);
-
3. Вычисление обратного вейвлет-преобразо-вания от множества модифицированных вейв-лет-коэффициентов.
-
4. Обнаружение пульсовой волны в обработанном сигнале артериальной пульсации крови на основе трехточечной методики детектирования систолического максимума.
На рис. 1 приведена структурная схема декомпозиции сигнала артериальной пульсации крови, включающая обработку сигнала высокочастотным и низкочастотным фильтрами и процедуры децимации (здесь: H(n) – импульсная
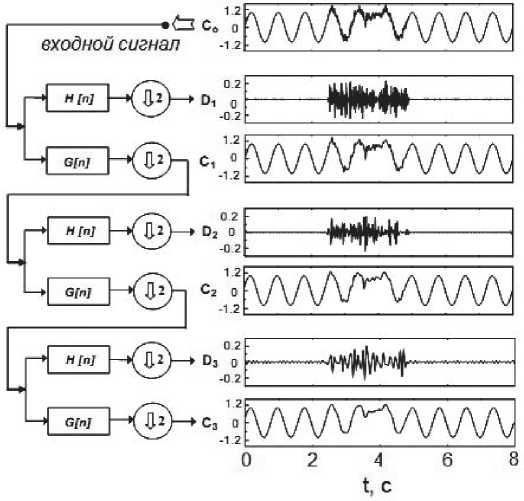
Рис. 1. Структурная схема обработки сигнала на стадии декомпозиции и зависимости изменения биосигналов на различных этапах обработки от времени
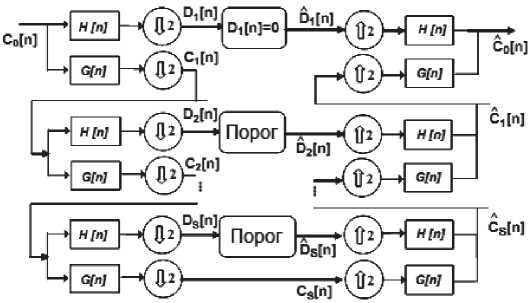
Рис. 2. Блок схема обработки сигнала артериальной пульсации крови на основе применения вейвлет-преобразования
характеристика высокочастотного фильтра, G(n) – импульсная характеристика низкочастотного фильтра, D – детализирующие коэффициенты вейвлет разложения, C – аппроксимирующие коэффициенты вейвлет-разложения), а также зависимости изменения сигнала от времени на различных этапах обработки.
На рис. 2 приведена блок-схема обработки сигнала артериальной пульсации крови на основе применения вейвлет-преобразования. На первом этапе обработки осуществляется декомпозиция исходного сигнала, далее детализирующие коэффициенты, полученные на первом уровне, приравниваются к нулю, а на поздних стадиях проходят пороговую обработку, на заключительном этапе осуществляется реконструкция сигнала, включающая в себя процедуры интерполяции и обратного вейвлет-преобразования.
Качество фильтрации сигнала будет определяться выбором значения порогового уровня. В качестве порога в данной работе предлагается использовать значение, определяемое следующим образом:
T = p • V2ln( N) , где: T – пороговое значение, N – общее количество отсчетов обрабатываемого сигнала, p –ме-диана абсолютного значения последовательности детализирующих коэффициентов, лежащих на самом первом уровне разложения.
В данной работе наилучшие результаты цифровой обработки сигнала артериальной пульсации крови были получены при использовании вейвлета Добеши 4-го порядка в качестве базисного вейвлета, число уровней вейвлет-разложе-ний было равно 6, при этом была применена мягкая пороговая функция обработки массива значений детализирующих коэффициентов.
Альтернативным и более простым методом обработки сигнала артериальной пульсации крови может служить фильтрация во временной области на основе использования фильтра скользящего среднего (ФСС) [6]:
1 N
A ( n ) = X x ( n - j )
N,ti ,
где: x(n) – входной сигнал, N – порядок фильтра, A(n) – выходной сигнал.
Применение ФСС приводит к сглаживанию исходного сигнала, и обычно, используется для устранения ошибок квантования и для устранения высокочастотных шумов в сигнале. Свойства такого рода фильтров полностью определяются величиной порядка фильтра N , которая в свою очередь будет зависеть от величины частоты дискретизации обрабатываемого сигнала.
Для обнаружения пульсовой волны используется пороговый обнаружитель, на вход которого поступает сигнал артериальной пульсации крови после прохождения процедуры предварительной фильтрации с использованием метода вейвлет-преобразований или фильтрации скользящего среднего. В качестве характеристической точки распознавания пульсовой волны использовалась точка систолического максимума.
Пороговый обнаружитель пульсовой волны состоит из порогового устройства и последовательно соединенного детектора максимума. Пороговое устройство формирует скользящее окно длительностью 2 секунды, для каждого временного окна определяется величина порога ( Lev ) как медиана выборки отсчетов биосигнала артериальной пульсации крови A(n) в пределах данного окна, на вход детектора максимума попадают только те отсчеты биосигнала, для которых выполняется следующее условие: A(n)>Lev.
Использование адаптивного порогового детектора, у которого абсолютное значение порога зависит от величины амплитуды обрабатываемого сигнала в пределах временного окна фиксированной длительности, обеспечивает повышение эффективности обнаружения пульсовой волны за счет адаптации применяемого алгоритма к нестационарному характеру биосигнала артериальной пульсации крови.
Детектор максимума производит выделение характеристической точки пульсовой волны сигнала артериальной пульсации крови на основе трехточечной схемы детектирования при одновременном выполнении следующих условий:
A(n)>A(n+1) & A(n)>A(n – 1)
Оценкой эффективности методов детектирования пульсовой волны сигнала артериальной пульсации крови в условиях присутствия дыхательных помех и двигательных артефактов может служить чувствительность обнаружения характеристических точек биосигнала. Чувствительность обнаружения ( S ) оценивается как относительная доля успешно обнаруженных характеристических точек ( P+ ) к общему числу характеристических точек ( P ) в рассматриваемой реализации биосигнала.
Для апробации разработанных методов обработки биосигналов артериальной пульсации крови с целью детектирования пульсовой волны была сформирована группа добровольцев, включающая в себя 12 человек. Для регистрации биосигналов использовался сертифицированный компьютерный фотоплетизмограф “ЭЛДАР”, имеющий стандартные технические характеристики: динамический диапазон усиления сигнала 40 дБ; полоса пропускания по уровню –3 дБ: 0,05 – 15 Гц; частота дискретизации биосигнала 500 Гц; разрядность АЦП 10 бит. Все испытуемые дали добровольное согласие на включение их в данное исследование.
В качестве анализируемых вариантов реализации цифровой обработки сигнала артериальной пульсации крови в данной работе использовались предлагаемая методика на основе вейв-лет-преобразований сигнала, а также методика на основе применения ФСС, реализуемая при различных значениях порядка фильтра.
На рис. 3 приведены зависимости измене- ния исходного сигнала артериальной пульсации крови от времени до применения методов компьютерной обработки (А), после использования предлагаемого в данной работе метода вейвлет-разложения сигнала (Б) и после применения ФСС (В), маркерными метками показаны обнаруженные систолические максимумы пульсовой волны.
Анализ зависимостей, приведенных на рис. 1, позволяет сделать вывод о том, что использование предлагаемого метода вейвлет-разложения сигнала артериальной пульсации крови на основе кратномасштабных преобразований, позволяет достичь заметно более сильного сглаживания исходного сигнала, чем при использовании ФСС, что обеспечивает более эффективную работу порогового устройства при детектировании пульсовой волны. Использование ФСС на стадии предварительной обработки сигнала артериальной пульсации крови приводит к появлению ошибок ложного обнаружения или пропуска при детектировании характеристических точек пороговым устройством.
В табл. 1 приведены значения показателей эффективности обнаружения характеристических точек сигнала артериальной пульсации крови для 12 различных фрагментов сигнала артериальной пульсации крови, искаженного дыхательными помехами и двигательными артефактами различной интенсивности.
Анализ полученных результатов показал, что применение метода обработки сигнала артериальной пульсации крови на основе использования вейвлет-преобразований позволяет получить максимальную чувствительность обнаружения характеристических точек биосигнала, близкую к 100%, в то время как обработка сигнала на основе использования ФСС дает заметно худшую чувствительность. Необходимо отметить, что использование фильтра скользящего среднего с величи-
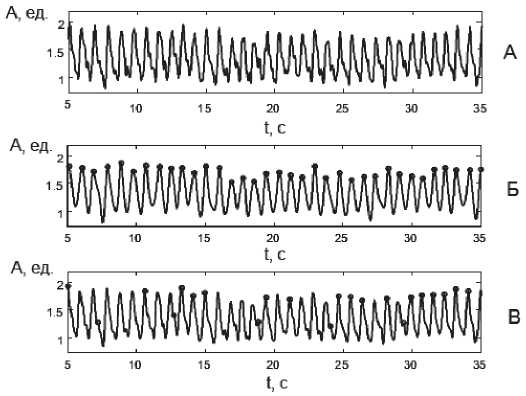
Рис. 3. Зависимости изменения сигнала артериальной пульсации крови от времени: А – исходный сигнал, Б – после обработки на основе метода вейвлет-разложения, В – после обработки ФСС
Таблица 1. Эффективность обнаружения опорных точек сигнала артериальной пульсации крови на основе использования ФСС и вейвлет-преобразований
|
Обследуемый |
A |
B |
C |
D |
E |
F |
G |
H |
I |
J |
K |
Ср едн ее значение |
|
P, шт |
123 |
109 |
115 |
93 |
176 |
135 |
149 |
114 |
131 |
117 |
145 |
|
|
P+ (вейв.), шт |
122 |
106 |
114 |
82 |
166 |
134 |
147 |
113 |
129 |
114 |
141 |
|
|
P+ (ФСС), N=250, шт |
115 |
99 |
108 |
76 |
123 |
128 |
128 |
105 |
119 |
96 |
113 |
|
|
P+ (ФСС), N=125, шт |
114 |
104 |
113 |
69 |
161 |
130 |
141 |
105 |
125 |
93 |
135 |
|
|
P+ (ФСС, N=62, шт |
114 |
69 |
106 |
76 |
155 |
125 |
144 |
89 |
120 |
62 |
127 |
|
|
S (вейв.), % |
99,2 |
97,3 |
99,1 |
88,2 |
94,3 |
99,3 |
98,6 |
99,1 |
98,5 |
97,4 |
97,2 |
97,3 |
|
S (ФСС), N=250, % |
93,5 |
90,8 |
93,9 |
81.7 |
69,9 |
94,8 |
85,9 |
92,1 |
90,8 |
82,1 |
77,9 |
86,4 |
|
S (ФСС), N=125, % |
92,7 |
95,4 |
98,3 |
74,2 |
91,5 |
96,3 |
94,6 |
92,1 |
95,4 |
79,5 |
93,1 |
91,6 |
|
S (ФСС), N=62, % |
92,7 |
63,3 |
92,2 |
81,7 |
88 |
92,6 |
96,6 |
78,1 |
91,6 |
53 |
87,6 |
82,8 |
ной порядка равной ј от величины частоты дискретизации (N=125) позволяет обеспечить наилучшую чувствительность обнаружения характеристических точек биосигнала.
Несмотря на заметно более высокую чувствительность обнаружения характеристических точек пульсовой волны, достигаемую при использовании на стадии предварительной обработки метода вейвлет-преобразований сигнала артериальной пульсации крови, необходимо заметить, что обработка биосигнала с помощью фильтра скользящего среднего обладает неоспоримым преимуществом в быстродействии и простоте алгоритмической реализации.
Таким образом, применение фильтра скользящего среднего может быть целесообразным в портативных системах оперативного мониторинга биосигнала артериальной пульсации крови при обработке в режиме реального времени, в то время как использование метода вейвлет-преобразо- ваний может быть реализовано при компьютерной offline обработке биомедицинских сигналов.
Список литературы Анализ методов обнаружения пульсовой волны сигнала артериальной пульсации крови
- Allen J. Photoplethysmography and its application in clinical physiological measurement//Physiological Measurement. 2007. Vol. 28. P. 1-39.
- Webster J.G. Design of Pulse Oximeters. The Medical Science Series, Taylor & Francis, 1997. 260 p.
- Калакутский Л.И., Манелис Э.С. Аппаратура и методы клинического мониторинга: Учебное пособие. Самара: СГАУ, 1999. 160 с.
- Fu T.H. Heart rate extraction from photoplethysmogram waveform using wavelet multi-resolution analysis//Journal of medical and biological engineering. 2008. Vol. 28 (4). P. 229-232.
- Strang G. Nguyen T. Wavelets and Filters Banks. Wellesley-Cambridge-Press, 1996. 490 p.
- Рангайян Р.М. Анализ биомедицинских сигналов. Практический подход [пер. с англ. Под ред. А.П. Немирко]. М.: Физматлит, 2007. 440 с.


