Анализ микробного пейзажа у пациентов с перипротезной инфекцией тазобедренного сустава
Автор: Ермаков А.М., Богданова Н.А., Матвеева Е.Л., Гасанова А.Г.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.31, 2025 года.
Бесплатный доступ
Введение. Концепция патогенеза перипротезной инфекции (ППИ) заключается в способности патогенных микроорганизмов колонизировать поверхности имплантатов, инфицирование которых осуществляется во время операции или гематогенной диссеминации бактерий. Это раскрывает причину неудовлетворительных результатов лечения ППИ. Микробиологическая идентификация вида возбудителя является золотым стандартом в диагностике ППИ. Цель работы — определить характер микробиологического пейзажа у пациентов c инфекцией, ассоциированной с ортопедическими имплантами тазобедренного сустава. Материалы и методы. Выполнен анализ ревизионных вмешательств (n = 294) по поводу ППИ тазобедренного сустава. В 2010–2021 гг. прооперировано 147 пациентов: 82 (56 %) мужчины и 65 (44 %) женщин. Свищевая форма ППИ отмечена у 105 (71 %), отек и гиперемия области послеоперационного шва — у 29 (20 %), открытые раны — у 13 (9 %) пациентов. Объектом исследования служили образцы костных и мягких тканей, полученные при иссечении инфицированного сустава, а также удаленные элементы эндопротеза. Посев производили на плотные питательные среды. Изучая бактериальные культуры, их идентифицировали общепринятыми методами, используя бактериологические анализаторы TB Expression (BioMerieux, Франция) и Walk Away 40 (США). Результаты. У подавляющего большинства пациентов (93 %) установлена этиология перипротезной инфекции, у остальных пациентов определить возбудителей не удалось. Бактериологический анализ выявил микробные ассоциации у 31 % больных, грамположительную микрофлору у 52 % и грамотрицательную микрофлору — у 10 %. Обсуждение. Наиболее распространенными видами микроорганизмов являются грамположительные бактерии с тенденцией роста резистентных штаммов. Выделение грамотрицательных бактерий при инфицировании суставов наблюдается значительно реже. Результаты демонстрируют изолированную грамнегативную культуру в 10 % случаев. Полимикробная инфекция является второй по частоте встречаемости (31 %) причиной инфицирования протезированного сустава. Микробные ассоциации встречаются в 10–45 % случаев, такая клиническая ситуация на старте лечения усложняет эмпирический выбор препаратов для антибактериальной терапии. Заключение. Микробиологическое исследование позволило установить этиологию инфекционного процесса у 93 % пациентов. Более чем в половине случаев (52 %) причиной возникновения имплантассоциированной инфекции являются гpампозитивная микрофлора, а 31 % случаев — и микробные ассоциации. Рецидивы инфекционного процесса в 41 % случаев отмечены у больных с полимикробным пейзажем.
Перипротезная инфекция, микрофлора, воспаление, эндопротезирование
Короткий адрес: https://sciup.org/142244807
IDR: 142244807 | УДК: [616.718.5/.6-007.24-089.227.84:004.9]-089.168 | DOI: 10.18019/1028-4427-2025-31-3-307-313
Analysis of the microbial landscape in patients with periprosthetic infection of the hip joint
Introduction The concept of the pathogenesis of periprosthetic joint infection (PJI) is the ability of pathogenic microorganisms to colonize the surfaces of implants, which are infected during the surgery or by hematogenous dissemination of bacteria. It causes poor results of PJI treatment. Microbiological identification of pathogen species is the gold standard in the diagnosis of PJI. Purpose To assess the etiology of the infectious process in patients with periprosthetic hip joint infection. Methods The study analyzed revision interventions (n = 294) for PJI of the hip joint performed within the period from 2010 throughout 2021. A total of 147 patients were operated on: 56 % (n = 82) were men and 4 % (n = 65) were women. At the time of hospitalization, the fistula PJI type was diagnosed in 71 % (n = 105); 20 % (n = 29) had edema and hyperemia of the postoperative suture area, and 9 % (n = 13) of cases had open wounds. The object of the study was bone and soft tissue samples obtained during excision of the infected material, as well as removed implant components. Cultures were grown on dense nutrient media. Bacterial cultures were identified by generally accepted methods using TB Expression (BioMerieux, France) and Walk Away 40 (USA) bacteriological analyzers. Results The etiology of periprosthetic infection was identified in the majority of patients (93 %), while pathogens could not be detected in the remaining cases. Bacteriological analysis revealed microbial associations in 31 % of patients, gram-positive microflora in 52 % of patients, and gram-negative microflora in 10 %. Discussion The most common types of microorganisms are gram-positive bacteria with a tendency for resistant strains to grow. Gram-negative bacteria are isolated in joint infection, but less frequently. The results demonstrate isolated gram-negative cultures in 10 % of cases. The second most common cause of periprosthetic joint infection is polymicrobial infection, which was detected in 31 % of cases. Microbial associations occurr in 10–45 % of cases; such a clinical situation at the start of treatment complicates the empirical choice of drugs for antibacterial therapy. Conclusions Microbiological study allowed identification of the etiology of the infectious process in 93 % of patients. In more than half of the cases (52 %), the cause of implant-associated infection is grampositive microflora, and in 31 % of cases are microbial associations. Reinfection was noted in 41 % of cases in polymicrobial patients.
Текст научной статьи Анализ микробного пейзажа у пациентов с перипротезной инфекцией тазобедренного сустава
Концепция патогенеза перипротезной инфекции (ППИ) строится на динамическом равновесии взаимодействия импланта и иммунной системы человека [1]. Засев имплантов патогенными микроорганизмами осуществляется либо во время операции, либо при гематогенной диссеминации бактерий [2–6]. Многие бактерии формируют биопленки на металлических и полиэтиленовых поверхностях компонентов эндопротезов [2, 7–9]. Эта способность микроорганизмов (так называемых сесильных форм) обеспечивает их персистенцию и выживаемость в госпитальной среде. Кроме того, бактерии, устойчивые к противомикробным препаратам, оказываются устойчивы к ним и в форме биопленок, и в этом виде они становятся наименее уязвимыми для действия антибиотиков. [10, 11]. Длительное заживление послеоперационных костных ран зачастую связано с проникновением патогенов и возникновением в костной ткани микроабсцессов, колонизацией остеобластов [12–14]. Вместе с тем, существуют трудноизлечимые виды возбудителей ППИ, такие как штаммы стафилококков, резистентные к антибактериальным препаратам трех и более классов, фторхинолон-резистентные и карбапенем-резистентные грамотрицательные микроорганизмы, грибковая микрофлора [2, 15, 16]. Все вышеперечисленные факторы раскрывают причину неудовлетворительных результатов лечения ППИ и подчеркивают необходимость определения этиологии патологического процесса.
Микробиологическая диагностика осуществляется методом выделения и идентификации возбудителя после забора материала из нескольких наиболее контаминированных пораженных тканей [17]. Для деструкции биопленки осуществляют обработку ультразвуком удаленных компонентов эндопротеза, с этой же целью возможно применение раствора дитиотpеитола [18–21]. Время инкубации био-пленочных бактерий составляет 14–21 день, что ведет к их более высокой выживаемости, в сравнении с моноинфекциями, у которых инкубационный период составляет 5–14 суток [22].
Цель работы — определить характер микробиологического пейзажа у пациентов c инфекцией, ассоциированной с ортопедическими имплантами тазобедренного сустава.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проведено на материале, полученном от 147 пациентов (56 % мужчин и 44 % женщин) после ревизионных операций по поводу перипротезной инфекции тазобедренного сустава. Возраст пациентов составил (54,7 ± 12,7) г. Число образцов исследования — 294. У 105 (71 %) пациентов наблюдали свищевую форму ППИ сустава, у 29 (20 %) отмечали гиперемию, отек в области послеоперационного шва, в 13 (9 %) случаях имелись открытые раны. У 28 (19 %) пациентов наблюдали острое течение инфекционного процесса (продолжительность инфекции в среднем 21,8 дн., Me — 22; 95 % ДИ от 19,7 до 24,0) и у 119 (81 %) — хроническое (продолжительность инфекции в среднем 26,3 мес., Me — 13; 95 % ДИ от 20,5 до 32,3).
В 114 (78 %) случаях гнойно-воспалительное осложнение развилось после первичного эндопротезирования и лишь в 33 (22 %) случаях — после ревизионного вмешательства. Лечебный процесс в значительной степени усложняло тяжелое коморбидное состояние пациентов по шкале ASA ( англ .: American Society of Anesthesiology), выявленное у 82 (56 %) больных.
Объектом исследования служили образцы костных и мягких тканей, полученных при иссечении инфицированного сустава, а также удаленные элементы эндопротеза пациентов с ППИ тазобедренного сустава. На основе рекомендованных методов, посев производили на плотные питательные среды (желчно-солевой агаp, агаp Cабуpо, среда Левина, колумбийский агаp и питательный агаp с 5 % бараньей крови). Образцы помещали в термостат и инкубировали при 37 °C в течение 24–48 ч. Подсчитывали количество колоний в чашках Петри, полученный результат переводили в десятичный логарифм, выражая в КОЕ/мл. Для создания анаэробных условий использовали газогенераторные пакеты «Анаэ-рогаз», выращивая грибковую флору в течение 5 сут. при температуре 30 °С.
Изучая бактериальные культуры, их идентифицировали общепринятыми методами, а также используя бактериологические анализаторы TB Expression (BioMerieux, Франция) и Walk Away 40 (США).
Статистическая обработка данных выполнена с помощью пакета программ Statistica for Windows, v. 13.0 (Stat Soft Inc., США) и Microsoft Excel (Microsoft, США). Для характеристики микробиологического спектра выполнены процентные расчеты. Описательные статистические результаты представляли собой среднее значение ± стандартная ошибка (SЕ) для количественных данных. Распределение данных анализировали с помощью тестов нормальности Шапиро – Уилка и Колмогорова – Смирнова. Сравнение между несвязанными выборками проводили с использованием критерия Манна – Уитни. Различия считали значимыми при p < 0,05.
РЕЗУЛЬТАТЫ
В интраоперационном биологическом материале выделено 196 штаммов патогенных микроорганизмов, спектр которых представлен на рис. 1. Доминирование семейства Staphyloсoссaсeae было отмечено в 64 % случаев, значительную часть выделенных штаммов составляли также Enterobacteriaсeae (10 %), Enteroсoссaсeae (9 %) и Рseudomonadaсeae (9 %).
В 39 наблюдениях (20 %) выявлены MRSA и MRSE, в 17 (9 %) — Р. aeruginosa (рис. 1).
Идентификация микроорганизмов для верификации таксономической принадлежности патогенных бактерий показала, что среди выделенных и идентифицированных бактерий основную часть микрофлоры составило семейство Staphylococcaceae с преобладанием штаммов Staphylococcus aureus , Staphylococcus epidermidis и Staphylococcus saprophyticus .
У 137 пациентов (93 %) микрофлора идентифицирована, однако у 10 пациентов идентифицировать возбудителей не удалось. У 76 пациентов (52 %) определяли изоляты грамположительной микрофлоры, у 15 пациентов (10 %) — грамотрицательная микрофлора в монокультуре. У 46 пациентов (31 %) наблюдали наличие микробных ассоциаций (рис. 2).
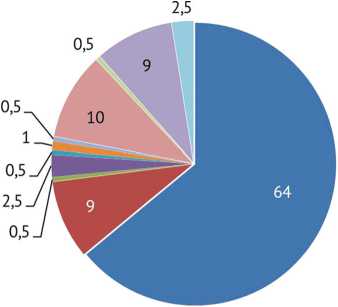
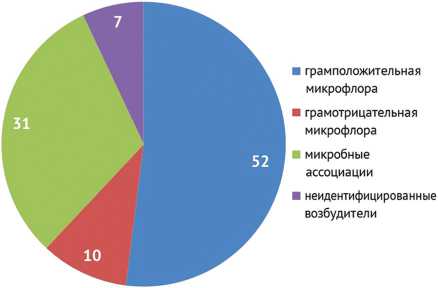
Рис. 2. Выявленные микрофлоры
-
■ Staphylococcaceae
-
■ Enterococcaceae
-
■ Actinomycetaceae
-
■ Corynebacterioceae
-
■ Micrococcaceae
-
■ Peptostreptococcaceae
: i Streptococcaceae
-
■ Entero bacteriaceae
Vibrionoceae
-
■ Pseudomonodaceoe
Moraxellaceae
Рис. 1. Спектр возбудителей ППИ тазобедренного сустава
Следует отметить, что в 22 % случаев, т.е. у 17 из 76 пациентов с изолированной грамположительной микрофлорой (доминирующим штаммом золотистого, а также эпидермальным стафилококком) произошел рецидив гнойно-воспалительного процесса. Повторное нагноение у 15 пациентов с грамо-трицательной микрофлорой (представленной преимущественно штаммами Pseudomonas aeruginosa ) отмечено только в двух случаях (13 %). Наиболее часто в составе полимикробной инфекции выделялись семейства Staphylococcaceae (78 %), Enterobacteriaceae (28 %), Enterocоccaceae (26 %), Pseudomоnadaceae (15 %) и Moraxellaceae (6,5 %).
Очевидно в результате предшествующей терапии антибактериальными препаратами, у пациентов с ППИ достаточно распространены и занимают второе место после грампозитивной микрофлоры по-лимикробные ассоциации. Микробная ассоциация из двух агентов выявлена у 34 пациентов (74 %), из трех агентов — у 11 (24 %). Рост четырех микроорганизмов выявлен у одного больного.
Общее количество пациентов с рецидивом инфекционного процесса при наличии микробных ассоциаций составило 19 человек (41 % наблюдений), что было самым высоким числом осложнений. С целью купирования воспалительного процесса шести пациентам с рецидивированием инфекции проводили повторную хирургическую обработку, восьми пациентам осуществили замену спейсера, остальным — резекционную артропластику.
При не идентифицированном составе микрофлоры у двух из 10 пациентов произошло повторное нагноение в период нахождения в стационаре. Этим пациентам проведено двухэтапное ревизионное вмешательство.
Сравнительная оценка результатов интраоперационного исследования микробиологического спектра возбудителей у пациентов с острой и хронической формами имплант-ассоциированной инфекции представлена на рис. 3.
В структуре оперативных вмешательств по поводу ППИ у 28 (19 %) пациентов манифестация инфекции составила 22 дн. (МКИ-17 — 27,5 дн.), а у 119 пациентов продолжительность гнойного процесса составила 26 мес. (8–35 мес.).
В структуре микробного пейзажа пациентов с острой и хронической формами инфекционного процесса вклад изолированной грамположительной (44 % и 55 %) и грамотрицательной (7 % и 10 %) микрофлоры был сопоставим (рис. 3). Однако отмечено, что микробные ассоциации и MRSE штаммы статистически значимо ( p < 0,05) чаще встречались у пациентов с острой формой инфекционного процесса. Метициллин-резистентные штаммы эпидермального стафилококка являлись причиной развития острого инфекционного процесса практически в каждом третьем случае (29 %). В целом, рецидив случился у 7 (25 %) пациентов с острым и у 39 (33 %) пациентов с хроническим вариантом течения инфекционного процесса ППИ.
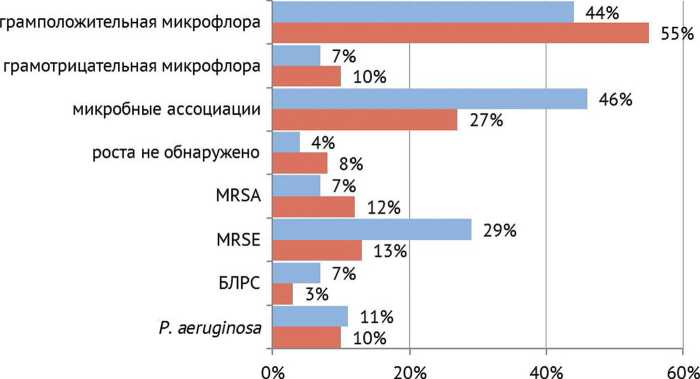
■ острая форма ■ хроническая форма
Рис. 3. Микробиологическая характеристика посевного материала больных с острой и хронической формами ППИ тазобедренного сустава
ОБСУЖДЕНИЕ
Оценивая микробный пейзаж пациентов с имплант-ассоциированной инфекцией, следует заметить, что клетки микроорганизмов, особенно в условиях биопленок, приобретают все более выраженную резистентность к противомикробным препаратам. Это, в свою очередь, требует новых подходов к оценке рисков и лечению инфекционного процесса, развившегося после эндопротезирования тазобедренных суставов. В течение всего срока нахождения в организме ортопедического импланта сохраняется риск развития ППИ, основными возбудителями которой являются грамположительные бактерии (чаще всего золотистый и эпидермальный стафилококки), характеризующиеся ростом резистентных штаммов [23–26]. Отсутствие мишеней для проявления действия антимикробной терапии у многих грамположительных микроорганизмов приводит к отсутствию контроля над резистентными штаммами, вызывая закономерную тревогу лечащих врачей, что нашло свое отражение, как в отечественных, так и в зарубежных публикациях [27–30].
Второй по значимости этиологической причиной нагноения эндопротезов является полими-кробная инфекция. Частота встречаемости полимикробной инфекции имеет тенденцию к росту, мы наблюдали ее в 31 % случаев. Полимикробная инфекция у наших пациентов представлена предсказуемым спектром: Staphylococcaceae — 78 %, Enterobacteriaceae — 28 %, Enterococcaceae — 26 %, Pseudomonadaceae — 15 % и Moraxellaceae — 6,5 %. Такая клиническая ситуация усложняет выбор адекватного режима антибиотикотерапии и, зачастую, приводит к худшим исходам в сравнении с ППИ с мономикробной микрофлорой, что отмечалось и в литературных источниках [31, 32]. Ряд исследователей указывают на необходимость учитывать экспрессию патогенности микроорганизмов, а также их способность к биопленкообразованию [33–37], в связи с чем определение спектра возбудителей ППИ приобретает большое значение.
У больных в нашем исследовании не выявлена грибковая микрофлора, но в зарубежных публикациях уделяется внимание грибковым инфекциям, которые встречаются в 1–4 % случаев, подавляющую их часть (80 %) составляют грибы рода Candida [38, 39]. Данная проблема характерна для иммуноком-проментированных больных [40, 41].
Проведенное микробиологическое исследование перипротезных тканей выявило этиологию инфекционного процесса в подавляющем большинстве (93 %) исследованных случаев. Наиболее частой причиной неидентификации возбудителя, очевидно, являлся прием антибактериальных препаратов до обнаружения патогена.
ЗАКЛЮЧЕНИЕ
Преимущественной причиной развития ППИ являются грампозитивная микрофлора и микробные ассоциации. Достоверные различия у больных с острым и хроническим типом ППИ отмечались по уровню микробных ассоциаций и присутствию штаммов MRSE c трендом на доминирование в группе с острым характером воспаления.


