Анализ нарушений функции гипофизарно-гонадной регуляции у пациентов с наличием новообразований яичек
Автор: Холбобозода Р.Ф., Костин А.А., Воробьев Н.В., Толкачев А.О., Крашенинников А.А., Кульченко Н.Г., Монаков Д.М.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Онкоурология
Статья в выпуске: 1 т.17, 2024 года.
Бесплатный доступ
Введение. Гипоталамо-гипофизарно-гонадная ось (ГГГО), является важнейшей частью гормональной системы, которая контролирует функцию яичек у мужчин. Известно, что новообразования яичек (НЯ) могут нарушать регуляцию ГГГО из-за возникновения гормонального дисбаланса. Однако изменения ГГГО у больных с НЯ мало изучены, особенно до начала лечения.
Новообразования яичек, гипоталамо-гипофизарно-гонадная ось, гормональный статус, тестостерон, гипогонадизм, гормональный дисбаланс, крипторхизм, курение, индекс массы тела
Короткий адрес: https://sciup.org/142241818
IDR: 142241818 | DOI: 10.29188/2222-8543-2024-17-1-68-74
Analysis of disorders of pituitary-gonadal regulation in patients with testicular neoplasms
Introduction. The hypothalamic-pituitary-gonadal axis (HPG) is the most important part of the hormonal system that controls testicular function in men. It is known that testicular neoplasms (TN) can disrupt the regulation of HPG due to the occurrence of hormonal imbalance. However, changes in HPG in patients with TN have been little studied, especially before the start of treatment.
Текст научной статьи Анализ нарушений функции гипофизарно-гонадной регуляции у пациентов с наличием новообразований яичек
экспериментальная и клиническая урология № 1 2024
Новообразования яичка (НЯ) наиболее часто встречается у лиц молодого возраста [1]. Это заболевание возникает в пиковый период репродуктивной жизни, в ключевой период для карьеры и семейной жизни.
Подход к активному лечению у этих пациентов начинается с орхифуникулэктомии (ОФЭ), что позво ляет удалить первичную опухоль и получить гистоло гическую верификацию заболевания. Приблизительно 50% больных в дальнейшем нуждаются в дополнитель ной лучевой терапии (ЛТ) или полихимиотерапии (ПХТ) при диссеминированном заболевании [2]. По данным литературы, эти методы лечения увеличивают риск дефицита тестостерона (ДТ) [3-6]. Однако другие авторы подчеркивают, что риск ДТ у этих пациентов не зависит от лечения, а связан с тестикулярным мик ролитиазом и тестикулярной атрофией, которые при сутствуют у таких пациентов еще до лечения [3, 7]
В настоящее время мало что известно об уровне половых гормонов в сыворотке крови у мужчин с НЯ до лечения. В работах, посвященных этому вопросу, указывается, что концентрации этих гормонов в сыво ротке крови аналогичны таковым у здоровых людей [8]. Другие исследователи считают, что при использовании комбинированной оценки лютенизирующего гормона (ЛГ) и общего тестостерона (Т) более чем у 25% паци ентов с НЯ отмечаются изменения в гипоталамо-гипо физарно-гонадной оси (ГГГО) [9]. Это состояние характеризуется повышенным уровнем ЛГ, в то время уровень Т либо нормальный, либо сниженный.
Таким образом, необходимы дополнительные ис следования для оценки ГГГО у мужчин новообразова нием в яичке.
Цель исследования. Оценить степень гормональ ных нарушений, влияющих на ГГГО у мужчин с НЯ до лечения.
МАТЕРИАЛЫ И МЕТОДЫ
Характеристика пациентов
За период с декабря 2021 по март 2023 г. на базе МНИОИ им. П.А. Герцена – филиала НМИЦ радиоло гии в отделении урологии обратились 49 мужчин с НЯ.
Пациенты были обследованы по стандартной ме тодике (компьютерная томография органов грудной клетки,брюшной полости и забрюшинного простран ства с внутривенным контрастированием,магнитно резонансная томография/ультразвуковое исследование (МРТ/УЗИ) органов мошонки, определение уровня он комаркеров – альфа-фетопротеина (АФП), бета-хорио нического гонадотропина (β-ХГЧ), лактатдегидро геназы (ЛДГ). После обследования и при подозрении на злокачественное новообразование всем пациентам была выполнена орхифуникулэктомия для гистологи ческой верификации опухоли и определения дальней шей тактики лечения.
В качестве факторов, влияющих на гормональный статус пациентов до хирургического лечения, мы оце нивали такие параметры как: возраст, степень ожире ния, курение, объем яичек, размер опухолевого образования, отягощенный онкологический семейный анамнез, наличие хирургического вмешательства в анамнезе по поводу крипторхизма, микролитиаз яичек и уровень β-ХГЧ. При этом размер опухоли, объем и наличие микролитиаза яичек определяли по результа там методов лучевой диагностики (МРТ/УЗИ).
Гормональный анализ
Забор крови для определения уровня гонадотроп ных (ЛГ, ФСГ, ПРЛ) и стероидных гормонов (общий те стостерона, эстрадиол), а также глобулин-связыва-ющих половых гормонов (ГСПГ) производился натощак между 8 и 10 часами утра. Анализ уровня гормо нов в сыворотке выполнена на оборудовании Beckman Coulter UniCel DxI 800, Immulite 2000XPi.
Пороговым значением, позволяющим разграни чить нормальное состояние и потенциальный ДТ, счи тали уровень 8 нмоль/л для общего тестостерона (Т) сыворотки крови. При уровне общего Т от 8 до 1 2 нмоль/л учитывали уровень ГСПГ с дальнейшим рас четом уровня свободного Т по формуле (описанной в работе A. Vermeulen и соавт), нижняя граница нормы которого принята <243 пмоль/л [10].
Для дифференциации первичной и вторичной форм гипогонадизма, а также выявления субклиниче ского гипогонадизма определяли уровень гонадотроп ных гормонов (ЛГ, ФСГ, пролактин) в сыворотке крови.
Так как повышенный уровень хорионического гонадотропина человека для мужчин (β-ХГЧ) можно наблюдать при НЯ [11 ], а данный гормон оказывает значительное влияние на гормональный уровень паци ента,то по этой причине мы разделили пациентов на две группы: 1 группа – с высоким уровнем β-ХГЧ
(n=19); 2 группа – с нормальным уровнем β-ХГЧ (n=30).
Методы статической обработки данных
Статистический анализ проводился с использова нием пакета программы IBM SPSS v.27 и StatTech v. 3.1.6 (разработчик – ООО «Статтех», Россия).
Количественные показатели, имеющие нормаль ное распределение,описывались с помощью средних арифметических величин (M) и стандартных отклоне ний (SD), границ 95% доверительного интервала (95% ДИ). В случае отсутствия нормального распределения количественные данные описывались с помощью ме дианы (Me) и нижнего и верхнего квартилей (Q1 – Q3). Категориальные данные описывались с указанием аб солютных значений и процентных долей.
Сравнение двух групп по количественному пока зателю, имеющему нормальное распределение, при неравных дисперсиях выполнялось с помощью t-кри терия Уэлча. Сравнение двух групп по количествен ному показателю, распределение которого отличалось от нормального, выполнялось с помощью U-критерия Манна-Уитни.
Направление и теснота корреляционной связи между двумя количественными показателями оцени вались с помощью коэффициента ранговой корреля ции Спирмена (при распределении показателей, отличном от нормального).
Статистически значимыми различия считали при уровне p ≤0,05.
РЕЗУЛЬТАТЫ
Клиническая характеристика обследуемых паци ентов представлена в таблице 1. Среди всей наблюдае мой когорты мужчин большая часть пациентов (81,6%), была молодого возраста, остальные были лица среднего возраста. Повышенный индекс массы тела
Таблица 1. Клиническая характеристика пациентов с НЯ (n=49)
Table 1. Clinical characteristics of patients with testicular tumors (n=49)
|
Показатели Indicators |
M ± SD / Me |
95% ДИ / Q ₁ – Q ₃ |
|
Возраст, (лет)/Age (years) |
34 ± 10 |
32 – 37 |
|
Вес, (кг)/Weight (kg) |
83 ± 18 |
78 – 88 |
|
Рост, (см)/Height (cm) |
180 ± 7 |
178 – 182 |
|
Размер опухоли, (см)/Tumor size (cm) |
3,88 ± 2,07 |
3,28 – 4,47 |
|
Объем пораженного яичка, (см3) Affected testicle volume (cm3) |
31,80±11,9 |
20,10 – 62,40 |
|
Объем здорового ячика, (см3) Healthy testicle volume (cm3) |
16,10±2,4 |
12,35 – 19,25 |
|
Общий объем яичек, (см3) Total testicular volume (cm3) |
49,95±9,6 |
31,62 – 77,17 |
был лишь у 6 (12,2%) мужчин. Операции в области мо шонки в анамнезе имелись у 11 (22,4%) человек. Боль шая часть пациентов имели вредную привычку – табакокурение (32; 65,3%).
По данным лабораторных исследований,до лече ния уровень β-ХГЧ был высоким у 19 (38,8%) пациен тов, и у 30 (61,2%) пациентов с НЯ он был в пределах референсных значений. Лабораторные признаки дефи цита тестостерона (ДТ) наблюдали у 15 (30,6%) из 49 пациентов, что 86,7% случаев приходиться на долю па циентов без повышенного уровня β-ХГЧ.
Гонадотропные гормоны: ЛГ, ФСГ, пролактин
Концентрация ЛГ в крови была ниже границы нормы у 18 (36,7%), в пределах референсных значений у 23 (46,9%) и выше границы нормы у 8 (16,3%) паци ентов с НЯ (рис. 1).
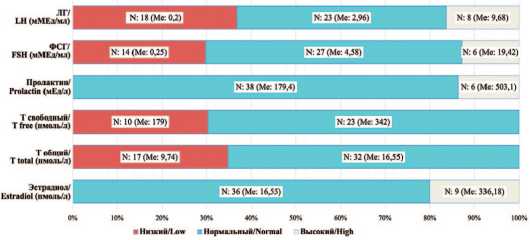
Рис. 1. Распределение пациентов с новообразованием яичка в зависимости от уровней гормонов.
Fig. 1. Distribution of patients with testicular tumors depending on hormone levels.
Были установлены существенные различия при сопоставлении уровня ЛГ в зависимости от уровня β ХГЧ ( p <0,001) и наличие крипторхизма ( p =0,023). Вы явленные различия объясняются более низким уровнем ЛГ у пациентов с высокими уровнями β-ХГЧ по сравнению с пациентами с отрицательными уров нем данного онкомаркера (рис. 2). Напротив, высокий уровень ЛГ наблюдался у пациентов с наличием крип торхизмом в анамнезе.
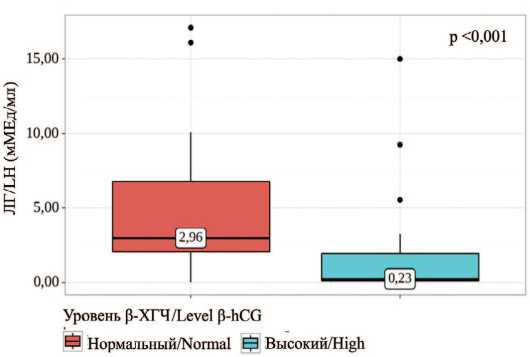
Рис. 2. Сравнение значений ЛГ в зависимости от уровня β-ХГЧ
Fig. 2. Comparison of LH values depending on β-hCG levels
Концентрация ФСГ в крови была низкой у 1 4 (28,6%), нормальной у 29 (59,2%) и повышенной у 6 (12,2%) пациентов с НЯ (рис. 1).
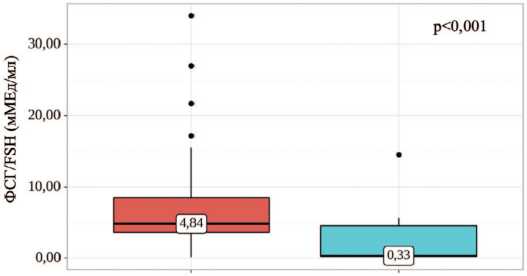
При анализе уровня ФСГ в зависимости от β-ХГЧ и наличия крипторхизма, также были выявлены суще ственные различия ( p <0,001). Высокий уровень β-ХГЧ был сопряжен со снижением уровня ФСГ в крови (рис. 3). Напротив, наличие крипторхизма в анамнезе сопровождалось повышением уровня данного гона дотропного гормона в крови.
Уровень Р-ХГЧ /Level p-hCG
S Нормальный/Nonnal $ Высокий/High
Рис. 3. Сравнение значений ФСГ в зависимости от уровня β-ХГЧ
Fig. 3. Comparison of FSH values depending on β-hCG levels
Уровень пролактина был высоким у 6 (1 2,2%), нормальным – у 43 (87,8%) пациентов. Однако при чинно-следственная связь установлена не была.
При корреляционном анализе выявлена связь между уровнем ЛГ ( p =-0,351; p =0,014), ФСГ ( p =-0,3; p =0,041) и размер опухолевого образования. При ана лизе зависимости уровня гонадотропных гормонов от возрастной группы, курения и ожирения статические значимые различия получены не были ( p >0,05).
Стероидные гормоны: общий тестостерон, свободный тестостерон, эстрадиол
Концентрация общего Т ниже 8 нмоль/л обнару жена у 3 (6,1%) пациентов. Значения тестостерона от 8-12 нмоль/л выявлены у 14 (28,6%) пациентов. Значения тестостерона выше 12,1 нмоль/л (>3,46 нг/мл) зарегистрированы у 32 (65,3%) пациентов.
Уровень свободного Т ниже 243 пмоль/л отмечался у 10 (30,3%), в пределах референсных значений – у 23 (69,7%) пациеннтов.
Уровень эстрадиола был высоким у 9 (20%), нормальным у 36 (80%) пациентов.
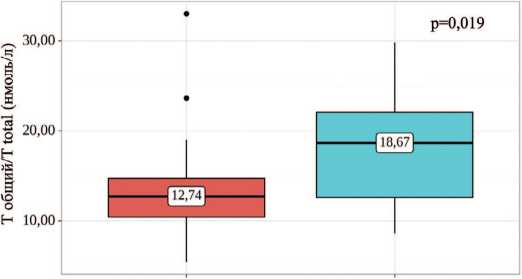
Согласно полученным данным,при сопоставлении уровня общего Т, свободного Т и эстрадиола (E2) с бета-ХГЧ нам удалось установить статистически значимые различия ( p =0,019, p =0,01; p =0,003) (рис. 4-6). Данное различие было обусловлено наиболее высокой концентрацией половых гормонов в крови у пациентов с уровнем β-ХГЧ выше референсного значения.
Уровень р-ХГЧ/Level P-hCG
$ Нормальный/Normal $ Высокий/High
Рис. 4. Сравнение значений общего тестостерона в зависимости от уровня β-ХГЧ
Fig. 4. Comparison of total testosterone values depending on β-hCG levels
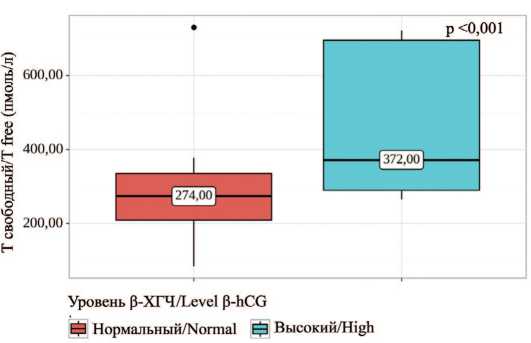
Рис. 5. Сравнение значений свободного тестостерона в зависимости от уровня β-ХГЧ
Fig. 5. Comparison of free testosterone values depending on β-hCG levels
Уровень Р-ХГЧ/Level p-hCG
$ Нормальный/Normal ^ Высокий/High
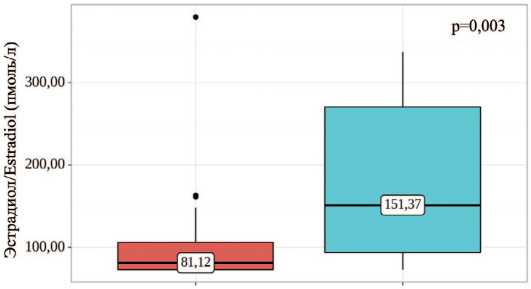
Рис. 6. Сравнение значений эстрадиола в зависимости от уровня β-ХГЧ
Fig. 6. Comparison of estradiol values depending on β-hCG levels
Также при анализе общего Т, свободного Т и Е2 в зависимости от наличия орхипексии в анамнезе,были установлены статистически значимые различия ( p =0,016, p =0,022, p =0,034 соответственно).
При оценке связи размера опухоли и Е2 была установлена умеренная прямая связь.
При анализе зависимости уровня стероидных гормонов от возраста пациентов,употребления ими табачных изделий, лишней массы тела статические значимые различия не были получены ( p >0,05).
ОБСУЖДЕНИЕ
В настоящее время важными целями при НЯ яв ляются минимизация последствий самого заболевания и его лечения для улучшения качества жизни (КЖ) па циента в долгосрочной перспективе. Одним из наибо лее важных аспектов КЖ у молодых мужчин,проле-ченных по поводу НЯ, является сохранение функции яичек (сперматогенез/стероидогенез).
В течение многих десятилетий наибольшее вни мание уделялось нарушению фертильности у пациен тов с НЯ, разработаны меры профилактики [12, 13]. В последнее время появляется все больше данных, сви детельствующих о том,что у этой группы пациентов также повышен риск развития гипогонадизма,связан ного с лечением [14, 15]. В то же время на сегодняшний день не существует научно обоснованных рекоменда ций для практикующих врачей по скринингу гипого надизма у пациентов с НЯ [16].
По мнению других специалистов, развитие гипо гонадизма у этих пациентов не зависит от методов лечения, а связано с тестикулярным микролитиазом и тестикулярной атрофией, которые присутствуют у па циентов еще до начала лечения [17, 18].
В многочисленных исследованиях изучали гормо нальный фон у мужчин с НЯ до лечения,и лишь не многие из них касались факторов риска, приводящих к гипогонадизму.
P.J. Wiechno и соавт. проанализировали уровень общего Т у 62 пациентов до ОФЭ и у 120 пациентов через 1 месяц после ОФЭ. Пороговым значением для ДТ считался уровень общего Т ниже 8 нмоль/л. Ав торы пришли к выводу о том, что 5% пациентов имели ДТ до ОФЭ по сравнению с 16% пациентов через месяц после ОФЭ [19]. Это свидетельствует о том, что у па циентов с НЯ до начала активного лечения уже име ется нарушения гормонального статуса.
P.M. Petersen и соавт. оценили качество спермы и репродуктивные гормоны (ЛГ, ФСГ, тестостерон, эстрадиол, ГСПГ) у 83 мужчин с НЯ перед ОФЭ. ДТ определялся как уровень ЛГ выше 10 МЕ/л и/или уро вень общего Т ниже 10 нмоль/л. Проанализировав ре зультаты, специалисты не наблюдали нарушения функции клеток Лейдига у этих пациентов.С другой стороны, авторы почеркнули, что из-за высокого уровня β-ХГЧ, который в свою очередь стимулирует клетки Лейдига,сложно исключить такое нарушение [20].
В литературе есть указания на то, что ЛГ и β-ХГЧ являются морфологически сходными полипептид ными гормонами, стимулирующими одни и те же ре цепторы [7] Этот факт объясняет разрушающее действие высоких концентраций бета-ХГЧ на ГГГО. Другие исследователи также предполагают, что кон центрация β-ХГЧ у больных раком яичка коррелирует с концентрацией тестостерона, пролактина, эстра диола и гонадотропинов [21].
Учитывая данную закономерность, M. Bandak и соавт. оценили функцию клеток Лейдига до и после ОФЭ у пациентов с 1 стадии НЯ [8]. До ОФЭ не было значительных различий в уровнях ЛГ и Т между паци ентами с нормальными уровнями β-ХГЧ и контроль ной группой. Однако, при оценке соотношении ЛГ/Т более чем у 30% пациентов имеется дисфункция клеток Лейдига. Кроме того, пациенты с повышенным уров нем β-ХГЧ перед ОФЭ имели заметное нарушение ги пофизарно-гонадной оси (ГГО) на исходном уровне с подавлением ЛГ, повышением T и E2 по сравнению с контрольной группой. Эти выводы согласуются с пред положением P.M. Petersen и соавт. [19].
При дальнейшем изучении этой проблемы в дру гом своем исследовании M. Bandak и соавт. показали, что примерно у четверти пациентов с НЯ,у которых нормальный уровень бета-ХГЧ, дисфункция клеток Лейдига наблюдается уже до лечения. Также, была об наружена значимая корреляционная связь между дис функцией клеток Лейдига и размером опухоли, наличием неоплазии зародышевых клеток in situ и воз растом [9].
J. Eberhard и соавт. изучали факторы риска гипо гонадизма у 143 пациентов с НЯ после лечения.Ав торы подчеркивали,что у мужчин наличие микро-литиаза яичка до лечения является сильным предик тором последующего гипогонадизма [3]. Однако в этих работах есть свои недостатки: небольшое количество пациентов,проблемы с измерением уровня тестосте рона и различные методики в определении ДТ.
Анализ отечественных литературных источников показал, что в России до сих пор не проводились по добного рода наблюдения. Полученные нами резуль таты исследования демонстрируют, что у трети пациентов наблюдались лабораторные признаки ДТ преимущественно у пациентов (в 87% случаев) с нор мальным уровнем β-ХГЧ. У мужчин c высоким уров нем β-ХГЧ мы наблюдали изменение ГПГ с подав лением уровня гонадотропинов (ЛГ, ФСГ) и повыше нием общего/свободного T и эстрадиола, что согласу ется с результатами исследования M. Bandak и соавт. [9] и P.M. Petersen и соавт. [19]. Однако, НЯ не позво ляет однозначно оценить гонадную функцию исходно что требует дальнейшего наблюдения за этой когортой пациентов с последующей повторной оценкой гормо нального статуса после активного лечения и нормали зации опухолевого маркера (β-ХГЧ).
ЗАКЛЮЧЕНИЕ
Таким образом, результаты проведенного нами исследования демонстрируют, что функция ГГГО на рушена у 30% пациентов с НЯ до лечения. У одной трети мужчин наблюдались лабораторные признаки ДТ. Требуется проведение дальнейших исследований с включением большего числа пациентов для выработки практических рекомендаций.
ПШАТШ/ШЕШШ
ИТЕРАШАШРЕЕЕШЕ
Сведения об авторах:
Холбобозода Р.Ф. – аспирант кафедры урологии и оперативной нефрологии с курсом онкоурологии РУДН; Москва, Россия;
Костин А.А. – д.м.н., профессор, член-корр. РАН, первый проректор-проректор по научной работе РУДН, заведующий кафедрой урологии и оперативной нефрологии с курсом онкоурологии Медицинского института ФГАОУ ВО «Российский университет дружбы народов»; Москва, Россия; РИНЦ Author ID 193454,
Воробьев Н.В. – к.м.н., заместитель по хирургии директора МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России, врач-уролог, доцент кафедры онкологии,радиотерапии и пластической хирургии ФГАОУ ВО «Первый Московский государственный медицинский университет им.И.М.Сеченова» Министерства здравоохранения Российской Федерации (Сеченовский университет); Москва, Россия;
РИНЦ Author ID 195018,
Толкачев А.О. – младший научный сотрудник отдела онкоурологии МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России; Москва, Россия; РИНЦ Аuthor ID 804977,
Крашенинников А.А. – к.м.н., заведующий отделением онкоурологии МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России; Москва, Россия; РИНЦ Аuthor ID 788905,
Кульченко Н.Г. – к.м.н., врач-уролог, врач ультразвуковой диагностики, доцент кафедры анатомии человека Медицинского института ФГАОУ ВО «Российский университет дружбы народов», Москва, Россия; РИНЦ Author ID 193454,
Монаков Д.М. – к.м.н., старший научный сотрудник отдела онкоурологии НМИЦ хирургии им. А. В. Вишневского; ассистент кафедры урологии и оперативной нефрологии с курсом онкоурологии РУДН; Москва, Россия; РИНЦ Author ID 995385,
Вклад авторов:
Холбобозода Р.Ф. – сбор и обработка материала, написание текста, 40%
Костин А.А. – дизайн исследования, 10%
Воробьев Н.В. – сбор и обработка материала, 10%,
Толкачев А.О. – сбор и обработка материала, оформление таблиц, 10%
Крашенинников А.А. – статистическая обработка материала, 10%
Кульченко Н.Г. – научное редактирование текста, работа с литературными источниками, 10%
Монаков Д.М. – написание текста, 10%
Конфликт интересов: Авторы заявляют об отсутствии конфликта интересов.
Финансирование: Исследование проведено без финансовой поддержки.
Статья поступила: 17.12.23
Результаты рецензирования: 29.01.24
Исправления получены: 02.02.24
Список литературы Анализ нарушений функции гипофизарно-гонадной регуляции у пациентов с наличием новообразований яичек
- Ghoreifi A, Djaladat H. Management of primary testicular tumor. Urol Clin North Am 2019;46(3):333-9. https://doi.org/10.1016/j.ucl.2019.04.006.
- Chovanec M, Cheng L. Advances in diagnosis and treatment of testicular cancer.
- BMJ 2022;379:e070499. https://doi.org/10.1136/bmj-2022-070499.
- Eberhard J, Ståhl O, Cwikiel M, Cavallin-Ståhl E, Giwercman Y, Salmonson EC, et al. Risk factors for post-treatment hypogonadism in testicular cancer patients. Eur J Endocrinol 2008;158(4):561-70. https://doi.org/10.1530/EJE-07-0684.
- Huddart RA, Norman A, Moynihan C, Horwich A, Parker C, Nicholls E, Dearna- ley DP. Fertility, gonadal and sexual function in survivors of testicular cancer. Br J Cancer 2005;93(2):200-7. https://doi.org/10.1038/sj.bjc.6602677.
- Ondrusova M, Spanikova B, Sevcikova K, Ondrus D. Testosterone deficiency and bone metabolism damage in testicular cancer survivors. Am J Mens Health 2018;12(3):628-33. https://doi.org/10.1177/1557988316661986.
- La Vignera S, Cannarella R, Duca Y, Barbagallo F, Burgio G, Compagnone M, et al. Hypogonadism and sexual dysfunction in testicular tumor survivors: a systematic review. Front Endocrinol (Lausanne) 2019;10:264. https://doi.org/10.3389/fendo.2019.00264.
- Pühse G, Wachsmuth JU, Kemper S, Husstedt IW, Evers S, Kliesch S. Chronic pain has a negative impact on sexuality in testis cancer survivors. J Androl 2012;33(5):886-93. https://doi.org/10.2164/jandrol.110.012500.
- Bandak M, Aksglaede L, Juul A, Rørth M, Daugaard G. The pituitary-Leydig cell axis before and after orchiectomy in patients with stage I testicular cancer. Eur J Cancer 2011;47(17):2585-91. https://doi.org/10.1016/j.ejca.2011.05.026.
- Bandak M, Jørgensen N, Juul A, Lauritsen J, Gundgaard Kier MG, Mortensen MS, et al. Preorchiectomy Leydig cell dysfunction in patients with testicular cancer. Clin Genitourin Cancer 2017;15(1):e37-e43. https://doi.org/10.1016/j.clgc.2016.07.006.
- Vermeulen A, Verdonck L, Kaufman JM. A Critical Evaluation of Simple Methods for the Estimation of Free Testosterone in Serum. J Clin Endocrinol Metab 1999;84(10):3666-72. https://doi.org/10.1210/jcem.84.10.6079.
- Duffy MJ. Clinical uses of tumor markers: a critical review. Crit Rev Clin Lab Sci 2001;38(3):225-62. https://doi.org/10.1080/20014091084218.
- Djaladat H, Burner E, Parikh PM, Beroukhim Kay D, Hays K. The association between testis cancer and semen abnormalities before orchiectomy: a systematic re- view. J Adolesc Young Adult Oncol 2014;3(4):153-9. https://doi.org/10.1089/ jayao.2014.0012.
- Sineath RC, Mehta A. Preservation of fertility in testis cancer management. Urol Clin North Am 2019;46(3):341-51. https://doi.org/10.1016/j.ucl.2019.04.010.
- Ni FD, Hao SL, Yang WX. Molecular insights into hormone regulation via sig- naling pathways in Sertoli cells: with discussion on infertility and testicular tumor. Gene 2020;753:144812. https://doi.org/10.1016/j.gene.2020.144812.
- Oldenburg J. Hypogonadism and fertility issues following primary treatment for testicular cancer. Urol Oncol 2015;33(9):407-12. https://doi.org/10.1016/j.urolonc.2015.01.014.
- Jacobs LA, Vaughn DJ. Hypogonadism and infertility in testicular cancer survivors. J Natl Compr Canc Netw 2012;10(4):558-63. https://doi.org/10.6004/jnccn.2012.0053.


