Анализ продуктов гидротермальной обработки хлорида иттрия в присутствии комплексона (лимонной кислоты)
Автор: Анненкова Ирина Павловна, Юдина Екатерина Петровна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Краткие сообщения
Статья в выпуске: 1 т.8, 2016 года.
Бесплатный доступ
Представлены результаты исследования продуктов гидротермального синтеза кислородсодержащих соединений иттрия из хлоридов иттрия в присутствии комплексообразователя - лимонной кислоты. Методом сканирующей электронной микроскопии и порошковой рентгеновской дифракции было зафиксировано образование пористых сферических фрагментов, имеющих аморфную структуру.
Хлорид иттрия, гидротермальный синтез, сканирующая электронная микроскопия, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147160348
IDR: 147160348 | УДК: 544.77+546.05 | DOI: 10.14529/chem160110
Analysis of products formed in hydrothermal processing of yttrium chloride in the presence of complexing agent (citric acid)
The study of yttrium compounds on the result of hydrothermal processing of yttrium chloride in the presence of citric acid is presented. Powder X-ray diffraction analysis and scanning electron microscopy have been used to characterize the properties of the products. Porous spherical particles with an amorphous structure are formed.
Текст краткого сообщения Анализ продуктов гидротермальной обработки хлорида иттрия в присутствии комплексона (лимонной кислоты)
В настоящее время мировой рынок соединений, полученных на основе редкоземельных элементов, активно развивается и расширяется. Соединения иттрия, отдельно и в комплексе с другими редкоземельными элементами, всё более активно начинают применяться при получении нанокерамики, люминофоров, сверхпроводников, катализаторов. Высокое качество этих материалов обеспечивается, в первую очередь, развитой удельной поверхностью, поэтому многие исследования посвящены вопросу синтеза соединений с устойчивой однородной структурой субмикронных размеров.
Наиболее часто для синтеза подобных соединений иттрия используют нитраты и хлориды иттрия [1–6]. При этом синтез проводят как в условиях близких к атмосферным [1–3], так и в условиях гидротермального синтеза под вакуумом при повышенной температуре [4–6]. Следует отметить, что именно соединения, полученные из хлорида иттрия, проявляют тенденцию к формированию чёткой структуры субмикронных размеров [4]. Можно предположить, что наличие комплексона в растворе может способствовать устойчивости формирующихся фрагментов. В данной работе представлены результаты исследования продуктов, формирующихся в условиях гидротермального синтеза из хлорида иттрия при различных значениях pH.
Экспериментальная часть
Для синтеза образцов использовали хлорид иттрия с концентрацией 0,1 моль/л, полученный растворением оксида иттрия в соляной кислоте с концентрацией 3 моль/л. Гидролитический агент – водный раствор гидроксида натрия с концентрацией 1 моль/л. Синтез проводили при различных рН растворов с введением лимонной кислоты после введения гидролитического агента. Значение рН синтеза образцов (8, 9 и 10) находилось ниже и выше рН точки нулевого заряда продуктов гидролиза солей иттрия, равного 9,2–9,3 ед. рН. Длительность синтеза – 24 ч, температура – 180 °C. Процесс осуществляли в термостате в автоклаве с саморегулирующемся давлением, ёмкостью 40 мл с заполнением 50 %. Образцы пятикратно отмывали дистиллированной водой (до отсутствия в промывных водах противоионов), затем сушили при 50 ºC под вакуумом до постоянной массы.
Рентгеновские дифрактограммы записали на порошковом дифрактометре Rigaku Ultima IV. SEM-изображения получили на сканирующем электроном микроскопе Jeol JSM-7001F.
Обсуждение результатов
На рис. 1 представлены микрофотографии образцов, синтезированных при различных рН. Образцы синтезированы при одинаковой температуре, давлении и времени; различие состояло только в значениях pH. Как видно из рис. 1, при данных условиях формируются полые частицы сферической формы.

а)

б)
в)
Рис. 1. Микрофотографии продуктов гидротермальной обработки хлоридов иттрия, полученных при различных pH: а) pH=8; б) pH=9; в) pH=10
Образующиеся частицы являются довольно хрупкими и растрескиваются при нанесении на подложку перед микроанализом. Наименьший диаметр (около 5 мкм) наблюдается для образцов, полученных при pH 9. При этих условиях сферические частицы наиболее устойчивы к механическим воздействиям и сохраняют свою форму в процессе пробоподготовки для сканирующего электронного микроскопа. На рис. 1 заметно, что образцы, полученные при всех использованных значениях pH, имеют в своих стенках поры. Но только при значениях pH, близких к точке нулевого заряда (рН 9), образуются поры наименьшего диаметра (1 мкм и менее).
Дифрактограммы образцов, полученных при различных значениях pH, представлены на рис. 2. Видно, что данные соединения имеют аморфный характер без выраженных признаков кристалличности. Существенных отличий между дифрактограммами, записанными для разных образцов, не наблюдается.
Краткие сообщения
Интенсивность, отн. ед.
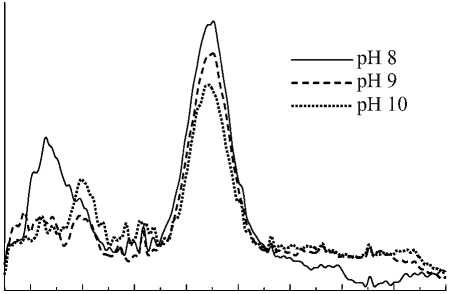
10 20 30 40 50 60 70 80 90
2 Θ , градусы
Рис. 2. Результаты порошковой рентгеновской дифракции продуктов гидротермальной обработки хлорида иттрия при различных значениях pH среды
Заключение
В присутствии лимонной кислоты в качестве комплексообразователя из хлорида иттрия в процессе гидротермального синтеза формируются пористые фрагменты сферической формы. Сферы наименьшего размера образуются в области значений pH, близких к рН точки нулевого заряда продуктов гидролиза водных растворов солей иттрия. Методом рентгеновской дифракции показано, что полученные продукты имеют аморфное строение.
Работа выполнена в рамках проектной части Государственного задания Министерства образования и науки Российской Федерации (грант № 16.2674.2014/K).
Список литературы Анализ продуктов гидротермальной обработки хлорида иттрия в присутствии комплексона (лимонной кислоты)
- Mellado-Vázquez R., García-Hernández M., López-Marure A., López-Camacho P.Y., Morales-Ramírez A.J., Beltrán-Conde H.I. Materials, 2014, vol. 7, pp. 6768-6778. DOI: DOI: 10.3390/ma7096768
- Shahroosvand H., Najafi L., Mohajerani E., Khabbazi A., Nasrollahzadeh M. Green Journal of Materials Chemistry. C, 2013, vol. 1, pp. 1337-1344. DOI: DOI: 10.1039/c2tc00411a
- Hannedouche J., Aillaud I., Collin J., Schulz E., Trifonov A. Chem. Commun., 2008, pp. 3552-3554. DOI: DOI: 10.1039/b804745f
- Shiba F., Tamagawa T., Kojima T., Okawa Y. Cryst. Eng. Comm, 2013, vol. 15, pp. 1061-1067. DOI: DOI: 10.1039/C2CE26485D
- Gruar R.I., Tighe C.J., Muir J. RSC Advances, 2012, vol. 2, pp. 10037-10047. DOI: DOI: 10.1039/c2ra21798h
- Brown P.D., Gill S.K., Hope-Weeks L.J. Journal of Materials Chemistry, 2011. vol. 21, pp. 4204-4208. DOI: DOI: 10.1039/c0jm03178j


