Анатомическое исследование: альтернативный кондуит в аорто-подвздошном сегменте
Автор: Бережной Кирилл Юрьевич, Замский Кирилл Сергеевич, Клещев Павел Викторович, Родивилов Борис Борисович
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 6 (52), 2016 года.
Бесплатный доступ
Одна из главных проблем сосудистой хирургии - инфицирование синтетического протеза. При возникновении инфекционного процесса в области трансплантата необходимо его полное удаление с созданием обходного пути кровообращения. В тоже время проведение экстраанатомического шунтирование не всегда представляется выполнимым в силу распространенности поражения. Одним из вариантов альтернативного трансплантата при последующем шунтировании в условиях инфекционного процесса является бедренная вена. Нами проведено анатомическое исследование для оценки анатомических особенностей бедренной вены в качестве альтернативного кондуита.
Инфекция протеза, бедренная вена, аорто-бедренное шунтирование
Короткий адрес: https://sciup.org/142211294
IDR: 142211294
Текст научной статьи Анатомическое исследование: альтернативный кондуит в аорто-подвздошном сегменте
Инфекция сосудистого протеза - одно из самых грозных осложнений в сосудистой хирургии [1]. Смертность при данной патологии достигает по разным данным 25-60%, а риск потери конечности 25%. [2–6]. Инфекция протеза - нередкое осложнение реконструктивных оперативных вмешательств. По данным мировой литературы, частота встречаемости составляет от 0,2 - 5% [7–10]. Стоит отметить, что частота инфицирования протеза при повторных операциях значительно выше и достигает 5-11% [11].Бедренная вена (БВ) хорошо подходит в качестве альтернативного кондуита для инфраингвинального, аортоподвздошного сегмента, а также для основных артериальных реконструкций.[12–17]. Впервые о сопоставимых результатах использования БВ и большой подкожной вены (БПВ) сообщил Schulmanв 1987 году. [18–20]. Хотя результаты операций, выполняемых в основном при критической ишемии вследствие атеросклеротической окклюзии бедренно-подколенного сегмента были хорошими с уровнем вторичной проходимости до 83% в течение 4-х лет, Schulman был подвергнут критике из-за значительно более травматичного варианта операции по сравнению с использованием БПВ. Но при этом на ранних стадиях исследования Schulman сообщил лишь о незначительных отеках нижних конечностей после изъятияБВ. В дальнейшем эти результаты подтвердили исследования Schanzer.[21]. Nevelsteen и Clagettвпервые начали развивать идею использования БВ при реконструкциях аорто-подвздошного сегмента в условиях развития инфекции. [22,23]. Гистоморфо-логические исследования показали, что коллаген и эластин в составе стенки БВ сравнительно схожсо структурой стенки артерии, что также объясняет низкую тенденцию к неоин-тимальной гиперплазии. [24]. В настоящее время описаны случаи использования БВ при инфекционных поражениях сосудистых протезов, стентов, стент-графтов. [25–32].
В нашей стране также активно занимаются проблемой инфекции в сосудистой хирургии. Затевахин И.И. и Комра-ков В.Е. представили результаты повторных операций при аррозионном кровотечении: в группе пациентов которым проводили удаление протеза с лигированием артерий и ампутацией летальность составила 72,2 %, в группе пациентов которым проводили ушивание дефекта анастомоза 80%, в группе пациентов перенесшим экстраанатомическое шун- тирование 41,7%. При этом стоит заметить, что летальность в последней группе пациентов преимущественно была связана с инфицированием экстраанатомических шунтов, что потребовало в свою очередь повторной операции в условиях генерализованной инфекции. В группе пациентов которым выполнялось экстраанатомическое шунтирование до развития аррозионного кровотечения летальность составила 11,7%. [6]. Хамитов Ф.Ф. показал что использование тактики полного замещения бифуркационного синтетического эксплантата на аутовенозный позволяет сохранить обе конечности в 83,6% наблюдений, одну конечность в 7,2% наблюдений, летальность составляет 3,6%. [33].
Опасения, что забор БВ приведет к значительным осложнениям из-за острой и хронической венозной гипертензии сохраняются, и большинство исследователей сообщают о возникновении венозных отеков сразу после вмешательства [34–37]. Тем не менее, некоторые исследователи получают результаты с минимальным количеством или результаты с не долгосрочными осложнениями, разрешающимися по прошествии определенного времени. В то же время другая часть исследований сообщает о значительном их количестве. Факторами, влияющими на наличие и тяжесть осложнений, являются состояние вен оставшихся после взятия кондуита, в частности, подколенной вены и оставшегося участка БВ. Таким образом, длина кондуита, компенсация венозного оттока за счет оставшихся глубоких вен после взятия материала и коллатералей между подколенной веной и глубокой вены бедра играет важную роль в предотвращении серьезных осложнений. С учетом этих факторов, мы провели анатомическое исследование трупов с целью определения анатомической пригодности поверхностной бедренной вены в качестве альтернативного кондуита при реконструкциях в аорто-подвздошном сегменте.
Материалы и методы
Материалом исследования послужили 34 бедренных вены, взятые в сроки 24-48 часов после наступления смерти, у нефиксированных трупов 13 мужчин и 17 женщин. В четырех случаях бедренная вена была исследована на обеих нижних конечностях. В ходе проведения опытов соблюдали Закон РФ 8-ФЗ от 12.01.96 г., и положения Приказа МЗ РФ № 407 от 10.12.96 г. Исключены из исследования случаи с предшествующей операцией или травмой на изучаемой конечности, ввиду возможных распространенных постромбофлебитических и рубцово-фиброзных изменений сосудов и мягких тканей. В исследование также не включены трупы лиц моложе 50 лет. Последнее условие связано с малой вероятностью атеросклеротического поражения магистральных артерий, а также иным анатомо-морфологическим состоянием венозной системы лиц молодого возраста. В ходе аутопсий нами применялся метод анатомического препарирования. Помимо исследовательской цели работы мы проводили совершенствование мануальных навыков и хирургических приемов, обращая внимание на взаимоотношение анатомических образований в доступе. Бедренная вена с притоками выделялась из протяженного доступа по всей передне-медиальной поверхности бедра в проекции линии Кэна. Традиционно доступ начинали с разреза в скарповском треугольнике, непосредственно от пупартовой связки. Бедренная вена выделялась от места слияния с большой подкожной веной, далее по ходу сосудистого пучка, до входа в верхний канал приводящих мышц (по В.В.Кованову). Следует учитывать, что в зависимости от положения конечности проекция канала может смещаться, и при ротации бедра кнаружи проекция на всем протяжении прикрывается контуром портняжной мышцы. Наибольшие сложности забора вены связаны с глубиной залегания сосудистого пучка в средней и нижней трети бедра. В некоторых случаях, особенно у мужчин с брахиморфной формой телосложения глубина локализации сосуда может достигать 8-10 см. Считаем возможным произвести полноценный забор вены без мобилизации и пересечения портняжной мышцы. В случае когда необходимо произвести забор сосуда максимальной длины возможна мобилизация портняжной мышцы из латерального в медиальный край доступа, с отведением кверху. При этом обязательным условием считаем необходимость вскрытия апоневротической площадки (laminavastoadductoria), являющейся передней стенкой нижнего канала приводящих мышц (гунтеров канал). При выполнении разреза в нижней трети бедра следует опасаться повреждения основного ствола большой подкожной вены, так как в последующем через подкожную венозную систему осуществляется компенсация венозного кровообращения после забора глубокой вены. Важным технологическим аспектом в заборе бедренной вены считаем способ лигирования притоков основного ствола. Отличительной особенностью забора подкожной вены в ходе операции при реваскуляризации миокарда является возможное клипирование металлическими скобками, что безусловно значительно минимизирует время подготовки шунта. Однако кондуит из большой подкожной вены не подвергается более «грубому» механическому и гидродинамическому воздействию. Так возможна несостоятельность культи притока при проведении трансплантата в канале из лапаротомного доступа в рану на бедре, а также при пуске кровотока из аорты по вновь сформированному протезу. Наиболее надежным методом лигирования считаем перевязку притоков лавсановой нитью, неоспоримым преимуществом является сохранение мануального контроля в ходе манипуляции. Недостатком лигирования притоков лавсановой нитью можно считать ее большую подверженность вторичному инфицированию, что может быть исключено применением монофиламентных нитей типа «Пролен». В последующем произведено измерение основных параметров поверхностной бедренной вены: длинны и диаметра, числа значимых впадающих притоков (2 мм и более), а так же количество и место расположения клапанов. Длина бедренной вены измерялась от места слияния с глубокой бедренной веной до нижнего края щели коленного сустава. При этом обязательным условием было сохранение одного клапана в дистальной культе (для предотвращения венозного рефлюкса) и одного значимого притока подколенной вены, что должно уменьшить проявления венозной недостаточности при заборе БВ. Для оценки количества и места расположения клапанов поверхностная бедренная вена вскрывалась продольно по всей длине. Также измерялось расстояние от параумбиликальной области до бифуркации общей бедренной артерии и сопоставлялось с длинной забранной вены на том же трупе.
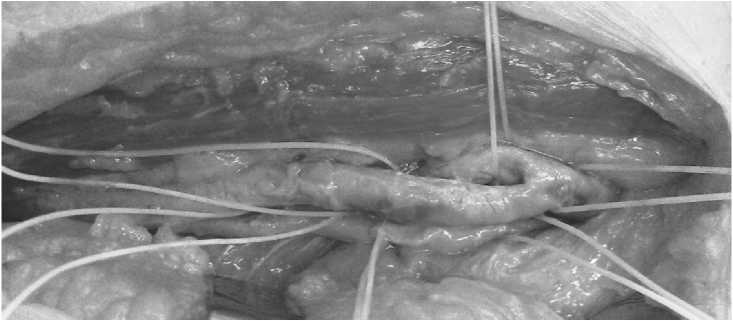
Рис. 1. Выделенная бифуркация бедренной артерии в верхней трети бедра
Результаты
Характеристика распределения по полу и возрасту в группе исследуемых выглядела следующим образом: 13 мужчин (средний рост 173±8 см) и 17 женщин (средний рост 154±6 см). Возраст трупов мужчин варьировал в пределах 70±7 , женщин 68±4 лет. Расстояние от параумбили-кальной области до бифуркации общей бедренной артерии в среднем у мужчин составило 22,5 см, у женщин 18,4 см. Проведен сравнительный анализ по данным анатомического исследования. Длинна бедренной вены а также расстояние до клапана и мест впадения значимых притоков в подколенной вене зависели от пола пациента, и не зависели от его роста и возраста. Так длинна бедренной вены у мужчин составила 27,6±4 см, у женщин - 21,4 см±3 см. Диаметр бедренной вены у мужчин 9,8±1,4 мм, у женщин 9,4 ±0,9 мм. Количество клапанов не составляло 4±1 в обеих группах. Количество притоков бедренной вены так же не отличалось в группах разного пола: притоки более 2 мм: 4±1, менее 2-х мм: 6±2. Количество клапанов подколенной вены также не зависело от пола и составило 2±1. Количество притоков подколенной вены составило у мужчин 5,6±2, у женщин 4,2±1. Таким образом, во всех случаях возможно формирование бифуркационного аорто-бедренного кондуита необходимой длины и подходящего диаметра, даже учитывая компрометацию бедренных артерий гнойно-воспалительным процессом.
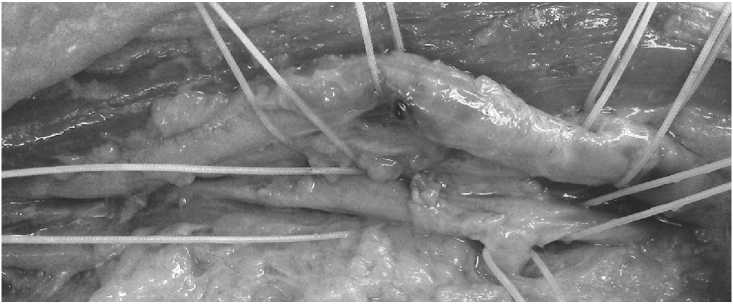
Рис. 2. Этап выделения поверхностной бедренной вены в верхней трети бедра
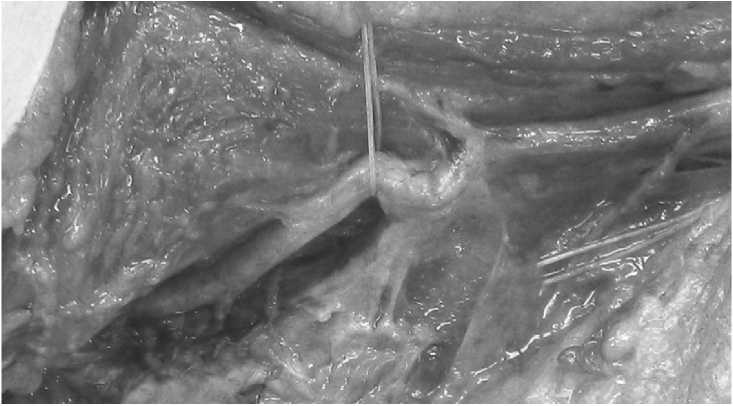
Рис. 3. Этап выделения поверхностной бедренной вены в нижней трети бедра. Продемонстрированы впадающие ветви
Выводы
Таким образом, анатомически пригодной бедренная вена оказалась у 100% исследуемых с условием наличия одного интактного клапана и одной коллатеральной ветви. Возможная длинна кондуита у мужчин 27,6±4 см и 21,4±3 см у женщин.
Обсуждение

Рис. 4. Измерение длины ПБВ
Инфекция сосудистого протеза в аорто-подвздошном сегменте осложнение требующее удаление инфицированного сосудистого трансплантата с последующей реваскуляризацией нижних конечностей для ликвидации ишемии. Ранее «золотым стандартом» в такой ситуации являлось аксило-бифеморальное шунтирование, однако, данное вмешательство имеет ряд тяжелых осложнений и плохие отдаленные результаты. [6, 38±41]. Ряд авторов сообщает о хороших результатах использования протезов импрегни-рованных серебром и антимикробных протезов с комбинированным полимерным покрытием. [41±43].
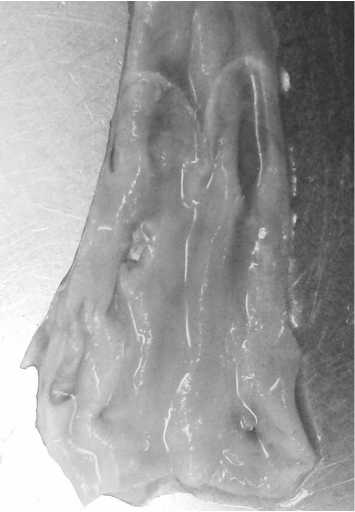
Рис. 5. Клапан ПБВ крупным планом
Использование БВ для реконструкции аорто-бедренного сегмента в условиях инфекции является сложным вмешательством, но оно доказало свою целесообразность в клинической практике с низким уровнем развития повторного инфицирования, хорошей проходимостью.
Существует довольно большая вариабельность в выраженности венозных осложнений после изъятия БВ. При анализе опубликованных статей выяснилось, что не существует единого мнения и протокола по выделению и изъятию БВ. Различия в подходах может объяснить различия в частоте возникновения осложнений после взятия материала и, следовательно, клинически "безопасная" длина БВ до сих пор не определена. Большинство случаев развития тяжелых венозных изменений (венозная гангрена, развитие трофических язв) связаны со случаями использования кондуита включавшего вену ниже щели коленного сустава. Наше исследование показывает, что БВ возможно использовать как альтернативный кондуит в аорто-подвздошном сегменте, определена длинна вены, которую можно изъять, не опасаясь серьезных венозных осложнений. В дальнейшем планируется прижизненное ультразвуковое исследование глубокой венозной системы нижней конечности с целью диагностики и определения пригодности сосудов глубокой венозной системы для реваскуляризирующих операций аорто-бедренно-подколенной зоны. В последующем, несомненно,требуются клинические исследования для подтверждения полученных данных.
Список литературы Анатомическое исследование: альтернативный кондуит в аорто-подвздошном сегменте
- Calligaro K.D., Veith F.J., Schwartz M.L. et al. Differences in early versus late extracavitary arterial graft infections. J VascSurg 1995, 22: 680-688.
- Eshan, O. and Gibbons, C.P. A 10 year experience of using femoro-popliteal vein for re-vascularisation in graft and arterial infections.Eur J VascEndovasc Surg. 2009; 38: 172-179
- Charlton-Ouw, K.M., Sandhu, H.K., Huang, G., Leake, S.S., Miller, C.C. 3rd, Estrera, A.L. et al. Re-infection after resection and revascularization of infected infrarenal abdominal aortic grafts. J Vasc Surg. 2014; 59: 684-692
- Calligaro, K.D. and Veith, F.J. Diagnosis and management of infected prosthetic aortic grafts. Surgery. 1991; 110: 805-813
- Swain, T.W. 3rd, Calligaro, K.D., and Dougherty, M.D. Management of infected aortic prosthetic grafts. VascEndovasc Surg. 2004; 38: 75-82
- Затевахин И.И. Инфекция в сосудистой хирургии/И.И.Затевахин, В.Е.Комраков.-М.,1998. -208 с.
- Coselli J.S., Crawford E.S., Williams T.W. et al. Treatment of post-operative infection of ascending aorta and transverse aortic arch, including use of viable omentum and muscle flaps.Ann ThoracSurg 1990; 50: 868-881.
- Berger, P., Vaartjes, I., Moll, F.L., De Borst, G.J., Blankensteijn, J.D., and Bots, M.L. Cumulative incidence of graft infection after primary prosthetic aortic reconstruction in the endovascular era. Eur J VascEndovasc Surg. 2015; 49: 581-585
- Swain, T.W. 3rd, Calligaro, K.D., and Dougherty, M.D. Management of infected aortic prosthetic grafts. VascEndovasc Surg. 2004; 38: 75-82
- O'Connor, S., Andrew, P., Batt, M., and Becquemin, J.P. A systematic review and meta-analysis of treatments for aortic graft infection. J Vasc Surg. 2006; 44: 38-45
- Kolakowski S., Dougherty M.J., Calligaro K.D. Does the timing of reoperation influence the risk of graft infection? J VascSurg 2007; 45: 60-64.
- Neufang A., Savvidis S. Operative technique and morbidity of superficial femoral vein harvest. Gefasschirurgie. 2016; 21(Suppl 2): 45-54.
- Schulman, ML, Badhey, MR, and Yatco, R. Superficial femoral-popliteal veins and reversed saphenous veins as primary femoropopliteal bypass grafts: a randomized comparative study. J Vasc Surg. 1987; 6: 1-10
- lagett, GP, Valentine, RJ, and Hagino, RT. Autogenous aortoiliac/femoral reconstruction from superficial femoral-popliteal veins: feasibility and durability. J Vasc Surg. 1997; 25: 255-270
- Clagett, GP, Bowers, BL, Lopez-Viego, MA, Rossi, MB, Valentine, RJ, Myers, SI et al. Creation of a neo-aortoiliac system from lower extremity deep and superficial veins. Ann Surg. 1993; 213: 239-249
- Hagino, RT, Bengston, TD, Fosdick, DA, Valentine, RJ, and Clagett, GP. Venous reconstructions using the superficial femoral-popliteal vein. J Vasc Surg. 1997; 26: 829-837
- Schulman, ML, Badhey, MR, Yatco, R, and Pillari, G. An 11-year experience with deep leg veins as femoropopliteal bypass grafts. Arch Surg. 1986; 121: 1010-1015
- Schulman ML, Badhey MR, Yatco R. Superficial femoral-popliteal veins and reversed saphenous veins as primary femoropopliteal bypass grafts: A randomized comparative study. J Vasc Surg. 1987;6:1-10 DOI: 10.1067/mva.1987.avs0060001
- Schulman ML, Badhey MR, Yatco R, Pillari G. A saphenous alternative: Preferential use of superficial femoral and popliteal veins as femoropopliteal bypass grafts. Am J Surg. 1986;152:231-237 DOI: 10.1016/0002-9610(86)90248-5
- Schulman ML, Badhey MR, Yatco R, Pillari G. An 11-year experience with deep leg veins as femoropopliteal bypass grafts. arch Surg. 1986;121:1010-1015 DOI: 10.1001/archsurg.1986.01400090036006
- Schanzer H, Chiang K, Mabrouk M, Peirce EC. Use of lower extremity deep veins as arterial substitutes: Functional status of the donor leg. J Vase Surg. 1991;14:624-627 DOI: 10.1016/0741-5214(91)90185-W
- Clagett GP, Bowers BL, Lopez-Viego MA, Rossi MB, Valentine RJ, Myers SI, et al. Creation of a neo-aortoiliac system from lower extremity deep and superficial veins. Ann Surg. 1993;218:239-248. doi: IO. 1097/00000658-199309000-00003.
- Nevelsteen A, Lacroix H, Suy R. The superficial femoral vein as autogenous conduit in the treatment of prosthetic arterial infection. Ann Vasc Surg. 1993;7:556-560 DOI: 10.1007/BF02000150
- Krasinski Z, Biskupski P, Dzieciuchowicz L, Kaczmarek E, Krasinska B, Staniszewski R, et al. The influence of elastic components of the venous wall on the biomechanical properties of different veins used for arterial reconstruction. Eur J Vasc Endovasc Surg. 2010;40:224-229 DOI: 10.1016/j.ejvs.2010.04.008
- Ali AT, Modrall JG, Hocking J, Valentine RJ, Spencer H, Eidt JF, et al. Long-term results of the treatment of aortic graft infection by in situ replacement with femoral popliteal vein grafts. J Vasc Surg. 2009;50:30-39 DOI: 10.1016/j.jvs.2009.01.008
- Clagett GP, Valentine RJ, Hagino RT. Autogenous aortoiliac/femoral reconstruction from superficial femoral-popliteal veins: Feasibility and durability. J Vasc Surg. 1997;25:255-270. doi: 10.1016/S0741-5214(97)70347-1.
- Daenens K, Fourneau I, Nevelsteen A. Ten-year experience in autogenous reconstruction with the femoral vein in the treatment of aortofemoral prosthetic infection. Eur J VascEndovasc Surg. 2003;25:240-245 DOI: 10.1053/ejvs.2002.1835
- Dorweiler B, Neufang A, Chaban R, Reinstadler J, Duenschede F, Vahl CF. Use and durability of femoral vein for autologous reconstruction with infection of the aortoiliofemoral axis. J Vasc Surg. 2014;59:675-683 DOI: 10.1016/j.jvs.2013.09.029
- Ehsan O, Gibbons CP. A 10-year experience of using femoro-popliteal vein for re-vascularisation in graft and arterial infections.Eur J VascEndovasc Surg. 2009;38:172-179 DOI: 10.1016/j.ejvs.2009.03.009
- Franke S, Voit R. The superficial femoral vein as arterial substitute in infections of the aortoiliac region. Ann Vasc Surg. 1997;11:406-412 DOI: 10.1007/s100169900069
- Heinola I, Kantonen I, Jaroma M, Alback A, Vikatmaa P, Aho P, et al. Treatment of aortic prosthesis infections by graft removal and in situ replacement with autologous femoral veins and fascial strengthening. Eur J VascEndovasc Surg. 2015
- Nevelsteen A, Lacroix H, Suy R. Autogenous reconstruction with the lower extremity deep veins: An alternative treatment of prosthetic infection after reconstructive surgery for aortoiliac disease. J Vasc Surg. 1995;22:129-134 DOI: 10.1016/S0741-5214(95)70106-0
- Хамитов Ф.Ф., Гаджимурадов Р.У., Лисицкий Д.А. Аортобедренное аутовенозное репротезирование при инфицировании синтетического эксплантата./Бюллетень НЦССХ им. А.Н. Бакулева РАМН. Сб. научных работ XXVI съезд сердечно-сосудистых хирургов. 2010, том 11, №6. С.106.
- Wells, JK, Hagino, RT, Bargmann, KM, Jackson, MR, Valentine, RJ, and Kakish, HB. Venous morbidity after superficial femoral popliteal vein harvest. J Vasc Surg. 1999; 29: 282-291
- Sladen, JG, Reid, JDS, Maxwell, TM, and Downs, AR. Superficial femoral vein: a useful autogenous harvest site. J Vasc Surg. 1994; 20: 947-952
- Downs, AR and Guzman, RP. Superficial femoral vein-an alternate vascular conduit.in: Advances in vascular surgery. Vol. 4.: CV Mosby, St. Louis; 1996: 173-182
- Coburn, M, Ashworth, C, Francis, W, Morin, C, Broukhim, M, and Carney, WI Jr. Venous stasis complications of the use of superficial femoral and popliteal veins for lower extremity bypass. J Vasc Surg. 1993; 17: 1005-1009
- Berger, P. and Moll, F.L. Aortic graft infections: is there still a role for axillobi-femoral reconstruction?.SeminVasc Surg. 2011; 24: 205-210
- Seeger, J.M., Pretus, H.A., Welborn, M.B., Ozaki, C.K., Flynn, T.C., and Huber, T.S. Long-term outcome after treatment of aortic graft infection with staged extra-anatomic bypass grafting and aortic graft removal. J Vasc Surg. 2000; 32: 451-461
- Lehnert, T., Gruber, H.-P., Maeder, N., and Allenberg, J.-R. Management of primary aortic graft infection by extra-anatomic bypass reconstruction.EurJVascSurg. 1993; 7: 301-307
- Бадретдинов И.А., Покровский А.В. Аорто-бедренные реконструкции InSitu при хирургическом лечении инфекции аортобедренных протезов/журнал Ангиология и сосудистая хирургия. 2015. -Т. 21.№3. С. 173-179
- Дибиров М.Д., Хамитов Ф.Ф., Гаджимурадов Р.У, Гулаев О.Г. Реваскуляризация InSitu с применением аутоэксплантатов и протезов импрегрированых серебром при инфицировании аортального протеза/Сборник научных работ XXVII международной конференции ангиология и сердечно сосудистая хирургия -2012 №2-18 С.427.
- Михайлов И.П., Леменев В.Л. Лечение гнойных осложнений после реконструктивных сосудистых операций с использованием синтетических протезов/журнал Хирургия.-1998.-№10.-С.54-57


