Антиген для иммунологических анализов
Автор: Хаертдинов К.С., Герасимов В.В., Уразов Н.Г., Вершинина В.И., Элдер Альфредо, Равилов Р.Х.
Статья в выпуске: 2 т.210, 2012 года.
Бесплатный доступ
В результате иммуноблотинга антигенов, полученных из культуральной среды, наиболее активным в иммунологических тестах оказался белок с молекулярной массой 38 кДа.
Антиген, ифа, культуральная среда, белковые фракции, иммуноблотинг
Короткий адрес: https://sciup.org/14287521
IDR: 14287521 | УДК: 619:616.9
Antigen for immunologic analyses
As a result of antigens immunobloting received from cultural medium, protein with molecular mass 38 kD has appeared the most active in immunologic tests.
Текст научной статьи Антиген для иммунологических анализов
Целью данной работы было определить возможность использования культуральной среды (КС) в качестве источника антигенов, пригодных для применения в иммуноблотинге и ИФА.
Клетки штамма «Академия» выращивали на твердой питательной среде Левинштейна-Йенсена в течение 40-60 дней, отмывали от питательной среды, переносили в жидкую питательную среду Сотона. Наращивание бактериальной массы в указанной среде проводили в аппарате «Bacteck» или на шейкере при 37°С в течение 14-28 суток. Клетки отделяли центрифугированием, а супернатант фильтровали через сэндвич из нитроцеллюлозных мембран Миллипор: 0,65 мкм, 0,45 мкм и 0,22 мкм под давлением 0,4 – 0,8 атмосфер, концентрировали в 10 раз в диализных мешках под струей воздуха или на концентраторе «Amicon» с использованием фильтров SM-1-10.
Полученная КС была исследована в ИФА с использованием положительных сывороток (сыворотки пациентов с установленным диагнозом – туберкулез) и отрицательных сывороток (сыворотки условно здоровых людей), а также контрольных сывороток, заимствованных из набора «Бест-туб-ИФА-стрип».
Полученные в ИФА показатели оптической плотности (ОП) с сыворотками больных туберкулезом были выше, чем с сыворотками условно здоровых людей. Однако показатели ОП с отрицательными сыворотками были также достаточно высоки (0,4-0,9 ед. оптической плотности).
Полагая, что присутствующие в КС метаболиты и прочие низкомолекулярные соединения могут конкурировать с белками, при сорбции на полистероле было проведено осаждение белков из КС этанолом.
Процедура была следующей: от спонтанного образовавшегося в во время хранения материала осадка освобождались центрифугированием при 6000 об/мин в течение 10 минут. К супернатанту приливали равный объем охлажденного до -20°С этанола и после 15 минутной экспозиции при -20°С отделяли осадок центрифугированием при 6000 об/мин в течение 10 минут. К полученному супернатанту повторно добавляли еще один, равный первоначальному объем этанола и повторно отделяли осадок. Дальнейшее добавление органического растворителя не приводило к выпадению осадка.
Полученные осадки, а также супернанант, после удаления этанола диализом против дистиллированной воды с последующим концентрированием в диализном мешке под струей воздуха были исследованы в ИФА. Иммобилизацию материалов в лунках полистеролового планшета проводили в забуференном физиологическом растворе (0,15М натрия хлористого в 0,05М натрий-фосфатном буфере, рН 7,2-7,4) при комнатной температуре в течение 18-20 часов.
Постановке ИФА использовали разведение положительной и отрицательной сывороток в разведение 1:100.
На рисунках 1 и 2 представлены показатели ОП антигенных препаратов: исходной КС, спонтанного выпавшего осадка, двух этанольных осадков и двух супернатантов. Первого – после удаления этанола, выдерживанием пробы в диализном мешке под струей воздуха, второго - после диализа против дистиллированной воды и последующего концентрирования в диализном мешке на воздухе. При проведении ИФА использовали положительную и отрицательную сыворотки в разведение 1:100.
Видно, что наиболее высокий коэффициент специфичности при сенсибилизации планшетов препаратами концентрацией в 120 мкг/мл проявляется на антигенном препарате, представляющем осадок, полученный при добавлении к КС равного объема этанола (наименьший коэффициент специфичности имеет препарат, представляющем осадок, полученный при добавлении к КС еще одного равного объема этанола).
На рисунке 3 представлены электрофоретические профили препаратов, которые были исследованы в ИФА. В качестве маркеров (белков с известной молекулярной массой) использовали набор белков с известной массой «Prestained SDS-PAGE Standarts High Range»(BIO-RAD) / Фракционирование проводили в пластинчатом 15% ПАГ по Леммли (1970). Белковые фракции выявляли с помощью красителя кумаси G-250.
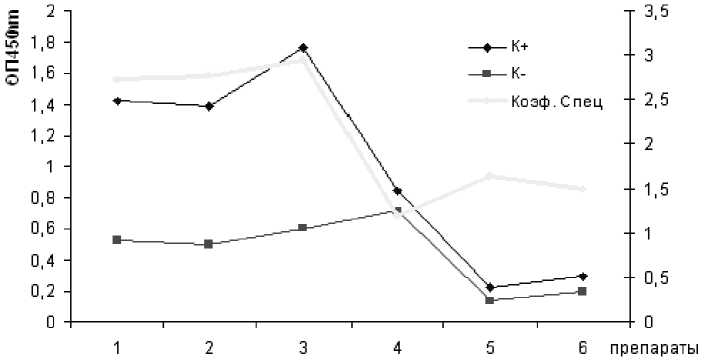
Рис.1. Показатели ОП антигенных препаратов выделенных из культуральной среды
Препараты: 1) исходная КС; 2) спонтанный осадок; 3) осадок, полученный после добавления к КС равного объема этанола; 4) осадок, полученный после повторного добавления к КС еще одного объема этанола; 5) супернатант, после удаления этанола и диализа; 6) супернатант, после удаления этанола.
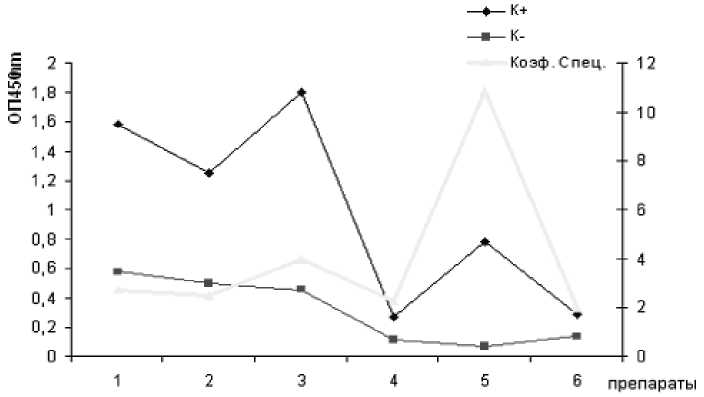
Рис. 2. Показатели ОП антигенных препаратов выделенных из культуральной среды
Препараты: 1) исходная КС; 2) спонтанный осадок; 3) осадок, полученный после добавления к КС равного объема этанола; 4) осадок, полученный после повторного добавления к КС еще одного объема этанола; 5) супернатант, после удаления этанола и диализа; 6) супернатант, после удаления этанола.
Треки: 1 2 3 4 5 М
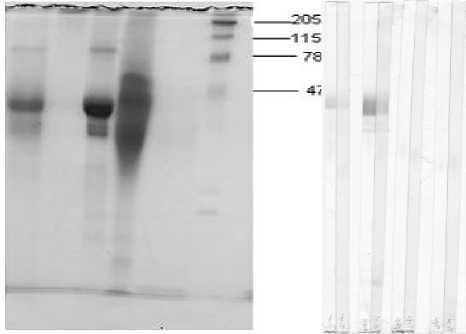
Рис. 3. Электрофоретические профили препаратов полученных из КС.
Треки: 1) исходная КС; 2) спонтанный осадок; 3) осадок, полученный после добавления к КС равного объема этанола; 4) осадок, полученный после повторного добавления к КС еще одного объема этанола; 5) супернатант.
На рисунке 3 видно, что в исходной КС львиная доля по белку приходится на фракцию с молекулярной массой в 39 кДа. Значительно меньшее количество содержится во фракциях с молекулярной массой в 29,5 кДа и 86 кДа. В ней присутствуют также и низкомолекулярные белки, которые мигрируют со скоростью лидирующего красителя -бромфенолового синего.
Основная доля белков спонтанно выпавшего в хранении КС осадка составляют высокомолекулярные белки, остановившиеся на границе концентрирующего и разделяющего гелей и упомянутых выше белков, мигрирующих со скоростью лидирующего красителя.
Видимые на треке исходной КС фракции четко проявляются в осадке, полученном при добавлении к КС равного объема этанола.
Обращает внимание резкое отличие белкового спектра осадка, полученного после повторного добавления еще одного объема этанола. Основное количество белка располагается в диапазоне молекулярных масс 60-20 кДа. В указанном диапазоне просматриваются 4 пика с молекулярными массами 56 кДа, 43 кДа, 29 кДа и 25 кДа. Следует отметить также появление двух минорных фракций имеющих несколько меньшую скорость миграции, чем упомянутая выше низкомолекулярная фракция.
Задачей следующей серии экспериментов состояла в определение наиболее активно реагирующих фракций содержащихся в КС с сыворотками пациентов, больных туберкулезом (рисунок 4).
А Б
1 2 3 4 М 1 2 3 4
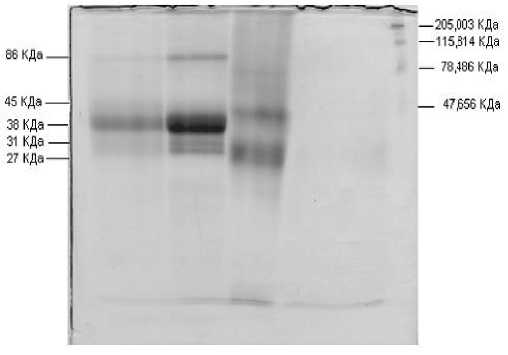
Рис.4. А) Гель, с которого был проведен электроперенос белков на нитроцеллюлозную мембрану и с которого были сняты денситограммы.
Треки: 1) исходная КС; 2) осадок, полученный после добавления к КС равного объема этанола; 3) осадок, полученный после повторного добавления к КС еще одного объема этанола; 4) супернатант.
Б) Иммуноблоты, полученные на антигенах № 1, 2, 3 и 4.
Сыворотки: слева положительная, справа – отрицательная
На рисунке 4 представлены последовательно гель с фракционированными в нем 4 антигенными препаратами, с которого был осуществлен элетроперенос белков на нитроцеллюлозную мембрану, 4 пары иммуноблотов, соответственно количеству фракционированных препаратов и денситограммы 3 антигенных препаратов которые были получены и этого гена. Фракционирование проводили в пластинчатом 15% ПАГ по Леммли (1970). Белковые фракции выявляли с помощью красителя кумаси G-250.
Результаты фракционирования антигенных препаратов (рис.4А) свидетельствуют, что в исходной КС основная доля белка приходится на белок с молекулярной массой 38 кДа и несколько меньшую долю составляют белки с молекулярными массами 30-32 кДа и 86 кДа. Более четкое проявление на электрофореграмме указанных белков в препарате, полученном при внесении в КС равного объема этанола, свидетельствует о том, что указанные белки являются наиболее гидрофобными белками КС.
Результаты иммуноблотинга, представленные не рис 4Б свидетельствуют о том, что серололически наиболее активными является белок с молекулярной массой 38 кДа, несколько уступает ему по активности белки с молекулярными массами 31-30 кДа. Следует также отметить, что указанные белки проявляют серологическую активность с сыворотками условно здоровых пациентов, но в меньшей степени, чем с сыворотками пациентов больных туберкулезом.
Выводы. 1. В исходной КС основная доля белка приходится на белок с молекулярной массой в 38 кДа, несколько меньшую долю составляют белки с молекулярными массами 30-32 кДа и 86 кДа. 2. Указанные белки являются одними из самых гидрофобных белков КС, поскольку первыми выпадают в осадок при внесении в КС органического растворителя. 3. Серололически наиболее активными является белок с молекулярной массой 38 кДа, несколько уступает ему по активности белки с молекулярными массами 31-30 кДа. 4. Указанные белки проявляют серологическую активность с сыворотками условно здоровых пациентов, но в меньшей степени, чем с сыворотками пациентов больных туберкулезом.
АНТИГЕН ДЛЯ ИММУНОЛОГИЧЕСКИХ АНАЛИЗОВ
Хаертдинов К.С., Герасимов В.В., Уразов Н.Г., Вершинина В.И., Альфредо Элдер, Равилов Р.Х.
Резюме
В результате иммуноблотинга антигенов, полученных из культуральной среды, наиболее активным в иммунологических тестах оказался белок с молекулярной массой 38 кДа.
ANTIGEN FOR IMMUNOLOGIC ANALYSES
Khaertdinov K.S., Gerasimov V.V., Urazov N.G., Vershinina V.I., Alfredo Elder, Ravilov R.Kh.


