Аренсульфонаты дифенилвисмута Ph2BiOSO2R
Автор: Шарутин В.В., Сенчурин В.С.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 1 т.17, 2025 года.
Бесплатный доступ
Взаимодействием эквимолярных количеств трифенилвисмута с мезитиленсульфоновой, нафталин-1-сульфоновой, (1S)-(+)-камфора-10-сульфоновой и 2,5-дихлорбензолсульфоновой кислотой (1:1 мольн.) в эфире синтезированы соответствующие аренсульфонаты дифенилвисмута и структурно охарактеризованы мезитиленсульфонат дифенилвисмута (1) и нафталин-1-сульфонат дифенилвисмута (2), представляющие собой координационные полимеры, в которых атомы висмута имеют искаженную тригонально-бипирамидальную координацию с атомами кислорода сульфонатных групп в аксиальных положениях (Bi-О 2,404(4), 2,500(4) для 1 и 2,398(14)-2,435(13) Å для 2) и атомами углерода фенильных заместителей в экваториальных (Bi-С 2,221(18)-2,250(18) Å). Третье положение в экваториальной плоскости занимает неподеленная электронная пара. По данным РСА кристаллы 1 [C21H21BiO3S, M 562,42; сингония моноклинная, группа симметрии P21/n; параметры ячейки: a = 11,821(5), b = 9,056(5), c = 19,275(9) Å; a = 90,00°, β = 99,083(17)°, g = 90,00°; V = 2037,5(17) Å3; Z = 4; rвыч = 1,833 г/см3; m/мм-1 8,772; F(000) 1080,0; 2q 5,7-57 град.; всего отражений 38408; независимых отражений 5147; число уточняемых параметров 239; Rint = 0,0572; GOOF 1,084; R1 = 0,0339, wR2 = 0,0690; остаточная электронная плотность (max/min): 2,16/-2,47 e/Å3], 2 [C44H34O6S2Bi2, M 1140,79; сингония моноклинная, группа симметрии P21/c; параметры ячейки: a = 17,098(8), b = 11,939(6), c = 19,818(8) Å; a = 90,00°, β = 90,070(17)°, g = 90,00°; V = 4045(3) Å3; Z = 4; rвыч = 1,873 г/см3; m/мм-1 8,838; F(000) 2176,0; 2q 5,84-55,98 град.; всего отражений 120306; независимых отражений 9672; число уточняемых параметров 487; Rint = 0,1780; GOOF 1,207; R1 = 0,1183, wR2 = 0,2024; остаточная электронная плотность (max/min): 1,84/-4,84 e/Å3].
Трифенилвисмут, дефенилирование, аренсульфоновая кислота, аренсульфонат дифенилвисмута, синтез, строение
Короткий адрес: https://sciup.org/147248055
IDR: 147248055 | УДК: 547-305.2+546.87+547.53.024+548.312.4 | DOI: 10.14529/chem250115
Diphenylbismuth arenesulfonates Ph2BiOSO2R
The corresponding diphenylbismuth arenesulfonates have been synthesized by the interaction of equimolar amounts of triphenylbismuth with mesitylenesulfonic, naphthalene-1-sulfonic, (1S)-(+)-camphor-10-sulfonic and 2,5-dichlorobenzenesulfonic acids (1:1 molar) in ether and the structural characteristics have been found for diphenylbismuth mesitylenesulfonate (1), diphenylbismuth naphthalene-1-sulfonate (2); they are coordination polymers in which the bismuth atoms have a distorted trigonal-bipyramidal coordination with the oxygen atoms of the sulfonate groups in the axial positions (the Bi-O distances are 2.404(4), 2.500(4) Å for 1 and 2.398(14)-2.435(13) Å for 2) and the carbon atoms of phenyl substituents in the equatorial positions (the Bi-C distances are 2.221(18)-2.250(18) Å). The third position in the equatorial plane is occupied by an unshared electron pair. According to the X-ray diffraction data, crystals 1 [C21H21BiO3S, M 562.42; monoclinic syngony, symmetry group P21/n; cell parameters: a = 11.821(5), b = 9.056(5), c = 19.275(9) Å; a = 90.00°, β = 99.083(17)°, g = 90.00°; V = 2037.5(17) Å3; Z = 4; rcalc = 1.833 g/cm3; m/mm-1 8.772; F(000) 1080.0; 2q 5.7-57 deg.; total reflections 38408; independent reflections 5147; number of refined parameters 239; Rint = 0.0572; GOOF 1.084; R1 = 0.0339, wR2 = 0.0690; residual electron density (max/min): 2.16/-2.47 e/Å3], 2 [C44H34O6S2Bi2, M 1140.79; monoclinic syngony, symmetry group P21/c; cell parameters: a = 17.098(8), b = 11.939(6), c = 19.818(8) Å; a = 90.00°, β = 90.070(17)°, g = 90.00°; V = 4045(3) Å3; Z = 4; rcalc = 1.873 g/cm3; m/mm-1 8.838; F(000) 2176.0; 2q 5.84-55.98 deg.; total reflections 120306; independent reflections 9672; number of refined parameters 487; Rint = 0.1780; GOOF 1.207; R1 = 0.1183, wR2 = 0.2024; residual electron density (max/min): 1.84/-4.84 e/Å3].
Текст научной статьи Аренсульфонаты дифенилвисмута Ph2BiOSO2R
Молекулы производных трехкоординированного висмута (электронная конфигурация Bi s2p3) имеют пирамидальное расположение трех связей с неподеленной электронной парой на атоме висмута. Вовлечение в образование связей d-орбиталей приводит к увеличению координационного числа атома висмута и обусловливает разнообразие структур соединений Bi(III), которые имеют тенденцию к ассоциации и формированию димеров и полимеров. Большинство из описанных структур димеров и полимеров не содержит связей Bi-C [1-3] и только некоторые из них относятся к элементоорганическим соединениям [3–7]. Все соединения, как правило, синтезировали из трифенилвисмута и карбоновых кислот в растворе арена. При избытке карбоновой кислоты имело место образование трикарбоксилата висмута, при мольном соотношении 1:2 конечным продуктом реакции являлся дикарбоксилат фенилвисмута. Обработка трифенилвисмута аренсульфоновой кислотой приводила, как правило, к образованию дисульфонатов фенилвисму- та [8-11], которые являются прекурсорами необычных четырехядерных л-ареновых производных висмута [12, 13] и ионных комплексов висмута с тетрафенилстибониевыми катионами и биядер- ными анионами [14]:
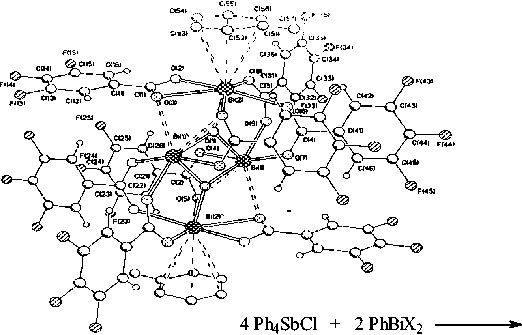
- 2 Ph4SbX
X = OSO2C6H3(Me2)-2,5
[Ph 4 Sb]+ 2
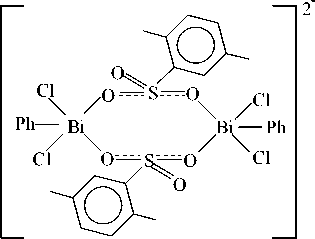
Можно предположить, что при замене в последней реакции хлорида тетрафенилсурьмы на аренсульфонат тетраарилсурьмы будет иметь место образование комплекса подобного строения с аренсульфонатным лигандом при атоме висмута.
Но, если синтез аренсульфонатов тетрафенилсурьмы [15-21] не представлял трудностей, то получение дисульфонатов фенилвисмута описано на малом числе примеров [8-10], поэтому це- лью настоящей работы являлись синтез диаренсульфонатов фенилвисмута Ph2BiOSO2R (R = C6H2(CH3)3-2,4,6, С10H7-1, C10H15O, C6H3Cl2-2,5) и установление особенностей их строения.
Экспериментальная часть
Трифенилвисмут синтезировали по методике, описанной в [22]. В работе использовали аренсульфоновые кислоты производства фирмы Alfa Aesar. Элементный анализ выполнен на элементном анализаторе Carlo Erba CHNS-O EA 1108. Температуры плавления измерены на синхронном термоанализаторе Netzsch 449C Jupiter.
Мезитиленсульфонат дифенилвисмута ( 1 ). Смесь 0,30 г (0,68 ммоль) трифенилвисмута и 0,14 г (0,68 ммоль) мезитиленсульфоновой кислоты в 5 мл диэтилового эфира выдерживали в закрытой ампуле в течение 7 дней при комнатной температуре. После медленного испарения растворителя получили 0,25 г (64 %) неокрашенных кристаллов соединения 1 с т. разл. 209 °С. Найдено, %: С 44,56; Н 3,87. C 21 H 21 BiO 3 S. Вычислено, %: С 44,81; Н 3,73. ИК-спектр ( ν , см–1): 3031, 1565, 1474, 1379, 1259, 1129, 1075, 851, 731, 677, 524, 442.
По аналогичной методике получены:
Нафталин-1-сульфонат дифенилвисмута ( 2 ), неокрашенные кристаллы, выход 73 %, т. разл. 212 °С. Найдено, %: С 45,96; Н 3,03. C 44 H 34 O 6 S 2 Bi 2 . Вычислено, %: С 46,28; Н 2,98. ИК-спектр ( ν , см–1): 3043, 1507, 1476, 1394, 1236, 1098, 1029, 800, 726, 687, 516, 440.
(1S)-(+)-камфора-10-сульфонат дифенилвисмута ( 3 ), неокрашенные кристаллы, выход 65 %, т. разл. 246 °С. ИК-спектр ( ν , см–1): 3048, 1571, 1476, 1394, 1246, 1109, 1073, 853, 731, 692, 537, 452.
2,5-Дихлорбензолсульфонат дифенилвисмута ( 4 ), неокрашенные кристаллы, выход 61 %, т. разл. 243 °С. ИК-спектр ( ν , см–1): 3059, 1568, 1474, 1374, 1262, 1121, 1057, 856, 823, 684, 537, 440.
ИК-спектры соединений 1 - 4 записывали на ИК-спектрометре Shimadzu IRAffinity-1S в таблетках KBr в области 4000–400 см–1.
РСА кристаллов 1 и 2 проведен на дифрактометре D8 Quest фирмы Bruker (MoKα-излучение, λ = 0,71073 Å, графитовый монохроматор) при 296(2) К. Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [23]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [24] и OLEX2 [25]. Структуры определены прямым методом и уточнены методом наименьших квадратов в анизотропном приближении для неводородных атомов. Основные кристаллографические данные и результаты уточнения структур 1, 2 приведены в табл. 1, основные длины связей и валентные углы - в табл. 2. Полные таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджском банке структурных данных (№ 2164819 (1), № 2221091 (2); ; .
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структур 1 и 2
|
Параметр |
1 |
2 |
|
Стехиометрическая формула |
C 21 H 21 BiO 3 S |
C 44 H 34 O 6 S 2 Bi 2 |
|
М |
562,42 |
1140,79 |
|
Сингония |
Моноклинная |
Моноклинная |
|
Пространственная группа |
P 2 1 /n |
P 2 1 /c |
|
a , Å |
11,821(5) |
17,098(8) |
|
b , Å |
9,056(5) |
11,939(6) |
|
c, Å |
19,275(9) |
19,818(8) |
|
α, β, γ, град. |
90,00 |
90,00 |
|
α, β, γ, град. |
99,083(17) |
90,070(17) |
|
α, β, γ, град. |
90,00 |
90,00 |
|
V , Å3 |
2037,5(17) |
4045(3) |
|
Z |
4 |
4 |
|
ρ выч, г/см |
1,833 |
1,873 |
|
µ , мм–1 |
8,772 |
8,838 |
|
F (000) |
1080,0 |
2176,0 |
Окончание табл. 1
|
Параметр |
1 |
2 |
|
Размер кристалла, мм |
0,45 × 0,32 × 0,09 |
0,2 × 0,15 × 0,03 |
|
Диапазон сбора данных по 2 θ , град. |
5,7 - 57 |
5,84 - 55,98 |
|
Диапазон индексов |
–15 ≤ h ≤ 15, –12 ≤ k ≤ 12, –25 ≤ l ≤ 25 |
–22 ≤ h ≤ 22, –15 ≤ k ≤ 15, –26 ≤ l ≤ 26 |
|
Число измеренных рефлексов |
38408 |
120306 |
|
Чисто независимых рефлексов |
5147 |
9672 |
|
R int |
0,0572 |
0,1780 |
|
GOOF |
1,084 |
1,207 |
|
Число параметров |
239 |
487 |
|
R -факторы по I > 2 σ ( I ) |
R 1 = 0,0339, wR 2 = 0,0690 |
R 1 = 0,1183, w R 2 = 0,2024 |
|
R -факторы по всем рефлексам |
R 1 = 0,0418, wR 2 = 0,0723 |
R 1 = 0,1617, w R 2 = 0,2217 |
|
Остаточная электронная плотность (max/min), e/A3 |
2,16/–2,47 |
1,84/–4,84 |
Таблица 2
|
Связь \ |
d , Å 1 |
Угол 1 |
ω , град. |
|
1 |
|||
|
Bi1–O1 |
2,404(4) |
O1‒Bi1‒O31 |
165,56(13) |
|
Bi1–O31 |
2,500(4) |
C11‒Bi1‒O1 |
88,45(16) |
|
Bi1–C11 |
2,224(5) |
C11‒Bi1‒O31 |
83,23(16) |
|
Bi1–C1 |
2,244(5) |
C11‒Bi1‒C1 |
98,13(18) |
|
S1–O1 |
1,478(4) |
C1‒Bi1‒O1 |
81,23(16) |
|
S1–O2 |
1,432(4) |
C1‒Bi1‒O31 |
88,26(15) |
|
S1–O3 |
1,480(4) |
O1‒S1‒O3 |
108,5(2) |
|
S1–C21 |
1,785(5) |
O1‒S1‒C21 |
106,0(2) |
|
O3‒Bi12 |
2,500(4) |
O2‒S1‒O1 |
111,5(3) |
|
C11‒C12 |
1,389(7) |
O2‒S1‒O3 |
113,7(3) |
|
C11‒C16 |
1,397(7) |
O2‒S1‒C21 |
109,4(2) |
|
C21‒C22 |
1,406(7) |
O3‒S1‒C21 |
107,4(2) |
|
Преобразования симметрии: 1 ½ - x, - ½ + y, ½ - z; 2 ½ - x, ½ + y, ½ - z |
|||
|
2 |
|||
|
Вi1–O1 |
2,407(14) |
O1‒Bi1‒O4 |
166,8(5) |
|
Bi1–C11 |
2,226(18) |
C11‒Bi1‒O1 |
82,9(6) |
|
Bi1–O4 |
2,420(16) |
C11‒Bi1‒O4 |
84,9(6) |
|
Bi1–C1 |
2,242(18) |
C11‒Bi1‒C1 |
97,8(7) |
|
Bi2–O6 |
2,398(14) |
C1‒Bi1‒O1 |
92,2(6) |
|
Bi2–O31 |
2,435(13) |
C1‒Bi1‒O4 |
84,4(6) |
|
Bi2–C31 |
2,250(18) |
O6‒Bi2‒O31 |
166,2(5) |
|
Bi2–C21 |
2,221(18) |
C31‒Bi2‒O6 |
93,2(6) |
|
S1‒O1 |
1,478(14) |
C31‒Bi2‒O31 |
82,9(6) |
|
S1‒O3 |
1,465(14) |
C21‒Bi2‒O6 |
83,3(6) |
|
S1‒O2 |
1,431(16) |
C21‒Bi2‒O31 |
84,1(6) |
|
S1‒C41 |
1,79(2) |
C21‒Bi2‒C31 |
96,7(7) |
|
S2–O5 |
1,411(15) |
O1‒S1‒C41 |
104,5(9) |
|
S2–O5 |
1,411(15) |
O3‒S1‒O1 |
107,7(9) |
|
S2‒O6 |
1,485(14) |
O3‒S1‒C41 |
106,8(9) |
|
S2‒O4 |
1,449(14) |
O2‒S1‒O1 |
112,6(10) |
|
S2‒C51 |
1,761(18) |
O2‒S1‒O3 |
114,9(10) |
|
O3‒Bi22 |
2,435(13) |
O2‒S1‒C41 |
109,7(10) |
|
Преобразования симметрии: 1 +x, - 1+y, +z; 2 +x, 1+y, +z |
|||
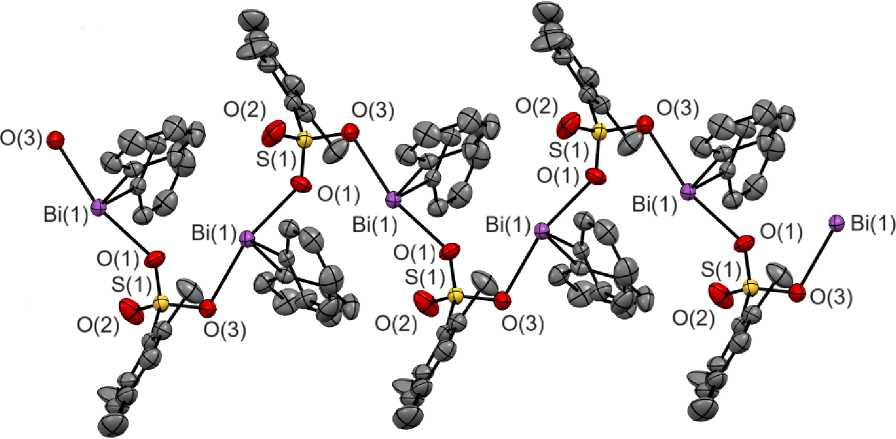
Рис. 1. Фрагмент координационного полимера мезитиленсульфоната дифенилвисмута (1). Атомы водорода не показаны. Проекция вдоль кристаллографической оси b
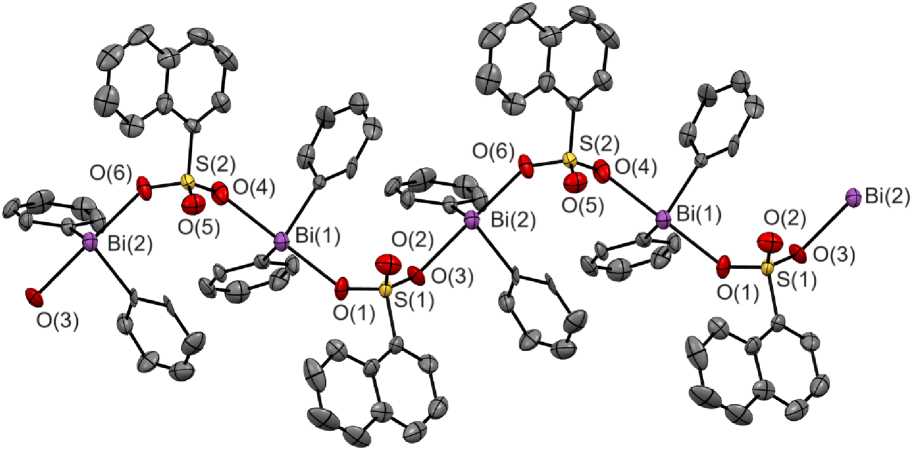
Рис. 2. Фрагмент координационного полимера нафталин-1-сульфоната дифенилвисмута (2). Атомы водорода не показаны. Проекция вдоль кристаллографической оси b
Обсуждение результатов
В настоящей работе органосульфонаты дифенилвисмута синтезировали дефенилированием трифенилвисмута органосульфоновой кислотой в эфире.
n Ph 3 Bi + n HOSO 2 R → [Ph 2 BiOSO 2 R] n + n РhH,
R = C 6 H 2 (CH 3 ) 3 -2,4,6 ( 1 ), С 10 H 7 -1 ( 2 ), C 10 H 15 O ( 3 ), C 6 H 3 Cl 2 -2,5 ( 4 )
Нагревание (90 °С, 1 ч) реагентов в мольном соотношении 1:2 приводило к образованию целевых продуктов в виде мелкокристаллических неокрашенных веществ с высоким выходом (61 - 73 %). Высокие температуры разложения и плохая растворимость в ароматических и алифатических углеводородах соединений 1 - 4 предполагали их полимерное строение.
ИК-спектры соединений 1-4 содержат характерные полосы валентных колебаний углеродного скелета ароматических фрагментов в области 1474‒1571 см–1 [26]. Валентным колебаниям связей CAr–H соответствуют полосы поглощения средней интенсивности при 3031‒3059 см–1; пло- скостным деформационным колебаниям этих же связей – полосы при 1109‒1073 см–1, внеплоско-стным деформационным колебаниям – при 853‒800 см–1. Также присутствуют характерные полосы поглощения сильной интенсивности при 1236-1259 см-1 и средней интенсивности при 1029-1075 см-1, которые отвечают асимметричным и симметричным валентным колебаниям сульфонатной группы SO3. Полосы поглощения высокой интенсивности валентных колебаний связи S‒O расположены при 692‒677 см–1.
По данным РСА, комплексы 1 и 2 являются линейными координационными полимерами со структурными звеньями [Ph 2 BiOSO 2 CR]. Полимерные цепочки в кристалле 1 связаны с соседними цепочками через контакты O 2 SO∙∙∙H Ph-p (2,67 Å), которые много меньше суммы ван-дер-ваальсовых радиусов атомов-партнеров (2,67 Å (3,32 Å) [27]). В кристалле 2 полимерные цепочки не имеют между собой коротких контактов, соответствующих сильным межмолекулярным взаимодействиям. Отметим к тому же присутствие в последнем кристалле двух типов кристаллографически независимых фрагментов [Ph2BiOSO2CR], из которых состоит полимерная цепь. Атомы висмута с учетом стереохимически активной неподеленной электронной пары имеют, с учетом “фантом” лиганда (неподеленной электронной пары), искаженную тригонально-бипирамидальную координацию с атомами кислорода сульфогрупп в аксиальных положениях и двумя атомом углерода фенильных групп в экваториальных. Аксиальные углы ОBiO составляют 165,56(13) ° и 166,8(5) ° соответственно, экваториальные углы CBiC составляют 98,13(18) ° и 97,8(7) ° , валентные связи Bi-O (2,404(4) и 2,407(14) А) короче координационных связей Bi^^^O (2,500(4) и 2,420(16) A). Длины связей Bi–C (2,224(5), 2,244(5) Å и (2,226(18), 2,242(18) Å) меньше суммы ковалентных радиусов атомов-партнеров (2,31 Å [27]). Расстояния между атомом серы и мостиковыми атомами кислорода (1,478(4), 1.480(4) и 1,465(14), 1,478(14) A) длиннее терминальных связей S=О (1,432(4) и 1,431(16) A).
Заключение
Таким образом, дисульфонаты фенилвисмута, полученные с выходом до 73 % из трифенилвисмута и органилсульфоновой кислоты, являются координационными полимерами, в которых атомы висмута имеют искаженную тригонально-бипирамидальную координацию с атомами кислорода сульфогрупп в аксиальных положениях и двумя фенильными лигандами с неподеленной электронной парой - в экваториальных. Особенностью структуры 2 является присутствие в полимерной цепи двух типов чередующихся кристаллографически независимых фрагментов [Ph2BiOSO2CR], при этом полимерные цепочки не имеют между собой коротких контактов, соответствующих сильным межмолекулярным взаимодействиям, в то время как в кристалле 1 такие контакты присутствуют.


