Артефакты форменных элементов и плазмы крови птиц, их происхождение и диагностическое значение
Автор: Колесник Е.А., Дерхо М.А.
Статья в выпуске: 4 т.248, 2021 года.
Бесплатный доступ
Работа посвящена изучению литературных данных (гуманной и ветеринарной медицины) и практическому анализу артефактов форменных элементов и плазмы в мазках периферической крови птиц в модели бройлерных кур Gallus gallus L. раннего постнатального онтогенеза. Возраст исследуемых клинически здоровых цыплят и молодых кур составил: 1 -сутки, 7-е сутки, 23-е сутки и 42 сутки (n=40). Было изучено 158 (n=158) цветных с высоким разрешением микрофотографий полей зрения, в мазках крови окрашенных по Паппенгейму. В результате этого были идентифицированы единичные артефакты эритроцитов птиц: цитоплазматические вакуоли различного характера, фестончатые «укушенные» края клеток. Обнаружены артефакты плазмы крови: околоклеточная и адгезированная на поверхности клеток окрашенная коагулированная зернистость. В некоторых случаях, данная зернистость имитировала токсические формы гранулоцитов и агранулоцитов периферической крови птиц. Необходимо отличать артефакты клеток и плазмы в мазках периферической крови от адаптационных изменений и симптомов инфекционных, инвазионных и незаразных болезней.
Артефакты эритроцитов, артефакты лейкоцитов, артефакты плазмы крови, этилендиаминтетрауксусная кислота (эдта), морфология крови
Короткий адрес: https://sciup.org/142231402
IDR: 142231402 | УДК: 619:617.58.073 | DOI: 10.31588/2413-4201-1883-248-4-129-135
Artifacts of formed elements and plasma of bird blood, their genesis and diagnostic significance
The work is devoted to the study of literature data (humane and veterinary medicine) and the practical analysis of artifacts formed elements and plasma in peripheral blood smears of birds in a model of broiler chickens Gallus gallus L. of early postnatal ontogenesis. The age of the studied clinically healthy chicks and young hens was: day 1, day 7, day 23 and day 42 (n = 40). We studied 158 (n = 158) high-resolution color micrographs of the fields of view, in blood smears stained according to Pappenheim. As a result, single artifacts of avian erythrocytes were identified: cytoplasmic vacuoles of various pattern character, scalloped «bitten» edges of cells. Artifacts of blood plasma were found: pericellular and adhesioned on the cell surface of colored coagulated granularity. In some cases, this granularity imitated the toxic forms of granulocytes and agranulocytes in the peripheral blood of birds. It is necessary to distinguish artifacts of cells and plasma in peripheral blood smears from adaptive changes and symptoms of infectious, invasive and non-infectious diseases.
Текст научной статьи Артефакты форменных элементов и плазмы крови птиц, их происхождение и диагностическое значение
Исследователь, проводя изучение приспособительного процесса индивидуума к факторам среды жизнедеятельности, должен следовать холистическому принципу, то есть изучать реакции с позиции целостного организма. А значит, учитывать взаимодействия и взаимовлияния компонентов систем функций в организме [1, 2].
В этом ключе, необходимо понимать то, что конкретный видовой организм на воздействия окружающей среды отвечает теми морфофизиологическими и биохимическими ресурсами, которыми обладает здесь и сейчас, в независимости от геномного потенциала [1]. При этом ответ организма будет не специфичным и в случае неспецифических адаптационных реакций, и в случае реагирования при развитии той или иной патологии [2]. Примером здесь является система общего адаптационного синдрома с совокупностью этапов стресс-реакции [2]. Механизм специфического иммунного ответа будет вторичным по отношению к первичным базовым и эволюционно рано сформированным механизмам резистентности [1, 2].
В связи с выше обозначенным, важно чётко дифференцировать модификации форменных элементов крови, регистрируемые in vitro вследствие приспособления [3], клинические симптомы патологий [4, 12, 15] и в результате факторов приготовления мазка
[7, 12, 14].
Известно, что антикоагулянты – этилендиаминтетрауксусная кислота
(ЭДТА) в меньшей мере [7, 12, 14], а цитрат натрия [7, 14] и гепарин [4, 7] существенно в большей степени при хранении с ними образцов крови более двух часов при комнатной температуре (+20 – (+25) 0С) вызывают изменения цитоплазмы, мембраны и ядра, осаждение белков плазмы крови, имитирующие симптомы пойкилоцитоза эритроцитов и патологических форм лейкоцитов в мазках периферической крови. В этом случае часто регистрируют псевдоэхиноцитоз [4, 7, 12, 13, 15], они же «клетки заусенцев» [7, 12], встречается псевдостоматоцитоз [4, 13, 15], псевдодакриоцитоз [15], псевдошистоцитоз [15], псевдоакантоцитоз [4]. Регистрируют эритроциты с так называемыми «укушенными» краями (по R.V. Pierre (2002) [15]), то есть, с выемками плазмолеммы, А.И. Воробьёв обозначает данные изменения: эритроциты с
«фестончатыми» краями
При хранении образцов крови с антикоагулянтами более двух часов, может происходить с различной интенсивностью цитоплазматическая вакуолизация нейтрофилов и других гранулоцитов крови [4, 7, 12, 14].
Вместе с тем, обнаруживают псевдотоксические изменения лейкоцитов с множественными гранулами – продуктами артефактной коагуляции плазмы крови, которые адгезируются на поверхности лейкоцитов [4]. Данные артефакты могут имитировать симптомы вирусных и бактериальных инфекций [4]. При которых отмечают базофильно- и оксифильно- окрашенную токсигенную зернистость в грунулоцитах, в основном, в нейтрофилах, и агранулоцитах – встречается в лимфоцитах и моноцитах [4].
Необходимо обозначить механизмы образования артефактов клеток и плазмы крови in vitro.
Так, ЭДТА может вызывать повреждение мембран эритроцитов и лейкоцитов, сокращение эритроцитов из-за гипертонуса цитоплазмы с повышенной ионной концентрацией [12]. Дефекты, связанные с длительным (несколько часов) хранением форменных элементов в антикоагулянте (ЭДТА, цитрат натрия) могут варьироваться от зубчатости, шиповатости мембраны эритроцита до изменения плотности окрашивания [14].
Отмечается, что артефактные эхиноциты и стоматоциты могут формироваться вследствие химической и цитохимической реакции in vitro. В частности, высокий pH (щелочная среда) образующийся при реагировании плазмы с избыточно щелочным стеклом пробирки или предметного стекла вызывает псевдоэхиноцитоз [4, 15] и псевдоакантоцитоз [4, 15]. И наоборот, низкий pH (кислая среда), который аналогично, может быть индуцированным от примесей стекла, приводит к псевдостоматоцитозу [4, 15].
Интересны наблюдения авторов [15], так, псевдостоматоциты, равно, как и псевдоэхиноциты возвращаются к нормальной конфигурации эритроцитов in vitro при помещении их в плазму с физиологическим pH среды.
Стоматоциты также могут образовываться при воздействии на эритроциты различных химических веществ, обычно катионных, амфифильных веществ и лекарственных препаратов, например, фенотиазина и хлорпромазина [15].
Вследствие длительного, или напротив, быстрого высыхания мазков, могут образовываться артефакты, имитирующие различные формы пойкилоцитоза, в том числе эхиноциты, акантоциты, стоматоциты [13, 15].
По данным B.I. Dalal et M.L. Brigden [4], аутоантитела IgG могут вызывать агглютинацию клеток крови в присутствии ЭДТА, но не в цитратной крови.
Тогда как аутоантитела IgM часто не зависят от ЭДТА, поэтому агглютинация также наблюдается с другими антикоагулянтами. Здесь интересно то, что некоторые аутоантитела относятся к холодно-реактивному типу, т.е. активны только при комнатной температуре [4].
Весьма малочисленны литературные данные по артефактам клеток и плазмы крови птиц, представлены в основном, в зарубежных публикациях [5, 6, 8, 9], несмотря на то, что эритроциты птиц (Aves L.) более хрупкие и чувствительны к различным воздействиям в сравнении с млекопитающими (Mammalia L.).
Тем более, учитывая и то обстоятельство что кровь молодых птиц весьма сложна в диагностике, отличается обилием сенситивных незрелых форм эритроцитов [6, 8, 10] и лейкоцитов [6, 8, 11].
Целью работы явилось изучение литературных данных (гуманной и ветеринарной медицины) и практический анализ на предмет артефактов форменных элементов и плазмы в мазках периферической крови птиц в модели бройлерных кур раннего постнатального онтогенеза.
Материал и методы исследований. Работа выполнена в соответствии принципам гуманного обращения с подопытными животными, отмеченных в директивах Европейского Парламента и
Совета ЕС по охране животных, используемых в научных целях (Директива 2010/63/EU). Экспериментальная часть работы выполнена на ООО «Чебаркульская птица» (Чебаркульский р-н, Челябинская обл.). Объектом исследования служили бройлерные цыплята Gallus gallus L. кросса Hubbard ISA F15 промышленного стада, из которых в цехе выращивания (клеточное содержание), согласно принципам случайной выборки и сбалансированных групп, сформировали четыре группы (n = 40).
Возраст цыплят в каждой из групп составил 1, 7, 23 и 42 дня постнатального онтогенеза. Экспериментальные группы кур Gallus gallus L. по Anamnesis vitae клинически (status praesens) соответствовали: fusce sanitas status статусу здоровых животных. Кормление и содержание цыплят осуществляли в соответствии с зоогигиеническими нормами согласно рекомендациям (Руководство Hubbard ISA, URL: http://hubbardbreeders.com). Материалом исследований служила цельная кровь, которую собирали в стандартизированные вакуумные пробирки с ЭДТА путём декапитации птицы в 1- и 7-суточном возрасте и прижизненно – пункцией подкрыльцовой вены у 23- и 42- суточных цыплят [10, 11]. Окраску мазков периферической крови производили по Паппенгейму (А. Pappenheim) [10, 11]. Цветные высокого разрешения микрофотографии получали с помощью большого биологического микроскопа («МББ - 1А», «ЛОМО», Россия), оснащенного микрографической окулярной видеокамерой с матрицей разрешением 5 мегапикселей (Full HD High resolution “HAYEAR” CMOS 5.0 Megapixel microscope video camera, КНР) с визуализацией в программе ToupView (ToupTek Photonics, КНР, URL: http://www.touptek.com/) [10, 11], c построенной светодиодной системой освещения микропрепаратов белым спектром (реализован принцип Кёлера (A. Köhler) [10, 11]. Для наиболее качественного изображения клеток крови, применяли 90-кратный апохроматический объектив масляной иммерсии с апертурой 1,3 («ЛОМО», Россия), позволяющий получать микрофотографии со специальной коррекцией хроматических аберраций. Калибровку видеокамеры производили по шкале объект-микрометра для проходящего света с ценой деления 0,01 мм («ОМП» ГОСТ 7513-55 «ЛОМО», Россия) в программе ToupView. В программе ToupView определяли масштаб изображений и на микрофотографиях размещали масштабную линейку с ценой деления в 10 микрометров (μm). На предмет изучения артефактов клеток и плазмы, был выполнен анализ 158 (n=158)
микрофотографий полей зрения в мазках периферической крови.
Результат исследований. Были идентифицированы различного морфологического характера единичные артефакты эритроцитов, лейкоцитов и плазмы периферической крови (Рисунок 1, 2). А.И. Воробьёв, подчёркивает (https://www.youtube.com/watch?v=Dor_ XUuTW2s), в мазке крови, в норме, могут в небольшом количестве встречаться эритроциты с фестончатыми краями (Рисунок 1: 1.2), это обычно нормальные артефакты вследствие приготовления мазка, то есть, механическом растаскивании ткани крови по поверхности стекла (https://www.youtube.com/watch?v=Dor_ XUuTW2s). Авторы [7;
https://eclinpath.com/atlas/hematology/blood-artifacts/ ] регистрировали вакуоли в цитоплазме эритроцитов. Представлены вакуольные артефакты в эритроцитах птиц, при этом, более мелкие вакуоли сравнительно многочисленны в отдельных эритроцитах (Рисунок 1: 1.1, 1.3), а крупные вакуоли единичны (Рисунок 1: 1.4).
J.W. Harvey отмечает, в процессе высушивания мазков крови, в эритроцитах могут образовываться артефакты, оптически визуализируемые в виде просвечивающихся лакун овальной, округлой или неправильной формы [9, p. 20], эти артефакты, ввиду оптического светопреломления выглядят полосчатыми зелёно-желтыми образованиями (см. рис.1: 1.3, 1.2).
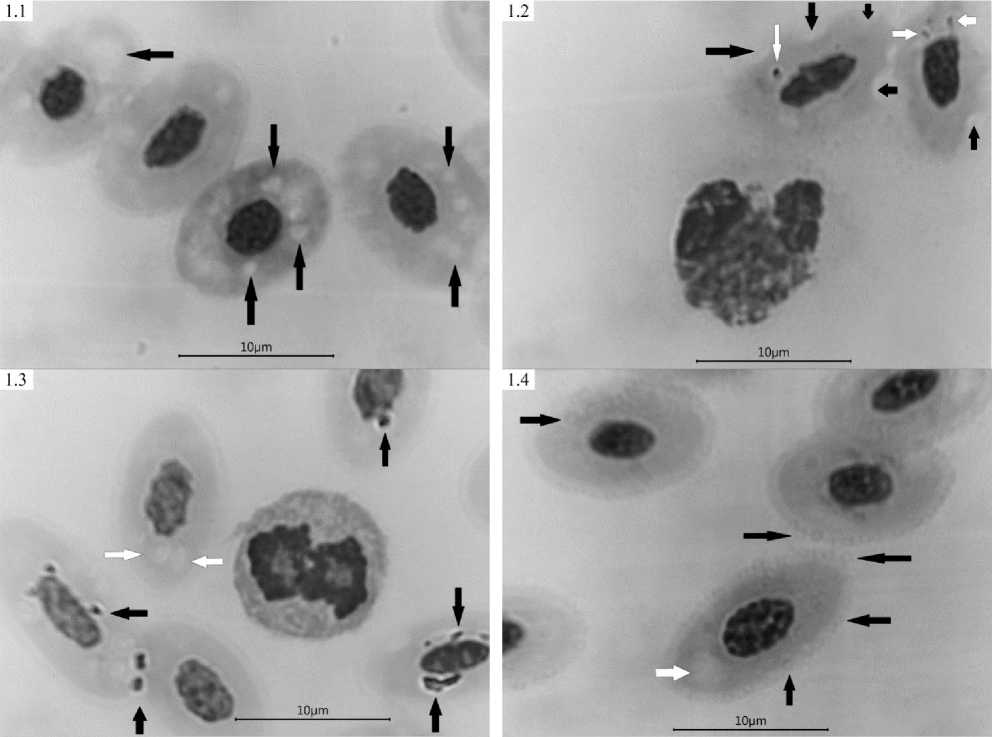
Рисунок 1 – Артефакты форменных элементов и плазмы крови птиц Gallus gallus L., окраска мазков по Паппенгейму, здесь и далее, в скобках указан возраст птиц. Вакуоли в цитоплазме эритроцитов: 1,1 (1-е сут.) – показаны черными стрелками, в центре полихроматофильный эритроцит; 1,3 (23-е сут.) – показаны белыми стрелками, в центре митотический базофильный эритробласт; 1,4 (1-е сут.) – показана белой стрелкой; фестончатые («укушенные») края эритроцитов: 1,2 (23-е сут.) – показаны черными стрелками, в центре сегментоядерный гетерофил; опалесцирующие лакуны в цитоплазме эритроцитов: 1.3 – показаны черными стрелками, 1,2 – показаны белыми стрелками; околоклеточная коагулированная зернистость плазмы: 1,4 (1-е сут.) – показаны черными стрелками. Здесь и далее, цена деления масштабной линейки десять микрометров (10 µm)
Аналогичной природы артефакты T.W. Campbell называет перинуклеарными кольцами [6, p. 40]. Данные образования в эритроцитах автор объясняет особенностью коагуляции стромы эритроцитов в ходе медленного высушивания мазков или воздействия химических фиксаторов, в частности паров формалина [6, p. 40]. P. Clark et al. показывают артефакты в цитоплазме зрелых эритроцитов зеленого карликового гуся (Nettapus pulchellus) в виде рефракционных пятен от красителя, возникающие вследствие недостаточного высыхания клеток перед окрашиванием [8, p. 19, 22].
Подобные артефакты в незначительном количестве неизбежны в практической работе. В помещении возможны колебания температурного и влажностного режимов, к тому же, учитывая физиологическую, сравнительно с млекопитающими животными, высокую температуру тела птиц, эритроциты в ходе приготовления мазка подвергаются существенному температурному шоку, и вследствие этого, могут формироваться подобные изменения.
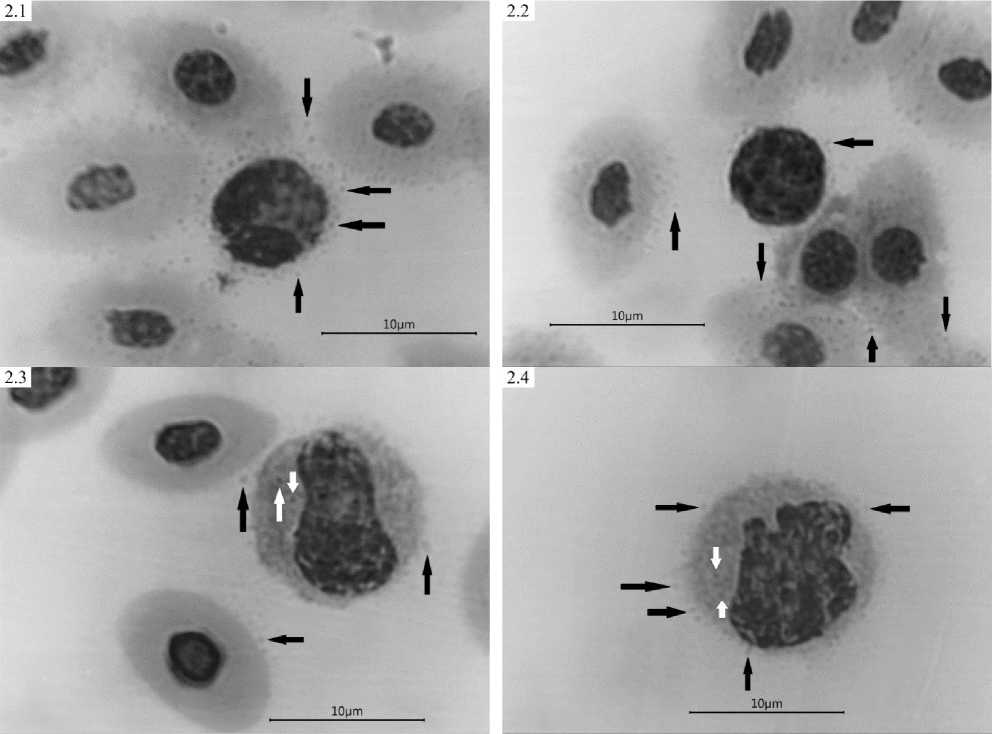
Рисунок 2 – Артефакты плазмы крови птиц Gallus gallus L., окраска мазков по Паппенгейму. Околоклеточная коагулированная зернистость плазмы: 2,1, 2,2 (1-е сут., в центре сегментоядерный гетерофил и базофил соответственно); 2,3, 2,4 (42-е сут., справа и в центре соответственно – моноцит) – показаны черными стрелками; адгезированная коагулированная зернистость плазмы на поверхности клеток: 2,3, 2,4 – показаны белыми стрелками
T.W. Campbell [5] отмечает возможное наличие мелкой зернистости вокруг форменных элементов в мазках крови (см. Рисунок 1: 1,4; Рисунок 2), по мнению автора, это является нормальным артефактом – особенностью коагуляции плазмы крови при фиксации мазка [5, p. 182, 183, p. 194]. При этом нередко, подобная зернистость плазмы крови может окрашиваться (см. Рисунок 1: 1,4; Рисунок 2) и в случае адгезии её на лейкоцитах – имитировать токсические формы гранулоцитов и агранулоцитов (Рисунок 2: 2,3, 2,4).
Заключение. Единичные морфологические изменения клеток и плазмы в мазках периферической крови являются нормальными артефактами полиэтиологичной природы.
Однако, важно дифференцировать артефакты форменных элементов и плазмы от модификаций адаптационного характера и изменений клеток крови, являющихся симптомами инфекционных, инвазионных и незаразных патологий.
Резюме
Работа посвящена изучению литературных данных (гуманной и ветеринарной медицины) и практическому анализу артефактов форменных элементов и плазмы в мазках периферической крови птиц в модели бройлерных кур Gallus gallus L. раннего постнатального онтогенеза. Возраст исследуемых клинически здоровых цыплят и молодых кур составил: 1 – сутки, 7-е сутки, 23-е сутки и 42 сутки (n=40). Было изучено 158 (n=158) цветных с высоким разрешением микрофотографий полей зрения, в мазках крови окрашенных по Паппенгейму. В результате этого были идентифицированы единичные артефакты эритроцитов птиц: цитоплазматические вакуоли различного характера, фестончатые «укушенные» края клеток. Обнаружены артефакты плазмы крови: околоклеточная и адгезированная на поверхности клеток окрашенная коагулированная зернистость. В некоторых случаях, данная зернистость имитировала токсические формы гранулоцитов и агранулоцитов периферической крови птиц. Необходимо отличать артефакты клеток и плазмы в мазках периферической крови от адаптационных изменений и симптомов инфекционных, инвазионных и незаразных болезней.
Список литературы Артефакты форменных элементов и плазмы крови птиц, их происхождение и диагностическое значение
- Колесник, Е. А. Стресс-реакция как защитный иммунный механизм, направленный на восстановление гомеостаза организма / Е.А. Колесник // Вестник Челябинского государственного университета. Образование и здравоохранение. – 2020. – № 4 (12). – С. 5–14. – doi: 10.6084/m9.figshare.16866886.v1.
- Колесник, Е.А. К проблеме физиологического адаптационного гомеостаза в модели организма теплокровных животных / Е. А. Колесник, М. А. Дерхо // Вестник Челябинского государственного университета. Образование и здравоохранение. – 2020. – № 4 (12). – С. 15–30. – doi: 10.6084/m9.figshare.16866820.v2.
- Сайфутдинова, Л.В. Влияние технологического стресс-фактора на морфологические особенности эритроцитов кур / Л.В. Сайфутдинова, М.А. Дерхо // Ученые записки Казанской государственной академии ветеринарной медицины им. Н.Э. Баумана. – 2020. – Т. 241. – № 1. – С. 171–176. – doi: 10.31588/2413-4201-1883-241-1-171-176.
- Dalal, B.I. Artifacts that may be present on a blood film / B.I. Dalal, M.L. Brigden // Clinics in Laboratory Medicine. – 2002. – V. 22 (1) – P. 81-100. – doi: 10.1016/s0272-2712(03)00068-4.
- Campbell, T.W. Hematology / T.W. Campbell, B.W. Ritchie, G.J. Harrison, L.R. Harrison (Eds.) // In book: Avian Medicine: Principles and Applications. – Lake Worth, Florida: Wingers Publishing, Inc., 1994. – P. 176-198.
- Campbell, T.W. Exotic Animal Hematology and Cytology. Fourth edition / T.W. Campbell. – Ames, Iowa: Wiley-Blackwell. A John Wiley & Sons, Ltd., Publication, 2015. – 403 p.
- Choudhary, S. Storage artefacts in peripheral blood smears / S. Choudhary, R.S. Katkar, D. Nagaram // IP Journal of Diagnostic Pathology and Oncology. – 2018. – Vol. 3 (3) – P. 187-191. – doi: 10.18231/2581-3706.2018.0039.
- Clark, P. Atlas of Clinical Avian Hematology / P. Clark, W.S. J. Boardman, S.R. Raidal. – Oxford: Wiley-Blackwell, 2009. – 200 p.
- Harvey, J.W. Veterinary Hematology: A Diagnostic Guide and Color Atlas / J.W. Harvey. – St. Louis, Missouri: Saunders / Elsevier Inc., 2012. – 384 p. – doi: 10.1111/vcp.12007.
- Kolesnik, E.A. Differential morphophysiological characteristics of erythrocyte precursors and mature erythroid cells in early postnatal ontogenesis of birds / E.A. Kolesnik, M.A. Derkho, V.K. Strizhikov [et al.] // International Journal of Biology and Biomedical Engineering. – 2020. – Vol. 14. – P. 101–108. – doi: 10.46300/91011.2020.14.15.
- Kolesnik, E.A. Functional morphology of birds' blood leukocytes / E. Kolesnik, M. Derkho, V. Strizhikov [et al.] // Journal of Experimental Biology and Agricultural Sciences. – 2020. – V. 8. – No Special Issue 2. – P. 374-380. – doi: 10.18006/2020.8(Spl-2-AABAS).S374.S380.
- Koolwal, M.S. Anticoagulant EDTA Induced Storage effect (Artifacts) on Peripheral Blood Cells / M.S. Koolwal // Journal of Medical Science and Clinical Research. – 2018. – V. 06. – I. 01. – P. 32430-32433. – doi: 10.18535/jmscr/v6i1.05.
- Longo, D.L. Atlas of Hematology and Analysis of Peripheral Blood Smears. Chapter e17. Part 2. Cardinal Manifestations and Presentation of Diseases / D.L. Longo. – New York: The McGraw-Hill Companies, 2012. – P. 12-17.
- Narasimha, A. Anticoagulant induced artefacts in peripheral blood smears / A. Narasimha, H. Kumar, B.R. Prasad // Indian J. Hematol. Blood Transfus. – 2008. – Vol. 24 (2). – P. 43-48. – doi: 10.1007/s12288-008-0027-6 ; PMID: 23100942 ; PMCID: PMC3453045.
- Pierre, R.V. Red cell morphology and the peripheral blood film / R.V. Pierre // Clinics in Laboratory Medicine. – 2002. – Vol. 22 (1) – P. 25-61. – doi: 10.1016/s0272-2712(03)00066-0 ; PMID: 11933577.


